1 Изобретение относится к способу прпучения оксисоединений, в частности d -ненасыщенных альдегидов или кетонов общей формулы RI О В2-Ч -Кз где R - водород у нормального или изо строения aifKiin с 1-6 атомами углерода; R - насыщенный или ненасыщен ный алкилостаток, который может быть связан с насыщенным или ненасыщенным щжлоалкилостатком, или насыщенный или ненасыщенный циклоалкилостаток с 20 ат мами углерода, FJ и R могут быть зам ты в насыщенный ИJШ ненасыщенный цикло алкилостаток; bj - водород, насыщенный И1Ш ненасыщенный алкилостаток, который может быт связан с насыщенным или ненасыщенным I никлоалкилостатком, или насыщенный или ненась щен1йлй циклоалк1;лостаток, нричск | алкпл- и циклоалкилостатки I замещеим в соответствующем случае imaiuiiM алки.чом, низшей аысокси-, оксигруппой, в соотмегсмвующем случае кетализированиой oKctirpyaпой, ниаишм алкаяоилом, ароилоМг Hnaujt ii ашсаноилокСи- или аронлоксигруппой. Эти соединения могут найти 1Т}Л1ме1)ение в парфюмерной промьпиленпости в области каротиноидов или стероидов. Известен способ получе ия иенасьицеи1 Ь х альдегидов, например цитраля, ;:1акл1(,. чающийся в том, что соответствуюиии aiu. типеиовый спирт подвергают изомеризации Б присутствии в качестве каталисзатор, соединение таких металлов, как ианади, пни-, бий, молибден, вольфрам, нащзимер триалкилки лортова надата. В известном способе примоняютси катализаторы, не отличающиеся достаточной ус. тоймивостью и высокой активностью. С целью устранения указан1Ш1х недос. ков и рас1иирения ассортимс нта конечных фодуктов предложен способ, заключаннли jcH в том, что ацетиловые спирты общей формулы Б:., 2 где R -I имеют указанные значения, 1 о подвергают изомеризации в присутстви катализатора общей формулы :)-&i-o o. , где KW - низший алкил, циклоалкил, фени или аралкил, причем названные остатки м гут быть в соответствующем случае заме щены низщим алкилом; R - KW - или (KW)o - Si. -группа:j П - целое число от 2 до 3; П 0,1 или 2, причем fU + М 3., Целевой продукт выделяют известными способами. В -формуле I Ц в качестве низшизс ал килов предпочтителен метил, в качестве I высших алкилов -изопрен или подобная изо 1рену структура, например 4-метил-пент-енил; 4,8-диметил-нона-3,7-диенил; 4,8 12-триметил-тридецил; 4-окси-4-метил-пентил и 4-метокси-4-метил-пентил. В соответствующем случае замещенный циклоалкилкомпонент остатка R может содержать в крайнем случае 20 атомов угдерода. Примерами таких циклоал- килостатков, связанных с насыщенными ил ненасыщенными, разветвленными или нера ветвленными алкилостатками J , предпоч- тительно алкилостатками, обладающими структурой изЪпрена или ему подобной стр 1турой, являются: 2-{2,6,6-триметил-циклогекс -1-ен-1 -ил)-вишш2-( 4-оксо-2,6,6-триметил-циклогекс-1-ен-1-ил)-винил; 2-{ 4-этилендиокси-2,6,6-триметил-цик логекс-1-ен-1-ил)-ви11ил; 6-(2,6,6-триметил-циклогекс-1-ен-1-и -4-метнл-гекса-1,3,5-триенил; 6-(4-оксо-2,6,6-триметил-циклогекс-1 -ен-1-ил)-4-метил-гекса-1,3,5-триенил J о-(4-этилендиокси-2,6,6-триметил-цик.логекс-1-ен-1-ил)-4-метии-гекс-1,3,51-триенилостаток. { в формуле I в качестве низших алкйлов является, пропил, в качестве высших2 6-димети л -гёпта-1,3 ,5-три нилостаток. В качестве исходных спиртов формулы .. Ц замкнуты в соответствуюП, где R, и щем случае в замещенный насыщенный или ненасыщетилй циклоалкилостаток, могут быть: 1-этинил-циклогексанол; 4-ЭТИНИЛ-4-ОКСО-1-ЧЖСО-3,5,5-триметил-циклогекс-2-ен;4-этинил-4-окси-1-этилендиокси-3,5, -триметил-циклогекс-2-ен. В качестве заместителей алкил- и циклоалкилостатков могут быть применены а килостатки с 1-6 атомами углерода, например метил, этил, пропил, изопропил и другие; низшие алкоксигруппы с 1-6 атомами углерода - метокси, этокси, пропокси, изопропокси и др.,- низшие алканоияостатки с 1-6 атомами углерода, такие как формил, ацетил, пропионил, бутирил и другие ароилостатки (в частности,, бензоил); низщие алканоилостатки с 1-6 атомами углерода, такие,как ацетокси, пропионилокси, бутирилокси и другие; ароилокси (в частности, бензоилокси). Оксогруппа может быть кетализирована низшими алканолами или гликолями, напри- мер метанолом или этиленгликолью.i В примененном катализаторе формулы III К VV -остаток представляет собой предпочтительно низший алкил, содержащий максимально 7 атомов углерода, например метил, этил, изопропил или Л-бутил, а также фенил замещенный или незамещенный, например толил, ксилил, бензил или фенилэтил. Из полученных соединений формулы I наиболее важными являются четыре группы соединений, которые можно представить следующими обшщми формулами: К 0 R замкнуты в замещенный в где соответствующем случае низшим алкилом, низщей алкокси-, оксигруппой, в соответствующем случае низшей кетаяизированной оксогруппой, насыщенный и;ш ненасыщенный циклоалкилостаток; Н о
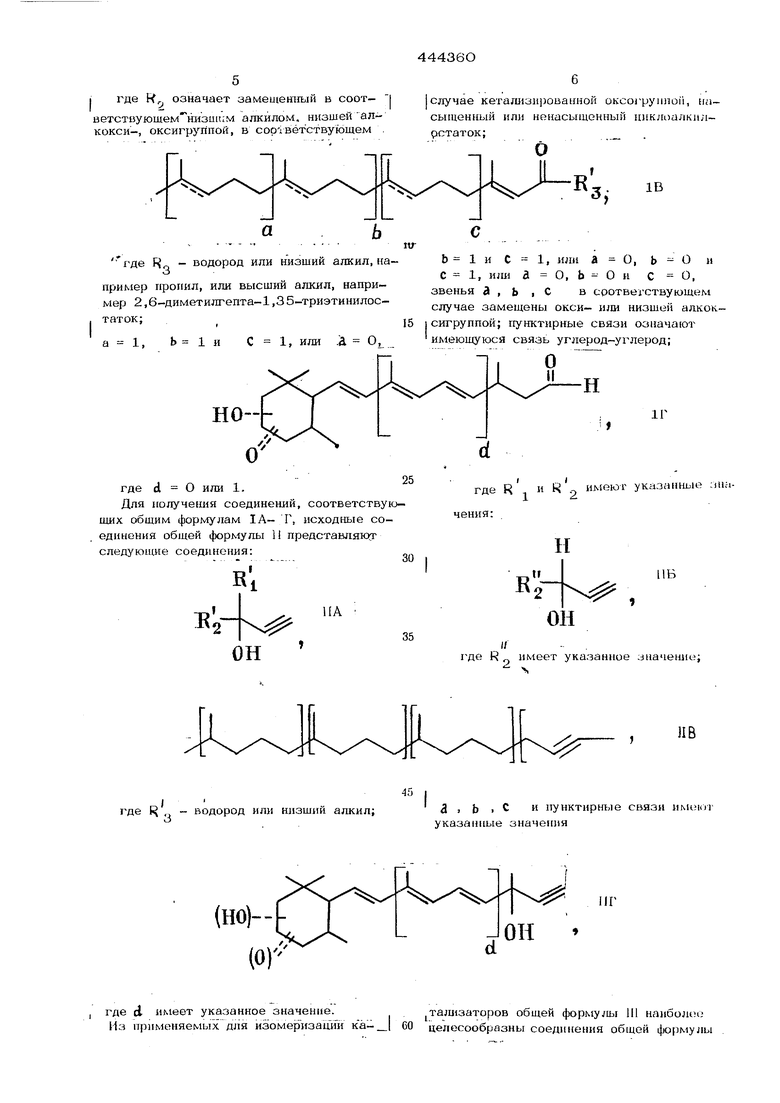
I где R означает замеи1ениый в соот- 1
ветствующем низшим апкйлом. низшейалКОКСИ-, оксигруппой, в сор вётствующем
6
случае кетализирова ной oKcoi-pyiinoii, насыщенный или ненасыщенный циклоалкилрстаток;
а
О
R
1В
з где RQ - водород или низший алкил, на пример пропил, или высший алкил, например 2,6-диметилгепта-1,35-триэтиниластаток;, , С 1, или . 0, НО где d О или 1. Для получеЕшя соединений, соответствую щих общим формулам 1А- Г, исходные соединения общей формулы 11 представляют следующие соединения: 24b 1 и С 1, шш а О, b о и С 1, ИШ1 а О, ь - О и с о, звенья Д , ь 1 С в соответствующем случае замещены окси- и;ш низшей алкок сигруппой; пунктирные связи означают имеющуюся связь углерод-углерод; где R и R.-, имею г указаЕ1Ные мпаЕ:--, е R имеет указанное значение;




| название | год | авторы | номер документа |
|---|---|---|---|
| Способ стабилизации катализатора | 1973 |
|
SU581846A3 |
| КОМБИНАЦИЯ 1-АЗА-3,7-ДИОКСАБИЦИКЛО[3,3,0]ОКТАНОВЫХ СОЕДИНЕНИЙ И ЭФИРОВ КРЕМНИЕВОЙ КИСЛОТЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ПРЕДШЕСТВЕННИКОВ ДУШИСТЫХ ВЕЩЕСТВ | 2012 |
|
RU2615755C2 |
| РЕТИНОИДЫ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ИХ СОДЕРЖАЩАЯ | 1997 |
|
RU2173683C2 |
| КАТАЛИЗАТОР ПОЛИМЕРИЗАЦИИ ОЛЕФИНОВ | 1994 |
|
RU2115663C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЦИТРАЛЯ | 1995 |
|
RU2091364C1 |
| Способ получения цитраля и метилцитраля | 1976 |
|
SU598864A1 |
| СОЕДИНЕНИЯ ДЛЯ КОНТРОЛИРУЕМОГО ВЫСВОБОЖДЕНИЯ АКТИВНЫХ МОЛЕКУЛ | 2002 |
|
RU2296118C2 |
| СПОСОБ ПРОИЗВОДСТВА ДЛИННОЦЕПОЧЕЧНОГО СПИРТА ЦИКЛОГЕКСЕНОНА ВЫСОКОЙ СТЕПЕНИ ОЧИСТКИ | 2017 |
|
RU2745062C2 |
| СПОСОБ ПРОИЗВОДСТВА ДЛИННОЦЕПОЧЕЧНОГО СПИРТА ЦИКЛОГЕКСЕНОНА ВЫСОКОЙ СТЕПЕНИ ОЧИСТКИ | 2017 |
|
RU2729186C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЭТИЛЕНОВЫХ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ | 1972 |
|
SU324739A1 |

ИВ
где Ц о - водород или низший алкил;
О
I где d имеет указанное значение.
Из применяемых для изомеризашТи ка3 , b С и пунктирнъяе связи имсмог указанные значе1П1Я
V,
иг
ОН
таш1заторов общей формулы III наиболее СО целесообразны соединения общей фо|)мулы
et-0
Й Й1 Где KVV имеет указанное значение и представляет собой преимущественно алки или фенилостаток. Характерными представителями соединений формулы JI1A являются окись трис-(триметил-силокси)-ванадия, а также окись трис-(трифенил-силокси)-ванадия. . Металлсодержащие соединения кремния общей формулы III и Ilia можно получить взаимодействием пятиокиси ванадия, например, с триалкил (или трифенил)-силаволом формулы (аякип) St ОН или (фенил) Si ОН с азеотропной отгонкой образующейся во время реакции воды и, например,- бензолом. Каталитическую изомеризацию ацетиленкарбинолов до ненасыщенных оксо .соединений целесообразно вести таким образом, что соответствующий карбинол после добавления 0,1-5 мол. % (предпочтительно 1,5-2 мол.%) катализатора (по отношению к исходному соединению II) на гревают в инертном растворителе. Реакци можно проводить в присутствии или отсут ствии воздуха. В качестве растворителя берут алифатические углеводороды (гепуа, цнклогек- сан, циклододекан, декалин, парафин и парафиновые масла); ароматические углеводороды (например, бензол, нитробензол, толуол или ксилол); галогенированные углеводороды (например, хлорбензол)} простые эфиры (например, анизол, или диоксан) или амины (например, N -метилани- лин). Кроме того, можно применять полимерные кремйийсодержащие растворителисиликоновые масла. Процесс изомеризации можно вести пр комнатной температуре и температуре кипения реакционной смеси. Целесообразно вести процесс при 5О-2ОО°С. При необходимости изомеризацию можно проводить при повыщенном давлении, например SO ата. Время реакции-2- 2О ч Применяемый, катализатор сохраняет в .течение изомеризации активность, в результате чего его можно многократно jjcпользовать. Продукт реакции выделякп- обычными способами, например ректификацией непро- реагировавшего исходного карбинола, кото
о , (ША) рый можно вновь применять для .изомеризации. В условиях предлагаемого способа степень превращения составляет 70-8О% в зависимости от применяемого исходного спирта, выходы достигают более 9О%. По предлагаемому споаобу получены также HOBbie оксосоединения. П р я-М в р 1. Смесь : 15,2 г 3-окси-3,7 -диметил-окта-6-ен-ина (дегидролиналорл), 0,52 г окиси трио-(-триметил-силокси)-ванадия и 750 г жидкого парафина (тч кип. выще 170°С 0,1мм рт. ст.) перемешивают в безводной атмо сфере при 125°С. Образующийся цитраль отде.гшют от непрореагировавщего дегид ролиналоола ректификацией. Степень превращения применяемого дегидролиналоола 11,7 г (77%). Выход цитраля по отнощению к прореагировавшему дегидролиналоолу 11,2 5 г (96%). Пример 2. 15,2 г дегидролиналоола, 2 г окиси трис-трифенилсилоксиванадия и 85 мл высркокипящего пара( 0,885) перефинового масла мешивают прй исключении влаги в течении 3 час 30 мин при 140°С. В реакции обмена участвует 10,5 г (69,2%) дегидролиналоола с образованием 9,3 г цитраля. Выход 88,5% по отношению к прореагировавшему дегидролиналоо.пу. После отгонки всех летучих продуктов ниже ЗО-С/Ю мм рт. ст. можно к раствору катализатора в парафиновом масле добавлять новый дегидролиналоол и подвергать реакции изомеризации согласно описанному методу. После трехкратного применения каталитическая активность этой , системы практически не изменяется и результаты остаются прежними. Пример 3. 15,2 г дегидролиналоола и 0,6 г окиси трис-(диметил-этил-силокси)-ванадия нагревают в 300 мл / силиконового масла в течение 5 час до 130°С. Степень превращения дегидролиналоола составляет 11,3 г, или 74,3%. Выход цитраля по отнощению к примененному дегидролиналоолу 9,7 г (85,8%). | Пример 4. 15,2 дегидролиналоола, 1,06 г окиси бис-(трифенил-силокси)-триметилсилокси-ваиадия, и 150 мл силиконового масла нагревают при перемеш1ша 1ни в атмосфере инертного газа в течение 3 час до 140 С. Степень превращения пр меняемого дегидролиналоола 10,9 г (71,7 Выход 1штраля по отношению к прореагировавшему дегидролиналоолу составляет 9,7 г (89%). Пример 5. 15,2 г дегидрош налоола, 1,5 г окиси бис-(триметилсилокси) трифенилсилокси-ванадия и 150 мл нитробензола нагревают в безводной среде в те чение 2 час до 15О°С. Степень превращения примененного дегидролиналоола 11,1 (73%). Выход цитраля по отношению к прореагировавшему дегидро;шналоолу составляе 9,4 г (84,6%). Пример 6. 15,2 г дегидролинало ола, 1 г окиси бис-(трифенилсилокси)- изо пропокси-ванадия и 90 мл высококипящего параф 1ювого масла ( D pp. 0,885) на гревают при исключении влаги в течение 10 час до 125°С. Степень превращения примененного дигидролиналоола 9,5 г (62,5%). Выход шгтраля по отношению к .прореагировавшему дегидролиналоол} со- ставляет 8,1 г (85,3%). Пример 7. 15,2 г дегидролинало ола, 0,92 г окиси трифенилсилоксибис-(изопропокси)-ванадия и 17О мл силикоаово О масла нагревают при исключении влаги в течение 6 час до 125 С. Степень мреврашешш применяемого дегидро- линалоола 7 г, wi 46%. Выход цитраля 5,75 г, иш1 82,2% (но отношению к прореагировавшему дегидрош1налоолу). Пример 8. 8,4 i- 3-окси-3-метил-бут-1-ина .1 г окиси трис-триметилcиJ oкcи-вaнaдия и 50 мл высококиияшего I riapaiJMHOBoio масла ( J) 0,885) неремеи1ивают при исключен 1и влаги в течег ние 30 час при . Степень превращения применяемого ацегиленкарбинола 5,9 г (70,3%). Выход З-метил-бут-2-ен -1-аля-1 сосчавляет 5,4 г (91,5%). II р и м, е р 9. 22 г З-окси-2,7,11-триметил-додека-6,1О-дие1 -1-ина, 0,7 г окиси трис-триметилсилокси-ванадия и 2ОО мл силиконового масла нагревают в течение 6 час при исключении влаги до 1 ЗО-С. Степень превращения ирименяемо1 ацетиленкарбинола 13,2 г (6О%). Выход 3,7, I 1-триметил-додека-2,6,1О-триен-1I-аля составляет I 1,2 г (84,8%). П р и м е р 10. 29,4 г З-окси-3,7, | 11,15-тетраметил-гесадец-1-ина, 0,7 5 г окиси трис-триметилсилокси-ванс1дия и 50О мл вь сококипящего napacjinнового масла нагревают в течение 8 час щзи исключении влаги до 125 С. Степень превращения применяемого ацетнле1жарбинола 11,3 г(34,8%). Выход 3,7,11,15.-тетраметилгексадец-2-ен-1-аля составляет 9,1 г (80,5%). Пример 11. 18,4 г З-окси-7- -метокси-3,7-диметил/окт- 1-ина (7-ме- токсидегидрояиналоола), 0,7 г окиси трис- -триметилсилокси-ванадия и 150 мл выококипяшего парафиноврго масла перемешивают при исключении влаги в течение 7 час при 125 С. Степень превращеьшя ирименяс,мого ацетиленкарбинола 11,6 г (63%). Выход 7-метокси- : 7-димет1.ц1- окт-2-ен- - 1-аля составляет 10,8 г (93,2%). Пример 12. 12,4 г 1-этинил-1-циклогексанола, 2 г окиси трис.-три(|1е.нилсилокси-ванадия и 1ОО мл высококинящего парафинового масла нагревают и()и исключении влаги до 130 С в течение U ч;1с. Степень превращения применясгмо и ацетиленкарбинола составляет 8,9 г (71,7%). В результате реакции выделены спслующие продукты изомеризации: циклoгoкcиJПl-| ден-ацетальдегид (I) и циклогекс-1-ен-ил-ацетальдегид (П). Общий выход этих продуктов ио отношению к прореагировавшему исходному материалу составляет 7,8 г (87,6%); молярное соотношение образующих альде1Ч1ДО1.) 38,4 :61,6. е р J 3. 13,2 г 3-окси-З- jJeнил-пpoпил-1-ина, 2 г окиси трис-трифенилс1шо1 си-ванадия и J ОО мл CHJHIKOHO- вого масла нагревают ири исключении 1зла- ги до 14О°С в 1-ечение 6 час. Степень превращения применяемого ацети.)1енкарби.нола составляет 12,1 г (91,6%). Выход коричного альдегида 11,4 г (91,3.и).I Пример :14. J2,6 г 2-ОКСИ-2-метил-гепт-3-ина, (7 окиси грис--ч-рим(тилсилокси-ванадия и 15О мл ныс:ококипящего иарафинового масла нагревают ири исключении влаш до J ЗО С в течение 5 час. Стеиень преврашения применяими о ацетиленкарбинолс составляет 1 I ,t) j(92%). Выход 2-метил-гепт-2-ен-1-1.1Нс1 11,0 г (94,8%). Пример 15. 1О г 4-этини.ч--1.-окси- 1,1-этилендиокси-3,5,5-триметилдиклогекс-2-ена, 0,15 г гидрохинона, О,02 мл окиси трис-(триметилсилокси)
Авторы
Даты
1974-09-25—Публикация
1972-05-06—Подача