+ Н-ДНК)..), таким образом, обнаруживает отклонения от монотонности, характер которых зависит от конкретных условий.
Недостатком известного способа обнаружения модифицирующего влияния молекул ДНК на состояние воды является то, что эти модельные нредставления, положенные в его основу, могут быть оспорены. Так, например, можно допустить, что растворитель не испытывает модифицирующего влияния со стороны макромолекул и представляет собой единую фазу, а немонотонная форма кинетики прямого водородного обмена, полученная в эксперименте, целиком является следствием происходящих в молекулах ДНК периодических синфазных в макрообъеме раствора копфармационных изменений, существование которых в настоящее время доказано для некоторых других молекул биополимеров, находящихся в растворимом состоянии.
Цель изобретения - повыщение воспроизводительности результатов способа обнаружения аномалий подвижности растворителя в растворе биополимера, основанного на определении кинетики прямого водородного изотопного обмена между растворителем и растворенными молекулами.
Согласно изобретению, поставленная цель достигается тем, что в исследуемый раствор, состоящий из воды и растворенных в ней молекул ДНК, заранее вводят третий комнонент - низкомолекуляряое по сравнению с ДНК вещество Р-Н, содержащее обменоспособный водород. .При этом количество обменоснособного водорода должно быть много больще, чем количество обменоспособного водорода ДНК (первое условие); скорость его обмена с водородом окружающей воды должна быть соизмерима со скоростью обмена водорода между молекулами самого растворителя, не содержащего растворенных веществ (второе условие).
В такой системе третий компонент выполняет функции опосредственного свидетеля состояния растворителя.
Так, кинетика прямого включения меченого водорода из растворителя в обменоспособиый водород органики будет складываться из двух процессов:
ННЮ -I:;H-ДНК (3)
Н-R(4)
Согласно первому условию, измеряемая в эксперименте кинетика включения изотопа из растворителя в растворимые вещества будет целиком определяться уравнением (4). Если в системе растворитель не подвергается модифицирующему влиянию ДНК и представляет собой единую фазу, то в силу молекулярно-статистической природы водородного обмена будет наблюдаться монотонная кинетика прямого изотопного водородного обмена из растворителя в вещество - свидетель.
Если в системе существуют две фазы растворителя, то равномерно распределенное в
обоих фазах вещество - свидетель будет накапливать изотон в различных условиях. Так, согласно второму условию, задолго до наступления равновесия в реакции (2) произойдет накопление метки в Н-Ri, которое постепенно сменится исчезновением ее до уровня равновесных значений реакции (2) но мере достижения изотопного равновесия в ней. В то же время в аномальной фазе II растворителя включение метки в Н-Rrj будет ocynteствляться монотонно но мере накопления метки в этой фазе.
В результате суммарная кинетика будет немонотонной, однако теперь такое отклоненис невозможно трактовать с позиций конфармационной подвижности молекул ДНК и надежность вывода о наличии именно модифицирующего влияния ДНК на растворитель становится абсолютной.
Способ был реализован с раствором ДНК
(м. 1В. 1 10 дальтон при концентрации 500 мкг/мл. В качестве метки использовался тритий .в виде НТО пр« концентрации 10 мкюри/мл. ВеществОлМ - свидетелем служил цитрат натрия в концентрации 0,04 М. Началом реакции обмена служило соединение 0,01 мл раствора НТО в 0,15 М МаС1иО,04М цитрата натрия и 0,1 мл раствора ДНК в в 0,15 М NaCl и 0,04 М цитрата натрия.
Обмен происходил при комнатной температ)фе, остановка его осуществ.чялась замораживанием образцов при температуре жидкого азота. Лиофилизация осуществлялась в два этапа: при -30°С в течение 6 час, затем при ностепенном подъеме температуры до 45°С в течение 8 час. Измерение образцов производилось на двухканальном жидкостном сцинтилляционном счетчике «Picker-Nuclear со сцинтиллятором обычного
состава (3 г РРО + 0,3 г РОРОР+100 г нафталина на 1 л диоксана) при эффективности 30%.
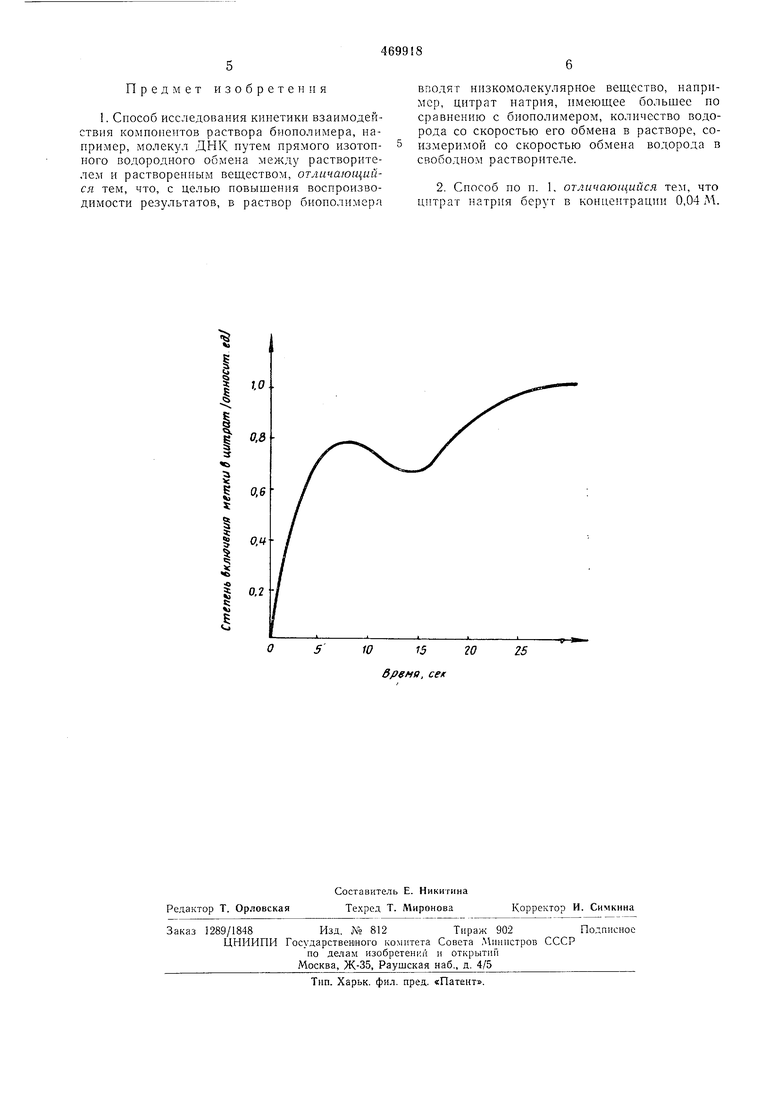
Вид кинетики включения трития в цитрат
натрия показан на чертеже. Форма этой кинетики свидетельствует о наличии в растворе фазы воды с ограниченной способностью к водородному обмену.
Предлагаемый способ может быть полезен не только при обнаружении модифицирующего влияния растворенного биополимера на растворитель. Он может быть использован, например, для обнаружения взаимодействия
биополимера с самим веществом - свидетелем с целью оценки характера этого взаимодействия. В этом случае должна меняться кинетическая характеристика кривой включения метки в Р-Н в присутствии бионолимера.
Предмет изобретения
1. Способ исследования кинетики взаимодействия компонентов раствора биополимера, наиример, молекул ДНК путем прямого изотопного водородного обмена между растворителем и растворенным веществом, отличающийся тем, что, с целью повышения воспроизводимости результатов, в раствор бионолимера
вподят низкомолекулярное вещество, например, цитрат натрия, имеющее большее по сравнению с биополимером, количество водорода со скоростью его обмена в растворе, соизмеримой со скоростью обмена водорода в свободном растворителе.
2. Способ по п. 1, отличающийся тем, что цитрат натрия берут в коьщентрации 0,04 М.




Авторы
Даты
1975-05-05—Публикация
1972-07-12—Подача