изобретение относится к способу попу чения замешенных, бензоилфенипизотиомоч вины обшей ({юрмухЕЬ NH-CQRg N C-NH-COOR i -алкйл С . - С, „, щпслоалкил, 1 1л о содержащий до 8 атомов углерода, алкенил, содержащнй до 12 атомов углерода или аралкип, незамещенный ия}5 замещенный в арильной части одной или несколькими груттамн: алкила и/или алкокснла с С--С. и/или галогена; алкил С|-С.; -водород, алкил C.-C-g, не замещенный или эамещеиньШ галогенцианг. алкоксигруппой с С - Сд, алкоксикарбонипом с С.-С-., фенокси-, галогенфенокси-, X о алкилфенокси- или алкоксифеноксигруппой; цнклоалкил , арил или аралкиЛ, о о незамещенные или замешенные, галоген-алкил - илг алкоксигруппой с С.Сд, 1-фурил или группа - NR R , в которой R - водород ияи алкил , °Д°РЭД апкйл C.,, незамещенный или замешенный гапоген, цкан, алкоксигруппой с ., алкокси- . iН карбонйлом с С -С, ылклоа жип с , аралкил, незамещенный или замешеиньиЧ в арильной части галоген-, низшей алкип- и/илн |низшейалкокснгруппой, фе НИЛ, незамещенный или замещенный гало- ген-, низшей алкил- и/нли низшей алкоксигруппой, ацил, содержащий до 18 атомов углерода, незамещенный или замещенный галоген-, низшей алкокснгруппой, ароил, незамещенный или замещенный галоген-, низшей алкил-, низшей алкоксигруппой, алкнлсульфонил, содержащий до 18 атомов углерода, арилсульфонил, незамещенный или замещенный галоген-, амино-, низшей алкил-, гизшей алкоксигруппой, диалкил аминогруппа, содержащая до 4 атомов углерода, или Р и Р образуют совмест но с атомом азота гетероциклическое кольцо с Сд-С„, которое может содержат другие гетероатомы, например кислород или серу, которые обладают антигельминт ным действием. Получение соединений основано на известном способе ; алкилирования чевины. Однако применение соответствующих исходных веществ позволяет полу1а новые соединения, обладающие . .улучшенными свойствами по сравнению с и; вестными, Предлагаемый способ заключается в том, что тиомочевину общей формулы ( Усо / -нн-соЯр NM CS-COOR где R. и К2. имеют указанные значения, подвергают взаимодействию в щелочн среде в присутствии разбавителя С соед нением обшей формулы , R -У (111) где R имеет ук.азапное значение; У - галоген, арнлсульфоновая или алкилсульфон вая группа, с последующим выделением целевого продукта известными приемами, В качес ве разбавителей в способе могут примеnsiTbCsi вода или органические растворители, такие.как спирт, ацетон, диметилсульфоксид, днметплформамкд или ацето ЛИ их смеси с водой. Ддя создания щелочной средь можно применять любые щелочи. Однако предпо . тнтельнее примепеюю едких кали и нат .ра, карбоната или бикарбоната натрия. Те.мпература реакции от -10 до +4О предпочтительно от О до ЗО°С. При осуиюствлении сг особа, как правило, на 1 моль амидобе зоилфепилтио, мочевины берут 1 моль ашилируюшего средствл (соединения обшей формулы -11 н 1 моль 1ИСДОЧИ. Однако можно приме1шть избыток алкил11 уюшого средства и шелочи. При переработке реакционной смеси ее выливают в воду, отжимают выпавший продукт, суиат и очищают перекристаллизацией. В качестве новых действующих начал ; могут быть названы следующие вещества: N -(2-ацетамидо-5-бензоилфенил) -метоксикарбонил- S -метилизотиомочевина;fij -(2-ацвтамидо 5-бензоилфеннл) М -этоксикарбонил- S -метилчзотиомочевина;N -(2-ацетамидо 5-бензоилфенил)-| |-изо-прСПоксикарбонил- 3 -метил1 эотиомочевш-а;N; -(2 ацетамидо-5-бензоилфенил)-N-втор.-бутоксикарбонил- S -метилизотиомочевина;N -{2-пропионамидо-5-6ензоилфенил)- N -метоксикарбо1гал- -метилизотиомог чевина;.. Н (2-бутирамидо-5-бензоилфенил)-К) -метоксикарбонил- S -метилизотиомочевина;Ь1 -(1-изо-б7ТИрамидо-5-бензоилфвнил)-М -метоксикарбонил- S -метилизотиомочевина;N -(2-валерамидо-5-бензоилфенил)- М -метоксикарбонил- g -метшшзотиомо- чевина, N -{2-изо-валерамидо-5-бензоилфенил)-ы-метоксикарбонил-3 -метилизотиомочевина;N -(2-капронамидо-5-бензоилфенил)- |-метоксикарбонил - мётилизртиомочегi вина; N -(2-изо-капронамидо-5-бензоилфенил)- -метоксикарбонил- 5 -метилизотио- мочевина; N -(2-циклопентанкарбонамидо-5-бенэвн зоилфенил)- -метоксикарбонил- S -метйлизотиомочевина;{Ы {2-.:ЦикЛ гексанкарбонамид1 -5--&е1язоилфенил)- М-метоксикарбонил- $ -метйЙ-г изотиомочевина;1 N -(2-фанилаиотамидо-5-бензоилфенил)-М метоксикарбонил-S -метилизотиомоче-, вина; N -(2-феноксиацетамидо-5-бензоилфенил)| -метокс1жарбонил- S -метилизотиомочевина;N (2-бензамидо-5-бензоилфенил)- -метоксикарбонил- S -метилизотиомочевина;М - 2-{2-метилуреидо)-5-бензоилфенил -. -метоксикарбонил- $ -метилизо- тиомочевина; N - 2-(2-этилуреидо)5-бензоилфенил -f,|-метоксикарбонил-S -метилизотиомочевина;; N (2-бутипуреидо)-5-бензоилфе; нип| - -метоксикарбонип- $ -метилиэо|тиомочев1ша;1 N (2-(0 -цианпентилурвидо)-5|-бвнзоилфеш1пЗ-к-метоксикарбонил-Si-метипиэотиомочевина; N (2- -метоксиэтипурвидо)-5 -бвнзоилфенилЗ - Kl -метоксикарбонил- S 1 -мети/шзотиомочевина; К -{2(2-бензилуреидо)5-бензоилфвнил - ji -метоксикарбонил- S - метилизот . мочевина, ; XJ -t2-{2-фeнилypeидo)-5-бeнзoилфeниJЗ м метоксикарбонил-S -метилизоти ; мочевина; N - 2-ацетамидо-5-бензоилфенил)- N -метоксикарбонил- S -этилизотиомочевина N -(2-ааетамидо-5-бензрилфенил)-J4 -метонсикарбонил- 8 -изопропклизотиомочевина;N -(2-ацетамидо-5-бензоипфенил)-}J -метоксикарбонил- $ -аллилизотиомо чевина; N -(2-ацетамидо-5-бензоилфенил)-} -метоксикарбоиил- § -циклогексилизотиомочевина;N -(2-ацетамидо-5-бенаоилфенил)-fl-метоксикарбонил- $ -бензилизотиомочевина. Пример 1. К 37,1 г (ОД моля IJ -(2-ацетамидо-5-бвнзоилфенил)- N -метоксикарбонил-тиомочевины с т. пл. и 4 г (ОД моля) N аОН в ЗОО мл воды при перемешивании и комнатной температуре прикапывают 12,6 г (ОД моля) диметилсульфата, в течение 3 час смесь перемешивают. Полученную -f2-ацетамидс-5-бензоил-фенил)- { - -метоксикарбонил- S -метилизотиомочеви«у отжимают под вакуумом, повтгорно , растворяют и кристаллизуют из этиловог спирта. Т, пл. 172°С (разложение), выход 31г. Аналогично получают кн-сое M- C-NH-COOCH, .SCHj т. пл. 158° (разложение) МН- со-C-NH-COQCH, (разложение) NH-CO-CgHe C WH-COOCH, I (разложение) ино 5-бензоклфенил)л- -метялизотиомо NH-CO-CH. «C-NH-COO-CoH SCHj (разложение) H-CO-CH, -NH-COO1 SCH, разложение) NH-CO-CH. NH-COO SCH.J (разложение)
NH-CO
N C-NH-COOCH3
SCH т. пл, 14О (разложение)
NH-CO-CH,-CH,
55 :
N-C-NH-COOCsH
I
SCHj
1 60 I. т. ПЛ; 168 (разложсзние)
NH-CO-CH2.CH,
N-C-KH-COOH n I
SCHj ПД. 170 (разложение)
СО ЫН-СО СНг-СН,
/ N-C-NH-COQ -/ SCH,
Ti nn. (разложение) NH-CO-n-CgHy
N-C-NH-COOCgHg 8CH,
T. ПЛ, 155 (разложение)
.
f VcOHf у HH-CO-n-C H
N C-HH-COO- и 8Ш5
т. ПЛ. 151 (разложение) 1
HH-CO n -CjH7
ы-е-ш-соо-- N) SCH,
ir. пп. 142° (разложение)
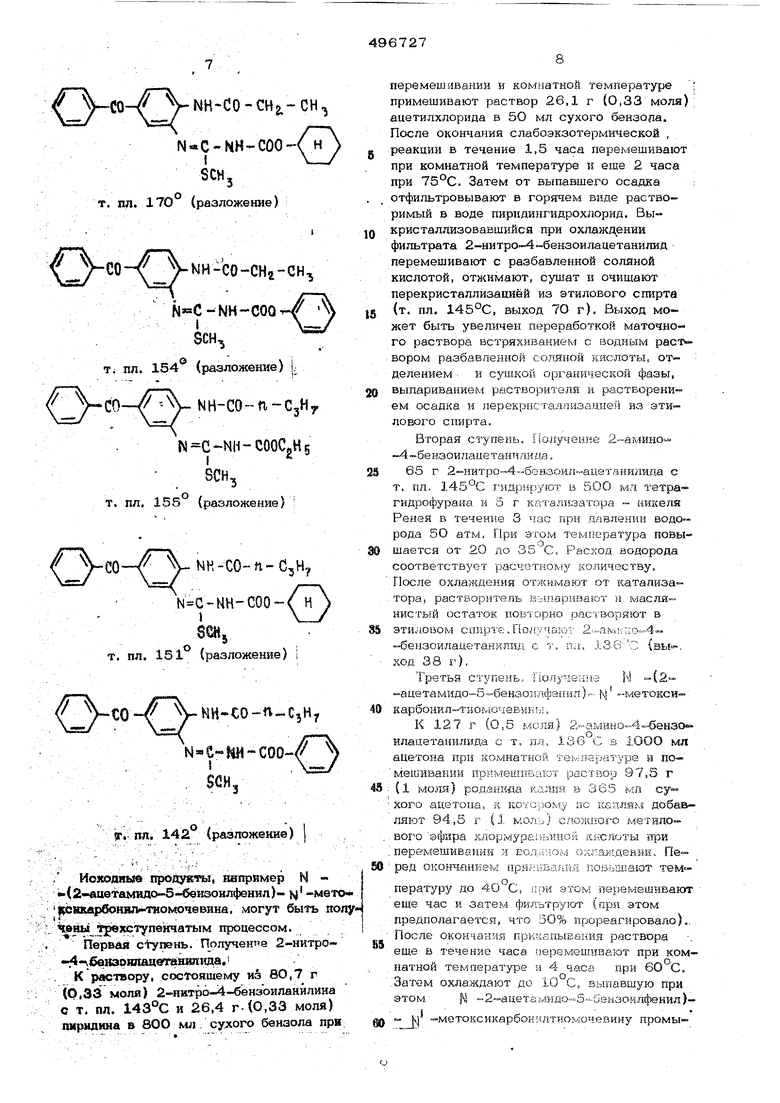
/ Иохоаяые прЬдукты, ниприме :) N (2-аавтамидо-5-бензоилфенил)-- hj -мето 1(СШшрбоиШ1 т11Омочевииа, могут быть иолу1 ; . ,., ,.,, .
,4&нь1 tjtexcTyneH4aTbiM процессом.
Первая с+упень. Получение 2-нитро -4певкзрюшцвтанипида, i
К раствору, сосГояшему из 80,7 г (0,33 моля) 2-иитрЬ--4-бензоиланилина ст. ПЛ. 143°С и 26.4 г-(0,33 моля) юфидина в 8ОО мл cyjcoro бензола при
перемешивании и комнаткой температуре примешивают раствор 26,1 г (0,33 моля) ацетилхлорнда в 5О мл сухого бензола. После окончания слабоэкзотермической ,
. реакции в течение 1,5 часа перемешивают при комнатной температуре и еше 2 часа при 75°С. Затем от выпавшего осадка :
отфильтровывают в горячем виде растворимый в воде пирндингидрохлорид. ВыQ кристаллизовавшийся при охлаждении фильтрата 2-нитро-4-бензоилацетанилид перемешивают с разбавленной соляной : КИСЛОТОЙ, отжимают, сушат и очищают перекристаллизацией из этилового сш1рта (т. ПЛ. 145°С, выход 7О г). Выход может быть увеличен переработкой маточного раствора встряхиванием с водным раст. вором разбавленной соляной кислоты, отделением и сушкой ор1 анической фазы, выпариванием растворителя и растворением осадка н перекристаллизацией из этилового спирта.
Вторая ступень, .лучев,ке 2-аминО -4- -бензоилацетант1лида,
25 65 г 2-нитро™4--6еи.зоип-ацетвнилида с т. ПЛ. 145°С гидриру от в 500 мл тетрагидрофурана и о г каталкзаГора никеля Ренея Б течение 3 гас при давлении водо рода 5О атм. При этом температура повы-
3Q шается от 20 до 35 С, Расход водорода соответствует расчет5- ому количеству. После охлаждения отжимают от катализатора, растворитель Е;:-;.паривают и маслянистый остаток повторно растворяют в
35 этиловом спирте.Г1ол:учаю; 2--ам -;по - 4-. «бензоилацетанилид с т, 136 С {вы«-. ход 38 г).
Третья ступень, Получекие N С2-« -ацетамидо.-5- бензоилфанип) - М -метокси40 карбоиил-тиомочевины.
К 127 г (0,6 моля) 2-амино-- 4--бензо
о илацетанилида ст. пл. 136С в iOOO мл
ацетона при комнатнсш теКЛтаратуре а помешивании пркмешиБают растзор 97,5 г 4S ; (1 моля) роданида калия в 365 мл су- хого ацетона, к кого юму пс каплик добавляют 94,5 г (J. МОЛЬ; сполигого метило- . вого эфира хлормурагйзиной ккспоты при . перемешивании и волкнам охлаждении, Пе°50 рад окончанием при пшаппй пов1 ;шзют теМ
перат фу до 40 С, .п:ри эгоья перемешивают еще час н затем фильтруют (при этом предполагается, что 30% прореагировало).. После окончания прк:;.апь Еания раствора еще в течение часа перемешивают при комнатной температуре и 4 часет при . .Затем охла.ждают до .10 С, вьтавшую при этом|4 -2-ацетаглидо «5---бензоилфенил)-
1-
80 N оксикарбоннлтиомочевину промы Гвают в небольшом количестве ацетона и :сушат (т. пл. 199°С, выход 153 г). Аналогично могут быть получены другие применяемые исходныеN -(2-ациламино 5-бенэЬилфенил)- -апкокс Карбонил-тиомочевины формулы П. Ф о р м у л а из обретения Способ получения замещенных бензоип энилиэотиомочевины общей формулы HH-CO-Rj N e-NH-COOR Я - апкип , цикноалкил X J, содержащий до 8 атомов углерода, алкерил, содержащий до 12 атомоа углерода |или аралкил, незамешенный или аамещен|ный в арильной части одной или несколь™ кими группами алкила . и-или алкоксила с С.,Сд и/или галогена; R. - алкил .; 1 - водород, алкил С.. неза мещенный или замещенный галогенциан-, влкоксигруппой с алкоксикарбони |лом с С„-Ср,, фенокси-, галогенфеноксИ алкилфенокси-, илм алкоксифеноксиг-руппой |цшслоалк Ш Cf.,-Co арил или аралкил, не 1аамещенные или замещенные галоген-, |алкил- - или айкоксигруппой с С.,-Сд, 1-фурил или группа - NR R 16 которой R - водород или алкил ш - водород, алкил , |незамещенный или замещенный галоген-., I циан-, алкоксигруппой с , алкоксикарбонилом с Cp-Cg, циклоалкил , |аралкил, незамещённый или замещенный в 1арильной части |галогён-, низа-ей алкил: и/или низщей алкоксигруппой, фенил, незамещенный или замещенный галоген-, низшей алкил и/или низшей алкоксигруппой, ацил, содержащий до 18 атомов углерода, незамещенный или замещенный галоген, низшей алкоксигруппой, ароил, незамещенный или замещенный галоген-, низщей алкил-, низшей алкоксигруппой, алкилсульфонил, .содержащий до 18 атомов углерода арилсульфонип, незамещенный или заме цен1а1й галоген-, амнно-, низщей алкил-, низшей а жоксигруппой, диалкиламиногруппа, содержащая до 4 атомов углерода, или R и R образуют совместно с атомом азота гетвродиклргческое кольцо с , которое может содерлсать другие гетеро- атомь, например кислород или серу, о т.;л и чающийся тем, что тиомочевш1у общей формулы (Vco-f VMH-coR, «-w«/ Л :; Х NH- CS- NH-COOR где R. и R, « ,. имеют указанные значения, подвергают взаимодействию в щелочной среде в гфнс тствии разбавителя с соединением общей где К имеет указанное значение, У галоген, арилсульфоновая или алкилсульфоиовая группа, с последующим вьщелением целевого продукта известными приемами.



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения замещенных бензоилфенилгуанидина | 1974 |
|
SU498903A3 |
| ПРОИЗВОДНЫЕ СУЛЬФОНИЛАМИНОКАРБОНИЛТРИАЗОЛИНОНА И ИХ СОЛИ, ИСХОДНЫЕ СОЕДИНЕНИЯ ДЛЯ ИХ ПОЛУЧЕНИЯ И ГЕРБИЦИДНОЕ СРЕДСТВО НА ИХ ОСНОВЕ | 1993 |
|
RU2125559C1 |
| Способ получения производных амидофенилизотиомочевины | 1973 |
|
SU490285A3 |
| ХЛОРИДЫ ХЛОРПИРИДИНИЯ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1995 |
|
RU2138481C1 |
| Способ получения 1-этилимидазолов | 1973 |
|
SU501671A3 |
| ПРОИЗВОДНЫЕ БИФЕНИЛПИРИДОНА И ИХ СОЛИ | 1992 |
|
RU2100350C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ФЕНИЛИМИДАЗОЛИЛАЛКАНОВ | 1971 |
|
SU415875A3 |
| ПРОИЗВОДНЫЕ ДИГИДРОПИРИДИНА, СМЕСЬ ИХ ИЗОМЕРОВ, ИНДИВИДУАЛЬНЫЕ ИЗОМЕРЫ ИЛИ ИХ ФИЗИОЛОГИЧЕСКИ ПЕРЕНОСИМЫЕ СОЛИ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1992 |
|
RU2081872C1 |
| ПРОИЗВОДНЫЕ ЦИКЛОАЛКАНО-ИНДОЛА И АЗАИНДОЛА, СМЕСЬ ИХ ИЗОМЕРОВ ИЛИ ОТДЕЛЬНЫЕ ИЗОМЕРЫ И ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, ПРОИЗВОДНЫЕ КАРБОНОВОЙ КИСЛОТЫ В КАЧЕСТВЕ ИСХОДНЫХ СОЕДИНЕНИЙ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ИНГИБИРУЮЩАЯ ВЫСВОБОЖДЕНИЕ АССОЦИИРОВАННЫХ С АПОЛИПОПРОТЕИНОМ В-100 ЛИПОПРОТЕИНОВ | 1995 |
|
RU2157803C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1,2.4^ТРИАЗИН-5-ОНОВ | 1972 |
|
SU433681A3 |


Авторы
Даты
1975-12-25—Публикация
1974-01-23—Подача