,1
Изобретение относится к способу получения новых соединений, которые могут найти применение в медицине.
Известен способ получения производных ряда имидазола замещением по N-водородному атому соответствующих имидазолов, однако способ получения предлагаемых соединений, обладающих высокой биологической активностью, не известен.
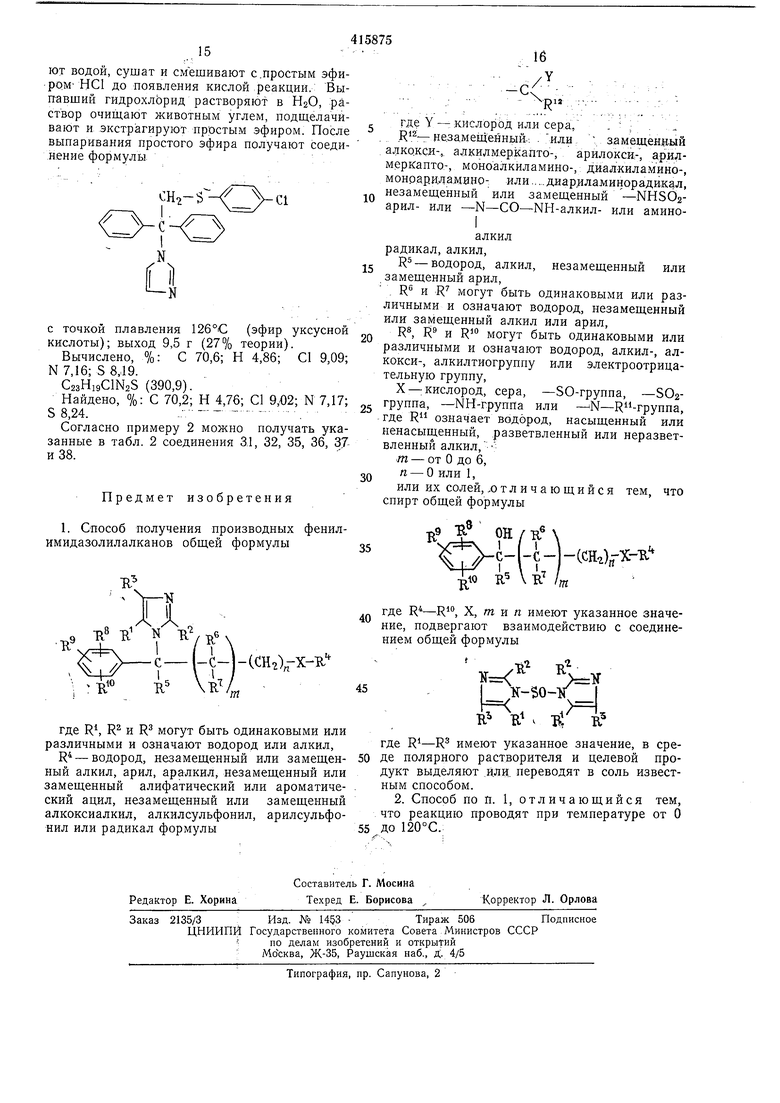
Предлагается способ получения производных фенилимидазолилалканов общей формулы
R
И
, 1R«ll N
,,.-С- Ц- -(CH,)-X-R Б К VtfA
где R, R и R могут быть одинаковыми или различными и означают водород или алкил,
R4 - водород, незамещенный или замещенный алкил, арил, аралкил, незамещенный или замещенный алифатический или ароматический ацил, незамещенный или замещенный
алкоксиалкил, алкилсульфонил, арилсульфонил или радикал формулы
.У
С Н
где Y - кислород или сера,
R12 - незамещенный или замещенный алКОКСИ-, алкилмеркапто-, арилокси-, арилмеркапто-, моноалкиламино-, диалкиламино-, моноариламино- или диариламинорадикал, незамещенный или замещенный - НН5О2-арилили -N-СО-NH-алкил- или аминорадикал, I
алкил алкил,
R5- водород, алкил, незамещенный или замещенный арил,
R и R могут быть одинаковыми или различными и означают водород, незамещенный или замещенный алкил или арил,
R, R и R° могут быть одинаковыми или различными и означают водород, алкил-, алКОКСИ-, алкилтиогруппу или электроотрицательную группу,
X -кислород, сера, -SO-rpynna, -SOzгруппа, -NH-группа или -NR -rpynna, где
R означает водород, насыщенный или ненасыщенный, разветвленный или неразветвленный алкил,
т - от О до 6,
п - О или 1,
или их солей, который заключается в том, что спирт общей формулы
Г/Г ,
--9- (сшьх-и
к
т
где R - R°, X, m и n имеет указанное значение,
подвергают взаимодействию с соединением общей формулы
nl-ni
4
L K-so-i(
I
RV -к
RV-K Б те
где имеют указанное значение, в среде полярного растворителя и целевой продукт выделяют или переводят в соль известным способом.
Алкильные радикалы R, R и R предпочтительно содержат от одного до четырех атомов углерода, в особенности один атом углерода. Особенно желательно, чтобы R R и W обозначали водород. Алкильные алкокси- и алкилмеркаптогруппы R, R и R предпочтительно содержат один-четыре, в особенности один атом углерода. Алкильные группы R®, R и R или алкильные компоненты радикалов R R и R могут быть неразветвленными или разветвленными и содержать двойную или тройную связь. Электроотрицательными заместителями R, R и R могут быть галогены, т. е. фтор, хлор, бром и йод, предпочтительно хлор и бром, нитро- и тригалогенметильная группы, предпочтительно группа CFj и CN-rpynпа, а также SO-алкильная: и 502-алкильная группы, причем алкильпые компоненты этих групп состоят из одного - шести атомов углерода, предпочтительно из одного - четырех атомов углерода и могут быть неразветвленными или разветвленными, насыщенными или ненасыщенными. В качестве особенно предпочитаемых заместителей R, R и применяют водород, хлор и бром.
Замещенные в случае надобности арильные радикалы R предпочтительно содержат от щести до десяти атомов углерода и могут быть замещены одним или несколькими, предпочтительно одним или двумя, указанными при R, R и R° одинаковыми или различными радикалами. В качестве предпочитаемого ароматического радикала R используют замещенный хлором или бромом фенильный радикал, в особенности незамещенный фенильный радикал.
Алкильные радикалы R являются неразветвленными или разветвленными и предпочтительно содержат один - восемь, в особенности один - четыре атома углерода. Алкильные радикалы R и R могут быть неразветвленными или разветвленными, насыщенными или ненасыщенными и содержат один - восемь предпочтительно один - пять, в особенности один - четыре атома углерода.
Арильные радикалы R и R предпочтительно содержат от щести до десяти атомов углеро да. Алкильные и арильные радикалы R ц R могут содержать один или несколько, предпочтительно один или два, указанных при
R8, W и Ri° радикалов.
Алкильные радикалы R могут быть неразветвленными или разветвленными, насыщенными или ненасыщенными и содержат от одного до десяти, предпочтительно один-щесть,
в особенности один - четыре атома углерода, а также замещены одним или несколькими, предпочтительно одним или двумя, указанными в качестве R®, R и R радикалами. Алкильный компонент аралкильных радикалов R предпочтительно содержит от одного до четырех атомов углерода.
Замещенные в случае надобности арильные радикалы R, а также арильные компоненты аралкильных групп R предпочтительно содержат от щести до десяти атомов углерода и могут быть замещены одним или несколькими, предпочтительно одним или двумя одинаковыми или различными, указанными в качестве R, R® и R радикалами. В качестве
предпочитаемого арильного радикала R применяют замещенный в случае надобности атомом хлора, брома или фтора или нитрогруппой фенильный радикал. Алифатические ациловые радикалы R могут быть неразветвленными или разветвленными, насыщенными или ненасыщенными и содержат от одного до восьми, предпочтительно от одного до шести, в особенности от одного до пяти атомов углерода. Кроме того, алифатические ациловые радикалы могут быть однократно или многократно замещены, предпочтительно однократно или двукратно, галогеном, предпочтительно фтором, хлором или бромом, в особенности хлором или бромом
или фенильными группами.
Замещенные в случае надобности ароматические ациловые радикалы R предпочтительно содержат от щести до десяти атомов углерода в арильной части и могут быть замещены одним или несколькими, предпочтительно одним - тремя одинаковыми или различными, указанными как R, R и R° радикалами. В качестве предпочитаемого ароматического
ацилового радикала R используют фенилациловый радикал, замещенный одним или несколькими, предпочтительно одним - тремя атомами хлора, брома, фтора, метилом, метокси- и/или нитрогруппами, фенилациловый
или нафтилациловый радикал,
Алкоксиалкильные и алкилсульфонильные радикалы R могут быть неразветвленными или разветвленными, насыщенными или ненасыщенными, содержат от одного до восьми, предпочтительно от одного до шести, в особенности от одного до четырех атомов углерода и могут содержать один или несколько, предпочтительно один или два одинаковых или различных, указанных как R, R и R°, радикалов.
Замещенные в случае надобности арилсульфониловые радикалы R содержат от шести до десяти атомов углерода в ариловой части и могут быть замещены одним или несколькими, предпочтительно одним или двумя одинаковыми или различными, указанными как R, R и R радикалами. В качестве предпочитаемого арилсульфонилового радикала используют фенилсульфониловый радикал, в особенности незамещенный или замещенный атомом хлора или брома фенилсульфониловый радикал. Алкокси-, алкилмеркапто-, моноалкиламино- и диалкиламино - группы R предпочтительно содержат от одного до четырех, в особенности один или два атома углерода в каждом алкильном компоненте, причем алкильная часть может быть неразветвленной или разветвленной, насыщенной или ненасыщенной и замещена одним или несколькими, указанными как R R и R°, радикалами. Кроме того, алкильная группа моноалкиламинорадикала R может быть замещена в особенности -СОО-алкилгруппой, причем алкил предпочтительно состоит из одного - четырех, в особенности одного или двух атомов углерода.
Замещенные в случае надобности арилокси-, арилмеркаито- и моно- и диариламинорадикалы R а также арильная часть группировки -ЫН5О2-арил содержат шесть или десять, предпочтительно шесть атомов углерода на арильную часть и могут быть замещены одним или несколькими, предпочтительно одним или двумя, указанными как R, R и R, радикалами. В качестве предпочитаемого арильного компонента используют фенильный радикал, в особенности незамещенный или замещенный одним или двумя атомами хлора или брома или метильной группой, фениловый радикал.
В радикале R, т. е. -N-СО-NH-алкил,
i
алкил
обе алкильные группы могут быть одинаковыми или различными и содержать предпочтительно один - четыре, в особенности один или два атома углерода.
Алкильные радикалы . могут быть неравветвленными или разветвленными, насыщенными или ненасыщенными и содержать предпочтительно один - четыре, в особенности один или два атома углерода.
В качестве солей целевых соединений предпочтительны соли с физиологически переносимыми кислотами. Примерами таких кислот
являются галогенводородные кислоты, как например хлорводородная, бромводородная кислота, фосфорные, моно- и бифункциональные карбоновые кислоты и оксикарбоновые кислоты, как например уксусная, малеиновая, янтарная, фумароновая, винная, лимонная, салициловая, сорбиновая, молочная кислоты и 1,5-нафталиндисульфоновая кислота.
В качестве подходящих растворителей можно применять ароматические растворители, как бензол, толуол, низшие диалкиловые эфиры, например диэтиловый эфир, хлорированные углеводороды, например метиленхлорид, хлороформ и тетрахлоруглерод, и низшие алкилнитрилы, например ацетонитрил.
Реакцию обычно проводят при температурах приблизительно от О до 120°С, предпочтительно приблизительно при 20-80°С. Требуемые для получения новых соединений исходные соединения известны или их можно получать известными способами.
Пример 1. 52,5 г (0,2 моль) фенил-4хлорфенилтиометилкетона (получен из 4-хлортиофенола и «-хлорацетофенона) в 400 мл абсолютного простого эфира и 100 мл бензола прикапывают в раствор Гриньяра из 5 г магния и 38,8 г бромбензола в 200 мл абсолютного простогоо эфира. После окончания экзотермической реакции отделяют небольшое количество остатка и затем отгоняют в вакууме с помощью простого эфира. Остаток смешивают с ледяной водой и разбавленной серной кислотой и извлекают метиленхлоридом. После промывки водой сушат и растворитель отгопяют в вакууме. При регенерировании остатка абсолютным простым эфиром получают еше немного исходного продукта с т. пл. 80°С, который отсасывают. Фильтрат отгоняют в вакууме. Полученное таким -образом
соединение формулы
Л-С1
45
имеет т. пл. 55°С (лигроин); выход 30 г (44% теории). Рассчитано, %: С1 10,42.
CsoHiyClOS (мол. вес. 340,5) Найдено, %: С1 11,15.
В табл. 1-7 (в конце описания) приведены предлагаемые соединения.
Аналогично получают исходные спирты для описанных в табл. 2 соединений 31, 32, 35, 36, 37 и 38, а также остальные применяемые согласно изобретению спирты этого типа. Соединение Т. пл. .пригменяемогл в . 2честве исходного сбединения спирта, °С 3288
35107
3651 38 99
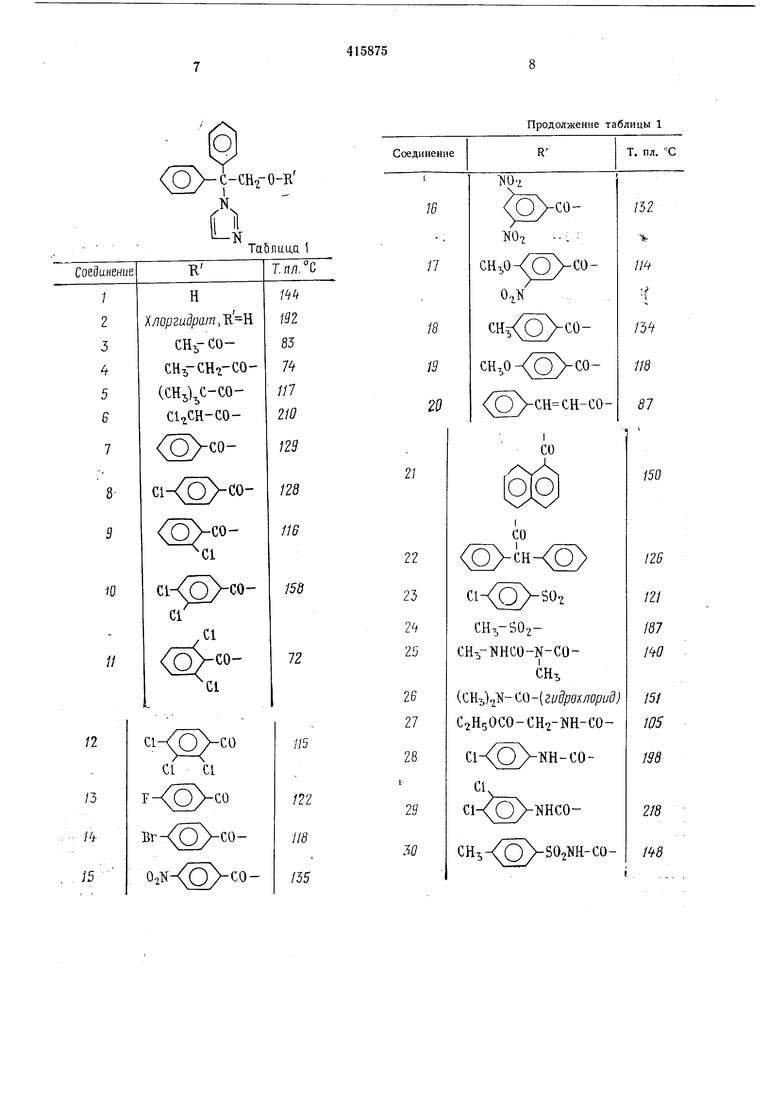
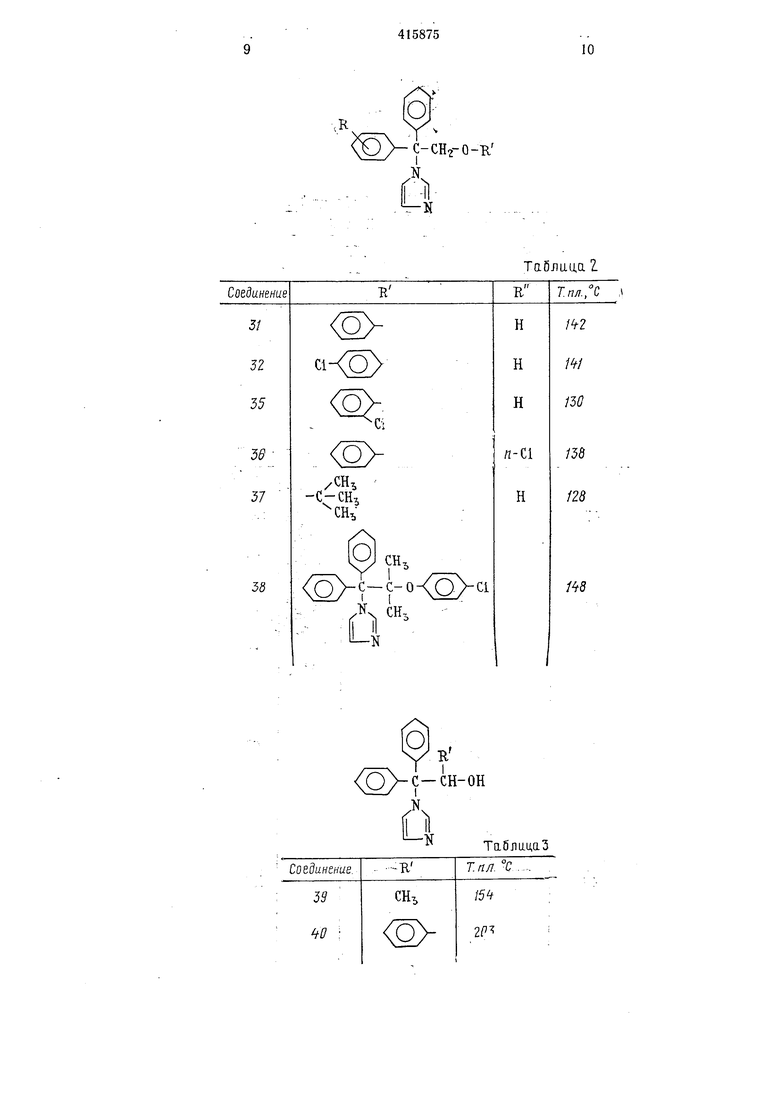
O -c-cH,-o-R
Таблица
Продолжение таблицы 1



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 1,3,3-тризамещенных 3-азолилпропинов | 1971 |
|
SU447887A1 |
| СПОСОБ ПОЛУЧЕНИЯ 1,3,3-ТРЕХЗАМЕ1ЦЕННЫХ 3-АЗОЛИЛПРОПИНОВ | 1971 |
|
SU430551A1 |
| Способ получения 1-этилимидазолов | 1973 |
|
SU501671A3 |
| СПОСОБ РАЦЕМОСЕЛЕКТИВНОГО СИНТЕЗА АНСА-МЕТАЛЛОЦЕНОВ | 2005 |
|
RU2391350C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМБИНАЦИЯ ОПИОИДА И ПРОСТАГЛАНДИНОВОГО СОЕДИНЕНИЯ | 2008 |
|
RU2488398C2 |
| СПОСОБ ПОЛУЧЕНИЯ 3-ГАЛОГЕНАЛКИЛ-1Н-ПИРАЗОЛОВ | 1996 |
|
RU2169143C2 |
| МЕЗО-СЕЛЕКТИВНЫЙ СИНТЕЗ АНСА-МЕТАЛЛОЦЕНОВ | 2004 |
|
RU2362782C2 |
| Способ получения производных бензиламина | 1974 |
|
SU532338A3 |
| ПОЛИЭТИЛЕН ДЛЯ ЛИТЬЕВОГО ФОРМОВАНИЯ | 2005 |
|
RU2395527C2 |
| ДИКЕТОН В КАЧЕСТВЕ ПРОМЕЖУТОЧНОГО ПРОДУКТА ПРИ ПОЛУЧЕНИИ 3-ГАЛОГЕН-1Н-ПИРАЗОЛОВ | 1996 |
|
RU2251543C2 |

115
122
118
/35
2/
/50
I СО
:ovtHчР
126
С1ЧО
-so
Ш
CH,,-S02187CH.,-NHCO-K-CO1 0
СНь
(CHj,)- (-(гидроклорид)
151 С Н50СО-СН2-Ш-СО105
ci Oy H-coт т
ci oyNHcoсНь- Ол- 02Ш-со- т
.R,
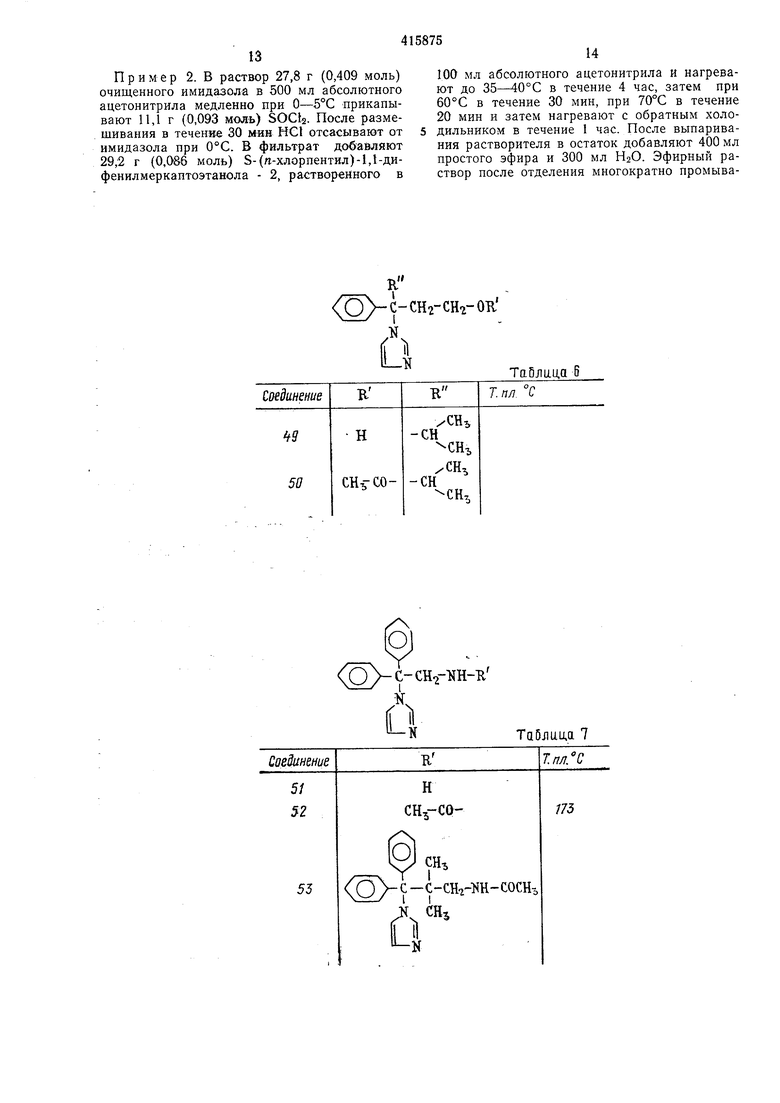
C-CH2-0-K
(t
.L-N
Таблица Z
PJ r S/ U
I O/-C-CHCriy I
u
-K
О
К
C-GH20I
.N,
П
ССНгСНгОК
Таблица 4
Таблица 5 пример 2. В раствор 27,8 г (0,409 моль) очищенного имидазола в 500 мл абсолютного ацетонитрила медленно при О-5°С прикапывают 11,1 г (0,093 моль) SOC12. После размешивания в течение 30 мин НС1 отсасывают от имидазола при 0°С. В фильтрат добавляют 29,2 г (0,086 моль) 5-(«-хлорпентил)-1,1-дифенилмеркаптоэтанола - 2, растворенного в
C-CH2-CH2-OU
(
L-N
Таблица S
O C-CH - NH-U
1
TaDjiuu, 7 100 мл абсолютного ацетонитрила и нагревают до 35-40°С в течение 4 час, затем при 60°С в течение 30 мин, при 70°С в течение 20 мин и затем нагревают с обратным холодильником в течение 1 час. После выпаривания растворителя в остаток добавляют 400 мл простого эфира и 300 мл HjO. Эфирный раствор после отделения многократно промыва
Даты
1974-02-15—Публикация
1971-08-19—Подача