(54, СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 1-ФТАЛАЗОНА





| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных 1-фталазона | 1973 |
|
SU610489A3 |
| ПРОИЗВОДНОЕ ДИГИДРОПИРИДАЗИН-3,5-ДИОНА | 2014 |
|
RU2662832C2 |
| Способ получения двухядерных гетероциклических/диглицидиловых соединений | 1971 |
|
SU468420A3 |
| ПРОИЗВОДНЫЕ 6-АМИНОХИНАЗОЛИНА ИЛИ 3-ЦИАНОХИНОЛИНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРА РЕЦЕПТОРНЫХ ТИРОЗИНКИНАЗ EGFR ИЛИ HER-2 | 2010 |
|
RU2536102C2 |
| ПРОИЗВОДНЫЕ ДОЛАСТАТИНА 15 | 1998 |
|
RU2195462C2 |
| ПРОИЗВОДНЫЕ АМИНОМЕТИЛПИРРОЛИДИНА, ИМЕЮЩИЕ АРОМАТИЧЕСКИЕ ЗАМЕСТИТЕЛИ | 2000 |
|
RU2255938C2 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ, ВКЛЮЧАЮЩАЯ ИНГИБИТОРЫ SGLT И ИНГИБИТОРЫ DPP4 | 2009 |
|
RU2481106C2 |
| СПОСОБ ПОЛУЧЕНИЯ ИНГИБИТОРА ФАКТОРА СВЕРТЫВАНИЯ КРОВИ XIA И ЕГО ИНТЕРМЕДИАТА | 2019 |
|
RU2779013C2 |
| ПРОИЗВОДНОЕ ПИРИМИДИН-4,6-ДИАМИНА, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ЕГО ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2022 |
|
RU2834353C2 |
| ПРЕДШЕСТВЕННИКИ АНТИАРИТМИЧЕСКИХ СОЕДИНЕНИЙ, СПОСОБЫ СИНТЕЗА И СПОСОБЫ ПРИМЕНЕНИЯ | 2006 |
|
RU2422447C2 |

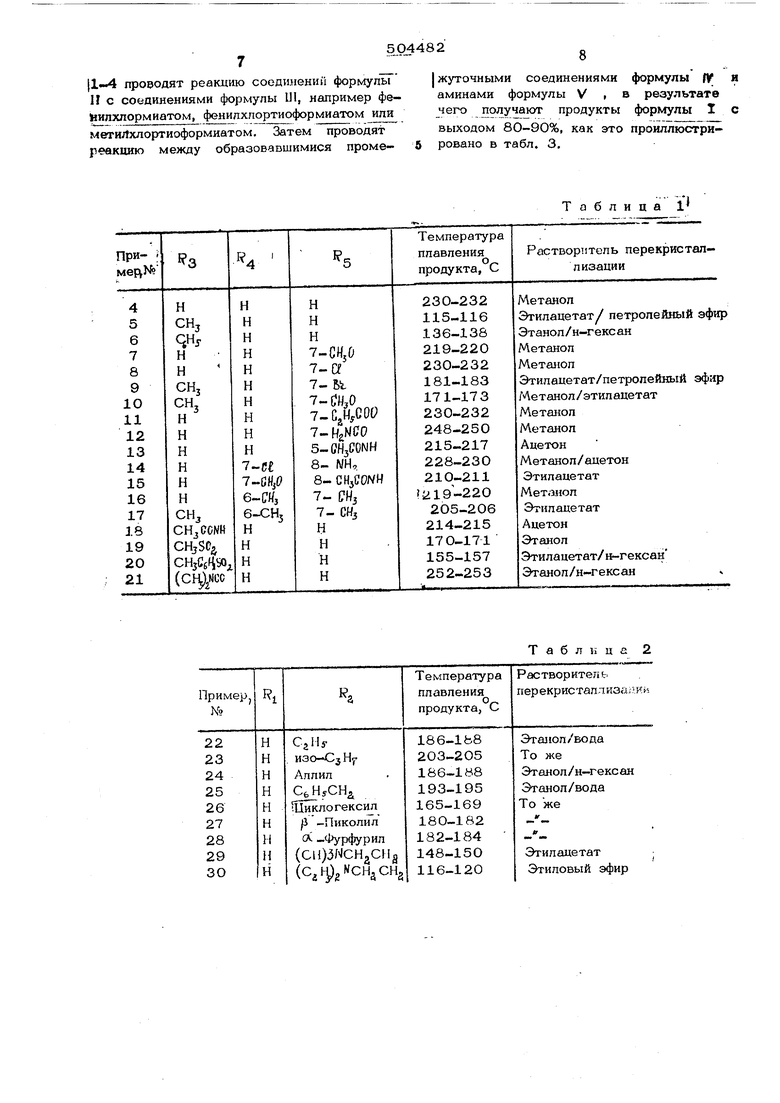
Т1эобрётёнйе относится к способу по- 1пучения новых соединений - производных il - фтапазона формулы CH iOCNI iRj, где RI -атом водорода или алкип, содержащий 1-6 углеродных атомов, в осо- (бенности апкип, содержащий 1-3 угперод ных атома; Р, - атом водорода, апкип нераэветвпенный или разветвленный, причем 1в соот ветствии с предпочтительным вариантом этот алкип содержит 1-6 углеродных ат МОЕ, циклоалкил, алкенил, причем согласно л рёдпочтитёлКному варианту этот аякелил содержит 2-5 углеродных атомов, в особенности апкенил, содержащий 2 - 4 угперод1ых атома, арил, 1предп6чтитеЪыю фенип или топил, арапкил, причем в соответствии с предпочтительным вариантом - бензил или фенетил, диалкиламшюалкип, предпочтительно диалкил, содержащий 15 углеродных атомов, аминоалкил, последний алкильный радикал которого содержит 1 или 2 углеродных атома, фурфурильная (Группа, пиколильная или пиридипьная группа;R, - атом водорода, алкил, предпо«1тительп но алкил, содержащий 1 - 6 углеродных laTOMOB, в особенности алкил с 1 - 3 угле {родными атомами, арил, предпочтительно фенил или толил, карбамоильная группа, N -алкилкарЪамоильная группа, предпочтительно N -алкил (PI - Cjj) карбамоиль- ная группа, N , N -диалкилкарбамоильная группа, предпочтительно N , Л/ -диал;кил ( Ct-j ) карбамоильная группа, ал- килсульфонильная группа, предпочтительно алкил ( CI-У ) сульфонильная группа, в особенности алкил ( Cj, ) сульфонильная группа, или арилсульфонильная группа, ар почтительно фолнльлая или толилсупьфопнль лая группа: атом водорода, атом галогена, например хлора, брома, йода или фтора, предпочтительно хлора или брома, алкил, пред- почтительно алкил с J.-6 углеродными атомами, в особенности алкип с 1-3 углеродными атомами, или алкоксил, предпочтитель но апкоксш, содержащий 1-4 углеродных атома j 13 -атом водорода, атом галогена, наприм . хпора, брома, йода или фтора, предпочтител хлора или брома, алкил, предпочтительно ал l-S в особенности алкил C-f.j , алкоксил, Предпочтительно алкоксил С1-4, аминогруппа адиламиногруппа, предпочтительно ацила- миногруппа Cj.j ., алкоксикарбонильная группа, предпочтительно алкокси C.j, карбонильная группаили .карбамоильная группа; R и Rj могут совместно означать двухвалентный алкиденовый остаток, содер жащий или. несодержащий гетероатом, пред почтительно атом кислорода или азота (по мимо атома азота группы, которая отвечает обшей формуле WRi j) Эти соединения обладают физиологической активностью и могут быть использованы в качестве лекарственных препаратов. Способ получения производных формулы 11 основан на известной реакции карбамилгалогенидов с аммиаком или аминами и заключается в том, что соединения формулыгде , Rj . R имеют у азанш ю значения, подвергают взаимодействию с соединениями формулы И А-С-Сг где А-aixiM хлора или алкоксил, арилок сил, а;1килтио-или артилтиогруппа, с последующим проведением взанмодей- ствия образующегося соединения формулы CHgOC-A где 1 , 1 и Ру и Л имеют указанные начения, с амиаком или амином формулы У где. и j имеют указанные значения. . При необходимости промежуточное соединение формулы IV можно выделить и очистить. Поскольку промежуточное соединение фор.мулы , W . .где А - атом хлора, является неустойчивым и его трудно оаис- тить, то процесс предпочтительно проводить в одну стадию без выделениями очистки промежуточного соединения W. Однако в том случае, когда в формуле 1М А означает радикал, отличный от атома хлора, промежуточное соединение устойчивое и легко подвергается очистке. По предлагаемому способу проводят вза- имодействие между соединением формулы 11 растворенным или суспендированным в инертном растворителе7 и эквимолярным количеством или избытком, который мо- / жет изменяться, в частности, от 1,0 до 3 молей, соединения формулы 111 в присутствии или в отсучх твии дегидрохлори- руюшего агента. В качестве примеров таких растворителей или разбавителей можно привести бензол, толуол, ксилол, эти- |ловый эфир, диоксан, хлороформ, дихлор- этан и пиридин или их смеси, В предпочтительном варианте в качестве дегидрохлорирующего аге)та или катализатора в реакционную смесь добавляютсяаминьТ; такие как диметиллнип- ; этиланилин, триэтиламин, N -алгостлигт рцдин или пиридин. В предпочтитольнок воГианте первая стадия осуществляется Б диапазоне температур от -1О до +50 С и обычно протека ет з течение 1-25 до полного завер- шоиия реакции. В качестве примеров соединений формулы 111 можно назвать фосген, алкилхлорформиаты,, такие как метил или эт1шхлор4юрмиат, арилхлорформиаты, такие как фе11илхлор(1хэрмиат, алкилхлортиоформи- аты, такие как метил этилхлортиофор- миат, и арилхлортиоформиаты,. такие как фенилхлортио(}юрмиат. Предпочтительным арилхлорформиатом является фенилхлор- формиат, поскольку- он дешев и легко дос« тупет1. Фенил может быть замёщеЛньГм или незамещенным, например п-хлорфенильная, п.ромфенильная и гг-}1итрофенильная группа, а также ел - и р -«афтилькая группы, В качестве примеров соединений формулы W -ложно привести 4-метоксикарбони- локсиметил-1- пчитаоон; 4-4 нокснкарбони / поксиметигйчХ-фталазоН;, 4( п «.кпорфенок сикарбонилоксиметип)i canaaoH, 4.мет4а-1 тиокарбонипоксимети;|5-1а.« фталазон, 4..iMei ffii тиокарбонипоксиметип-1« фталазон и 4Ц)8« нилтиокарбонипоксиметил- фталааон« Предйочтительными являются производные 4™ -феноксикарбонилоксиметил«А«4 тапазона. Вторая стадия обычно осуществляете я при С, и реакция протекает до полного завершения за нескодько часов. Аммиак или аминформулы V может быть иопользован в избыточном количестве, и обы но достаточно бывает избытка от 1 до 10 молей шлина на 1 моль соединений фор« I мулы W . В качестве примеров аминов формут.1 М можно привести такие первич«« (ные амины, как метип этил нропил,- , изопропил-j, бутил , аплил«« цшшо««Теюгил-, бензил-f р .-диметипаминоэтил, -диэтиламинопропил, пигалил и фурфу риламин, и такие вторищтые амины, как ди« метиламин, диэтиламин, пирропаднн, пипери дин, N -«метилпиперазин к яйн. Кро. Еь ароматически ме того, могкножспольаоб :;:,),, ггапример я 1рвичные и вторичные ei опуидин и 3 амшюпир1и: ., ал):идин. . Когда А - атом хлор , горая стадия i&ro же самого ;;уычно протекает в cpsAt ,„. При проведе лзтворителя, что и riepi VSKH второй стадии в кач тве то. р|Е гующего агента может быть испомь. /;ан избыток реагирующего формулы У„ ) Отнако в т-ом спучае, когда А ке ; ,,ла. чает а:том хлораг вторая мйглет .-.ыт осуществлена в присутствии или отсутствии растворителя и в присутствии дехидрохлори руюшего/агента.1 Предпочтительными раатво рителями для осуществления второй стадии являются метан6л, -гтаноп и лропанол. Ко-, вечный продукт можно вьщелить и очистить в соответствии с обычными способами. Пример 1. 4 Феноксикарбонигаок- .симетил-1 4 талазон, К раствору 5 г 4.ксиметиП-1- фтала аона мл пиридина добавляют 6 г фенилхлорформиата при охлаждении. Оставляют на ночь при комнатной температуре. Реакдионную смесь упаривают при пониженном давлении и разбавляют водой. Осадок фильт руют и кристаллизуют из зфира, .6 )еноксикарбонилоксиметил- 1-фталазона с т.пд. 113-114с. 4 -Карбамоксиметим-1 |}тала;5ои. К раствору б г 4)онок.сикарбонилокси- меткп.-1- алаэоиа, описанному в вышеприведенном примере, Б 1ОО мн метилового спирта добавляют 2 г аммиака при комнатн температуре. Оставляют на ночь, а затем упаривают, остаток кристаллизуют из мети- лового спирта, получая 3,1 г 4-«:арбамоксиметил.1-фталазона с т..цл. С.. - Вычислено,%; €-54,79; Н-4Д4; -19,17, Найдено,%: С-55,03; Н-4,20; N-19,30 Пример 2. 4- N чиетилкарбамо1&симетш1|-7- етокси 2- детш1-1-фгалазон. , К перемешиваемой смеси 4 мл ЗО%-ного водного раствора монометиламина и 5О мл I метилового спирта, добавляют 2 г 4-фенок. сикарбонилоксиметил-7- четокси-2- летил и . -фталазона, полученного по примеру 1. 05,; ле этого реакционную смесь оставляют на ночь с. последующим упариванием раствори- теля. Остаток экстрагируют.,хпороформолл; и хлорофорь/шый экстракт промывают последовательно 59о-«ым раствором едкогю натра и водой. Далее хлорофорк отгоняют и;оста ;. Ток кристалхгазуют из смеси метилово го спирта с этиладетатом, получая 0,7 г , 4« (N -метилкарбамоксиметил) -7 -метокси-2 метил-1-4талаеона с т, пл. 171-173 С. Вычислено. %: С-59,76; Н-5,79;/(|-1б108: C,li |04:NjI Hatfi Ko, %: C-S9,65; Н-5,47; -15,32 Пример 3. 4 г 4- летилтиокарбо нилоксиметил-1-фталазона, полученного с . использованием в качестве исходных реагеНч тов 4-оксиметил-1- гтвлазона и метилхлор4 тиоформиата по прг;меру 1, растворяют в 20 мл метилового спирта. После этого, к раствору добавляют 1 г диметиламина при перемещивании. Далее реакционную смесь оставляют nptf комнатной температуре на 3 час, упарИЕшот при пониженном давлении, остаток кр;;сталяизуюгт из смеси этилаУштаЦ та с петропеЙ21Ь м эфиром, получая 0,6 г 4.-( К) 5 N -.д;метилкарбамоксиметил}««1- фталааона с т, гш. 174-176 С. Вычислено, %: ,28.Н-5,30; М-17,00 , Найдено, %: С-58,21; Н-5, -17,22 П р и- м е р ы 4-21. По примеру 1 получают производные 4-4|енокснкарбон Шокси- метил-1--фталазона формулы на основе реакции производных 4-оксиметил-1-фтала- зона П с фезишхлорформиатом. Затем проводят реакцию пронзвошсых 4 фенок-. сикарбонилоксиметил-1-фталазона 1У с метиламином аналогично примеру 2 , , и получают продукты формулы I с аыходом 80-90%, как это проиллюстрированно в табл. 1. По Примеру 2 проводят реакцию 4 $сноксикарбонилоксиметил-1-фталазола, получен- ного в примере 1, с аминами У. . В результате получают продукты, порочнсаен ные D табл. 2, с выходом 8О-9О%. Пример ы 31-5О. По примерам
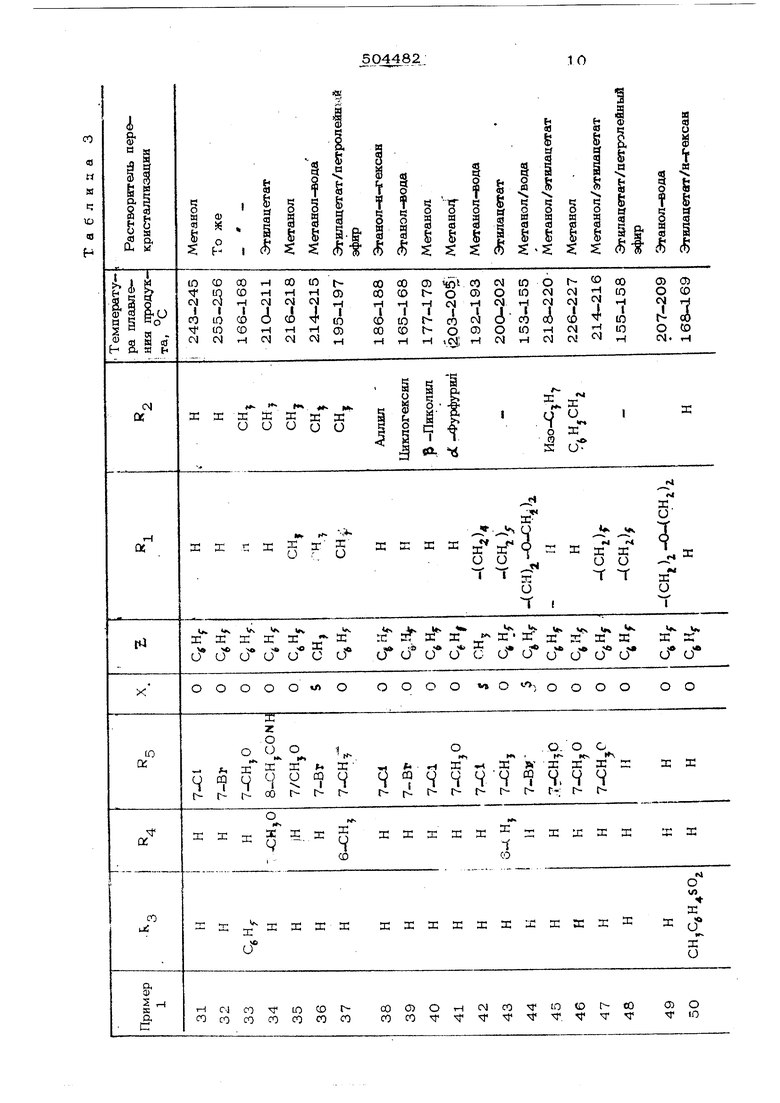
(1«-4 проводят реакцию соединениГ формулы И с соединениями формулы 1)1, например фе- илхлормиатом, фенипхпортиоформиатом или метиЛхлортиоформиатом, Затем проводят реакцию между образовавшимися проме жуточными соединениями формулы (Y аминами формулы V , в результате чего полу HajoT продукты формулы 1 выходом 80-90%, как это пройллюстр ровано в табл. 3.
Таблица 1
Таблица 2
Пример 51, К по{)омешиБаомому раствору 3,4 г 4-окс11мет1ш-1-фталазона и 3,2 г днметиллнилина в 100 мл сухого топубпа по каплям добавляют раствор 2,2 г фосгена в 20 мп толуола при 0-5 С,6
По завершении добавления реакционную смесь перемешивают в точение 3 час при 0-5 Сив течение 3 час при температуре приблизительно 10 С. Далее, поддерживая температуру смеси ниже 10 С, добав- 10 лякгт избыточное количество аммиака. За МСмесь выдерживают при температуре ниже 10 С и оставляют стоять при комнатной температуре в течение 3 час. После Toro смесь промывают водой, толуольный 15 «злой отделяют и водную фазу Экстрагируют этилацетатом. Далее совместный толуольный и этилацетатный раствор сушат и упаривают при пониженном давлении. Полученный остаток кристаллизуют из метилового 20 пирта, получая 4-карбамоксиметил-1- а- лазон с т. пл. 23О-232°С.
Пример 52. Раствор 9,2 г 7-хлор-4.оксиметил-2 гметил-1-фталазона и 7 г диметиланилина в ЗОО мл сухого толуола 25 Охлаждают до температуры от -5 до О С. Добавляют 5,5 г фосгена при перемешивании при температуре от -5 до О С. Смесь перемешивают при 0-5 С в течение 5 час, а затем при О-5 С и перемс;шивании добавг
П р и м о J) (Л., К раствору 3 г 4-ОК-.4 еноксикарбонилоксиметил -2-метил-1-фта-
симетил-2-мотип-1- 1Чс). в 15 мл пи-лазона с т. пл. 97-09 С, ридина при охшжд. MU11 и поромешивапии до-К раствору 4 г 4-4елоксикарбонилоксибавляют 3,5 г фо лпхпо «|юрмиата. Реакцион-ббмет1т-2-метил-1 фтш1аооиав 50 мп метаную смесь оставляют стоять при комнатнойнола при перемешивгшии добавляют в Г(Х -
температуре; в TeHoitsio 3 концентрируют-ДИметиламиноиропи/iaMiina.Роакшюннуюсмсхзь
упаривалиом, а затем })1Юбашшют водой.перемешивают при кок1латпой томиорачуре ц
ОбразовлвшпЛся осгщокфильтруют и кристалли..течение 5 час, после чего отгоняют мотазуют но этипоьо -о эфира, получая 4 г 4- (Юиол. Остаток растаоряют li этиаоиом ajjiipo.
ляют 5 мл ,-пого вошюго раствора метиламина, Реакциошгую смесь перемешивают в течение часа и оставляют стоять при комнатной температуре в точение 3 час. Далее смесь промывают водой и толуольный роствор сушат и упаривают.
Остаток кристаллизуют из этилацетата, получая 6,5 г 7-ooiop-4-( N -метилкарба- моксиметил)-2-метил-1-фталазона с т. пл. 148-149°С.
Вычислено,%:С-51,15;Н-4,26; -14,92
qi%O W, W
Найдено, %.- С-50,89; Н-4,35; N-14,79
Примеры 53-60, Аналогично пря мерам 51-52 получают продукты формулы 1 с использованием в качестве исходных про, дуктов соединений общей формулы II и аминов обшей формулы У,
Пример 60. Смесь, из 4 г 7-ч тор-4-оксиметил-2-метил-1-фталазона, 3 г дн- метиланилина, 2 г метилкарбамилхлЬрида и 40 мл абсолютированного диэтялового эфира нагревают с обратным холодильникам в тв- чение 5 час. Реакционную смесь промывают последовательно водой, 3%-ным раствором соляной кислоты и водой, сушат и упарива- ют. Полученный остаток кристаллизуют из этилацетата, получая 2,2 г 7-хлор-( N- -; -метилкарбамоксиметип)-2-метил-l- anflii зона с т. пл. 148-149 С.
Т а б лиц
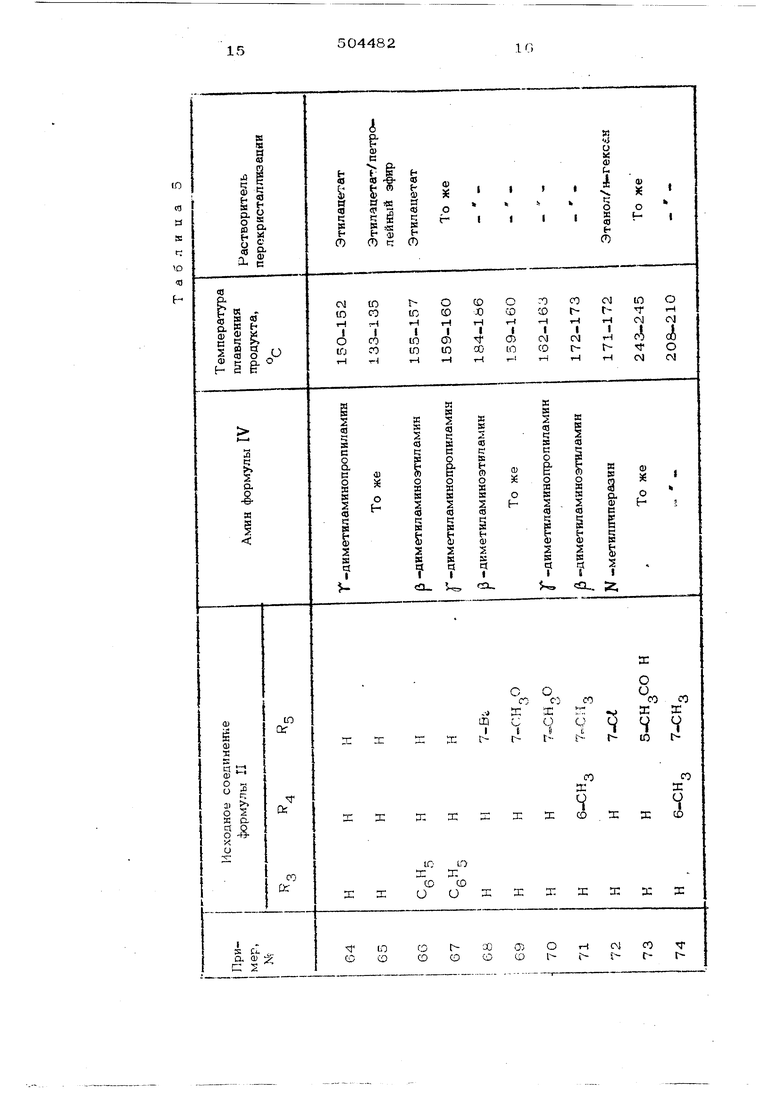
4 а эфирный раствор поспедоватепьно промывают 10%-ным раствором едкого натра и водой. После высушивания эфир отгоняют, а к маслянистому остатку добавляют 1 г щавелевой кислоты, и смесь кристалпизу- ют на этилового спирта, получая 3 г оксаЯа та 4 1 -( (С диметиламинопропил) -f1cap6aмоксиметил) -1-фталазона с т. пл. 168-169 Вычислено, %: С 52,93; Н 5,92;Nl3,2 9ЛРЛ(соон)а; Найдено, %: С 52,78; Н 5,86; Пример 62. 2г 4-феноксикарбо,нипбксиметил-1-4талааона, попученного в i .roTjB lO Mn метанола.: iK перемешиваемому jfacTBopy добавляют 4r N метилпиперазита. Реакционную смесь -метилпиперазита. Реакционную перемешивают при комнатной температуре в течение 3 час, -а затем отгоняют мета- нол. Остаток кристаллизуют из метанола, получая 1,3 г 4-. ,N -(этилевметиДй;мино-этилен)-карбамоксиметилЗ -1-фтапазоiHa,, Вычислено, %: С 59,59; Н 6,00N18,33 qjHfgOjN Н 5.89; Найдено, %: С 59,71; N:18,60 Пример 63. По примеру 61 по-4 лучают 4-феноксикарбоншюксиметип-2-мв4-. тил-1-4)талазон на основе 4-оксиметип-24 -метип-1-фтапазона, а затем проводят акцию 4-феноксикарбонилоксиметил-2-ме-, тил-Л-фталазона с р -диметиламиноэтипг мином. В результате получают 4- W - ; -( р -диметиламиноэтил)-карбамоксиметил -2-метил-1-фталазон с т. пп. 193-193 G (перекристаллизация из этанола).м ер ы 64-74, По примерам При 61-62 п проводят реакцию производйдх 4. -оксиметил-1-фтапазона общей формулы Т1 с фенилхлорформиатом, получая производные 4-4|еноксикарбонилокеиметил-1-фтала зона общей формулы 1У, Затем проводят реакцию соединений общей формулы 1у с аминами формулы У с обшим выходом прфдукта 70-90%, как это проиплюстрирова|ф в табл. 5.
in to
3
s
t D 0
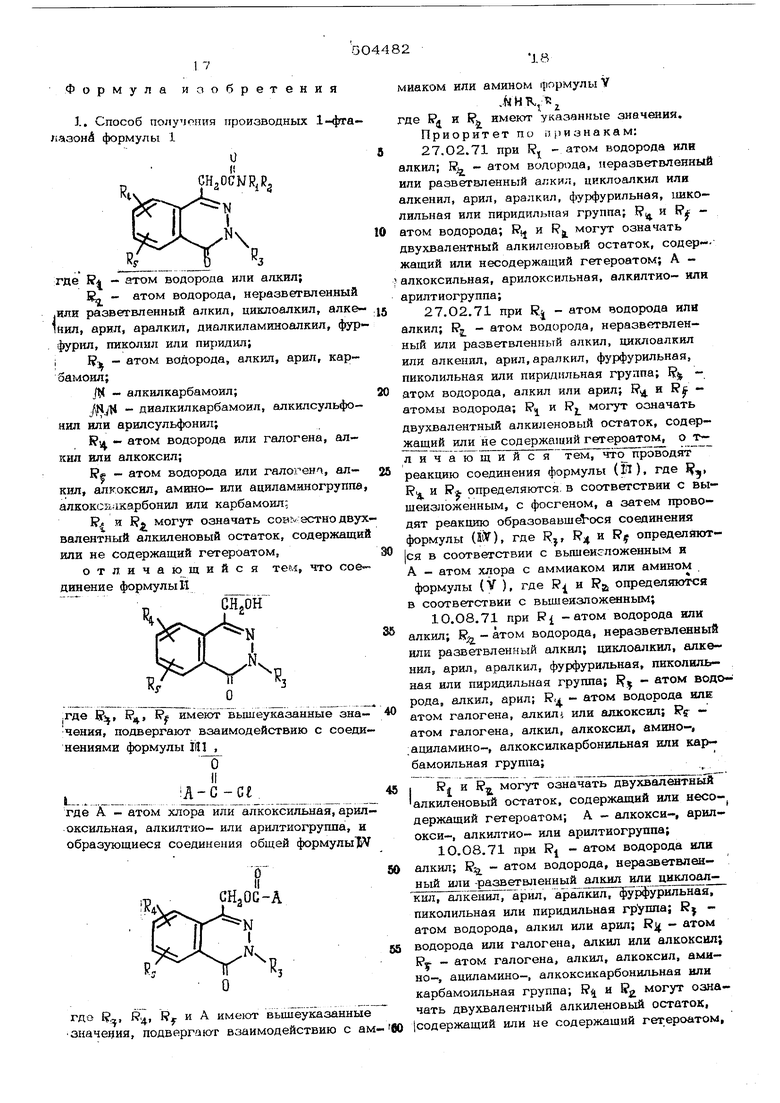
H 1 7 Формула иаоб р е т е н и я 1. Способ получония ироиаводных 1-фга лазонй формулы 1 CH., N где R - атом водорода или агасил; К - атом водорода, неразветвленный .или разветвленный алкил, циклоалкил, алке шил, арил, аралкил, диалкиламиноалкил, фур фурил, пиколил или пиридил; i R;b - атом водорода, алкил, арил, карбамоил; - алкилкарбамоил; j - диалкилкарбамоил, алкилсульфо- НИЛ или арилсульфонил; - атом водорода или галогена, алкнл или алкоксил; - атом водорода или галогена, алкил, алкоксил, амино- или ациламиногруппа алкоксйлкарбонил или карбамоил; 1 и F могут означать совместно двух валентный алкиленовый остаток, содержащи или не содержащий гетероатом, отличающийся тем, что сое динение формулы И |Где 1$, t, bff имеют вышеуказанные значения, подвергают взаимодействию с соеди нениями формулы iHl , где А - атом хлора 11ли а лкоксильнаяГарил оксильная, алкилтио- или арнлтиогругша, и образующиеся соединения общей фopмyлыIV СНзОС-А где R,,, R,, R вьииеукааанные значечия, подвергают взаимодействию с ам 2 миаком или амином формулы V ,WHR,T: где f(j и R имеют указанные значения. Приоритет по признакам: 27.02.71 при R, - атом водорода или алкил; Е - атом водорода, неразветвленный или разветвленный алкил, циклоалкил или алкенил, арил, аралкил, фурфурильная, ииколильная или пиридильная группа; атом водорода; R(j и Rj могут означать двухвалентный алкиленовый остаток, содер жащий или несодержащий гетероатом; А алкоксильная, арилоксильная, алкилтио- или арилт иогруппа; 27.О2.71 при R - атом водорода или алкил; Rj - атом водорода, неразветвленный или разветвленный алкил, циклоалкил или алкенил, арил,аралкил, фурфурильная, пиколильная или пиридильная группа; атом водорода, алкил или арил; R и Rt атомы водорода; Rij и R.j могут означать двухвалентный алкиленовый остаток, содер- кащий или не содержащий гетероатом, о т- л и ч а ю щ и и с я проводят реакцию соединения формулы (JT), где , R и R определяются в соответствии с вышеизложенным, с фосгеном, а затем проводят реакцию образовавщеЬося соединения формулы (SlV), где Rj, R4 и Ру определяются в соответствии с вьпиеисложеиным и А - атом хлора с аммиаком или амином формулы (V ), где R и Rg, определяются в соответствии с вышеизложенным; 10.08.71 при RI - атом водорода или I алкил; R - атом водорода, неразветвленный или разветвленный алкил; циклоалкил, алкенил, арил, аралкил, фурфурильная, пиколиль- ная или пиридильная группа; ij - атом водо рода, алкил, арил; R, - атом водорода ИЛЕ атом галогена, алкилi или алкоксил; - атом галогена, алкил, алкоксил, амино-, ациламино-, алкоксилкарбонильная или кар- бамоильная группа; 1 RI и R могут означать двухвалентный алкиленовый остаток, содержащий или несодержащий гетероатом; А - алкокси-, арил- ОКСИ-, алкилтио- или арилтиогруппа; 10.0 8.71 при RJ - атом водорода или алкил; R - атом водорода, нерааветвленный или -разветвленный алкил или циклоалкил, алкенил, арил, аралкил, фурфурильная, пиколильная или пиридильная группа; Rj атом водорода, алкил или арил; Rj - атом водорода или галогена, алкил или алкоксил; Ry атом галогена, алкил, алкоксил, ами- но-, ациламино-, алкоксикарбонильная или карбамоильная группа; R и 1 могут означать двухвалентный алкиленовый остаток, |содержащий или не содержащий гетероатом, от дят Н,, 19.50448220 личающийся тем, что прово-выше; А - атом хлора с аммиаком или амиреакцию соединения формулы (П), гденом формулы (Y }, где R; и R имеют энаRU и Ру. имеют значения, определенныечения, определенные выше.
Авторы
Даты
1976-02-25—Публикация
1973-11-22—Подача