Изобретение относится к способам получения новых соединений - 1-(5/ б , 78-тетрагидро-1 - или 2 -нафтил) 2-алкияаминопропанолй1В-1 общей формулы
,Ш-(5н-иК2
йЛ он снз
обладающих ценными Фармакологическими свойствами..
Известны нафтоксизамещенные алканоламины, представляющие собой фармакологически активные соединения,
Однако в литературе отсутствуют какие-либо сведения о соединениях формулы I .
Предлагается способ получения соединений формулы I , представляющих интересдля фармакологии, заключающийся в том, что нафталин подвергают взаимодействию с cd-бромпропионил Бромидом в различных органических растворителях по реакции лриделяКрафтса в присутствии хлористого алюминия,.- причем в зависимости от растворителя получают: в хлороформе 1-(об-нафтил)-2-бромпропанон-1, а в нитробензоле -1-(-нафтил)-2-бромпропанон-1. Полученный 1-( или р-нафтил)-2-брЬмпропанон-1 подвергают взаимодействию с избытком соответствующего алкиламина, такого, как изопропиламнн, диэтиламин, пиперидин, в среде инертного растворителя, например бензола, выделенный аминокетон в виде хлоргидрата восстнавливают каталитически в автоклаве лод давлением. В качестве катащизатора гидрирования используют скелетный никель. Целевой продукт выделяют в виде соли, обычно в виде хлоргидрата.
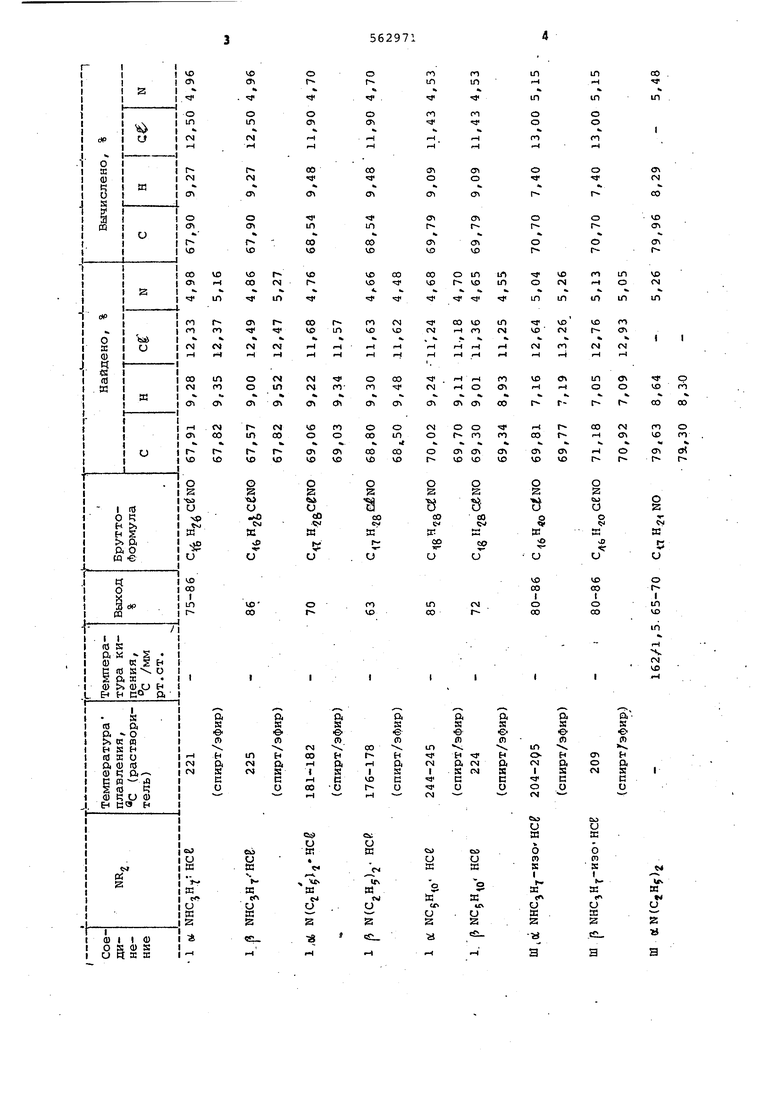
Свойства синтезированных продуктов приведены в таблице.
о
GO
ч in
о
vfi
о
0



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных 1-арил-2-аминоэтанола-1 | 1983 |
|
SU1299500A3 |
| СПОСОБ ПОЛУЧЕНИЯ | 1973 |
|
SU367103A1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-(4- ГИДРОКСИ -3- ГИДРОКСИМЕТИЛФЕНИЛ)-2- (N- ТРЕТ- БУТИЛБЕНЗИЛАМИНО) ЭТАНОНА ГИДРОХЛОРИДА | 1988 |
|
RU1616078C |
| ПРОИЗВОДНЫЕ ХИНОЛИНА, В ЧАСТНОСТИ 5,6,7-ЗАМЕЩЕННЫЕ 1-(2-ХЛОРХИНОЛИН-3-ИЛ)-4-ДИМЕТИЛАМИНО-2-(НАФТАЛИН-1-ИЛ)-1-ФЕНИЛБУТАН-2-ОЛЫ, СПОСОБ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ СОЕДИНЕНИЙ | 2011 |
|
RU2486175C2 |
| ПРОИЗВОДНЫЕ ХИНОЛИНА, В ЧАСТНОСТИ 6,7-ЗАМЕЩЕННЫЕ 1-(2-ХЛОРХИНОЛИН-3-ИЛ)-4-ДИМЕТИЛАМИНО-2-(НАФТАЛИН-1-ИЛ)-1-ФЕНИЛБУТАН-2-ОЛЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ СОЕДИНЕНИЙ ДЛЯ ЛЕЧЕНИЯ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ МИКОБАКТЕРИАЛЬНОЙ ПРИРОДЫ, В ЧАСТНОСТИ ТУБЕРКУЛЕЗА | 2013 |
|
RU2530493C1 |
| ЗАМЕЩЕННЫЕ N-[2-(1-АДАМАНТИЛАМИНО)-2-ОКСОЭТИЛ]-N-(АМИНОАЛКИЛ)АМИДЫ НИТРОБЕНЗОЙНЫХ КИСЛОТ | 2011 |
|
RU2500666C2 |
| Способ получения /3,3-ди (тиенил-3)-3- оксипропил /-(1-фенил-1-оксипропил-2) амина или /3,3-ди (тиенил-3) пропен-2-ил/ - (1-фенил-1-оксипропил-2) амина или их солей | 1978 |
|
SU784774A3 |
| Способ получения 2-диметиламинометил-3-оксипиридина | 1982 |
|
SU1018940A1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-АЛКОКСИКАРБОНИЛМЕТИЛПИРРОЛИДОНОВ-2 | 1992 |
|
RU2032668C1 |
| Способ получения производных 1-/3-(3,4,5-триметоксифенокси)-2-пропил/-4-арилпиперазина | 1978 |
|
SU893133A3 |
СПОСОБ ПОЛУЧЕНИЯ 1-
о о
(ft
fО.
s «
со
§ г
с и
о
as
U4
S
N
и
eSL
TS
а
S
о о
о.
S
& т
н о.
N
о гч
kO
S
о
о
VO
Со
и
ffi
S
ас
г Пример. 1-(«/-Нафтил)-2бромпропанон-1 (II (и). В трехгорлую колбу с мешалкой, хлоркальциевой трубкой и капельной воронкой помещают 7 г (0,052 моль) хлористого алюминия и 20 мл сухого хлороформа, К этой смеси в течение 30 мин при хорошем перемешивании прикапывают 10,6 г (5,2 мл, 0,052 моль) -бромпропионилбромида, разбавленного 10 мл сухого хлорофор ма. Температуру бани повышают до 30®С и при этой температуре перемешивают до тех пор, пока раствор не становится прозрачным, после чего температуру понижают до комнатной, Прикапывают раствор 6 , 4 г 0,952 моль нафталина в 20 мл сухого хлороформа при этом выделяется бромистый водород. Затем температуру бани вновь повышают до 35-40 С и перемешивают 30 мин. Реакционную смесь выливают в лед (150 г), добавляют 10 мл концентрированной соляной кислоты и оставляю на ночь . Отделяют органический слой, промьшают его водой (2-3 раза и сушат сернокислым магнием. Раство ритель отгоняют и полученный l-(cv нафтил)-2-бромпропанон-1 перекриста лизовывают из петролейного , Получают 9 г вещества, 1- (-Нафтил) -2-бр.омпропанон-1 (11R). К 120 г (0,91 моль) хлористого алюминия в 340 мл сухого нитробензола при хорошем перемешивании медленно прикапывают 189 г (0,89 моль) ot-бромпропионилбромида в 170 мл сухого нитробензола. Реакционную смесь охлаждают льдом до и в течение 1 ч прикапывают раствор 110 г (0,89 моль) нафталина в 340 мл нитробензола. Перемешивание продолжают затем 1 ч при комнатной температуре и 1 ч при 30-35°С, Реакционную смесь выливают на лед, обрабатывают 100 мл концентрированной соляной кислоты и оставляют на ночь. Обрабатывают, как указано раньше. После отгонки растворителя 1-(р-нафтил)-2-бромпропанонперегоняют в вакууме. Получают масл слегка желтоватого цвета, которое при стоянии кристаллизуется, 1-( -Нафтил)-2-изопропиламинопропанон-1 (111,НК -НЫС-}Н7-изо) 30 г (0,012 моль) 1-(«-или. -наф тил)-2-бромпропанона-1 растворяют в 150 мл сухого бензола и приливают 24 мл (16,5 г, 0,03 моль) изопропил амина. Смесь оставляют на сутки при 15-16 С, При более высокой температуре происходит почти полное ос моление реакционной смеси. Выпавший осадок бромистйводородной соли изопропиламина отфильтроБывают, промывают дважды небольшим количеством сухого бензола. По коли честву бромистоводородной соли судят о степени прохождения реакции. Бензол отгоняют. Оставшееся масло растворяют в 120 мл разбавленной соляной кислоты (1:1), Солянокислый раствор оставляют в холодильнике на сутки. Выпавший осадок солянокислой соли 1-(оС-или р-наЛтил)-2-изопропиламинопропанона-1 отбильтровывают, фильтрат упаривают досуха и остаток присоединяют к основному осадку. Все перекристаллизовывают из спирта с эфиром. 1- (ос-или р -Нафтил) -2-диэтиламинопропанон-1 (Oi,(C2Hj), Это соединение получают, как изопроп-иламинопроизводное, описанное раньше. К 57 г (0,216 моль) 1-„( -нафтил) -2-бромпропанона-1 в 300 мл сухого бензола приливают 57.мл (38,5 г, 0,525 моль) диэтиламиjja и оставляют на трое суток при 15-1бс, Реакционную смесь обраба.тывают, как указано раньше. Из солянокислого раствора выделяют 8 г непрореагировавшего исходного бромкетона. Кислый раствор подщелачивают до сильнощелочной реакции 40%-ным раствором едкого натра, вьщeливlJeecя основание экстрагируют бензолом или хлороформом. Экстракты сушат сернокислым магнием. Растворитель отгоняют и продукт перегоняют в вакууме. Получают 35 г (64%, считая на взятый бромкетон, 74%, считая на прореагировавший), Аминокетон быстро темнеет и поэтому сразу после перегонки должен быть переведен в соляно кислую соль, которую обычно получают следующим образом. К ацетоновому раствору аминокетона добавляют эквивалентное количество 10%-ного ацетонового раствора хлористого водорода при охлаждении. Смесь оставляют в холодильнике на 2-3 ч. Осадок солянокислой соли отфильтровывают, к фильтрату добавляют сухой эфир и получают еще некоторое количество соли. Общий выход солянокислой соли 90-95%. 1- (о:-или ( -Нафтил) ) -2-пиперидинопропанон-1 (Ili,NRj-N Н ) , Соединение получают аналогично указанным аминопроизводннм, 4,2 г (0,016 моль) бромкетона, 3,4 г (0,039 моль) пиперидина в 30 мл сухого бензола оставляют на двое суток при 16-18 С, Смесь обрабатывают как указано раньше. Солянокислыйраствор кипятят с углем, охлаждают и подщелачивают при охлаждении до сильнощелочной реакции 40%-ным раствором едкого натра. Выделившийся осадок желтоватого цвета отфильтровывают и сушат на воздухе. ,
1-(5,6,7 8-Тетрагидро-Г-или 2-нафтил)-2-алкиламинопропанол-1 (loi или I ).
Восстановление хлоргидратов аминокетонов проводят под давлением в автоклаве при 60-70 атм и температуре 10О-11О®С. В качестве катализатора используют скелетный никель, растворителем является водный спирт или иной подходящий растворитель. Йродолжите.ьность восстановления эависит от активности катализатора (6-24 ч). О прохождении реакции , судят по количеству поглощенного во дорода, а также по исчезновению полосы поглощения -СО- в ИК-спектрах.
По окончании восстановления катализатор отфильтровывают, растворитель отгоняют досуха. Остаток Солянокислой соли аминоспирта перекристаллизовывают из подходящего растворителя (например, из спирта с эфиром).
При подщелачивании солянокислых водных растворов аминоспиртов могут быть выделены свободные основания. Строение аминоспиртов доказало ИК-, ЯМР-спектроскопией и подтверждено элементным анализом.
Авторы
Даты
1983-12-15—Публикация
1974-06-25—Подача