лопропанкарбоновой кислоты o6uieft фор мулы If /«3 МОССН СС И / о С Кч НзС 1Нз где R и R . имеют приведенные значения , М щелочной или щелочноземельный металл или третичный алкиламмоний подвергают взаимодействию с соединением формулы Ш- где А, Rj, tn и П имеют приведенные значения; В - атом галогена или тозилоксигруппй, в среде воды или инертного органического растворителя при температуре от ком ватной до температуры кипения реакционной массы. Желательно процесс вести в присутствии катализатора, такого как четвертичная соль аммония или фосфония. В качестве растворителя могут быть использованы галоидуглеводороды, простые или сложные эфиры,кетоны или амиды Пример 3.. В раствор из 1,25 {0,008 моль) 2,2н1иметил-3-(1-транс-лропенил)-щиклопропанкарбоновой кислоты и 1,50 г триэтиламина в 2О мл диме тилформамида добавляют по каплям раствор 2,50 г (0,О1 моль) З-фенокси-оС-цианобензилхлорида в 1О мл диметилформамида По окончании добавления температуру постепенно повышают до 7О°С и при этой температуре перемешивают в течение 2 ч. Получают белый осадок. После охлаждени реакционную смесь выливают в холодную воду и экстрагируют толуолом, промыва(от 2%-ным едким натрием и насыщенным раствором хлористого натрия. Толуольный раствор пропускают через колонку с 20 г ак тивированного глинозема. После испарения растворителя получают 3,О2 г 3-4енокси -с(-иианобензил-2, 2 -диметил-3-( 1 -транс-пропенил)наиклопропанкарбоксилат в виде бесцветного маслянистого rqpo- ДУКга. g П д 1,5432. Выход 1ОО%, Найдено, %: С 76,91; Н 6,23; N 3,67. ЗЪ 23 3Вычислено, %:С 76,43; Н 6,41; N 3.88. ИК-спектр: 174О, 159О, 691 см Я-МР(ССе4 ): 1,05-1,35 (м. 6Н), 1,66 {широкий 6,7 щ ЗН), 1,40-2,40 {м. 2Н), 5,ОО-5,9О (м. 2Н), 6,29-6,34 {псевдо д, 1Н), 6,80-7,51 (м. 9К). Пример 2. В раствор 1,68 г {О,01 моль) хриэантемовой кислоты и 1,5 г триэтиламина в 2О мл диметилфэрмамида .добавляют по каплям раствор 3,93 г (0,О1 моль) 3-метил-5-фенокси-о{.-Н1ианэбензилтозилата в О мл днметилформами- да при комнатной температуре. Смесь обрабатывают аналогично, как в примере 1, и получают 3,3 г 3-метил 5-фенокси-о1.-цианобензилхризантемата в виде бесцветного маслянистого продукта. 1,5498. Выход 84,7%. Найдено, %: С 77,34; Н 6,63; N 3,52. ,. Вычислено, %: С 77,О9; Н 6,99; Ы 3,6О. ИК-спектр: 1740, 1591, 69О см ЯМР.(ССе4 ): 1.1О-1,5О {м, 6Н), 1,75 (широкий С, 6Н), 1,15-2,40 {м. 2Н), 2,85 (С, ЗН), 4,70-5,50 {м. 1Н), 6,3 0-6,34 (псевдо д. 1Н), 6,80-7,49 (м. 8Н). Пример 3. В 32,6 г раствора хризантемной кислоты в смеси из 104,5 г воды и 96,0 г толуола каплями добавляют 30%-:ный водный раствор 24,6 г гидроокиси натрия для получения натриевой соли хризантемной кислоты. После добавлёния 1,4 г бромистого тетрабутиламмо- ния к раствору натриевой соли каплями добавляют раствор 50,7 г Л-нииано-З-4еноксибензилового бромида в 76 г толуола, и смесь нагревают при 70 С в течение 4 ч с перемешиванием. После охлаждения реакционной смеси добавляют водный раствор 5 г карбоната натрия в 15 г воды для перевода непрореагировавшей хризантемной кислоты в водный слой для отделения, а органический слой промывают 36 г 3%-ного водного раствора карбоната натрия и отделяю т. Орган ическнй слой промывают 36 г 10%-ного водного раствора хлористого водорода н отделяют, а затем промывают 36 г воды и отделяют. Органический растворитель отгоняют при пониженном давлении для получения 63 г 3-феноксицианобензилхризантемата с выходом 95%. Пример 4. Действуют аналогично примеру 3, но используют 6,8 г твердой гидроокиси кальция вместо ЗО%-ного раствора гидроокиси натрия, 63,1 г 3-
. -фенокси-о1-цианобензилхризантемата получают с выходом 95%.
Пример 5. В 53 г указанного ниже в табл. 1 растворителя растворяют 18,5 г (О,И моль) хризантемовой кислоты, и к полученному раствору аобавляют 13,7 г (О,ЮЗ моль) ЗО%-ного водного раствора едкого натра (или 36,5 г- 0,О52 моль 159&-нрго водного раствора углекислого натрия) и 54 г воды. В результате получают натриевую соль, К раствору дополнительно добавляют указанный ниже катализатор, что вызывает повышение температуры до 7О-75 С. К раство- ру по каплям добавляют 28,82 г (0,1 моль) бромистого 3-н| енокси-с1С-циано1бенз па, растворенного в 43 г того же растворителя, причем указанное добавление осуществляют в течение 1,6 ч при перемешивании. Затем смесь дополнительно перв мешивают в течение некоторого времени (см, таблицу) при той же температуре и охлаждают. Отделенный органический слой .последовательно промывают 15 г 2%-но- го водного раствора едкого натра, 15 г 1%-ного водного раствора соляной кислоты и 15 г Воды, после чего отгоняют
растворитель. В результате получают сырой сложный эфир.
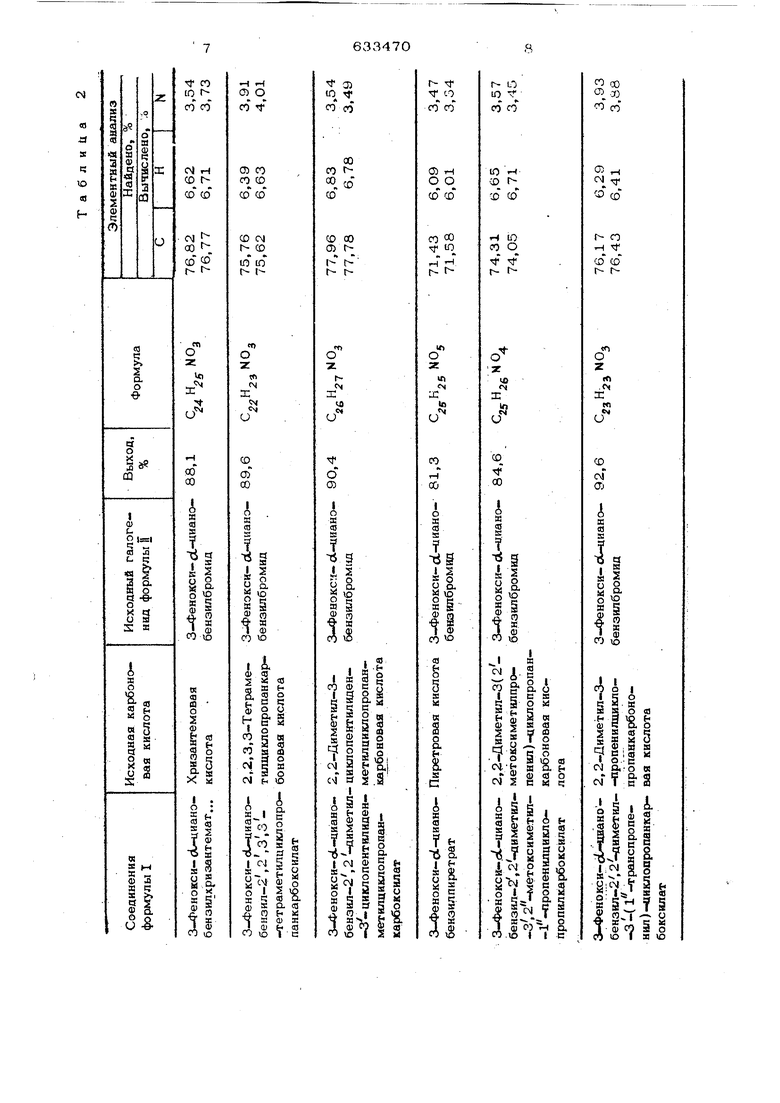
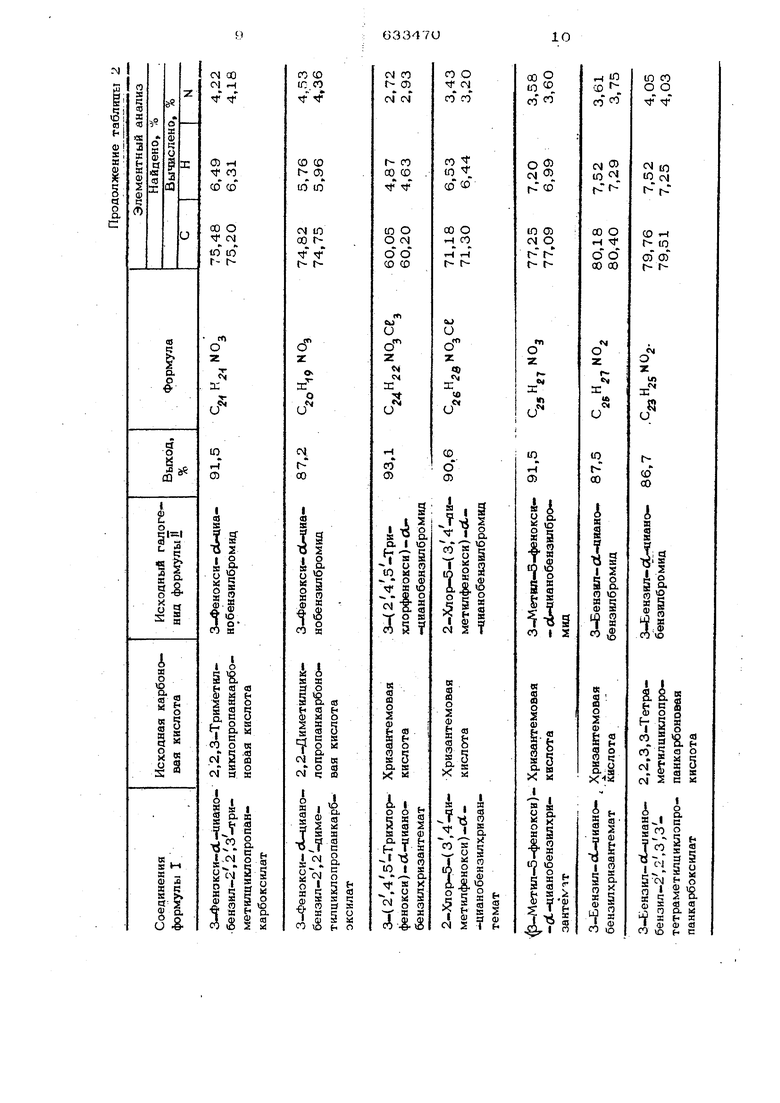
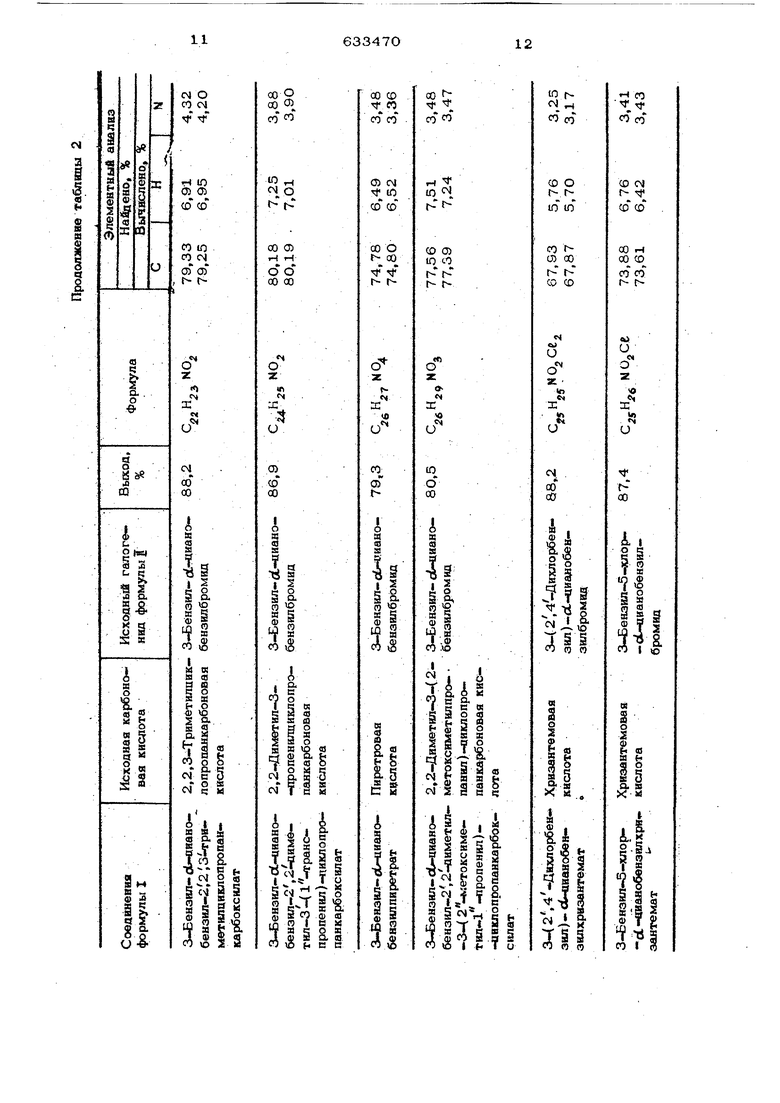
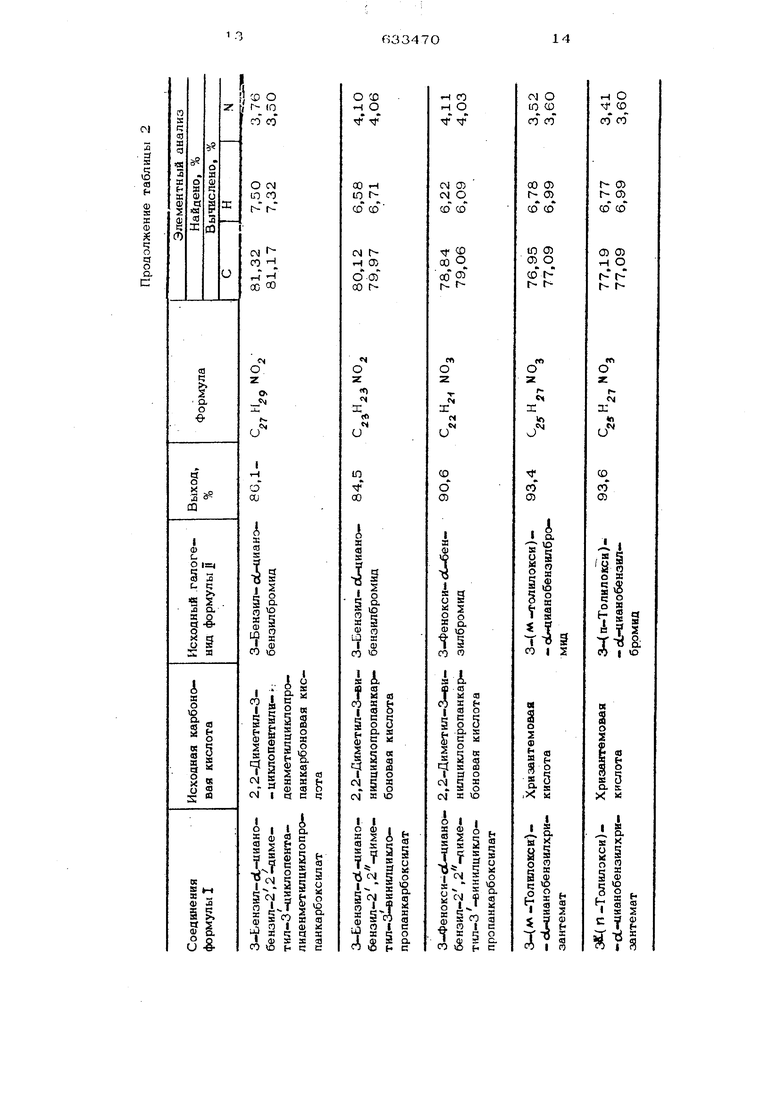
Пример 6, В 53 г ортохлорто- луола растворяют 18;5 г хризантемовой кислоты, и к полученному раствору с целью синтеза ее натриевой соли добавляют 54 г воды и 13,7 г (О,1ОЗ моль) ЗО%ного водного раствора едкого натра. Затем в полученный раствор дополнительно вводят 28,82 г (О,1 моль) 3-фенокси-оС-цианобензилбромида, растворенного в 43 г ортохлортолуола. Раствор постепенно нагревают и добавляют указанный выше растворитель с отгонкой воды и растворителя одновременно с водой, на что затрачивается один час. Затем раствор нагревают при слабом перемешивании в течение 3 ч при наличии обратного холодильника, до тех пор, пока температура раствора не достигнет 160С. Раствор охлаждают и обрабатьгоают его аналогично тому, как это делают в дополнительном примере 1. В результате получают 33,8 г (выход сырого вещества 9О%) темнокоричневого сырого сложного эфира. Физико-химические свойства и выходные данные других полученных соединений представлены в табл. 2.
Таблица 1



ТетрабутиламмоНаОНнийбромид
0,81
NOIOH
г- -4
НаОН МаОИ
Бромид бензил-6
триэтиламмония О,68
Бромид меТафен- 6 оксибензилтриэтиламмония О,87
ат
Бромид тетрабу- 4 тиламмония 0,81
Хлорид лаурилднил-
метилбенгйламмо- 8 ния 0,82
93,8
94,1
93,4 94,7
94,7 90,6 92,1
d
a g
01
л
S
ё
а fО)
о
CI
о
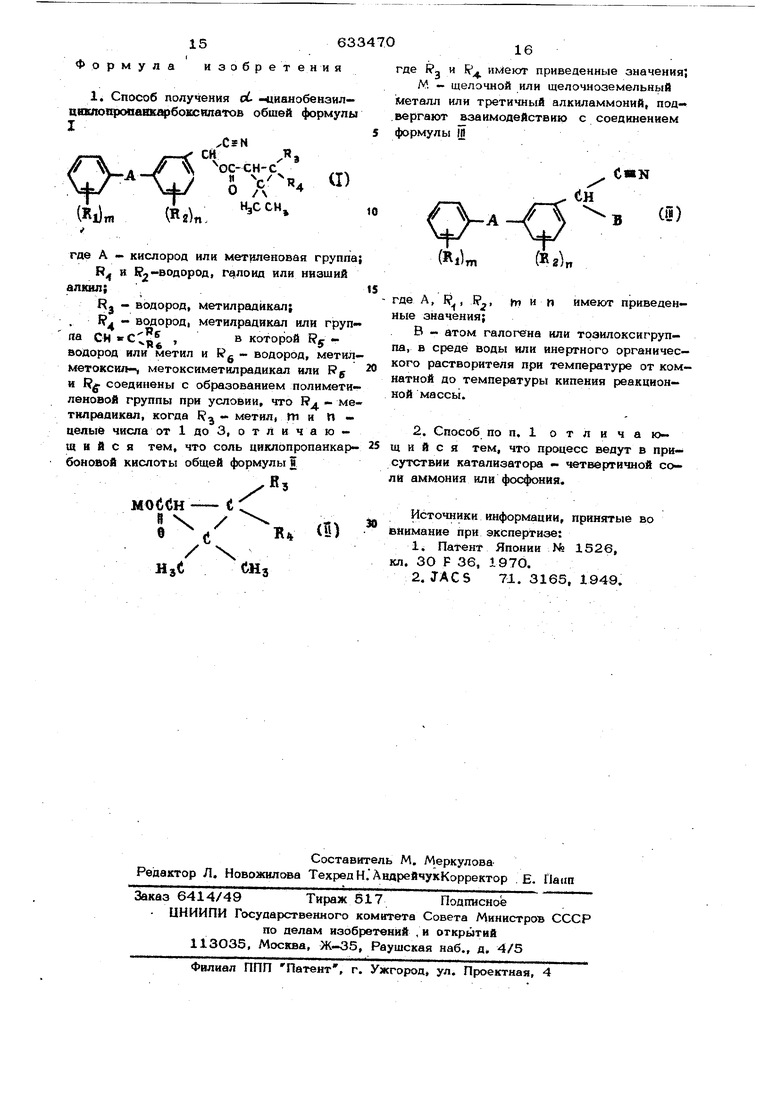
а С 15633 Формула изобретения 1. Способ получения d -«ианобензил- ашшо&ропвнк бокснлатов обшей формулы xCsN СИ. /- ff ОС-СН-С Лф/ S Х (Г,и. . где А - кислород или метиленовая группа R и &2 °Д°Р°Д« Га1лоид или низший алю1л; R, - водород, метилрадйкал; f. - водород, метилрадикал или груп rta ,в которой R водород или метил и К - водород, метил- метоксил-, метоксиметилрадикал или Rj и соединены с образованием полимети- леноаой группы при условии, что R - метклрадикал, когда R - метил, Щи П - целью числа от 1 до 3, о т л и ч а ю и и с я тем, что соль циклопропанкар(боновой кислоты общей формулы J 16 где К и R., имеют приведенные значения; К - щелочной или щелочноземельный металл или третичный алкиламмоний, под- вергают взаимодействию с соединением формулы Ш где А, Б , fi, (т и п имеют приведениые значения; В - атом галогена или трзилоксигруп- па, в среде воды или инертного органического растворителя при температуре от комнатной до температуры кипения реакционной массы. 2. Способ поп, 1 отличающ и и с я тем, что процесс ведут в присутствии катализатора - ютвертичной со- Л11 аммония или фосфсжия. Источники информации, принятые во внимание при экспертизе: 1.Патент Японии Ns 1526, кл. ЗО F 36, 1970. 2.JACS 71. 3165, 1949.
Авторы
Даты
1978-11-15—Публикация
1976-10-05—Подача