t
Изобретение относится к способу получения новых оС -цианрбензилциклрпропанкарбоксилатоБ, которые могут быть использованы в качестве биологически активных веществ в сельском хозяйсгве.
Известен способ получения эфиров циклопропанкарбоновой кислоты обшей формлы
« 1
гЧч
CH-C-OCH,-R,
х И 5
R, о
где F - водород, алкил , фенил или фенил, замешенный алкилом или ал коксилом С -Cw
-1лкил
Rg - фенил, фурил или их замещенные алкилом, алкиленом, галовдом, т&нилом, фур(рилом, алкилбензолом, или бензофурил, или алкилбеизофурил,
взаимодействием галоиДанГвдрида аик лопропанкарбоновой кислоты со спиртом
FpgCHgOH, где R имеют указанные значения, в присутствии основания l .
Целью изобретения является разработка способа получения новых оС-Цианобензилциклопропанкарбоксилатов, обладающих йнсекто-акарицидной активностью, которые по сравнению с известными соединениями 2j того ж6 назначения являются более эффективными.
Поставленная цель достигается способом получения оС -иианобензилциклопропанкарбоксилатов общей формулы I
CH-CHN
/«3
ос-сн-сС
II ч/
i)m : (R,)n ,
где А - кислород или метиленовая группа;
R1 и R - водород, галоид или низший ал- . кил; водород, метилрадикал} R.- водород, метилрааикалИЛИ груп Б па СН « С. в которой Rg - водород или метил и Rg- водород, метил-, мётокей-, метокси метиЛ1ЭйЙйкал ИЛИ Rg. и R,. соейиненЬг с . . - о о . -...- образовшием |1олиметиленовой группы, при условии, что R - метилрадккал, когда Rj - метил; шип- аблые числа от 1 до 3, Заключающийся в том, что галоидангидрид Циклопропанкарбоновой кислоты формулыП- - ..- С-СН-С:Г I XX Q СН, СНз где R и R имеют приведенные значения, X - хлор или бром, подвергают взаимодействию со спиртом формулы III : где А, R , , П1 и И имеют приведенные эначения, в среде инертного органиче&ко1хз рас вйритеЛя в npHcyTctBHH третичного амин при температуре от -10 С до температу ры кипения растворителя. В качестве третичного амина желател нб использовать пиридин, а растворителя бензол, . ,. . - Пример 1.К раствору 2,25 г (0,01, моль) 3-фенокси-оС-цианобензило вого спирта и 1О г пиридина в 20 мл сухого бензола добавлйот по каплям раствор 2,20 г (О,01 моль) 2,2- иметилг -циклопентилиденметилциклопропанкарбоновой кислоты в 10 мл сухого толуола при 2О С при охлаждении холодной водой.. Затем хлористоводородный Пиридин немедленно осаждшот. Смесь пе ремешивают 4 час при комнатной температуре и затем выливает в 2О мл во ного 2%-иого раствора соляной кислоты Отделившийся маслянистый слой промывают 20 мл 1%-чяого водного едкого на ра мл насыщенного раствора хлори того натрия и затем BbiteyuiHBfflOT над сульфатом магния. Рас;те«с йтепь удаляю перегонкой под уменьшенным давлением Остаток пропускают через хроматографическую колонку с 50 г силикагеля и экстрагируют бензолом и получают 3,51 г 3-ч})енокси-оС-1щанобензил-2,2-диметил-3-циклопентилиденметилциклопропанкарбоксилата в виде бледно-жёлтого масляг нйстого продукта. Выход 87,4%, II4 1,5420. Найдено, %: С 76,26; Н 6,73; N3,52.,.:-rr- - -.:;; .;;.:./. : CggHjy КОз Вычислено, %: с 77,78; Н 6,78; N3,49: . ;-.:;:: - : ИК (см-): ;174б, iSSO. 692. ЯМР ((Г, ССед): 1,05-1,40 (м,6Н), 1,15-2.50 (м, 10Н), 4,80-5,20 (м, 1Н), 6,25 (с, 1Н), 6,80-7,50 (м,9Н). П р и м е р 2, В раствор 2,25 г (0,01 моль) 3.-фенокси-оС.-аианобензияового спирта в йб мл толуолу по каплям при комнатной температуре дойавляют раствор 2,55 г (0,О11 моля) хризантемоилфомййа в 10 мл толуола. К получейнЬму раствору и6 каплям добавляЬот при 28-3О С раствор 1,5 г (0,015 мояя) триэтиламина в 5 мл толуола и соль сразу отделяют. По окончании добавления раствор еще в течение 20 мин перемёшиBfibi, за тем обра ба бывают, как в jttpHMepe 1,, и получают 3,27 г (выход 87,1%) 3-фенокси-оС-цианобензилхризантемата в виде светло-желтого масляного вещества, элементный анализ которого представлен в таблице. Пример 3. В раствор 3,04 г (0,01 моля) 3-(4-бромфенокси)-«Х,-ЦИанобензилового спирта в 20 мл толуола по каплям добавляют при комнатной темnepatype pacTBtOp 1,77 г (0,011 моля) 2,2«3|3-тетраметилш1клопропанкарбонилхлоркаа в 5 мл толуола. К полученному раствору, охлажденному до -10 С, снова по кшшям добавляют раствор 1,5 г (0,б15моля) три илймина и после выдерживания полученного растёора при этой же температуре раство|: дают стоять в течение ночи при комнатной температуре, затем его обрабатьшают, как в 1, и получают 3,89 г (выход 92,0%) 3-(4-бромфенокси)-с -Цианобензйл-2,2,3,3-тетраметилонкл опропанкс ,б(жсилагв в виде светло-желтого маслянистога вещбсгвд со следующими свойствами:- , т (1 см): 1741; 1589; 697. ЯМР (, С ceJ: 6,70-7,50 (м, 8Н), 6,22 (с,1Н), 1,28-1,18 (м, 12Н).
Найдено. %:С 61,63; Н 3,7Й;
.
Вычислено, %: С 62,57; Н 3,82;
N3,32.
П -р и м е р 4. В раствор 2,25 мл (О,01 моля) З-фенокси-оС-цианобензилового спирта в 20 мл бензола по каплям добавляют при комнатной температуре раствор 1,85 г (0,11 моля) хризантемоилхлорвда в 5 мл бензола. К полученному раствору при температуре кипения растворителя по каплям в течение около 1 О мин при перемешивании добавляют раствор 2,24 г (О,О15 моля) диэтиланилииа в 10 мл бензола, затем полученный раствор охлаждают до комнатной температуры, обрабатывают, как в примере 1, и получают 2,74 г (выход 73%) 3-фенокси-оС-цианобензИлхризантемата и виде светло-желтого маслянистого вещества. Элементный анализ представлен в таблице.
Пример 5. В раствор 2,25 г (0,О1 моля) 3-фенокси-оС-цианобензилового спирта в .20 мл каждого из перечисленных ниже растворителе по каплям
при комнатной температуре добавляют раствор 1,85 г (0,О11 моля) хризантемоилхлорида в 5 мл этого же растворителя. К полученному раствору по каплям в течение 10 мин добавляют при перемешивании раствор 1,5 г (0,015 моля) триэтиламина в 5 мл того же растворителя и полученный раствор перемешивают в течение 4 час. Затем раствор обрабатывают, как в примере 1, и получают указанное количество З-фенокси- - об-цианобензил хризантема та. РастворительВыход
Четыреххлористый
S
3,31 г (88,3%) углерод 3,29 г (87,6%)
Изопропиловый эфир 3,24 г (86,3%) Бутилацетат 2,82 г (75,1%) Метилизобутилкетон 2,60 г (69,2%) Диметилформамид Толуол (в этом случае в колбу предварительно наливают
3,18 г (84,7%) 20 мл воды)
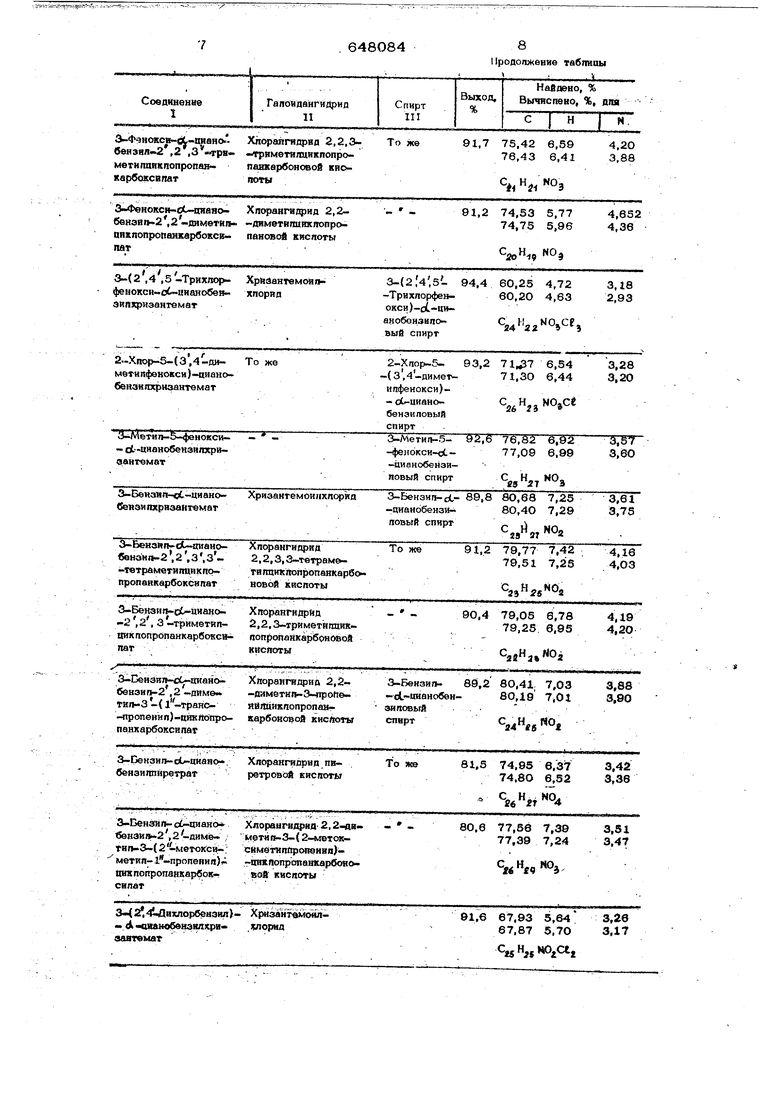
В таблице приведены выходные дан5ные и элементный анализ полученных соединений.




| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения -цианобензилциклопропанкарбоксилатов | 1976 |
|
SU634662A3 |
| Способ получения цианобензилциклопропан карбоксилатов | 1976 |
|
SU633470A3 |
| Способ получения циангидринов или их тозилатов | 1976 |
|
SU648086A3 |
| Способ получения циклопропанкарбоксилатов | 1972 |
|
SU527133A3 |
| Способ получения циклопропанкарбоксилатов | 1974 |
|
SU577968A3 |
| Инсектицидная композиция | 1976 |
|
SU738493A3 |
| Способ получения производных уксусных кислот | 1973 |
|
SU627749A3 |
| Способ получения эфиров замещенных циклопропанкарбоновой или фенилуксусной кислот | 1974 |
|
SU576911A3 |
| Способ получения циклопропанкарбоксилатов | 1974 |
|
SU1255048A3 |
| Инсектицидная композиция | 1974 |
|
SU671701A3 |

Хриэанте м он пхппри п
З-Фенокси-сХ-ЦИПнобутилхризангемат
89, 77,ОЗ 76,77 6,71
3,73
свмзтипаропвивп)-юге попропанкарбой вой: киспоты
ЗЦ2,4 8хпорбевзня}- Хризантвмоил i аши обв1Цш1хрВ- .viopua ааятемаг.
3,26
5,64 3,17 67,87 5,70
,се.
9
д-( м Топилокси)- Хряэангемояп- { -аиапобензищхр - хпоряп эантемат
3-( П-Топипокси)- То же - {(.-пидяобенаишфиаантематФормула изобретения 1. Способ получения oL -цианобенаи циклопропанкарбокснлатов общей формулы I ос-сн-с /р чО / 4 г)n ш са. где А - ксилород или метиленовая груп па;- 2 водороДш галоид или низший алкил; . R водород, метилрадикал; Кд - водород, мегвлрадикал, или
10
648О84
Лрс..попжение таблицы
3(лч Топипок- 91,4 77,26 6,81 3.56 си -ос-дианобен 77,09 6,99 3,60
зяпобыЯ спирт
SS.
3-{ п--Топипок- 91,8 77,О4 6,73 3,62 св)-о1.-цианобен-77,09 6,99 3,6О
звповый спирт
сил-, метоксиметилрадикал или и Rg Соединены с образованием полиметиле- новой группы, при условии, что R - метилрадикал, когда R мегил m и и - целые числа от 1 до 3, отличающийся teM, что ГИЛоидангидрид циклопропанкарбоновой кислоты формулы II хс-сн-ссГ и Х: R О си;сн, где R и R имеют приведенные значения, X - хлор или бром, подвергают взаимодействию со спиртом общей формулы ИГ
группа
R.
В KOTopicA Rg - Водород или метил и
- водород, метил-, меток
55
(Ri)m (R,)n 11 где А, R, Р шин приведенМ а ные эначёния, в среде HHOpTribro органического растВ4эрителя В:присутствии третичного амина при TetMnepjafype от -10 С до температуры «иления растворителя. 2, .Способ п. 1, о т л и ч а ю щ.и-Й--.С я ., что в качестве третичного амина используют пирвдин. 648084 щ рит во № 19 3. Способ по п. 1, о т л и ч а ю и с я тем, что в качестве раствоеля испольэуют бензол. Источники информации, принятые внимание при экспертизе 1. Патент СССР по заявке 118347О/04, кл. С О7 С 67/ОО, 66. 71, р/ 3165, 1949. 2. JACS
Авторы
Даты
1979-02-15—Публикация
1972-06-28—Подача