Действие препаратов изучалось в отно-В работу брались 1%-ные водные растении 8 штаммов грамм-положительных
микроорганизмов. Результаты испытаний всех соединений и определялась их приведены в табл. 1. Антимикробное деист-бактериостатическое и бактерипидное дейвие изучалось методом серийного развет,е- 5
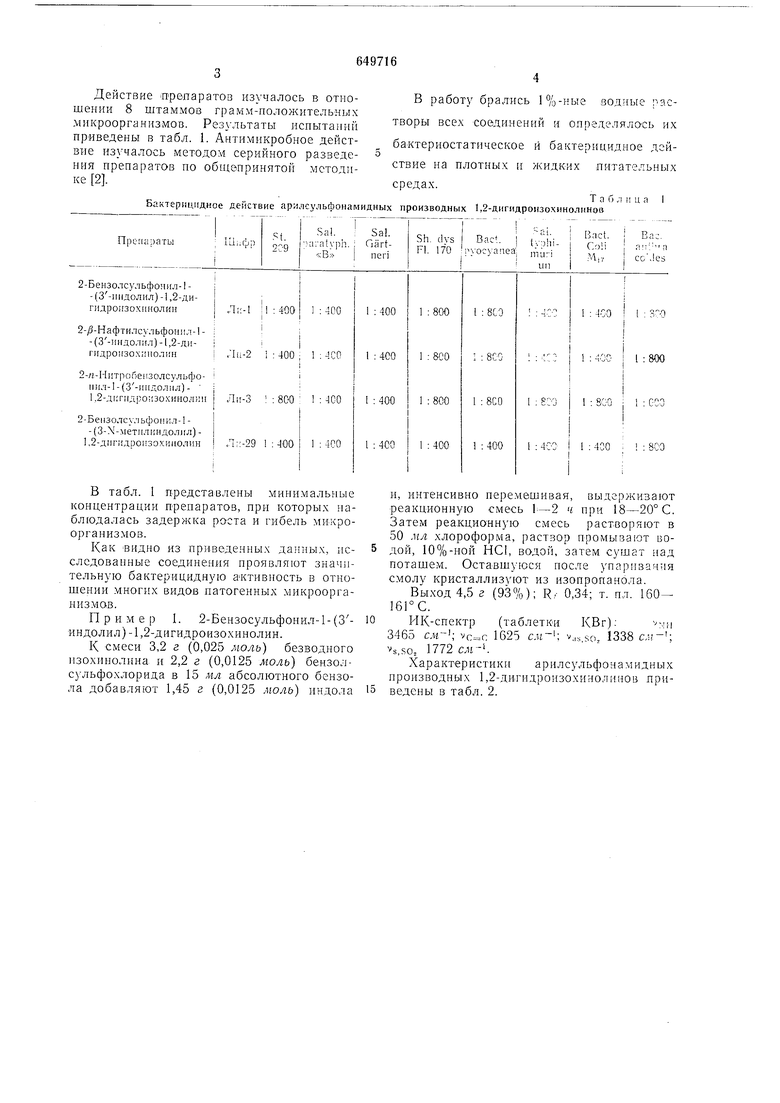
ния препаратов по общепринятой методи- ™ плотных и жидких питательных ке 2.средах. Бактерицидное действие арилсульфонамидных производных 1,2-дигпдро зохинолг.Нов
т а б л II ц а I 

| название | год | авторы | номер документа |
|---|---|---|---|
| {[1-(АММОНИО)-3,5,7-ТРИАЗААДАМАНТИЛ]МЕТИЛКАРБОНИЛОКСИПОЛИ(АЛКИЛЕНОКСИ)}ПРОПАН ХЛОРИДЫ, ОБЛАДАЮЩИЕ БАКТЕРИЦИДНОЙ И ФУНГИЦИДНОЙ АКТИВНОСТЬЮ, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2005 |
|
RU2288920C1 |
| ПРОИЗВОДНЫЕ 5-ОКСО-5Н-[1]-БЕНЗОПИРАНО-[5,6-B]4-ОКСО-4Н-[1,2]-ПИРИМИДО-1,4,5,6-ТЕТРАГИД РО-1,3-ТИАЗИНА | 1997 |
|
RU2169732C1 |
| Способ получения арилсульфонамидных производных 1,2-дигидрохинолина | 1975 |
|
SU575349A1 |
| Производные 1,2-гидросиламинокетонов, обладающие нейротропной активностью | 1976 |
|
SU657016A1 |
| НОВЫЕ БЕНЗОФУРОКСАНЫ, ОБЛАДАЮЩИЕ ФУНГИЦИДНОЙ И БАКТЕРИЦИДНОЙ АКТИВНОСТЬЮ | 2009 |
|
RU2428419C2 |
| Способ получения производного хинолина, или его фармацевтически приемлемого сложного эфира, или фармацевтически приемлемых солей указанного производного или его эфира | 1988 |
|
SU1588282A3 |
| 6-Алкилтиоимидазо /1,2-а//пиридины или их хлоргидраты,обладающие психотропной активностью,и способ их получения | 1976 |
|
SU653259A1 |
| ГЕПАТОПРОТЕКТОР | 1996 |
|
RU2156130C1 |
| Гологенированные норборненспиродикетоны,ОблАдАющиЕ бАКТЕРицидНОй и фуНгицидНОй АКТиВНОСТью,и СпОСОб иХ пОлучЕНия | 1976 |
|
SU677245A1 |
| Фосфорсодержащие производные мочевины и тиомочевины для борьбы с грибными заболеваниями растений | 1974 |
|
SU525398A1 |

В табл. 1 представлены минимальные концентрации препаратов, прп которых наблюдалась задержка роста и гибель микроорганизмов.
Как ВИДНО из приведенных данных, исследованные соединения проявляют значительную бактерицидную активность в отношении многих видов патогенных микроорганизмов.
Пример 1. 2-Бензосульфонил-1-(3индолил)-1,2-дигидроизохинолин.
К смеси 3,2 г (0,025 моль) безводного мзохинолина и 2,2 г (0,0125 моль) бензолсульфохлорида в 15 мл абсолютного бензола добавляют 1,45 г (0,0125 моль) индола
н, интенсивно перемешивая, выдерживают реакционную смесь I-2 ч при 18-20° С. Затем реакцио нную смесь растворяют в 50 мл хлороформа, раствор промывают водой, 10%-ной НС1, водой, затем сушат над поташем. Оставшуюся после упаривания смолу кристаллизуют из изопропанола.
Вььход 4,5 г (93%); R,- 0,34; т. пл. 160 61°С.
ИК-спектр (таблетки КВг);vvn
3465 сл4-; 1625 c.u-; v,,s,so, 1338 см-; vs.so, 1772 сиг-.
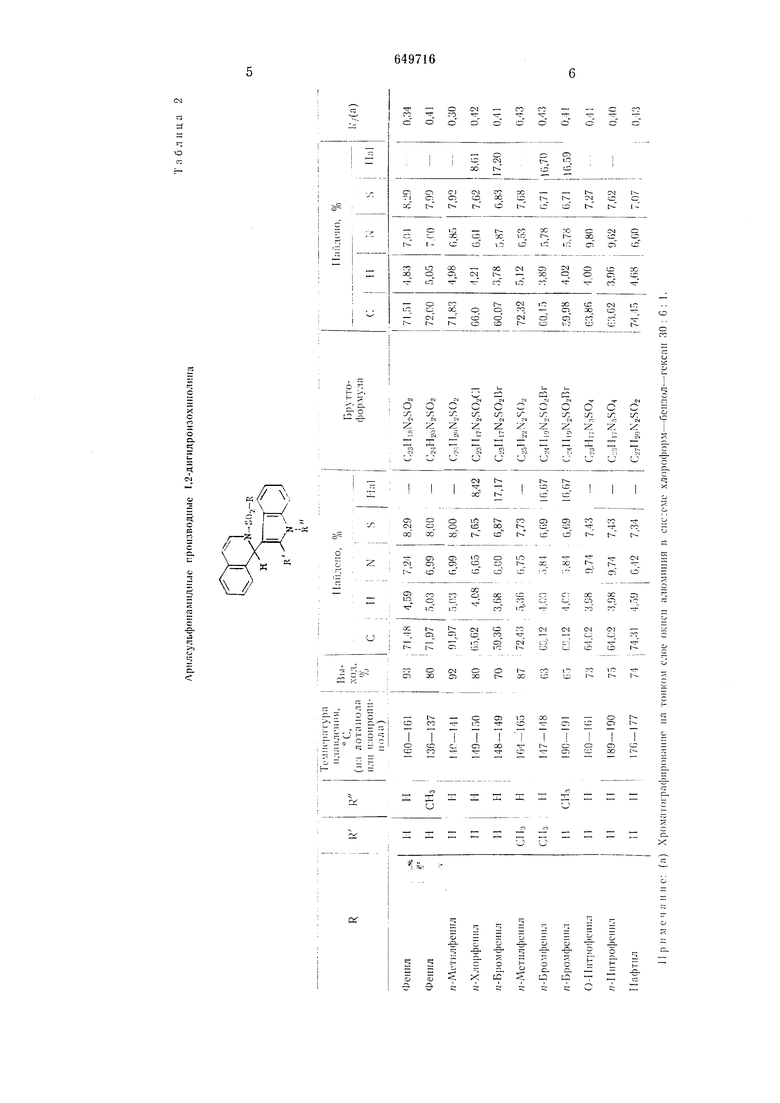
Характеристики арилсульфонамидных производных 1,2-ди.гндроизохинолинов приведены в табл. 2.
- со го -
X Г f c tOOO- CCCNC NOc
QOO j C4 «aDOOcr;
сс с: со
О
О О С С
J-. у с У} с/
Х
2
я:
е
(N 1
-
сс г--
о; 05
см
см о
- -
о го
Ci, СХ -
I I X С
Формула изобретения /
Способ получения арилсульфонамндных пропзводных 1,2-дпгидрОИзохинолнна формулы
,N-
где R - пндолил-3; 2-метилиндолил-З илп -метплиндолнл-З;
R - фенил, /г-метилфенил, /г-бромфеНИЛ, rt-хлорфенил, л-нитрофенил, О-нитрофеппл, нафтил.
отличающийся тем, что арплсульфохлорпд или замещенный арилсульфохлоркд подБергают взаимодействию одновременно с изолннолином и индолом или его производным 2-метил 1ндолом или N-метили.чдолом в среде шертного органического растворителя при температуре 18-20° С.
информации,
принятые во гкспертизе:

Авторы
Даты
1979-02-28—Публикация
1977-03-21—Подача