Изобретение относится к способу получения новых соединений - производных 1,2бензизотиазолинона-3 или их кислотноаддитивных солей, обладающих биологически активными свойствами. Известен способ получения биологически активных производных 1,2-бензизотиазолинона-3, в частности N-алкилпроизводных, диспропорционированием соответствующего 2,2-дитио-бис-бензамида, например, обработкой щелочью - водным раствором едкого натра, при нагревании 1. Целью изобретения является получение новых производных 1,2-бензизотиазолинона-3, расширяющих арсенал средств воздействия на живой организм. Эта цель достигается основанным на известной реакции способом получения производных 1,2-бензизотиазолинона-З формулы. .-(сНгЬ-ц, где RI и .Ri - одинаковые или различные, атом водорода или хлора, низший алкил или низшая алкоксигруппа; Ra-пиридил, пиримидинил, тиазолил, низший алкилтиазолил, морфолил, 3-азабицикло 3,2,2 нон-З-ил, пирролидинил, тетрагидрохинолино, тетрагидроизохинолино, 1,2 - бензизотиазолин-3 - он-2 - ил, ниридиламино, 4 - этоксикарбонилтиазол - 2-иламино, пиперидинил, низший алкилпиперидинил, 4 - этоксикарбонилпиперазинил или гомопипернди}шл; п - целое число от О до 6, или их кислотно-аддитивных солей, который заключается в том, что соединение формулы «н-(СНг) S где RI, R2 и RS имеют указанные значения, обрабатывают основанием, хлором или бромом и выделяют целевой продукт в свободном виде или в виде кислотно-аддитивной соли, Пригодные кислотно-аддитивные соли включают неорганические соли, например сульфаты, нитраты, фосфаты или бораты,
галогенводородные соли, например хлористоводородные или йодистоводородные, а также аддитивные соли органических кислот, например ацетаты, оксалаты, тартраты, малеаты, цитраты, сукцинаты, бензоаты, аскорбаты, метансульфонаты или «-толуолсульфонаты.
В качестве основания можно использовать 10%-ный водный едкий натр или водный раствор другой щелочи и реакцию можно осуществлять при комнатной температуре или при повышенной. Если применяют хлор, его барботировать через раствор соединения II в инертном растворителе, например четыреххлористом углероде.
Пример I. 5,6-Диметокси-2- |3-(2-пнридил)-этнл -1,2-бензизотиазолин-3-он.
К суспензии 4,4,5,5 - тетраметокси - 2,2дитиодибензоилхлорида (2,0 г; 4,32 ммоль) в безводном эфире (100-мл), содержащем
пиридин (4 мл), добавляют по каплям 2-(2аминоэтил) пиридин (1,60 г; 13,0 ммоль) в безводном эфире (50 мл) при перемешивании при комнатной температуре. Смесь перемешивают в течение 1 ч, оставляют на 18 ч, затем отгоняют растворитель при пониженном давлении. Раствор остатка в дихлорметане промывают водой, затем встряхивают с 2 н. соляной кислотой. Кислый
слой подщелачивают 10%-ным раствором гидроокиси натрия и смесь двукратно экстрагируют дихлорметаном. Органические экстракты соединяют и сушат над сульфатом магния. После удаления растворителя
получают твердое вещество желтого цвета.
После перекристаллизации из изопропанола получают продукт в виде игл кремового цвета (1,18 г; 43%); т. пл. 154,5-
156,5°С.
Аналогично получают соединения I, приведенные в табл. 1.
Таблица 1



Пример 5. По примеру 1, получают 5,6-диметил - 1 - (,р-1-пирролидинилэтил)-1, 2-бензизотиазолин - 3 - он; т. пл. 105- 107°С.
Пример 6. К перемешиваемой суспензии N,N-6uc- 2- (4-метил-2-тиазолил) -этил 2,2-дитио-б«с-бензамида (3,1 г, 5,6 ммоль) в четыреххлористом углероде (50 мл) в виде одной порцин добавляют раствор брома (0,89 г, 5,6 ммоль) в четыреххлористом углероде (10 мл). Смесь перемешивают при комнатной температуре в течение 10 мин. Полученный о-бромтио - N - 2-(4-метил-2тиазолил)-этил - бензамид отфильтровывают, промывают четыреххлористым углеродом, а затем суспендируют в ледяной уксусной кислоте (30 мл); после чего нагревают с обратным холодильником в течение 20 мин. Реакцио1П1ую смесь охлаждают, уксусную кнслоту отгоняют в вакууме, а
остаток подщелачивают 10%-ным водным раствором гидроокиси натрия. Смесь разбавляют водой (50 мл), экстрагируют дихлорметаном (2X50 мл) и органическую фазу сушат (безводным MgS04). После удаления осушителя и растворителя получают смолообразный продукт (3 г), из которого с выходом 68% в результате хроматографического разделения на глиноземе с применением дихлорметана в качестве элюента получают чистый (4-метил-2-тиазолил)-этил - 1,2-бензизотназолин - 3 - он (2,1 г); т. пл. 82-83°С.
Пример 7. По примеру 6 получают (4 - метил - 2 - тиазолил) -этил -5-метил-1,2 - бензизотиазолин-3-ои; т. пл. 129- 130°С; выход 42%.
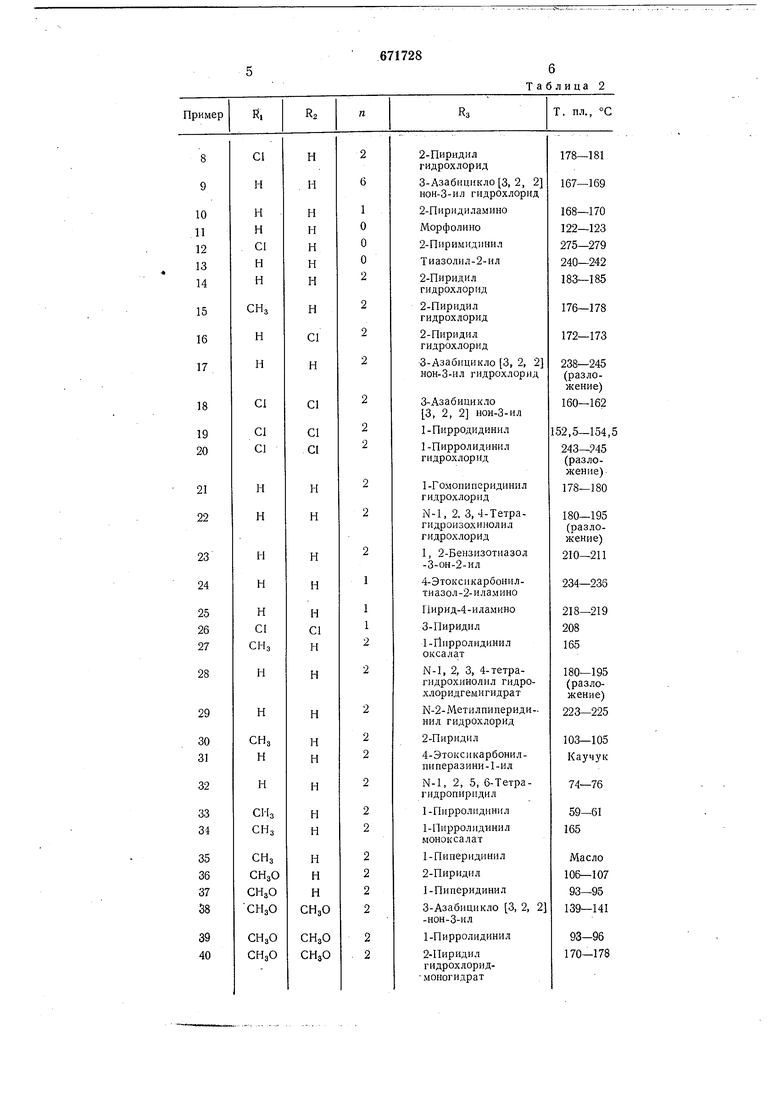
Аналогично примерам I и 6 получают соединения I, приведенные в табл. 2.
Таблица 2
Формула изобретения
Способ получения производных 1,2-бензизотиазолинона-3 формулы
1--.;::гХ,./
1 | w-(CHj)n-R3 -- ч . -.
где ,Ri и Ra - одинаковые или различные, атом водорода или хлора, низший алкил или низшая алкоксигрупиа;
Кз - пиридил, пиримидинил, тиазолнл, низший алкилтиазолил, морфолил, 3-азабицикло 3,2,2 нон-З-ил, пирролидинил, тетрагидрохинолино, тетрагидроизохинолино, 1,2-бензизотиазолин - 3 - он-2-ил, пиридиламино, 4 - этоксикарбонилтиазол - 2 - иламино, ниперидинил, низший алкилииперидинил, 4 -этоксикарбонилпиперазинил или гомопиперидинил;
Продолжение
л - целое число от О до 6,
или их кислотно-аддитивных солей, отличаюш,ийся тем, что соединение формулы
Г
1Ш-(,СНг)л-аз S
где Ri, Rz, RS и и имеют указанные значения, обрабатывают основанием, хлором или бромом и выделяют целевой продукт в свободном виде или в виде кислотно-аддитивной соли.
Источники информации, принятые во внимание при экспертизе . Патент США № 3517022, кл. 260-304, опублик. 1970.
Авторы
Даты
1979-06-30—Публикация
1977-04-04—Подача