1
Изобретенне относится к новым соеднненням формулы I
Осгт
где RI - алкил Ci-Сэ, С7, Сц,
Й4 - водород или метнл, и если R4 - метил, то RI - тоже метил,
проявляющим органолептнческий эффект.
При добавлении одного или более энолэфиров формулы I к употребляемым продуктам получают следующие эффекты.
В пищевых продуктах, отдушках для пищевых продуктов, жвачке, зубиой пасте и лечебных препаратах ароматы дамаскеиона, сладкий, какаоподобный, сухофруктов, фруктовый, яблочного сока, сладкого морковного сока, ладана, пряностей, дерева, древесной смолы, вииа, восточный, гвоздичный, камфарный, роз, мал1Г ны, малиновых листьев, винограда, фиалок, и/или ароматы цветов с ферменпфованным чаем и табаком; вкусы чая, нюансы табака и сладких овощей, чая, мимозы, груши, чернослива, древесный камфарный, кедровой щ евесной смолы, вина, сена, малиновых зернышек со сладким привкусом.
В табаке и табачных отдушках сладкий, изе5 точный, фруктовый, древесный, пряньш, слегка сладковатый аромат до курения и сладкий, табачный при курении.
В духах, одеколонах и подобных изделиях сладкий фруктовый, кисло-фруктовый, сухо 0 фруктов, цветочный, дамаскеиона, древесный, зелени, оттенки иоиона и нюансы табака и ферментированный чай и оттенки табака, коньяка, бальзама, табачные подтона.
Целью изобретения является расширение ассортимента соединений, которые проявляют органолептическнй эффект и могут быть использованы для придания (изменения, увеличения или улучшения) вкусов и ароматов различным материалам. Эти вещества используют для замены природных Материалов и для получения более однородных свойств в конечном продукте.
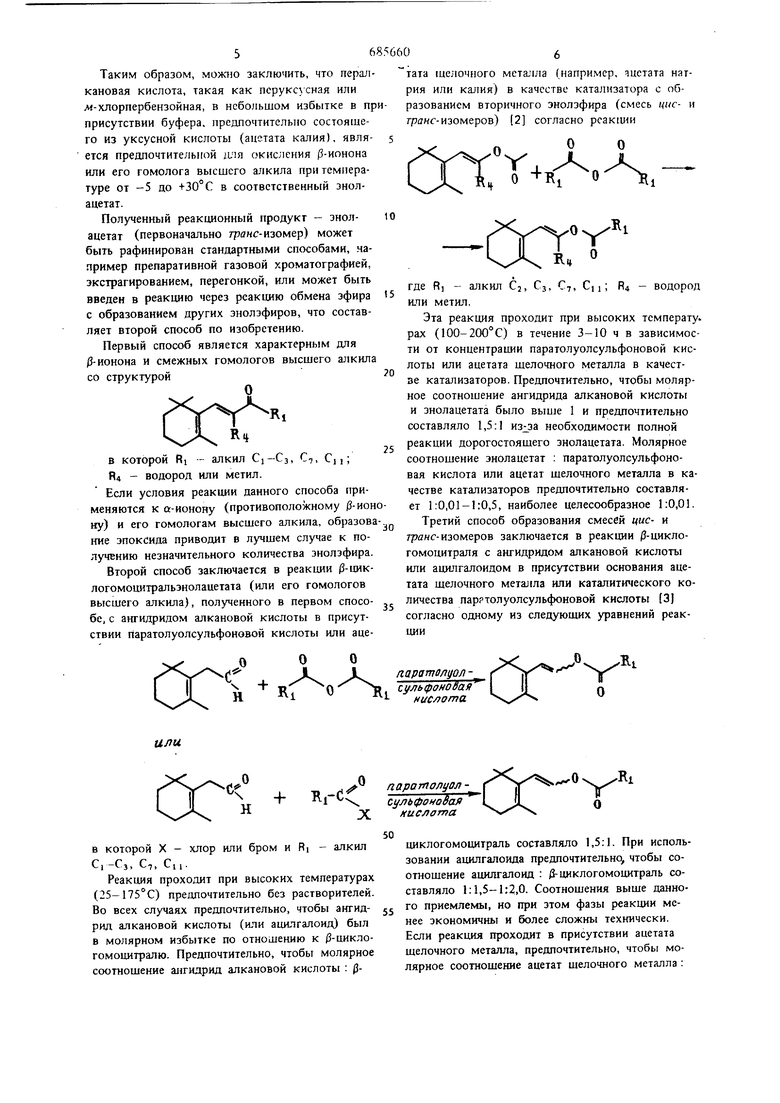
Соединения формулы I могут быть, получены одним из известных способов. 368 Один из способов заключается в реакции окиочсния ионона или гомолога высшего алкила (З-ионона пермуравьиной кислотой или перпропионовой или м-хлорпербензойной кислотой с образованием энолэфира f. В чвст 1ости, указанный способ включает реакцию |3-ионона или его гомолога высшего алкила формулы V д с перкислотой формулы к.-с 0-0-Н В которой RI, R4 имеют указанные значения, а Rj является либо водородом, этилом, метилом или л -хлорфенилом, в присутствии незначительного количества растворителей, которые реагируют с одним из реагентов (например, перкислотой), например N, N-диметиланилина, и, кроме того, в случае отсутствия буфера при отсутствии значительного количества растворителя - диметилформамида, в присутствии одного или более следующих растворителей: метиленхлорида, уксусной кислоты муравьиной кислоты, пропионовой кислоты, бен зола, циклогексана, формамида и хлороформа, с образованием jpanc- изомера энолэфира следующей формулы О .Hi и эпоксида, имеющего одну из формул Этот прюцесс предпочтительно проводить в присутствии буфера, например соли щелочного металла низщей алкановой кислоты или карбоната щелочного металла и в присутствии низщей алкановой кислоты, уксусной кислоты или муравьиной кислоты при указанных ниже условиях. Реакция пре шочтительно проводится при тем пературе от - 10 до + 75°С. При более низких тем iieparypiix реакция протекает не полностью и в некоторых случаях реакционная масса замораживается, а при температурах выще 75° С получают низкий выход целевого продукта и высокое процентное содержание побочных продуктов. Наиболее предпочтительный интервал температур от -5 до +30°С. Небольшой молярный избыток (10-15%) перкислоты дает более высокий выход продукта. Большой избыток (примерно 200%) приводит к образованию дигидроактинодиодила следующей структуры с выходом 30-35% без буфера (например, ацетата калия) в реакционной массе. При замене ацетата калия карбонатом калия в качестве буфера выход полученного продукта примерно тот же. Сравнительно низкий выход продукта получают при замене ацетата калия ацетатом натрия в качестве буфера. При замене уксусной кислоты муравьиной в реакционной массе получают низкий выход продукта. При отсутствии буфера (в сильно кислотных условиях) отмечаются неполная реакция, более низкий выход, значительное увеличение побочных продуктов II незначительный выход или отсутствие выхода энолэфира При использовании диметилформамида в качестве растворителя. Применение диметилформамида в качестве растворителя без буфера (например, ацетата натрия) приво:щт к исключительному, но очень медленному образованию -ионона эпоксида следующей структуры с выходом более 70%. Применение моноперфталевой кислоты (получешюй in situ из фталевого ангидрида и перекиси водорода) дает /3-иононэпоксид с выходом 60-70%. Поскольку А(-хлорпербензойная кислота применяется при получении энолэфиров по изобретению, использование пербензойной кислоты вместо пералкановой или.м-хлорпербензойной кислоты дает повыщеиный выход / -иононэп.оксида. Безусловно, при применении 2 молей пербензойной киспоты увеличивается образование соответственного эпоксиэноладетата. Применение пермалеиновой кислоты дает высокий выход /3-иононэпоксида и только следы целевого энолацетата. 56 Таким образом, можно заключить, что першь кановая кислота, такая как перуксусная или л«-хлорпербензойная, в небольшом избытке в пр присутствии буфера, предпочтительно состоящего из уксусной кислоты (ацетата калия), является предпочтительной IUIH окисления (5-ионона или его гомолога высшего алкила при температуре от -5 до +30°С в соответственньсй энолацетат. Полученный реакционный нродукг - знолацетат (первоначально троне-изомер) может быть рафинирован стандартными способами, например препаративной газовой хроматотрафией, зкстрагированием, перегонкой, или может быть введен в реакцию через реакцию обмена зфира с образованием других энолзфиров, что составляет второй способ по изобретению. Первый способ является характерным для -ионона и смежных гомологов высшего алкила со структурой в которой RI - алкил Cj-Сз, С, Cj i; R4 - водород или метил. Если условия реакции данного способа применяются к а-ионону (противоположному /3-ион ну) и его гомологам высшего алкила, образова кие эпоксида приводит в лучшем случае к получению незначительного количества знолэфира. Второй способ заключается в реакции -циклогомоцитральзнолацетата (или его гомологов высшего алкила), полученного в первом способе, с ангидридом алкановой кислоты в присутствии Царатолуолсульфоновой кислоты или аце0тата щелочного металла (например, эцетата натрия или калия) в качестве катализатора с образованием вторичного энолзфира (смесь цис- и гране-изомеров) 2 согласно реакш1и Оо оА,, где R - алкил Cj, С,, С,, С, i; R4 - водород или метил. Эта реакция проходит при высоких температу. pax (100-200°C) в течение 3-10 ч в зависимости от концентрации паратолуолсульфоновой кислоты или ацетата щелочного металла в качестве катализаторов. Предпочтительно, чтобы молярное соотношение ангидрида алкановой кислоты и знолацетата было 1 и предпочтительно составляло 1,5:1 ш:за необходимости полной реакции дорогостоящего знолацетата. Молярное соотношение энолацетат : паратолуолсульфоновая кислота или ацетат щелочного металла в качестве катализаторов предпочтительно составляет 1:0,01-1:0,5, наиболее целесообразное 1:0,01. Третий способ образования смесей цис- к транс-изомеров заключается в реакции -циклогомоцитраля с ангидридом алкановой кислоты или ацилгалоидом в присутствии основания ацетата щелочного металла или каталитического количества парятолуолсульфоновой кислоты (3J согласно одному из следующих уравнений реакции
ОО О
(JL JL лараглолдол -I- R, О , сульфоноеай
Н1 1- ниелота
О





















| название | год | авторы | номер документа |
|---|---|---|---|
| Способ изменения, модифицирования и усиления аромата и /или вкуса пищевых продуктов | 1978 |
|
SU988175A3 |
| Способ получения производных диизоамилена | 1981 |
|
SU1194268A3 |
| КОМПОЗИЦИЯ ДЛЯ АРОМАТИЗАЦИИ КУРИТЕЛЬНОГО ТАБАКА | 1992 |
|
RU2033739C1 |
| Способ изменения вкуса и запаха пищевых продуктов,вкусовых веществ и парфюмерных изделий | 1975 |
|
SU1098539A1 |
| Сложные эфиры 3-фурантиола в качестве вкусовых добавок к пищевым продуктам | 1975 |
|
SU583133A1 |
| АРОМАТИЗИРОВАННАЯ КОМПОЗИЦИЯ ДЛЯ УМЕНЬШЕНИЯ АДСОРБИРОВАННОГО ТАБАЧНОГО ЗАПАХА И СИГАРЕТА | 2012 |
|
RU2580682C1 |
| НОВЫЕ ПРОИЗВОДНЫЕ ПИРАНА, ИХ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ В ПАРФЮМЕРИИ | 2009 |
|
RU2577250C2 |
| НОВЫЕ БИЦИКЛИЧЕСКИЕ ДИОКСАНЫ, ИХ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ В КАЧЕСТВЕ АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ | 2010 |
|
RU2562973C2 |
| Способ изменения органолептических свойств продуктов потребления | 1974 |
|
SU580804A3 |
| Способ изменения вкуса и запаха пищевых продуктов,вкусовых веществ и парфюмерных изделий | 1975 |
|
SU731951A1 |

ч- ИгС
паратолуал -
сульфоно8ая
о кислота
в которой X - хлор или бром и RI - алкил С,-С,, С,, Си.
Реакция проходит при высоких температурах (25-175°С) предпочтительно без растворителей. Во всех случаях предпочтительно, чтобы ангидрид алкаиовой кислоты (или ацилгалоид) был в молярном избытке по отношению к (3-циклогомоцигралю. Предпочтительно, чтобы молярное соотношение ангидрид алкановой кислоты : циклогомоцитраль составляло 1,5:1. При использовании ацилгалоида предпочтительно, чтобы соотнощение ацилгалоид : Д-циклогомоцитраль составляло 1:1,5-1:2,0. Соотношения выше данного приемлемы, но при зтом фазы реакции менее экономичны и более сложны технически. Если реакция проходит в присутствии ацетата щелочного металла, предпочтительно, чтобы молярное ссютнощение ацетат щелочного металла:
циклогомоцитраль составляло около 0,1:1. Если реакция проходит в присутствии ацетата щелочного металла, то она протекает при высоких температурах (100-200°С) в течение 310 ч. Если реакция проходит с применением катализатора в виде паратолуолсульфоновой кислоты, предпочтительно, чтобы молярное соотношение lJ-циклогомоцитраль : паратолуолсульфоновая кислота составляло 1:0,01-1:0,1, наиболее подходящее 1:0,02. При применении в качестве катализатора паратолуолсульфоновой кислоты реакцию проводят при нагревании с обратным холодильником в течение 10 ч в зависимости от экономичности способа и целевого выхода.
Один или более энолзфиров по H3o6peTeFiHKi способен придавать и/или сделать возможными некоторые нотки вкуса и аромата, которых обычно недостает многим фруктовым вкусам (например ягод, включая малину, винограда и яблочного сока), гвоздичный вкус, вкус корицы, чая, меда, сухофруктов, вина и какао, а также табака. Кроме того, /3-циклогомоцитральзнолзфиры по изобретению придают некоторые нотки, недостающие многим изделиям парфюмерии, например, роз. Нижеследующая табл. 1 дает органолептические свойства специфических знолэфировпо предмету изобретения.
ё
а
о
s о
5
(U
2
«
нч
о.
I S
е с
U
s о
S
и а са
,
1
X
1
4J и
SSIi
§8S§,
о2о :
X0ия
g 15Г1 Термигы HiiNTCiiHih, смягчать и увеличинать означают приданать н.чи сог) вкусошм характер или ноту сраиншсльмо безвкусопым веществам или увеличипать существующий вкус, если природный нелостаточен. или придавать существующие икусо ые впечатления с изменением качества, характера. Термин улучи1ать означает И11Т{Ч1Сифищфовать вкусовые или ароматические характеристики или ноту без изменения качества. Термин нищевой продукт включает твердые и жилкие съедобные материалы, которые имеют пищевое предназначение. 1ищевые продукты включают супы, съестные припасы, напитки, ежедневную пищу, сладости, овонхи, злаки, прохдтадите.чьные напитки, закуски и т. д. Термин лекарственный продукт включает твердые и жидкие вещества, принимаемые внутрь нетоксичные материалы, которые имеют медицинское предназначение, например сиропы и ка ли от каи1ля, аспирин и таблетки, которые необходимо жевать. Термин жвачка подразумевает композицию, которая включает водонерастворимую жевательную резинку, например жвачку или ее заместители, вк.лючая студенистые, гутаксевые каучуко вые или некоторые натуральные или синтетические смолы или воски. Вместе с основной резинкой в смеси могут быть пластификаторы или агенты размягчения, например глицерин, и отдушки, которые включают один или более предлагаемых энолзфиров и, кроме того, агент подслашения, например сахара, включая сахаро или декстрозу и/или искусственные подсластите ли, например цикламаты или сахарин. Можно вводить также друтие факультативные ингредиенты. Вещества, применяемые в качестве соингредиентов или вкусовых присадок, хорощо известны и описаны в литературе. Необходимо, чтобы такой материал можно было легко глотать, чтобы он был нетоксичным, а также не отставал от органолептического стандарта, т. е. вкус и/или аромат материала не должен изменяться под действием аромата и вкуса присадок. Такие вкусовые присадки включают стабилизаторы, отвердители, поверхностно-активные вещества, ко}иищионеры и другие вкусовые интенсификаторы. Очевидно, что энолэфир или смеси зфиров по изобретению можно использовать для смягчения, изменения или улучшения сенсорных качеств, в частности ортанолептических, например аромата и/или вкуса разнообразных материалов. Пример 1-8, 10, 17, 25, 26, 34, 42-44, 4752, 54-58 и 64 служат jvifl иллюстрации способов получения энолэфиров по изобретению. Примеры 9 и 53 показывают, что невозможно осуществить один из этих способов, когда используют диметилформамид при отсутствии неортанического буфера в окислительной реакции / -ионо)1а с перуксусной кислотой. Пример 3 показывает, что реакция невозможна без буфера, например ацетата натрия. Пример 45 доказывает невозможность проведения способа с применением ангидрида перфталевой кислоты в качестве агента окисления. Пример 46 свидетельствует о том, что невозможно проводить способ с использованием диметила1шлинового растворителя, в котором диметиланиЛИН окисляется над /З-иононом. Примеры 11-15, 18-24, 27-30, 35-40 и 60-62 иллюстрируют полезность знолэфиров по изобретению. Пример 16 иллюстрирует возможность проведения способа при образовании а-иононолэфира при применении а-ионона. Все части и процентное содержание даны по весу, кроме особо указанных случаев. Пример 1. Получение трдис- З-циклогомоцитральэнолацетата из /3-ионона. В сосуд емкостью 2 л, снабженный мешалкой, термометром, обратным холодштьником, воронкой и кожухом охлаждения, вводят раствор 96 г |3-ионона в 300 см хлороформа и 90 г ацетата натрия. Затем добавляют 95 г 40Л-ной перуксусной кислоты при охлаждении до 100°С в течение 1 ч. Реакционную массу перемешивают при 10°С еще в течение 1 ч и затем раствор оставляют медленно нагреваться до комнатной температуры. Выливают в 1 л воды и отделяют полученные органическую и водную фазы. Водную фазу экстрагируют 100 см х;гороформа и полученные органические фазы отводят. Растворитель упаривают из органической фазы с получением 99,5 г масла, которое затем подвергают хроматографии на 1000 г дезактивированного глинозема и злюируют. Ниже приведены полученные результаты.
Фракции 1 -4 состоят в основном из фднс-Р-11иклогомоцитральэнолацетата.
Примеры 2-10. При использовании технологии примера 1 иллюстрируют результаты, когда изменяются параметры реакции окисления (3-иоиона и перуксусной кислоты, например бу47
24
12
52
40
29
52
25
30
31
49
21
36
фер, растворитель, температура органического основания и соотношение органической алкановой кислоты и перуксусной кислоты. Полученные результаты приведены в табл. 2. Данные процентные соотношения полу}ены хроматографическим анализом-реакционной смеси через 30 мин. и не дают выхода материала.
1аблица 2
Уксусная кислота 150 см
Ацетат натрия 20 г /3-Ионон 30 г Перуксусная кислота 20 г
Уксусная кислота 150 см
-Ионон 30 г Перуксусная кислота 30 г
Циклогексан 150 см
Ацетат натрия 20 т -Ионон 30 г Перуксусная кислота 30 г
Уксусная кислота 150 см
Ацетат калия 35 г -Ионон 30 г Перуксусная кислота 30 г
Муравьиная кислота 150 см
Ацетат калия 50 г -Ионон 30 г Перуксуснал кислота 30 г
Уксусная кислота 150 см
Ацетат калия 35 г Ионон 30 г Перуксусная кислота 33 т
Уксусная киагота 150 см
Ацетат калия 35 г -Ионон 20 г Перуксусная кислота 33 г
55
17
10 Примечание: 1.Во вс кислоту 2.В при 4 дня 1 Пример 11. Розовый состав. Для иллюстрации применения 7ранс-(3-ц гомоцигральэнолацетата в розовом состав чена следующая композиция (вес. ч.) : Фенилэтиловый спирт Гераниол ТрихлорметилфенилкарбонилацетатФенилэтилацетат Ундециленовый альдегид (10% в диэтилфталате) «-Ионилальдегид (10% в дизтилфтапате) Мускусный кетон Мускусный амбрз Эугенолфенилацетат Цитронелол; Ванилин (10% в диэтилфталате) Эугенол Цитронелкл формат Геранилацетат Линаллол. Геранилфенилацетат иис- 7 - Гексенилацетат гране- Цик логомоцитральэнолацетат, полученный по примеру 1 Добавка 0,6% циклогомоцитральэнол дает больше крепости розовому благоух Походит на цветущий и тяжелый натурал сладкий розовый аромат. Продукт обычно применяется в колич ® 01-10% в композициях для косметики (Получения специального эффекта можно нять более высокие концентрации (боле Пример 12. Получение композиции
Продолжение тзбл. 2
Диметилформамид 150 см (3-Ионон 30 г Перуксусная кислота 33 г
Уксусная кислота 150 см Ацетат калия 105 г -Ионон 96 г Перуксусная кислота 105 т используют 40%-ную перуксусную 10 температура 25°С, в примере 9 100 г мыльных стружек сменшвают с 1 г омпозиции по примеру 11 до получения гомоенной композиции. Мыльная композиция дает яркий розовый аромат со сладкими, цветными и фруктовыми нотами. Пример 13. Получение детергентной композиции. 100 г детергентного порощка смещивают с 0,15 г композиции по примеру II до получения гомогенной композиции. Великолепный розовый аромат со сладкими, цветочнымн и фруктовыми нотами. Пример 14. Состав малинового вкуса. Получают следующий состав с малиновым вкусом (вес. ч.): Ванилин2,0 Мальтон5,0 Парагидроксибензилацетон5,0 а-Ионон (10% в пропиленгликоле)2,0 Этилбутират6,0 Этилацетат16,0 Диметилсульфид1,0 Изобутилацета т13,0 Уксусная кислота10,0 Ацетальде1ид10,0 Пропиленгликоль930,0 транс- (3- Циклогомоцитральэнолацетат добавляют к половине указанного состава в количестве 2,0%. Состав без -циклогрмоцитральэнолацетата сравнивают с составом с -цнклогомоцитральэнолацетатом в количестве 0,01% (100 ч. на 1 тыс) в воде. Аромат состава, содержащего 7ранс-/3-циклогомоцитральэнолацетат, имеет более сладкие ноты и сладкий малиновый, малиновых зернышек и сладкий послевкус, недостающий в основной малиновой композиции. Шкала указывает, что 21 /раи -{3-цнклогомоцитральэнопацетат придает вкус и очень походит на натуральный аромат и вкус малины. Пример 15. Готовый морковный сок тща тельно смешивают с 15 ч,з I тыс. транс- -циклогомоцитральэнолацетата и затем полученную смесь сравнивают с тем же неразбавленны соком. Аромат и вкус заметно улучшены и да ют ноту свежего морковного сока и сладости. Оценки пяти человек показывают, что предпочи тается разбавленный сок с 7ракс-(-циклогомоцитральэнолацетатом. Пример 16. Состав а-иононэпоксида из аионона. В сосуд емкостью 50 мл, снабженный термо метром, мешалкой, воронкой и обратным холодильником, помешают материалы в следующем порядке; Уксусная кислота150 см Ацетат калия35 г а-Ионон30 г Затем по каплям добавляют 33 г 40%-ной перуксусной кислоты при перемещивании при 25. С в течение 15 мин. Происходит экзотермическая реакция в течение 1 ч, и затем массу оставляют для доведения до комнатной температуры в течение 15ч. Реакционную массу затем выливают в 500 мл воды и продукт экстрагируют трижды по 150 см диэтилэфира. Эфирные экстракты собирают и промывают дважды по 100 см насыщенного раствора хлорида натрия и сушат над безводны сульфатом магния. Остаточное масло получают после отделения растворителя и перегонки при 93-99°С, при 0,5 мм рт. ст. с выходом 23,3 г чистой бесцветной жидкости. Пример 17. Получение трднс-р-циклогомо цитральэнолацетата. в сосуд емкостью 2 л, снабженный мешалко термометром, дополнительной воронкой и охлаждением, загружают материалы в следующем порядке: Уксусная кислота150 Ацетат калня105 г Э-410НОН96 г добавляют 105 г 40%-ной перуксусной кислоты по каплям при охлаждении при поддержании массы 25 ± 2°С в течение 2 ч. Затем перемешивают еще 3 ч( течение первого часа .легкий экзотермический эффек1 при 25°С. Затем реакционную массу выливают в 1000 мл воды и полученный продукт экстрагируют триж ды по 300 см объема диэтилэфира. Эфирные экстракты соб1фа1от и промывают дважды по 150 см насыщенного раствора хлорида натрия. Полученный промытый эфирный экстракт выпа ривают и получают 113 г масла, ЯМР, ИК и МС 0 анализы подтверждали, что материал являлся 777от г-/3-циклогомоцитральэнолацетатом. Пример 18. Табачный состав. Получают табачный состав при смешивании следующих ингредиентов (вес. ч.): Брайт40,) Барлей24,9 Мериленд1,1 Турецкий11,6 Стим14,2 Глицерин2,8 Вода5,3 изготавливают из этого табака. Получают спепующт вкусовой состав (вес. ч.): Этилбутират0,05 Этилвалерат0,05 Малтол2,00 Экстракт какао26,0 Экстракт кофе10,0 Этиловый спирт20,0 Вода41,90 Указанный табачный состав наносят в количестве 0,1% на все сигареты, полученные из указанного состава табака. Затем половину сигарет обрабатывают 500 или 1000 ч, на 1 тыс. гранс- циклогомоцнтральэнолацетата, полученного по примеру 17. Контрольные сигареты без транс-f-циклогомоцитральэнолацетата и зкспериментальные сигареты с содержанием трснс- циклогомоцитральэнолацетата, полученного по примеру 17, сравнивают и оценивают, получают следующие результаты. Экспериментальные сигареты при курении были слаще, ароматнее, более табачнь1е и со сладкими, цветочш 1ми и фруктовыми нотами. Табак экспериментальных сигарет до курения имеет сладкие, цветочные и фруктовые ноты. Все сигареты оценивают на вкус курения с 20 мл фильтра из целлюлозоацетата. транс- /3- Циклогомоцитральэнолацетат, полученный по примеру 17, улучшает табачный вкус и аромат сигарет и придает им сладкие натуральные табачные ноты. Пример 19. Получение композиции для косметической пудры. Косметическую пудру получают смешиванием в шаровой мельнице 100 г талька с 0,25 г транс- циклогомоцитральэнолацетата по примеру 17. на имеет прекрасный сладкий, цветочный, руктовый аромат. Пример 20. Парфюмерный жидкий детергент. Концентрированные жидкие детергенты со сладким, цветочным и фруктовым запахом получают с содержанием 0,10, 0,15 и 0,20% транс-/ -циклогомоцитральэнолацетата, полученного по примеру 17. Их цолучаю введением и гомогенным смешнванием соответствующего количе236ства фанс-/3-|ц1клогомоцентральэнолацетата в жидком детергенте. Детсрге}гты обладают сладким, цветочным, фруктовым ароматом, интенси ность его возрастает с увеличнием концентрации 7раис-/3-циклогомо1щтральэиолацетата. Пример 21. Получение одеколона и духов для носовых платков. трднс- -Циклогомоцитральэнолацетат по примеру 17 вводят в одеколон при концентрации 2,5% (в водном этаноле) и в духи для носовых платков нри концентрации 20% (в 95%-ном водном этаноле). Ясный и определенный сладкий, цветочный, фруктовый аромат придается одеколону и духам. Пример 22. Получение одеколона и духов для платков. Композицию по примеру 11 вводят в одеколон при концентрации 2,5% (в 85%-ном водном этаноле) и в духи при концентрации 20% (в 95%-ном водном этаноле). Применение -диклогомоцитральэнолацетата в композиции по при меру 11 придавало ясный и определенно крепкий розовый аромат со сладкими, цветочными и фруктовыми нотами одеколону и духам. Пример 23. Получение мыльной композиции. 100 г мыльных стружек смешивают с 1 г 1ракс- циклогомоцитральэнолацетата до получения гомогенной композиции. Композиция им ет прекрасный сладкий, цветочный, фруктовый аромат. Пример 24. Получе1ше детергентной композиции. 100 г детергентного порошка смешивают с 0,15 г77мнс-0-циклогомоцитральэнолацетата по примеру 17 до получения гомогенной компози ции. Она имеет сладкий, цветочный, фруктовы аромат. Пример 25. Получают перпропионовую кис лоту следующим образом. Смесь материалов (А): 160 мл пропионовой кислоты 1 мл серной кислоты (концентрирова1шой) 40 г 50%-ной перекиси водорода оставляют на 20 ч при комнатной температуре. Следующие реагенты (смесь Б) помещают в сосуд емкостью 500 мл, снабженный мешалкой и охлаждением: 140 мл пропионовой кислоты 75 г ацетата калия 60 г Э-нойона К перемешанной смеси Б добавляют по каплям смесь А в течение 60 мин при 25 ± 2 С пр при охлаждении извне. После завершения введе ния реакционную смесь оставляют на 2 ч при 25°С. Реакционную смесь затем выливают в 1000м воды и дважды экстрагируют по 250 мл диэгилэфира. Собранные эфирные экстракты промывают вначале водой (трижды по 100 мл) и затем насыщенным раствором хлори,ца натрия (150 мл). Затем эфирный раствор сушат над безводным сульфатом магния и упаривают растворитель с получением 78 г неочищенного масла, содержащего пропионовую кислоту и транс-/3-циклогомоцитральэнолацетат. Пример 26. Пермуравьиную кислоту получают следующим образом. 20 г 50%-ной перекиси водорода и 80 мл муравьиной кислоты смещивают, реакционную массу оставляют при комнатной температуре на 1,5 ч. К смеси, состоящей из 50 г ацетата калия, 70 мл уксусной кислоты и 30 г |3-ионона, добавляют Пермуравьиную кислоту, полученную выше, по каплям в течение 30 мин при под(Держании температуры перемещиваемой реакционной массы 25°С путем внепшего охлаждения. После завершения добавления смесь перемешивают еще 90 мин при 25° С и затем выливают в 800 мл воды. Продукт экстрагируют дважды по 200 мл диэтилэфира. Эфирные экстракты собирают, промывают дважды по 150 мл насыщенного раствора хлорида натрия и затем сушат. При упаривании растворителя получают 32,5 г неочищенного масла. Пример 27. 10 вес. ч. желатины добавляют к 90 вес. ч. воды при 150°Ф. Смесь перемешивают до полной желатинизации и раствор охлаждают до 120 Ф. 20 вес. ч. жидкой комПОЗИ1ШИ по примеру 14 добавляют к раствору, образуется эмульсия с размером частиц 2- 5 мкм. Материал хранят при во избежание кристаллизации желатины. Коацервацию проводят путем медлешюго и равномерного введения 40 вес. ч. 20%-ного раствора сульфата натрия. В процессе коацервации молекулы желатины равномерно располагаются на каждой капле масла. Застудневание осуществляют путем соединения нагретой коацервированной смеси в 1000 вес .ч. 7%-ного водного раствора сульфата натрия при 65°Ф. Полученный кристаллизованный коацерват можно профильтровать и промыть водой при температуре ниже точки плавления желатины для удаления соли. Затвердевания фильтровального осадка добиваются путем промывки 200 вес. ч. 37%-ного раствора формальдегида в воде. Затем кусок промывают для удаления остаточного формальдегида. Пример 23. Жевательная резинка. 00 вес. ч. жвачки смещивают с 4 вес. ч. вкусовой композиции, полученной по примеру 27, 300 ч,сахарозы, добавляют 100 ч кукурузного сиропа и смешивают в-смесителе с двойными боковыми стенками. 25 Попученную смесь жевательной резинки зат раскатывают в полоски шириной 25,4 мм и толщиной 2,54 мм. Полосы затем режут на резки длиной 76,2 мм. При жевании получаю стойкий и приятный вкус малины. Пример 29. Жевательная резинка, 100 вес. ч. жвачки смешивают с 18 вес , ч композиции по примеру 28. Добавляют 300 сахарозы и 100 ч кукурузного сиропа. Смеш вают в смесителе с двойными стенками. Полученную смесь затем раскатывают на п лосы шириной 25,4 мм и толщиной 2,54 мм режут на части длиной 76,2 мм. При жевании получали стойкий малиновый вкус. Пример 30. Витаминные таблетки для ж вания. Материал примера 19 добавляют к составу жевательных витаминных таблеток в количест ве 100 г/кг, а указанные таблетки получают рледующим образом. В миксере перемалывают до однородности следующие материалы (1000 таблеток): Витамин С (аскорбиновая кислота) - смесь аскорбиновой киспоты и аскорбата натрия 1:1 Витамин BI (тиамин мононитрат) - Рокоат тиамин мононитрат, 33 л/3% (Гофман.ла Рош) . Витамин 82 (рибофлавин) - Рокоат рибофлавин, 43 л/3% Витамин Е (пиридоксигищ)охлорид) - Рокоат пиридоксингидрохлорид, 33 л/3% Ниацинамид-Рокоат ниаюшамид, 32 л/3% Пантотеиат кальция Витамин BU (цианокобаламин). Мерк 0,1% в желатине Витамин Е - сухой витамин Е ацетат, 32 л/3% а- Биотин Краплак (Как ук композиция примера 27 зано вы ше) Сахариниатрий (подслащение) Стеарат магния (смазка) Манитол 14 меш. Вначале перемалывают до размера Затем добавляют 13,5 г сухого витамина А ацетата и 0,6 г витамина D в виде шариков. Затем из материала на прессе получают табле ки 0,5 г. При жеваний получают приятный ст кий вкус малины в течение 12 мин. Пример 31. Получение -циклогомоцитральэнолбутирата. Реакция 0 о . tHScb цис/транс В сосуд емкостью 100 мл добавляют следующие материалы: -Циклогомоцитраль16,6 г (0,1 моля) Масляный ангидрид27,0 г (0,17 моля) Ацетат калия1 г (0,01 моля) Реакционную массу нагревают при 170° С 9,5 ч. В этот период времени анализ ГЖХ указывает на почти полное исчезновение Д-циклогомоцитраля и образование двух новых пиков. ГХ, МС анализ указывают, что пики представляют собой цис- и ipflKc-изомеры -циклогомоцитральэнолбутирата со структурами: Неочищенную реакционную массу, полученную выше, смешивают с 100 мл диэтялэфира. Полученный раствор диэтилэфира промывают дважды по 100 мл воды и одаой порцией в 25 мл насыщенного бикарбоната натрия. Промытый эфирный раствор сушат над безводным сульфатом магния, фильтруют и отгоняют с получением 32,4 г продукта, содержащего значительное количество знолбутирата. Компоненты отделяют подготовительной ГЖХ. транс- Циклогомовдгтральэиолбутират при концентрации 2 ч. на 1 тыс. имеет сладкий, розовый, фруктовый аромат. При 5 ч, на 1 тыс. сладкий-розовый, розовых бутонов, розовыйфруктовый аромат и розовый-фруктовый вкус. При 20 ч. иа 1 тыс. сладкий-розовый, фруктовый аромат и вкус с деликатным оттенком дамаскеона. Чыс-|8-ЦиклЬгомоцитральэнолбут1фат при 0.2 ч, а1 тыс. имеет горький послевкус. При 2 ч. на 27 1 тыс. слабый розовыГт аромат; при 6 ч. на 1 тыс. слабый розовый аромат и горький гюслев кус. 685660 Пример 32. Получение |3-циклогомоцитральэнолбутирата. Реакция В реакционный сосуд емкостью 100 мл зафу жают следующие материалы: (3-Циклогомоцитраль16,6 г (0,1 моля) п-Толуолсульфоновая г (0,03 моля) кислота0,5 Масляный ангидрид39,5 г (0,25 моля) Реакционную массу нагревают при перемешивании до и выдерживают при этой темпе ратуре 9,5 ч. Неочищенный материал перемешивают со 100 мл эфира и полученный эфирный раствор промывают дважды по 100 мл воды и 25 мл бикарбоната натрия. Промытый эфирный раствор затем сушат над безводным сульфатом магния, фильтруют и отгоняют на выиаривателе. Полученный продукт весит 32,4 г и содержи значительную порцию; . Д-циклогомоцитральэнолбутирата. 25 мл диэтилэфира смешивают с неочищенным продуктом и эфирный раствор прюмывают дважды по 25 мл воды и 25 мл раствора бикарбоната натрия. Промытый эфирный раствор затем супит над безводным сульфатом магния, фильтруют и отгоняют в выпаривателе с получе нием продукта, содержащего значительное количес во транс-0-циклогомоцитральэнолбутирата. П р и м е р 33. Витаминные таблетки для жевания. Материал примера 19 добавляют к составу жевательных витаминных таблеток в количеств 100 г/кг, а указанные .таблетки получают следующим образом. В миксере следующие материалы перемалывают до однородности (100 таблеток) 1 1 н Витамин С - смесь аскорбиновой кислоты и аскорбата натия 1:170,0 Витамин BI (тиамин мононитрат) Рокоат тиамин мононитрат, 33 л/3% (Гофман ла Рот)4,0 транс- Изомер (- циклогомоцитральзнолизобутират имеет сладкий, древесный, розовый, фрук товый, розового куста, пряный, яблочиого сока аромат с фруктовой, яблочной-малиновой древесной, сладкой, розового куста, чая вкусовой характеристикой. В отношении парфюмерных качеств он имеет кислый, фруктовый, дамаскеноновый аромат с крепкими нюансами табака, крепче (ыс-изомера по указанным качествам. чис-Изомер циклогомоцитральэнолизобутират имеет сладкий, восточный, деликатный розовый, фруктовый, иононовый, гвоздичный, камфарный аромат с розовой, древесной, гвоздичной, мимозной, иононовой, мускусной и камфарной характеристиками по вкусу. В парфюмерии имеет сладкий, древесйый, зеленого табака аромат с фруктовыми и смолистыми нотами, не такой фруктовый, как факс-изомер. i uc-Изомер имеет также крепкие иононовые и мимозные нюансы. Следует отметить, что цис- и трамс-изомеры имеют примеиения для вкусов, отличньп один от другого, чмс-Изомер применяется в гвоздичных и коричных вкусах, а транс-изомер в яблочном соке, чае, малине и меде. Пример 34. Получение циклогомоцитральзнолоктаноата. Реакция
Сс
в реакционный сосуд емкостью 100 MJF, снабженный мешалкой, термометром и обратным холодильником, загружают следующие ингредиенты: (3-Циклогомоцитраль16,6 г (0,1 моля) Октановый ангидрид41 г (0,17 моля) Ацетат калия1 г (0,01 моля) Реакционн -ю массу нагревают 1 ч при 170190°С. Затем добавляют 100 мл диэтилэфира после охлаждения реакционной массы до комнатной температуры. Полученную смесь затем промывают дважды по 100 мл воды и 100 мл насыщенного водного бикарбоната натрия. Органический слой отделяют от водного слоя, затем сушат над безводным сульфатом магния, фильтруют, отгоняют растворитель с получением 31,4 г масла. 1 «с-Изомер имеет сладкий, розовый, Дамаскеноновый сухофруктовый, какао аромат и сладкий, деликатный розовый, черносливовый, чайный, яблочного сока, табачный вкус. транс-Изо мер имеет иононовый, древесный аромат с ион новым, древесным, мускусным вкусом. чис-Из мер предпочтительнее транс-изомера привыбор вкуса. Для парфюмерии: чмс-изомер имеет древесный, жирный, довольно острый аромат с нюансами ионона; транс-изомер имеет древесный, жирный аромат с более теплыми, фруктовыми нотами, чем чыс-изомер, с коньячными, бальзамовыми и табачными нюансами. Пример 35. Основной малиновый состав, содержащий чыс-3-циклогомоцитральзнолбутнрат Получают следующий основной малиновый состав (вес. ч.): Ванилин2 Мальтон4 Парагидроксибензилацетон5ot-Ионон (10% в пропиленгликоле) Этилбутират Этилацетат Диметилсульфид Изобутил ацетат Уксусная кислота Ацетальдегид Пропиленгликоль Состав делят на две части. К первой добавляют «ыс- циклогомоцитрапьзнолбутират по примеру 32 в количестве 100 ч. на 1 тыс. в ви де 5%-ного раствора в пищевом водном этаноле. Ко второй части ничего не добавляют. Сравнивают составы. Предпочтителен состав, содержащяй 4UC-изомер циклогомоцитральзнолбутирата, он имеет сладкий малиновый аромат и вкус. Пример 36. Вкусовой состав с применением циклогомоцитральэнолоктаноата. В количестве 3 ч. на 1 тыс. (ыс-(3-цикло1омоцитральэнолоктаноат по примеру 34 добавляют к стандартному составу чая для мгновенного приготовления. Чай получают с добавлением кипящей воды. Горьковатые, танинные ноты горячего чая значительно улучшены путем добавления ч«с-изомера -циклогомоцитральэнолоктаноата. Фруктовая-деликатная розовая, приятная чайная нота аромата и фруктовый-де ликатный, розовый-чайный вкус добавлены к основному вкусу чая и аромату путем добавления / «с-изомера /3-циклогомоцитральэнолокта оата. Пример 37. Вкусовой состав с применением транс-изомера (З-циклогомоцитральзнолизо- бутирата. В количестве 3 ч, на 1 тыс. транс-изомер Дциклогомощпральзнолизобутнрата добавляют к стандартному чаю мгновенного приготовления. До добавления чай не имеет чайного аромата. Доминируют танинные ноты. При добавлении транс- изомера р- циклогомоцитральэнолизобутирата в количестве 3 ч на 1 тыс. к горькому чаю с последующим добавлением кипящей воды получают легкий, фруктовый, яблочный, прятный чайный аромат и улучшенный вкус с деликатными-фруктовыми чайными нотами. Пример 38. Использование изомера -циклогомоцитральзнолбутирата в напитке. В количестве 1 ч, на 1 тыс. транс-изомер (3циклогомоцитральзнолбутирата по примеру 36 добавляют к напитку (содержащему 10% вкноградного сока). Добавление транс-изомера /3-циклогомоцитральзнолбутирата к напитку в количестве 1 ч.на 1 тыс. в виде 1%-ного раствора пропиленгликоля улучшает высокие ноты и придает деликатный виноградный вкус и аромат. Пример 39. Основной гвоздичный состав с применением цмс-изомера /3-циклогомоцитральэнолацетата. Получают следующий гвоздичный состав (вес. ч.): Ванилин2 Кариофилен8 Гуанколь (10%-ный раствор в 95%-ном водном пищевом зтаКуминальдегид5-Метилфурфурол Эуагенол Состав делят на две части. К первой добавляют в количестве 5% «ые-изомер -циклогомоцитральэноладетата по примеру 52 (ниже). Вторая часть остается без изменений. Примене1ше j{uc-изомера 1щклогомоцитральэнолацетата в основной гвоздичной композиции придает ей аромат и вкус cyxoio д(-рсва. Н результате добавления цис- изоме|1; 1и1клогч)М(И.и фаль зполацетата получают более деликтный гв(глчичнмн аромат, слегка горьковатый. I р и м е р 40. И.ъчучеиие 7/м/(г-/1-и.иклогомоцитральлюлпроииоиатаРеакция -f-HjC-C kjkо в сосуд емкостью 250 мл, снабженный мешалкой, воронкой, термометром и охлаждением, загружают следуюнше ингредиенты: п-Метилионон (9Гл-ной чистоты)22,6 г (0,1 моля) Вода40 мл Уксусная кислота50 мл Ацетат натрия17 г (0,17 моля) Массу перемеишвают 10 мин при комнатной температуре и добавляют 24,0 г (0,13 моля) 40%-ного раствора перуксусной кислоты в течение 15 мин при 25-30°С. После добавления массу перемешивают 2 ч при 25-30° С. Добавляют 200 мл воды и смесь экстрагируют 200 мл метилеихлорида и затем 100 мл метиленхлорида. Экстракты метиленхлорида собирают с органической фазой и экстракты промывают дважды по 100 мл воды. Полученный материал сушат над безводным сульфатом магния, фильтруют и отпаривают растворитель с получением 23 г продукта. транс- -Циклогомоцитральэнолпропионат имеет сладкий вдеточньш, иононовый, малиновый, сухофруктовый, табачный аромат со сладким, фру товым, КОНОНОВЫМ, малиновым, сухофруктовым табачным вкусом при 1 ч на 1 тыс. В два раза крепче, слаше, фруктовый и малиновый, чем транс- циклогомоцитральэнолацетат. В парфюмерии гране- -циклогомоцитральэнолпропионат имеет высокие табачные, древесные и иононовые ноты, но менее прятен, чем транс-ft-циклогомоиитральэнолацетат, который предпочти телек для духов. Пример 41. Пробное получение -циклогом цитральэнолацетата с применением ангидрида пермалеиновой кислоты. В сосуд емкостью 500 мл, снабженный ледяной баней, термометром и магнитной мешалкой помешают 150 мл метиленхлорида и 38,5 г (0,34 модя) перекиси водорода. Полученную смесь охлаждают до 0°С с применением едяной бани и добавляют 39,2 г (0,4 моля) маеннового ангидрида. Смесь неременшвают I ч затем нагревают с обратным холодильником. ри этом добавляют 38,4 г (0,2 моля) (3-ионона 40 г метиленхлорида в течение I ч. Затем ассу перемешивают 2 ч и получают две фазы: одную и органическую. Органическую фазу отеляют и промывают 150 мл насьиненного кароната натрия и затем 150 мл насыщенного ратвора хлорида натрия. Органическую фазу суат над безводным сульфатом магния и отпаивают с получением 37 г неочищенного продука. Анализ ГЖХ показывает выход 97,5% Д-ион поксида, только следы -циклогомопитральзнолдетата в продукте. Пример 42. Получение |3-пиклогомоцитральноладетата с использованием растворителя меилендихлорида. еакдия -l-HjC-ci kA о В сосуд емкостью 250 мл, снабженный мешалкой, термометром, охлажданием и воронкой, помещают следующие материалы: Метиленхлорид100 мл /3-Ионон19,2 г (0,1 моля) Ацетат натрия13 г (0,13 моля) Реакционную массу перемешивают при комнатной температуре 10 мин, после чего начинают добавлять 19,2 г (0,10 моля) 40%-ной перуксусной кислоты с экзотермической реакций примерно 45 мин при 25-30°С. После 45 мин реакционную массу перемешивают 1,5 ч. Образец в этот момент реакции показывает соотношение (3-циклогомоцитральэнолацетат : /3-иононэпоксид 1:1. Перемешивание продолжают еще 2,25 ч и анализ ГЖХ показывает то же соотношение знолацетата и эпоксида в образце. Через 3,75 ч реакционную массу добавляют в 100 мл воды с получением двух фаз, органической и водной. Водную фазу отделяют от органической и последнюю промывают трижды по 100 мл воды. Органическую фазу затем сушат над безводным сульфатом , фильтруют и отпаривают в Ротоваре с получением 10,5 г масла. Анализ ГЖХ неочищенного продукта по зывает:Количество, % 0,5 -Циклогомоцитраль транс- Циклогомоцитральэнолацетат336 Мепрореагировавший (3-ионон33 р-Иононэноксид42 Выход -циклогомоцитральэнолацетата опреде ляется 2()%-ной конверсией из -ионона в энол ацетате до 30%. Пример 43. Получение траке-р-циклогомоцитральэнолацетата с использованием растворите ля бензола. В сосуд емкостью 500 мл, снабженный мешапкой, термометром и воронкой, помешают следуюшие материалы: Безводный бензол100 мл /3-Ионон19,2 г (0,1 моля) Ацетат натрия13 г (0,13 моля) Реакционную массу перемешивают 10 мин при комнатной температуре. Начинают добавлять 19,2 г (0,10 моля) 40%-ной перуксусной кислоты и продолжают в течение 30 мин при 25-30°С. Массу перемешивают еще 3 ч и при этом добавляют 150 мл насыщенного раствора хлорида натрия. Добавляют 50 мл метиленхлорида. Органическую фазу отделяют от водной и первую промывают 100 мл насыщенного водно го хлорида натрия и 100 мл воды. Органическую фазу сушат над безводным сульфатом маг ния, фильтруют и отпаривают с выходом 22,8 г масла. Анализ ГЖХ неочищенного продукта показывает следующее: 25,0% (27,4%-ный гранс- Цшслогомоцитральзнолацетат27,5% (32,6%.ное Ионон восстановление) 36,1% (39,5%-ный Иононзпоксид Пример 44. Получение р-циклогомоцитраль энолацетата с применением растворителя бензол и агента окисления .м-хлорпербензойной кислоты. Реакция V4xK сг О-О-Н в сосуд емкостью 500 мл, снабженный мешалкой, термометром и воронкой, помещают следующие материалы: Бензол100 мл Ацетат натрия13 г (0,13 моля) -Ионон19,2 г (0,10 моля) Реакционную массу перемешивают 10 мин к начинают добавление 21,4 г (0,1 моля) 85%-ной хлорпербензойной кислоты. Добавление продолжают примерно 80 мин при 25-30°С. Затем реакционную массу перемешивают еще 2 ч и твердые прюдукты отфильтровывают от реакционной массы. Органический слой затем промывают 100 мл воды, сушат над безводным сульфатом магния, фильтруют и отпаривают растворитель в Ротоваре с получением 21,9 г масла. Анализ ГЖХ неочищенного продукта показывает следующее:7раи(Цкклогомо28,3% (29,7%-ный выход) цитральэнолацетат Ионон 22,6% (25,7%-ное восстановление) Иононэпоксид 37,8% (39,7%-ный выход) Пример 45. Пробное получение -циклогомоцитральзнолацетата с применением агента окисления ангидрида перфталевой кислоты и раст ;орителя циклогексана. Реакция -bHtOi - 5 (1,вГо) С (0,7% В сосуд емкость 500 мл, снабженный мешалой, термометром и воронкой, помешают слеующие материалы: Циклогексан150 мл 309 1-ная перекись водорода19,2 г (0,17 моля) Реакционную массу охлаждают до 0°С и меденно добавляют 19,6 г (0,2 моля) перфталевоо ангидрида. Массу перемешивают 1 ч и доавляют 19,2 г |3-ионона в 50 мл циклогексана течение 30 мин при 25 С. Через 30 мин масу перемешивают 3 ч и затем добавляют 150мл оды. Твердые продукты отфильтровывают, оранический слой отделяют от водного. Органиеский слой промывают 100 мл насыщенного одного раствора соли и сушат над безводным ульфатом магния, фильтруют и выпаривают 35 растворитель в Ротоваре с получением 20,0 г масла. Анализ ГЖХ неочищенного продукта по казывает следующее: траис-j3-Цик логомо1,8% (1,8%-ный цитральэнслацетат /J-Ионон 47,3% (51,4%-ное восстановление) /3-Иононэпоксид 40,7% (40,9%-ный выход) Пример 46. Пробное получение |3-циклого моцитральэнолацетата с применением растворит ля диметиланилина. В сосуд, емкостью 500 мл, снабженный мешалкой, термометром и воронкой, помещают следующие материалы; Диметиланилин100 мл /3-Ионон12,2 г (0,1 моля) Ацетат натрия13 г (0,13 моля) Реакционную массу перемешивают 10 мин и начинают добавление 19,2 г (0,01 моля) 40%-ной перуксусной кислоты при 25-30°С. Добавление проводят 30 мин при перемешивании и 25 -30 С.Затем реакционную массу пе- ремешивают еще 2 ч.В этот момент реакш™, масса имеет пурпурный цвет. Затем добавляют 300 мл воды и смесь добавляют к 300 мл диметилэфира с образованием эмульсии. Нагревают и оставляют последнюю на 2 ч. Эфирный слой отделяют от водного, анализ ГЖХ проводят на эфирном слое. Обнаружены следы |3-щ1клогомоцитральэнолацетата и |3-иононэпоксида. Водный слой имеет пурпурный цвет, указывающий, что амин окисляется предпочтительнее ионона Пример 47. Получение /3-циклогомоцнтральэнолацетата с применением формамида. Реакция
+ H/-f. Т
VO-RkA в сосуд емкостью 500 мл, снабженный мешалкой, термометром и воронкой, помещают следующие материалы: Формамид100 мл Ацетат калия13 г (0,13 моля) |3-Ионон, 19,2 г (0,1 моля) Полученную смесь перемешивают 10 мин. Затем начинают добавление 19,6 г (ОД моля) 40%-ной перуксусной кислоты при 25-30°С. Реакция средне-экзотермическая и не требует применения охлаждения. Добавляют перуксусную кислоту 30 мин. Затем массу перемешивают 2 ч. Потом реакционную массу добавляют в 200мл воды,к которой затем добавляют 200мл дизтилэфира. Образуется эмульсия,которая расслаивается при нагревании и отстаивании в течение ночи. Анализ ГЖХ эфирного слоя показывает главный пик - траис-Д-циклогомоцитральэнолацетат, а также небольшие количества -иононэпоксида и ионона. Водный и эфирный слои отделяют и последний промывают 100 мл водного насыщенного раствора хлорида натрия. Эфирный сло сушат над безводным сульфатом магния, фильт руют и выпаривают растворитель в Ротоваре с получением 21,9 г продукта. Анализ ГЖХ отпаренного неочищенного продукта показывает еле дующее; 9,7 г (46,6%-ный (3- Циклогомоцитральэнолацетат7,18 г (37,4%-ное Э-Ионон восстановление) 3 г (14,4%-ный -Иононэпоксид выход) Пример 48. Получение 1раис-|3-циклогомоцитральэнолацетата с применением растворителя диметилформамида и буфера. В сосуд емкостью 500 мл, снабженный мешалкой, термометром и воронкой, помещают следующие материалы: Диметилформамид100 мл Ионон19,2 г (0,1 моля) Ацетат калия13 г (0,1 моля) Полученную смесь перемешивают 10 мин и затем, начинают добавление 19,5 г (0,1 моля) 40%-ной перуксусной кислоты при 25-30° С. Добавляют в течение 50 мин при 25-30°С. Отмечают сред,НИИ экзотермический эффект. Затем массу перемешивают еще 2 ч при поддержании комнатной температуры. Массу добавляют к 200 мл и к полученной смеси добавляют 200 мл диэтилэф1фа. Отделяют органический и водный слои и первый промывают 100 мл водного насыщенного раствора хлорида натрия. Эфирный слой сушат над безводным сульфатом магния, фильтруют и выпаривают с получением 20,1 г масла. Анализ ГЖХ показывает следующие материалы:
4,26 г (20,4%-Hbir
выход)
10,8 г (56%-ное
восстановление)
13%-ный выход
Пример 49. Получение -циклогомоцитральэноладетата с применением окислителя А«-хлорпербенэойной кислоты (применяется растворителя на 50% больше, чем в примере 50). Реакция
Ч.0
...x
о
оензол х в сосуд, снабженный мешалкой, термометром и обратным холодильником, помещают еле дующие материалы: Бензол150 мл Ацетат натрия13 г (0,13 моля) -Ионон19,2 г (0,1 моля) Полученную смесь нагревают с o6paTiaiM холодильником и начинают медленно добавлять 21,4 г (0,1 моля) 85%-ной хлорпербенэоЙ1юй кислоты. Добавление проводят примерно 80ми Затем массу перемешивают при нагревании с обратным холодильником в течение еще 2 ч. П том массу добавляют к 200 мл воды с образо ванием двух фаз: водной и органической. Водную отделяют от органический и к водной добавляют 200 мл диэтилэфира. Органическую фа зу и эфирные остатки собирают и промывают 100 мл воды. Полученный органический слой .сушат над безводным сульфатом магния и фил труют. Полученный продукт весит 302,2 г. Материал затем выпаривают в Ротоваре с получением 38,2 г твердого остатка. Анализ ГЖХ показывает следующее: Циклогомоцитраль4,2 г (20%) энолацетат 6,1 г (32%) Ионон 13 г (62%) Э-Иононэпоксид Пример 50. Получега1е грт«с-Э-циклогомоцитральэнолацетата с применением растворителя формамида. Технология идентична примеру 53, но полученный 11родукт весит 26,5 г и анализ ГЖХ отпаренного продукта показывает следующее: 1ра«с- Циклогомоцитральэноладетат12,2 г (59%) |3-Ионон3.0 г (16%) (3-Иононзпоксид7,2 г (34%) Пример 51. Окисление Л-метилионона с об разованием соответственного транс-знолацегата. Реак,ция ССг -ь Hjd-c: 0-0-н В сосуд емкостью 250 мл, снабженный меШалкой, ворюнкой, термометром и охлаждением, помещают следующие материалы: Л-Метилионон24,8 г (0,1 моля) Вода40 мл Уксусная кислота50 мл Ацетат натрия17 г (0,17 моля) Полученную смесь перемешивают 10 мин и начинают добавление 24 г (0,13 моля) 40%-ной перзтссусной кислоты при 25-30°С. Добавление проводят 10 мин. Реакция идет со средним экзотермическим эффектом. После добавления массу перемеишвают еще 2 ч при 25-30С. Затем добавляют 200 мл воды и полученный материал экстрагируют 200 мл метилендихлорида и затем 100 мл метилендихлорида. Экстракты метилеидихлорида собирают и промывают дважды по 100 мл воды. Промытые экстракты метилендихлорида собирают и сушат над безводным сульфатом магния, фильтруют и отпаривают с получением 26,8 г неочищенного продукта. С точки зрения вкуса, а-2, 6, 6-гpимeтил-l-Iц клoгeкceн-rpflH6-l-этилaцeтaт имеет древесный, иононовый, газолиновый, томатный аромат с древесным, иоионовым, газолиновым характером вкуса растворителя при 1 ч. на 1 тыс. Аромат маслянистый, древесный, мускусный, масляный, иононовый и не такой сладкий или фруктовый, как |3-циклогомоцитральзнолацетата. При сушке имеет древесньуй аромат. Пример 52. Получение -циклогомоцитраль-«ыс-энолацетата. Реакция транс г/земер О Сс tfuc изомер В с(х;уд емкостью 100 мл, снабженный ме ишжой, термометром и обратньЕм холодильником, помещают следующие ингредиенты: -Циклогомоцитраль16,6 г (0,1 моля) Уксусный ангидрид17,3 г (0,17 моля) Ацетат калия0,1 г (0,01 моля) Массу нагревают с обратным холодильником нри перемешивании 9 ч. Затем добавляют 50 мл диэтилэфира. Потом промывают 5 раз по 50 мл воды. Полученный материал сушат над безводным сульфатом магния, фильтруют и отпариваю растворитель в Ротоваре. Анализ ГЖХ показыва ет наличие трех соединений: /З-циклогомоцитраля, циклогомоцитраль-транс-энолацетата и /3- циклогомоцитраль- цис- энолацетата. Полученный Д-даклогомоцитраль-чис-энолацетат имеет следующие органолептические свойства. Вкус: сладкий, цветочный, иононовый древес ный, фиалковый, фруктовый, кариофиленовый аромат с сенным, Кононовым, древесным, фиалковым, кедровым вкусом при 5 ч. на 1 тыс. Парфюмерия: землистый, камфарный, морской рромат с иононовым и фруктовыми нюансами, помимо сладкого, 13-иононового, табачного и фруктового нюансов. Пример 53. Пробное получение / -цнклогомоцитральэнолацетата с применением растворителя диметилформамида и без буфера.
40 мл воды, 26 г ацетата натрия, 38,4 г (0,2 моля) ионона, 76 г (0,4 моля) 40%-ной перуксусной кислоты
80 мл воды, 100 мл уксусной кислоты, 34 г ацетата натрия 38,4 г (0,2 моля)
. 3-ионона и 76 г (0,4 моля) 409)-ной перуксусной кислоты
Формамида 180 мл, ацетата натрия 26 г, )3-ионона 38,4 г (0,2 моля), 76 г 40%-ной перуксусной кислоты (0,4 моля)
Формамида 4500 мп, ацетата натрия 650 г, р-ионона
960 г и 40%-но, перуксусной кислоты 1900 г (10 молей)
Формамида 400 мл, /5-ионона, 38,4 г ацетата калия
(0,2 моля) и 76 г (0,4 моля) 40%-ной перуксусиой кислоты
-Циклогомоцитральэнолацетат 4,2%, /3-ионон 47%, |3-ионон (эпоксидированный) 39%
|3-Циклогомоцитральзнолацетат 46,8%, /3-ионои 10,3%, |3-ионон (эпоксидированный) 44,9%
0-5 5 ч
Д-Циклогомоцитральзнолацетат 50,1%, р-ионои 36,2%, эпоксидированный 0-ионом 15,9%
-Циклогомодатральацетат 52,6%, иойон 15,6%, зпоксидированный 0-ионон 25%
0- Циклогомоцитральзнолацетат 43%, 0-ионон 1,8%, эпоксидированный Д-ионон 43% В сосуд, снабженный мешалкой, термометром и воронкой, помещают следующие материалы:Диметилформамид100 мл (3-Ионон19,2 г При перемешивании в течение 30 мин при 25° С к реакш онной массе добавляют 19,6 г (0,1 моля) 40%-ной перуксусной кислоты. Затем перемешивание прекращают и массу оставляют на 144 ч. После добавляют 200 мл воды и 200 мл диэтилэфира при перемешивании. Образуется эмульсия, которую разделяют на два слоя: водный и органический. Водный экстрагируют 200 мл дизтилэфира. Эфирные промывки собирают с органическим слоем вместе и полученный раствор промывают 200 мл водного насыщенного раствора хлорида натрия. Органический слой сушат над безводным сульфатом магния, фильтруют и отпаривают от растворителя в Ротоваре с получением 34,5 г масла. Анализ ГЖХ показывает соотношение Д-ионона и (3-иононзпоксида 1:2 и только следы -циклогомоцитральэнолацетата. Примеры 54-58. Получение /3-циклогомоцитральэноладетата при ра:У1Ичнь х условиях. Используют сосуд, снабженный мешалкой, термометром и воронкой, технология примера 53. Условия реакции приводятся в табл. 3. Таблица 3 41 Пример 59. Получение /3-циклогомоцитра эноллаурата. Реакция ОС Н -i- (-(ijlHw) kj « . Ч-0/() в сосуд емкостью 50 мл, снабженный термп метром, нагревателем и магнитной мешалкой, помещают следующие материалы: Лауроилхлорид15,8 г (0,076 мол Циклогомоцитраль7,8 г (0,45 моля Ацетат калия1 г Реакционную массу нагревают 5 ч при 160200°С. При нагревании масса принимает пурпу ный цвет и затем зеленый и наблюдается выде ление хлорводорода. Затем массу охлаждают и выливают в 200 мл воды. Полученную водную фазу затем экстрагируют дважды по 150 мЛ метилеихлорида. Органические слои собирают, фильтруют и отпаривают от растворителя в Ро товаре с получением 22,5 г твердого темного остатка. Анализ ГЖХ показывает кислый пик и три новых пика с большим временем сохра еиия. Пример 60. Табачный состав. Получают табачную смесь при перемешивани следующих ингредиеитов (вес. ч.): Брайт40,1 Барлей24,9 Мериленд1,1 Турецкий11,6 Стим (высушенный)14,2 Глицерин2,8 Вода5,3 из этого табака изготовляют сигареты. Получают следующийвкусовой состав (вес. ч Этилбут1фат0,05 Этилвалерат0,05 Малтол2,00 Экстракт какао26,00 Экстракт кофе10,00 Этиловый спирт20,00 Вода41,90 Указанный вкусовой состав наносят в количестве 0,1% на все сигареты из вышеприведенного табачного состава. Пол,вину сигарет обра батывают 500-1000 ч.на 1 тыс. -циклогомоцитральэнолбутирата по примеру 32. Контрольн сигареты и экспериментальные сигарели, содержащие гране-Д-циклогомош1тра11ьЛ1илбутнрат по примеру 32, сравнивают и получают следующие результаты оценки. Экспериментальные сигареты имеют сладкий, цветочный, чайно-табачный, фруктовый, дамаскеновый аромат до курения и при курении. Натуральные табачный вкус и аромат улучшены в результате применения 7ранс-|3-циклогомоцитральзнолбутирата. Все сигареты имели фильтр 20 мм из целлю лозацетата. Пример 61. Табачный состав. Получают табачную смесь из следующих компонеитов (вес. ч.): Брайт40,1 Барлей24,9 Мэриленд1,1 Турецкий11,6 Стим14,2 Глицерин2,8 Вода5,8 Из зтого состава изготовляли сигареты. Получали следующий вкусовой состав (вес. ч.): Этилбутират0,05 Этилвалерат0,05 Малтол2,00 Экстракт какао26,00 Экстракт кофе10,00. Этиловый спирт20,00 Вода41,90 Состав наносят в количестве 0,1% на все сиареты. Половину обрабатывают 500 или 1000ч, а 1 тыс. чис-)3-циклогомоцитральэнолоктаноата о примеру 34. Контрольные и экспеиментальные с содержанием чмс- циклогомоитральэнолоктаноата по примеру 34 оценивают получают следующие результаты. Экспериментальные сигареты более сладкие, роматные и табачные и имеют лучший вкус о рту, чем контро.льные. Табак зкспериментальиых сигарет до и при урении имеет сладкий, холодноватый оттенки с нюансами смолы и табака.. Все сигареты имели фильтр 20 мм из целлюозацетата. Пример 62. Табачный состав. Получают табачную смесь при смешивании слеующих ингредиентов (вес. ч.): Брайт40,1 Барлей24,9 Мэриленд1,1 Турецкий11,6 Стим14,2 Глицерин2,8 Вода5,3 Изготавливают сигареты из этого табака.
Получают вкусовой состав (вес. ч.): Этилбутират0,057
Этилвалерат0,05
Малтол2,00
Экстракт какао26,00
Экстракт кофе10,00
Этиловый спирт20,00
Вода41,90
Состав наносят в количестве 0,1% на сигареты. Половину обрабатывают 500 или 1000 ч, на 1 тыс. факс- -циклогомоцитральэиолоктаноата по примеру 34. Контрольные сигареты и экспериментальные сигареты с гранс- -циклогомоцитральэнолоктаноатом по примеру 34 оценивали и получили следующие результаты.
Экспериментальные сигареты более сладкие, ароматные и табачные и имеют лучший вкус во рту, чем контрольные.
Табак экспериментальных сигарет до и при курении имеет сладкие и холодноватые нотки с табачными и смоляными нюансами.
Все сигареты имели фильтр 20 мл из целлюлозацетата.
Пример 63. Табачный состав. Получают табачную смесь из следующих ингрдиентов (вес. ч.):
Брайт40,1
Барлей24,9
Мзриленд1,1
Турецкий11,6
Стим14,2
Глицерин2,8
Вода5,3
Изготавливают сигареты из зтого табака. Получают вкусовой состав (вес. ч.): Этилбутират0,05
Этилвалерат0,05
Малтол2,00
Экстракт какао26,00
Экстракт кофе10,00
ЭтилоЙ11Й спирт20,00
Вода41,90
Вышеуказанный вкусовой состав наносят в количестве 0,1 на все сигареты. Половину затем обрабатывают 500 или 1000 ч. на 1 тыс. « ыс- циклогомоцитральзнолацетата по примеру 52. Контрольные сигареты и зкспериментальны с чмс- циклогомодитральэнолацетатом по примеру 52 оценивают и получают следующие результаты.
Экспериментальные сигареты более сладкие, ароматные и табачные и менее едкие, со сладкой, цветочной и фруктовой нотами. Табак экспериментальных сигарет при курении имеет лучшие цветочные и фруктовые ноты. Все сигреты имеют фильтр 20 мм из целлюлозацетата
«г/с-/3-Циклогомоцитральэнолацетат по примеру 52 улучшает табачный вкус и аромат, придает сладкие, табачные натуральные ноты.
Пример 64.
А. Поэтатшое получение /З-циклогомоштральэнолацетата с применением растворителя формамида и окислителя перуксусной кислоты при 0°С.
В сосуд емкостью 12 л, снабженныймешалкой, термометром, воронкой н охлаждением сухим льдом (ацетоном), загружают следующие материалы:
Формамид4500 мл
Ацетат натрия650 г (7,92 моля)
(3-Ионон960 г (5,0 моля)
Реакционную массу перемешивают при охлаждении до достижения температуры 0°С. Начинают добавление 1900 г 40%-ной перуксусной кислоты. Добавляют 3,5 ч при ОС. По окончании реакреакционную массу перемешивают еще 3,5 ч при 0°С. Затем переливают через воронку и добавляют 5 л теплой воды. Массу экстрагируют трижды по 1 л метиленхлорида и зкстракты промывают трижды по 1 л воды. Экстракты сушат над безводным сульфатом магния и фильтруют. Отпаривают растворитель через фарфоровую переходную колонку до температуры жидкости 100° С. Остаточное масло перегоняют при пониженном давлении с получением 984 г масла в семи фракциях. Анализ ГЖХ фракций показал следующее:
транс-13- Циклогомо52,6 цитральэнолацетат |3-Ионон15,6%-ное восстановление/3-Иононэпоксид15)tj
Б. Получение /3-циклогомоцитраля путем гидролиза катализированным основанием /3-цнклогомоцитральзнолацетата.
В сосуд емкостью 5 л, снабженный мешалкой.
термометром, воронкой и охлаждением сухим
льдом (ацетоном) помещают следующие материалы :
Вода1665 мл
Метанол1665 мл
Карбонат натрия500 г (4,71 моля)
Смесь перемешивают некоторое время. Начинают добавление 984 г смеси /3-циклогомоцитральэнолацетата, (3-ионона и -иононэпоксида из вышеуказанного дистиллята. Смесь добавляют в течение 45 мин при 25-30С. Затем перемешивают еще 2 ч при 25-30°С. Потом выливают через paздeлитeJrьнyю воронку и добавляют 3 л воды и 1 л хлороформа. Собирают орга ;ический слой. Водный слой экстрагируют дважды по 1 л хлороформа. Собирают органические экстракты, промывают дважды по 1 л насыщенного раствора соли, сушат над безводным сульфатом магния и фильтруют. Органи4568566ческий слой затем подвергают комбинированному отпариванию и пропускают при пониже1шом давлении через фарфоровую переходную колонку с получением 758 т масла. Затем его перегоняют через колонку Гудпо при пониженном дав- 5 лении с получением 686 г масла в 14 фракциях. Остаток 44 г, содержащий |3-ионона и (жонэпоксид, оставляют. Анализ ГЖХ фракций показывает следующее: (3- Циклогомоцитраль 583 г (70%-ный вы- 10 ход от /5-ионона) Д-Ионой 83 г {9%-ное восстановление) 9 г (0,8% на побоч|5-Иононэпоксидный продукт)15 Формула изобретения 2, 6, 6-Триметил-1-циклогексен-1-винилалка- 0 нраты общей формулы I где R, - алкил С,-Сэ, С,, С, j, R4 - водород или метил, и если Рд - метил, что RI - тоже метил, волнистая линия означает положение радикала в цис- или транс-конфигурашш, проявляющие органолептический эффект. Приоритет по признакам 07.10.75при RI - алкил С,-Сз. 01.03.76при RI - алкил €7, Сц. Источники информации, принятые во внимание при экспертизе 1.Бюлер К., Пирсон Д. Органические синтезы, ч. у. М., Мир, с. 312. 2.Там же, с. 298. 3.Там же, с. 328.
Авторы
Даты
1979-09-15—Публикация
1976-11-03—Подача