Изобретение относится к новым химическим соединениям ряда пирролидонов-2, которые могут найти применени в медицине. Ближайшими аналогами по структуре предлагаемым соединениям являются производные пирролидона-2 общей формулыИзвестны незамещенные по атому азота или Ы-ацилзамещенные 5-алкилпирролидоны.типа где R - Alk R- Н, ОСНд, которые обладают антимикробным действием в концентрации 75 Целью изобретения является расширение имеющегося арсенала средств воздействия на живой организм. Поставленная цель достигается 5-амил-Ы-(фенил- или. фенилзамещенные)-2-пирролидонами общей формулы
Указанные соединения получают восстановительным ариламиннроваиие 1 зтиловых эфиров Т(-кетокарбоновых кислот при использовании в качестве амииируюадих агентов анилина, п-фенилендиамина, п-аминофенола в присутствии катализатора промышленного никеля на кизельгуре с добавлением конденсирующих агентов (СНзСООМа, .) при 100-120°С, начальном давлении водорода 60 атм.
Антимикробная активность всех синтезированных соединений изучена методом двукратных серийных разведенийв бульоне Хотингера с ,2 в отношепни тесгг бактерий St , aureus 209, E.coli М-1.7, pr.VuJgari.s W 30, фунгистатическое действие изучено на среде Сабуро в отношении грибов Кандида.
Препараты растворяют в спирте с последующим разведением их стерильной дистиллированной водой до нужно концентрации. Испытания показывают, что препараты задерживают рост испытанных тест-микробов в концентрации 12-37 мкг/мп и обладают малой токсичностью, LDijo при однократном подкожном введении белым мышам составляет 80-100 мг/кг (см.табл.1).
Таблица 1
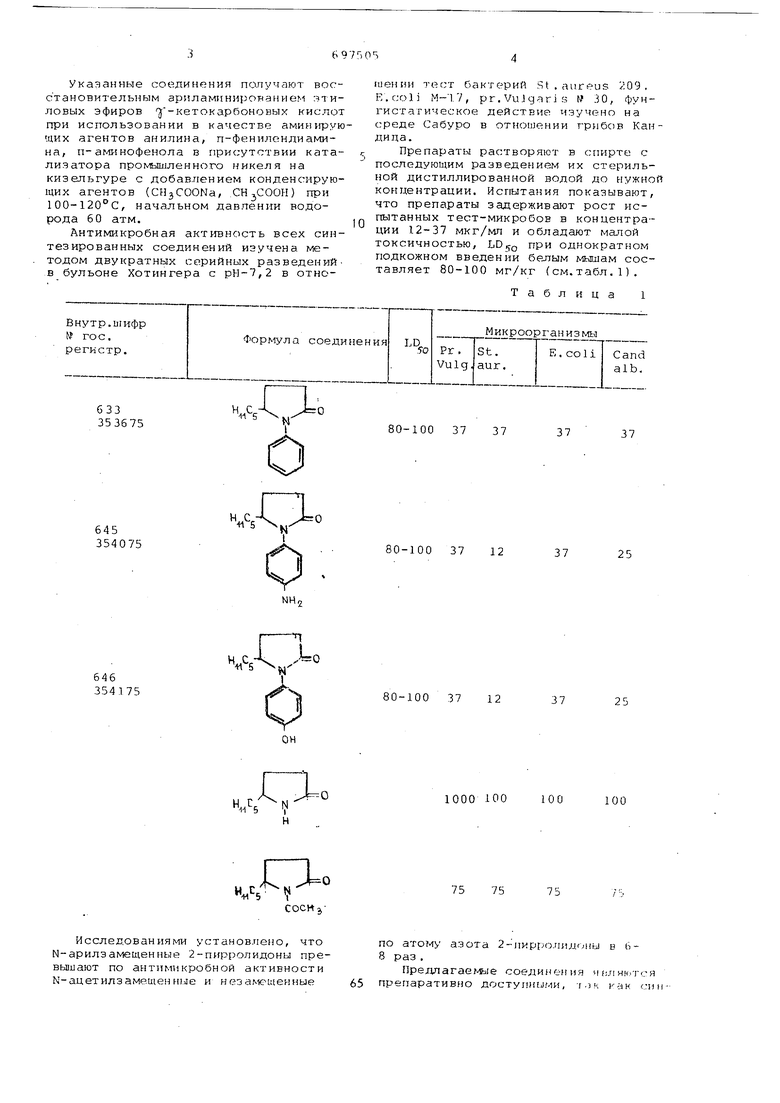


V5-4,,0
645 354075
80-100 37 12
37
646 354.175
80-100 37 12
37
25
1000 100100100
СОСНз
Исследованиями установлено, что N-арилзамещенные 2-пирролидоны превышают по антимикробной активности N-ацетилзамещен m.iie и незамечценные
75
75
75
по атому азота 2-11ирро. в 68 раз .
Предлагае -Ф11е соединения чслнютс-я 65 препаратив(ю досту1 ними, т.зк к-ак сиитезируются на основе эфиров J-кетокарбоновых кислот, сырьем для получения которых служит даиевый продукт фурфурол. Пример . 5-амил-Ы-(п-окси фенилен) 2-пирро.пидон . Во вращающийся автоклав емкостью 610 мл помещают 200 мл ьгетилового спирта, подкисленного 2 мл уксусной кислоты, 3 г уксуснокислого натрия, 16,8 г (0,01 моль) этилового эфира ЗГ-кетононановой кислоты, 2,8 г {0,01 моль) п-аминофенола, 4 г никел на кизельгуре (промьдиленного) . Процесс ведут при 100-120 и начальном давлении водорода 60 атм до полного поглощения рассчитанного количества водорода (8-10 час). Ги,црогенизат освобождают, от катализатора фильтрованием, остаток перегоняют при умень шенном давлении. Выход 16,3 г (791) т.кип. 190-192/2 мм, -1,4910. Найдено,%: С 72,72; Н 8,48 N 6,42 Вычислено,%: С 72,87-, Н 8,51 N 5,65 , ИК-спектр (см) VOH 3410. Пример 2. 5-амил-Ы -п-фенил -2-пирролидон.
IT а б л и ц а Получен по методике, описанной в примере 1, из 25 г этилового эфира кетононановой кислоты, 11,3 г анилина, Выход готового продукта 21 г (74, т. кип. 174-175°/3 мм, П .1,4900. Пример 3, 5-амил-Ы -п-,)минофенилен-2-пирролидон. Получен по етодике, описанной в примере 1, исходя из 20 г эт 1лового эфира кетононановой кислоты, 10 г п-Фенилендиамина. Получено готового продукта 15,47 г (77%, т.кип.167170°/2 мм, П 1,4890. В табл,2 приведены характеристики олученных 5-aмил-N-(арил) и Ы-(арил-амещенные) -2-пирроли;цоиов типа «л-ч
Авторы
Даты
1979-11-15—Публикация
1978-03-09—Подача