CH NHCOgCHj МГСОгСНз -о.нHJ- кнсогШз iI/ (OTOS ., мнсОгСНз Тоз ОТэСбН(15 которое обрабатьшают иодидом щелсч го металла в диметилформамиде при 85-1Г5°С, полученное иодопроизводное формулы 1У 12инсогснз -о.ни)- тмнсогСИз КНСОгСНз обрабатывают ..водородом в присутст вии никеля Ренея, палладия, солей палладия или производных платины .в инертном органическом раство рит ле с последующим ацилированием полученного соединения формулы У сдгынсогснз «нсогснз -о.нН/1V.NHC02CH кнсогСНз уксусным-ангидридом в присутствии органического основания, полученн ацетатное производное форм-улы У1 гагшсогснз «нсОгСНз J-o, н н I, SHCOgCHj подвергают кислотному гидролизу 50-70 С с последующим взаимодейс полученного соединения формулы У сн кнсогСНз J-о нн -чИНСОгСБз , соединением формулы У1( присутствии цианистой ртути в дискане при комнатной температуре с оследующим повышением температуыгдо 50-70°С,- полученную смесь t И рз -аномеров формул IX и 1х CHz NHC02 СН БНСОгСНз NliCOzCHj ШзСОО И снгжтсоггаз KiiOOjCHj н ,1л |JHCO CHj СИзСОО 1 {шсогСНз i7w% н.л m-i /, обрабатывают Е инертном органическом растворителе водородом в присутствии катализаторэг выбранного из группы: палладий на угле, соль палладия для платины, производного платины, родия, рутения или никеля, с последующим снятием амниои оксизащитных групп путем об:;аботки в щелочной среде, состоящей из гидроокиси бария или натрия в водно-спиртовом растворе и водного этанола, при вО-ЮЗ С с последующим выделением целевого продукта в виде свободного основания или соли Пример 1. 4-0-(2,6-диамино-2, 3, б-тридеэокси-а(,0-ри-богексопиранозил)-6-0-(З-метилами но-З, 4, .ридезокси-си .D-ксилогексопиранозил)-2-дезоксистрепта мин. Фаза А, 5,6-0-Циклогексилиден-З-О-тозил-тетра-Н-карбометоксинеамин. 100 г 5,6-0-Циклогексилиден-тет ра-№-карбометоксинеамин а растворяю в 2 л пиридина. Охлаждают до О°С и прибавляют порциями в течение 1 ч 150 г хлористого тозила. Дают температуре подняться до комнатной и перемешивают в течение 18 ч при . Затем прибавляют в течение 3 ч 52,5 г формиата натрия. Концентрируют под уменьшенным давлением и выливают остаток в воду. Экстрагируют хлороформом, промывают водой органический слой и сушат на сернокислом натрии. После выпарива ния растворителя и сушки в вакууме или 40с получают 112 г 5,&-0-циклогексилиден-З-О-тозил-тетра-Н-карбометоксинеамина в виде кристаллов который употребляется в следующей фазе. Этот продукт может бьгть перекри сталлизован при помсвди смеси этило эфир уксусной кислоты - эфир, хроматография в тонком слое -С. (двуокись кремния, хлороформметанол 95:5): ,3, Фаза Б. 5,6-0-Циклoгeкcилидeн-3 -дезокси-з -иодо-тетра-Ы-карбометоксинеамин. Смешивают 393 г иодида натрия и 790 мл диметилформамида. Нагревают до и прибавляют к полученному раствору 76 г полученного в фазе А продукта, Нагреваиот до 103°С.в те ченке 16 ч, а затем после охлаждени прибавляют 2,5 л хлористого метилена. Отсасывают полученное твердое вещество и прополаскивают хлористым метиленом. Фильтрат промывают водой и упаривают досуха органический сло Полученный кристаллический остаток экстрагируют хлористым метиленом, промывают два раза водой хлорметиле новый раствор и сушат его на сернокислом магнии. Выпаривают досуха хлористый метилен и получают 50,2 г 5,6-0 циклогексилиден-3 -дез экси-3 -иодо-тетра-н-карбомвтоксинеамина, который употребляется в таком, виде в следующей фазе. хроматография в тонком слое (двуокись кремния, хлороформ-метанол 95:5) R.0,4 Фаза В. 5 ,6-0-Циклoгeкcилидeн-3 -дeзoкcи-тeтpa-N-кapбoмeтoкcинeaмин. Смешивают 47,7 г полученного в фазе Б продукта, 1,5 л метанола, 95 см триэтиламина и около 300 см водной суспензии никеля Ренея, Пропускают при перемешивании в смесь медленный поток водорода в течение .:4 ч. Очищают смесь, пропуская азот, и фильтруют, промывая удержанный продукт на фильтре при помощи метанола. Фильтрат упаривают досуха, экстрагируют полученный остаток хлористым метиленом, сушат на сернокислом магнии и упаривают досуха. Получают 50 г 5,6-0-циклогексилиден-З-дезокси-тетра-Ы-карбометоксинеамина, который можно употреблять в та- ком виде в следующей фазе. лроматографированная на двуокиси кремния при элюировании смесью хлороформ-метанол (95:5) проба имеет следующие характеристики: Найдено,%: С 50,1; Н 6,9; N 8,7; C.26H42N Вычислено,%: С 50,5; Н 6,85; 20 N9,6 оО-0 + 3°(с 0,85%; хлороформ). хроматография на тонком слое (двуокись кремния, хлороформ - метанол 95:5) Rj 0,25. Фаза Г. 5,б-0-Циклогексилиден-4 -ацетил-З -дезокси-тетра-Н-карбометоксинес1мин. . 50 г полученного в фазе В продукта растворяют в 500 см пиридина, содержащего 250 см ангидрида уксусной кислоты. После выдержки в течение 5 ч при комнатной температуре упаривают досуха, совершенно удаляя при помощи толуола присутствующие жидкости. Получают 55 г 5,6-0-циклогексилиден-4 -ацетил-З -дезокси-тетра-М-карбометоксинеамина, который употребляют в таком виде в следующей фазе. хроматография в тонком слое (двуокись кремния, хлороформ-метанол 95:5) ; R О,, 45. Фаза Д. 4 -Ацетил-з -дезокси-тетра- Ч-карбометоксинеамин. 55 г полученного в фазе Г продукта растворяют в 500 см 3 уксусной кислоты, содержа 1ей 20% воды. Нагревают в течение 3 ч при 60°С, а затем (после охлаждения) упаривают досуха в вакууме. Полученный остаток хроматографируют на двуокиси кремния, элюируя смесью хлороформметан.ол .(56:4), .Получают 23 г 4-ацетил-3-дезокси-тетра-Ы-карбометоксинеамина; cL} 60,5° (с 0,55%; хлороформ). Хроматография на тонком слое (двуокись кремния, хлороформ-метанол 95:5) : «.0,30. Фаза Е. 4-0-(2,6-ди-Н-Карбомет6ксйамино-4-0-ацетйл-2 ,3 ,6 -тридезокси-и-рибогексопиранозил)-6-0- 3 -(кapбэтoкcи-N-мeтил)-амине-2 -О-бенэил-З ,4 ,6 -тридезокси-(1.,1)-ксилогексопиранозилЗ-1,3-диметилоксикарбонил -деэоксистре-птамин.
Растворяют 3,1 г 1-0-ацетил 2-0-бенэил-3- (.N-кapбэтoкcи N-мeтил) -амино-3, 4,6-тридезоксИ-; ксилогексопиранозы в 33 см диоксана, содержеодего 10% газообразной соляной кислоты и 6,6 ,см ацетилхлорида. смесь перемешивают в течение 2 ч при комнатной температуре и упариврют в вакууме. Полученный остаток экстрагируют 6,6 см диоксана и выливают при 60°С полученный раствор В; раствор 2,2 г 4-ацетил-3-дезокcH-TeTpa-N-Kap6oMeTOKCHaMHHa в 77 см диоксана, содержащего 3,3 г циановой ртути, выдерживают при перемешивании в теченрш 4 ч 30 мин при , а затем прибавляют 3,3 г циановой.ртути и хлорное производное из 3,1 г 1 0-ацетил-2-0-бензил 3-(N-кapбэтoкcи-N-мeтил -амино 3,4,б-гридезокси-О-ксилогексопйранозы, Переме1иивают еще в-.. течение 17 ч при 60°С, а затем , выпаривают диокса.н. Прибавляют водный расмвор кислого углекис-лого н.атрия при концентрации 45 г/л и экстрагируют хлороформом,. После сушки органического слоя на сернокислом магнии и упаривания досуха остаток хроматографируют на двуокиси кремния, элюируя смесью хлороформ- ацетон (7:3)„ Получают 2,8 г 4-0-(2 ,б --ди-Н-карбомвтоксиамино-4 0-ацвтил-2 ,3 ,6-тридезокси-D-рибогексопнранозкл) З - {Nкарбэто сси Н--метил) -амино 2 -0-бензил-З ,4 ,б тркдезокск-б(, D-ксилогексопиранозил -1,З-диматнлоксикарбоннл 2-дезоксистрвптаг«1ика з виде белого твердого вещества fi:. + 52 {с О,-55%; хлороформ)« хроматографйл в тонкохм слое (двуокись кремяыя, хг.Гй:роформ-ацетон 7s 3) ; R О ,25 ,
ФаЗсг Ж-;,- ч-О-( 2, б-диамнно-2 , 3 ,б -тр11дезокси-е4 D-рибогвксопираноэил) -6-0-- (3 -матиламино-3, 4 , б -тридезокси-с D-ксилогвксопиранозил) 2 -дезоксистрапташ1Н
4,5 г полученного s фазе Е продукта растворяют Е . 80 ом этанола, содержащего несколько капель хлористого метилена, 0,32 смЭ концен т щар.ован ной соляной кислоты и 2,7 г 10%-ного паллащия .на угле. nepQMesiiHBaioT в атмосфере водорода в течение 1 ч 30 мин Отфильтровывают катализатор .и упаривают досуха. Остаток xpo ia гoгpaфиpyют на двуокиси кремния, элюируя смесью хлороформ-метанол (95, 5).
1 г полученного чистого продукта, имеющего в хроматографии в тонком
лое с предыдущим элюэнтом ,15, :1г1ство.ряют в смеси, содержащей 4 см этанола, 8 см воды и 7,87 г гидратизированной окиси бария. Перемё1 ивают в течение 4 ч при 90-94°С, 5 ; затем охлаждают и фильтруют реак1,ионную смесь. Доводят фильтрат .П.О рН 3 при помощи нормального растйора серной кислоты, отсасывают осадивишйся сернокислый барий и Q нейтрализуют полученный фильтрат при помощи ионообменной смолы, находящейся в виде основания. Отделяют смолу и доводят досуха фильтрат Полученный оса,цок очищают
5 прохождением на ионообменной ко. лонка карбоксильного типа (в виде .аммония) и элюирозанием при помощи 0,15 н, водного раствора аг 1миака, а затем 0,5 н. водного
0 раствора аммиака. Продукт, элюированный 0,5 н. водньил раствором аммиака, хроматографируют на двуокиси кремния для отделения аномеров в положений 1., злюируя
с смесью хлороформ-метанол-раствор aiMMHaKa (). Получают 58 мг аномера целевого продукта и 143 мг аномера оС .
Аномер,с1: foG -г 124 (, 5%;
„ вода); R} 0,5 (двуокись кремния, хлороформ-метанол-раствор аммиака 2:2sl),
Аномер р) г -;- 52 , 5° ( , 2% ; вода) R 0,6 {двуокись кремния.
х;1ОрО(рорм-метанол-растг Ор .
2i2sl)
Употребленную в начале фазы Е 1-0-ацетил-2-0-бекзил 3-CN-карбэтокси-Ы-метил) -амико 3, 4 ,6-тридезокси-П-ксилогексопиранозу, можно 0 получить следующим образом:
Фаза 1„ Этил-3-(К-1 арбэтокси Ы Метил, aj iHKo 3, 4 .б-тридезокси-П ксилогексопиранозид,.
Растворяют 67 г этил-3-(N-карб5 этокси-Н-метил)-амино-3,4,6-три дезокси-2 0-зтоксикарбонил-П-ксилогвксопиранозида в 500 см этанола, а затем прибавляют 200 см 2 Но раствора е.дкого натрия,. 0Перемешивают в течение 1 ч при
комнатной температуре, а затем разбавляют водой и экстрагируют .клористым метиленом. Органический слой промывают водой и упаривают . 55 его досуха в вакууме. Получают
57 г целевого продукта в виде желтого масла, которое употребляют в таком виде в следующей фазе
Фаза 2. Этил-2-0-бензил 3-(Ыкарбэтокси-Ы-метил)-амино-3,4,6 Тридезокси-В-ксилогвксопиранозид. Вводят в суспензию 12 г диспергированного в минеральном масле гидрида натрия в 300 см тетрагидрофурана. При перемешивании прибэвляют раствор 57 г полученного в фа зе 1 продукта в 100 см тетрагидро фурана. Нагревают до кипения в течение 15 мин, а затем охлаждают до 25 С. Прибавляют 29см бромбензила и оставляют в течение 15 ч при комнатной температуре. Разбавляют водой и экстрагируют этилоBfciM эфиром уксусной кислоты. После выпаринания этилового эфира уксусу ной кислоты полученное масло хроматографируют на двуокиси кремния при помо1ди смеси бензол - этило вый эфир уксусной кислоты (8;2) . Получают 60 г целевого продукта в виде белого кристаллизованного твердого продукта; ТоПл, . Фаза 3„ 1-0-Ацетил-2-0-бензил-3- {Ы--карбэтокси-К-метил) -амино-3,4,6-тридезокси-В Ксилогексопираноза. Газообразный хлористый водород барботируют до насьлчения в смесь 600 см уксусной кислоты и 60 см ангидрида .уксусной кислоты при 25°С, Прибавляют 60 г полученного в фазе 2 продукта и оставляют в течение 16 ч при комнатной температуре, выдерживая барботаж . хлористого водорода. Затем упаривают досуха в вакууме, не превы,juaH 40°С. Полученное масло хроматографируют на двуокиси кремния при помо щи смеси хлороформ-ацетон ()o Получают 60 г продукта в виде бело го кристаллизованного, твердого продукта. Чистый аномер сС получают перекристалл из гщи ей в изопропиловом эфире; т.пл, 87 С. Найдено, %s С 62,7 Н 7,7; N 3,7 С-19 9.1 NO.S Выч1.слено, % S С 62,45, Н 7,45, N 3,83. . П р и : а р 2. Сульфат 4-0-(2 6 диамино 2 ,. З ,б-тридезокси-ci, D-рибогексопиранозил)-6-0-(З -мети ламино-з,4,б -тридезокси-сС D-кс логексопиранозил)-2-дезоксистрепта мина, 169 г полученного по примеру 1 аномера OL {Растворяют в 20 см воды Полученный раствор нейтрализуют при ПОМС8ДИ 0,1 и. раствора серной кисло ТЫ;- контролируя нейтрализсщию при помощи рН-метра. Таким образом, ра ход/ют 16 f 5 см кислоты. Фильтруют полученный раствор, концентрируют фильтрат в вакууме -и прибавляют метанол, в результате чего осаждается целевой сульфат. Получают 230 сульфат 4-0-(2,6 -диамино-2,З, б -тридезокси-оС, D-рибогексопиранозил)-6-О-(З -метиламино-3,4, 6-тр дезокси-о ТЭ-ксилогексопиранозил) -2 -дезоксистрептамина в виде твердого го вещества формулы C.Q H,qN O-5/2i + (С--0,8%; вода); ,5 {двуокись кремния, хлороформнол-раствор аммиака 2:2:1). Формула изобретения пособ получения 4-0-(2 ,б-диами ,3 ,6 -тридезокси-оС, Э-рибогекранозил)-6-0-(3 -метиламино-3, -тридезокси-а, D-ксилогексопизил)-2-дезоксистрептамина формуРКгШгN% NH н; (Х I-о Н I Лшснз - ли его солей, тличающийся тем, соединение -общей формулы И сшкисо снз шсогснз /-о.нН )-V ттсогснз (он Y кнсогснз ергают взаимодействию с п-тосульфохлоридом в присутствии пина при с образованием лпроизводного формулы Щ ШсогСНз кнсогСНз HJ-.шсогСНз о кнсогСНз Т05 СНзСбН ЗО) рое обрабатывают иодидом щелочметалла в диметилформамиде при
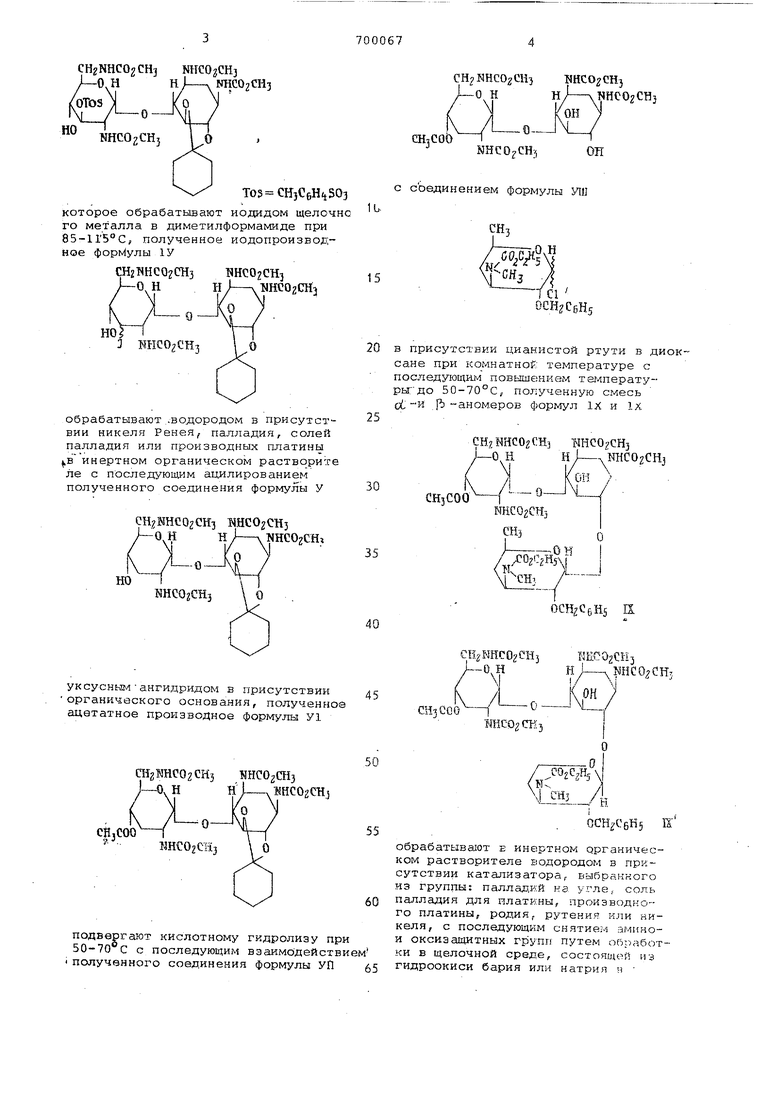
85-115°С, полученное иодопроиэводное формулы 1У ,
CHgKHCO OH шсогсну -ан HJ-vNHcozCHj
3
обрабатывают водородом в присутствии никеля Ренея, палладия, солей палладия ИЛИ производных платины в инертн 4 м органическом растворителе с последующим .ацилированием полученного сбединения формулы У
снгШСОгСН инсогШз
-О.НHjvNHCOzCHj
0НО
инсогСНз
уксусным ангидридом в присутствии органического основания, полученное ацетатное производное формузщ У1
CH NHCOgCHj
К HJ-.шсогснз
-О
CHjCOO
кнсогСН)
подвергают кислотному гидролизу при Q 5р-70°С с последующим взаимодействием полученного соедийения формулы УП
снхннсогснз
/-он
К л о -Л- CHjCOO
с соединением формулы УШ
Из
он
.
i NN
-сн.
I Cl
оснгСбН5
в присутствии цианистой ртути в диоксане при KONiHaTHofl температуре с последующим повышением температуры до 50-70°с, полученную смесь j к -аномеров формул ix .и lXi
снгкисо снз
-6ч НН
NHCO/Hj
0НзСОО
СНз
хСОгСгну
s
СНз
оснгСбН5 ff
i H NHCO CHsКНСОгСНз
-о,нп)-уКНсогШз
CHjCOO
«нсогснз
обрабатывают в инертном органическом растворителе водородом в присутствии катализатора, выбранного из группы: палладий на угле, соль палладия или платины, производного платины, родия, рутения или никеля, с последующим снятием аминои оксизащитных групп путем обработки 8 щелочной среде, состоящей из гидроокиси бария или натрия в водно-спиртовом растворе и водного этанола,при 80-105°с спосле1370006714
дующим вьаделением целевого продукта 1. Фиэер Л., Фиэер М. Реагенты
в виде свободного основания илиДля органического синтеза. - М.,
соли.Мир, 1970, с. 187,-Успехи органиИсточники информации,ческой химии. - М., Мир, т.З,
принятые во внимание при экспертизе1966, с, 158-248.







Авторы
Даты
1979-11-25—Публикация
1975-10-27—Подача