Изобретение относится к способу получения нового производного дезоксисгреп амина формуль CH2WH2 или его солей, которые обладают биологической активностью. Известен 4-0-12 ,0 -диамино 2 ,6 -дидезокси, ct , Q -глюкопиранозил З метиламино-3,4,С -гридезокси-о,Т}-ксилогексопиранозиЛ) -2-дезоксистрептамин, который обладает биологической активностью i Предлагаемый способ получения N -(-)-2-гидрокси-4-вминобутирил -4-О- 2 ,б-диамино-2,6 -дидезокси-оС.В - люкопиранозил - -б-О- З -метиламино-3,4,.гридезокси- А ,D -ксилогексопиранозил}-2-дезоксистрептамина или его со лей заключается в том, что соединение формулы NHj А HjvNHj -/--о 2 dH подвергают взаимодействию с соединением формулы Б смеси диметилформамид (ДМФА в течение 20 ч при О - (-10) С тем Б течение 24 ч при комнатно пературе, образующееся соединени лы (;Н2-Ш1 и о -ОН2оНОподвергают взаимодействию с сое ем формулы IIОО K--0-C-CH-(CH2)-NH-C-Q-(lH ОН в смеси вода - 1,2-диметоксиэта чение 1ч при 1-1О°С, затем в 15 ч при 3-i5°C, образующееся еся соединение формулы сн,-«н-с-о-сн, Iи/ LoH о вн /он ) ноМ обрабатывают водородом в прису тализатора - палладия, в смеси океан при комнатной температура ние 6 ч и выделяют целевой про свободном виде или в виде соли. Солями целевых соединений м например, соли с соляной, броми ной, азотной, серной, фосфорной, уксусной, муравьиной, бензойной, мапеиновой, фума- РОБОЙ, янтарной, БНННОЙ, бензиловой, лимонной, щавелевой, глиоксалевой, аспарагиноБОй алкал- или арилсульфоновой кислот. В качестве растворителя вместо смеси. /лМФА - вода можно использовать диметилацетамид, диоксан, тетрагидрофуран (ТГФ), пиридин, воду, ацетон, этанол, метанол и 1,2 диметоксиэтан или их смеси. В качестве растворителя вместо смеси вода - 1,2-диметоксиэтан можно употреблять диоксан, диметилацетамид, ЛМФА, ТГФ, диметиловый эфир пропиленгликоля, воду или их смеси. Обработку водородом в присутствии катализатора - палладия проводят в растворителе, смешивающемся с водой, таком, как диоксан, ТГФ, 1,2-диметоксиэтан или диметилоБый эфир пропиленгликоля. Соли целевых соединений могут быть получены при обработке последних кислотами (см. выше), предпочтительно в растворителе, таком, как вода, эфир, метанол, ацетон или их смеси. Пример l.Nj - L -(-)-2-Окси 4-аминобутирил -4-0- 2 ,б-диамино-2 ,6-дидезокси-сС,В -глюкопиранозил «.6-0- з -метиламино-3,4,в -тридезокCK-cL, D-ксилогексопиранозил -2-дезоксистрептамин. -Амино-6 -бензилоксикарбонил- амино-2 ,6 -дидезокси-о1,Т) -г-люкопиранозил -6-0- 3 -метиламино-3,4,6 -тридезокси-оС, -ксилогексопиранозил -2-дезоксистрептамин , К раствору 5,5 г 4-0-(2 ,б-диамино-2 б -дидезокси-о(.,Т) -глюкопира-нозил)„6-О- З -метиламино-3 , 4 , 6 -тридезокси-оС,В Ксилогексопиранозил)-2-дезокси- стрептамина, в 58 см дистиллированной воды добавляют 60 см ДМФА при 2025С. Охлаждают до -5°С .и медленно вводят раствор 3,01 г Nj -(бензилоксикарбонилокси )-сукцинимида в 6О см ДМФА, перемешивают 20 ч при -5°С и 24 ч при 20-25 С. Выпаривают досуха и экстрагируют водой, насыщенной н-бутанолом. Затем промывают н-бутанолом, насыщенным водой, разделяют фазы и выпаривают досуха. Остаток 6,21 г и 2,82 г после вына- ривания водной и органической фаз соответственно подвергают тонкослойной (ТСХ) хроматографии на силикагеле в системе хлороформ - мегаиол - гидраг окиси аммо ния (4:4:1). Остаток после выпаривания водной фазы содержит получаемый проду в большем количестве. Его очищают с п мощью ионообменной смолы карбоксиль- кого типа в МИ -форме и элю1:руют О,1 и. раствором гидрата окиси аммония Выход 1,72 г . N )-(2-Окси-4-бензилоксикар бониламйнобугирил -4-О- 2 -амино-6 -бензилоксикарбониламино-2 ,6 -дидезок си-о., В-глюкопиранозил -6-О- З-метил амино-З ,4,б -тридезокси-о, D-ксилогексопиранозил -2-дезоксистрептамин 1,8 г полученного выше вещества рас воряют в 14 см дистиллированной воды и 14 см 1,2- 1иметоксиэтана, охлаждают до 5 С и в течение 1 ч приливают раствор 1,1 г N -оксисукцинимида слож ного эфира кислоты -L -(-)-4-бензилоксикарбониламино-оС-оксибутирата в 28 с диметоксиэтана. Перемешивают 15 ч при 5-10 С, выпаривают досуха в вакууме и подвергают остаток тех в системе хлороформ - метанол- гидрат окиси аммония (75:25:5). Выход 473 мг, R 0,45 в системе меганол - хлороформ - гидраг окиси аммон,ия (2:2:1). К, -(-)-2-окси-4-аминобутирил}-4-О- 2 ,б -диамино-2 ,6-дидезокси-ol.I)-глюкопиранозил -6-О- 3 -метил. амино-З ,4,О-тридезокси-Ь(., D -ксиЛогексопиранозил -2.-дезоксистрептамин 473 мг продукта, полученного на предыдущей стадии, растворяют в 6 см дистиллированной воды, 6 см диоксана и О-О 0,15 см уксусной кислоты, при 2О-25 С вводят 90 мг палладия на угле, барботируют водород, через 5 ч добавляют ЗО мг катализатора, барботиру- ют водород в течение 1 ч, прекращают перемешивание и выдерживают в течение ночи в атмосфере водорода. Катализатор отфильтровывают, выпаривают фильтрат досуха в вакууме и подвергают оЪтагок тех в системе метанол .хлороформ - гидрат окиси аммония (2:2:1). Выход 115 мг. Этот продукт очищают, пропуская-через ионообменную смолу карбоксильного типа в N форме и элюируютО,5н. раствором гидрата окиси аммония. Выход 82,2% . Лля соединения формулы vo но-с-и I (СПзЬ ЯМР пекгр (Bj,0), ppm; А - 1,2 Л - 6 cpS ); В - 2,54 з ДУблег, h - 4,28 (Н, мультиплег); Д 5,25 (Н-аномер, дублет. 3 4 ср S ) П р и м е р 2. Сульфат N. L -(-)-(2-окси-4-аминобутирил -4-О- 2 ,6 -ди- амино-2 ,б-дидезокси-(Л., ТЗ-глюкопирано- зил -6-О- 3 -мегиламино-З ,4, дезокси-оС, D-ксилогексопиранозил -2-дезоксистрепгамкна. 1,8 г N . -(-)-2-окси-4-аминобугирил -4-0- 2 ,б-диамино-2,6 -ди- дезокси-оС.В -г люк оп Иран о зил -6-0- з -метиламино-3 ,4,б -гридезокси-оСТ) - -ксилогексопиранозиН -2-дезоксисгрепт- амина растворяют в 120 см дистиллированной воды, подкисляют до рН 2 путем добавления 13,5 см 1 н. серной кислоты, концентрируют до 2О см и фильтруют через закаленный стеклянный фильтр. Концентрируют до 10 см и добавляют 20О см метанола. Полученную белую суспензию выдерживают 20 ч в .холодильнике, фильгруюг через закаленный стеклянный фильтр, белые кристаллы промывают метанолом и высушивают. Выход 1,87 г. аточный раствор выпаривают досуха и получают еще 0,35 г продукта, с. +76,5 ±2,5° (с-0,6%, вода). ЯМР-спектр ( 2)гО), ppm; 1,21 (CHj-CH, ублет, I 6 ср5); 2,75 (CHj-JsI); ,15 (Н 1); 6,03 (Н 1). Формула изобретения Способ получения производного дезок- систрептамина - М, -.L -(-)-2-гидрокси-4-аминобутирил -1-О- 2,в-диамнно-2,6-дидезокси-а1,11.-глюкопиранозил -6-О- з -метиламино-3 ,4,0 -тридезок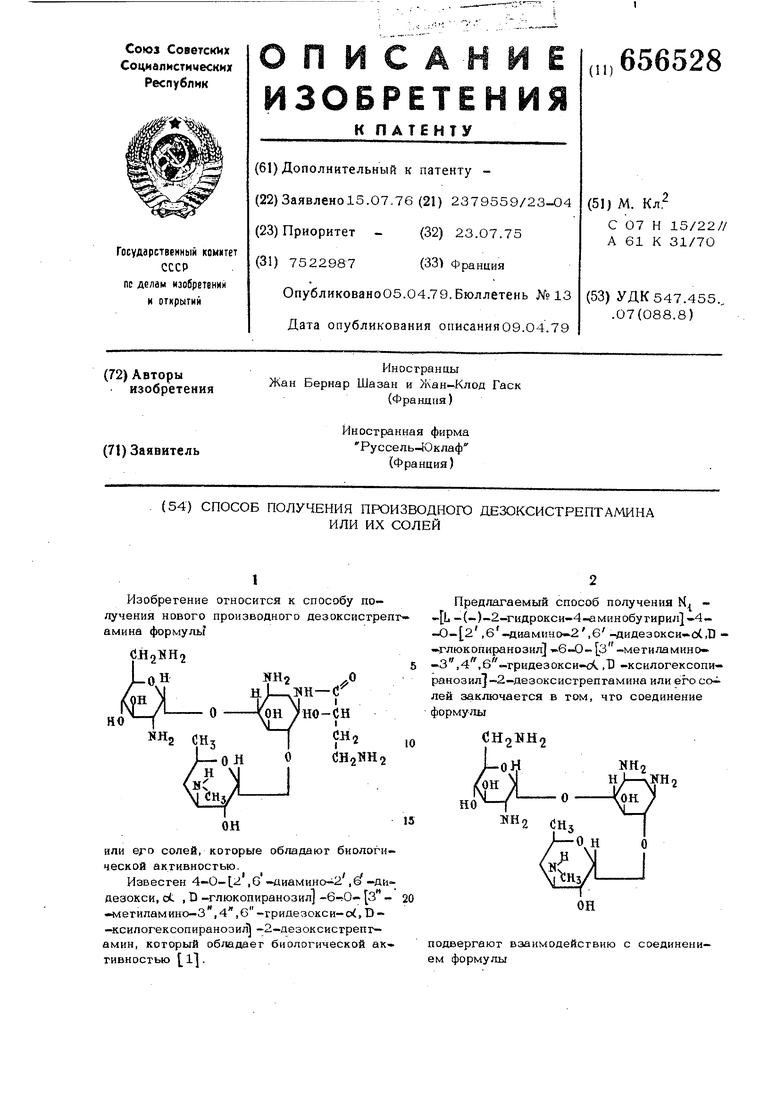




Авторы
Даты
1979-04-05—Публикация
1976-07-15—Подача