(54)
СПОСОБ ОПРЕДЕЛЕНИЯ ГЕТЕРОЗИСНОГО ЭФФЕКТА У ГИБРИДОВ ПЕРВОГО ПОКОЛЕНИЯ


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ анализа митохондриальной ДНК растений | 1990 |
|
SU1759334A1 |
| СПОСОБ ЗАКРЕПЛЕНИЯ ГЕТЕРОЗИСА ГИБРИДОВ | 2019 |
|
RU2759222C2 |
| Способ определения эмбриотропного действия микробных препаратов | 1988 |
|
SU1561036A1 |
| Способ определения гетерозисного эффекта у гибридов растений первого поколения | 1989 |
|
SU1708206A1 |
| СПОСОБ ВЫДЕЛЕНИЯ НИЗКОМОЛЕКУЛЯРНЫХ ЯДЕРНЫХ РИБОНУКЛЕОПРОТЕИДОВ (РНП) ИЗ ТКАНЕЙ И ОРГАНОВ МЛЕКОПИТАЮЩИХ | 2009 |
|
RU2422532C2 |
| СРЕДСТВО, СТИМУЛИРУЮЩЕЕ РЕПАРИРОВАНИЕ ПОВРЕЖДЕНИЙ, ОБЛАДАЮЩЕЕ ТКАНЕ-, ОРГАНО- И СТАДИЕСПЕЦИФИЧНОСТЬЮ И ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ | 2003 |
|
RU2238756C1 |
| СРЕДСТВО, СТИМУЛИРУЮЩЕЕ РОСТ ВОЛОС, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1998 |
|
RU2144366C1 |
| СПОСОБ ВЫЯВЛЕНИЯ КАНЦЕРОГЕННОСТИ ХИМИЧЕСКИХ СОЕДИНЕНИЙ | 2001 |
|
RU2223318C2 |
| Способ получения синтетической двунитчатой РНК, обладающей интерферониндуцирующей активностью | 1979 |
|
SU933001A3 |
| Способ получения гибридных клеток | 1983 |
|
SU1138412A1 |

Изобретение относится к сельскому хозяйству, в частности к селекции сельскохозяйственных растений. Известны способы определения гетерозисНог эффекта у гибридов первого поколения, по ко торым определяют содержание нуклеиновых кислот, в частности дезоксирибонуклеиновой кислотьт (ДНК), по величине которых судят о наличии гетерозисного эффекта 1 и 2. НедостаУ1 ами таких способов являются необходимость закладки полевых опытов и Длительность определения конечных результатов. Целью изобретения является сокращение сроков определения наличия гетерозисного эффекта и исключение закладки полевых опьпов Цель достигается тем, что содержание ДНК определяют в колеоптилях трехдневных проростков и по увеличению ее количества в клет ках гибридов по сравнении) с их родителями судят о наличии гетерозисного эффекта. Способ осуществляется следующим образом Семена гибриЯов и их родителей проращивают в питательном растворе Кнопа. У трехдневных прюростков снимают колеоптили, в ко торых определяют содержание ДНК ( в мг %) и число клеток, а полученные показатели ДНК пересчитывают на одну клетку. Для определения содержания ДНК колеоптили в количестве 2 г (свежего веса) гомогенизируют 10 мл холодного 95%-ного этанола, затем гомогенат переносят в центрифужные пробирки, добавляют еще 10 мл холодного 95%-ного этанола и центрифугируют. Центрифугат отбрасьтают. Осадок промьгоают следующими реактивами по 20 мл каждрго : 95%-ным этанолом - 1 раз при комнатной температуре; 50%-ным этанолом, подкисленным ледяной уксусной кислотой до рН 4,5 - 2 раза при комнатной температуре; 0,2 и. НС104 - 2 раза на холоде; 95%-ным этанолом - 1 раз при комнатной температуре; абсолютным этанолом с эфиром (3:1), прокипяченным с обратным холодильником 3 мин - 2 раза; эфиром при ком натной температуре - 1 раз. Далее осадок высушивают в вакуум - эксикаторе и взвещивают. Предварительно обработанный материал суспензируют 5 мл 03 н. раствора NaOH и инкубируют при 30 С в те3719566
ение 18 ч. Гидролизат центрифугируют и осаок промьгаают 5 мл 0,3 н. раствора NaOH.
Экстракт и промывной центрифугат соединят и к ним приливают 03 н. раствор NaOH до 0 мл. Осадок отбрасьтают. Соединенные эк- 5 тракты подкисляют 15%-ной НС 104 до рН 1, ыдерживают 40 мин при 4°С и . центрифугиуют. Центрифугат добавляют к фракции ДНК. бщий объем экстракта доводят водой до 25 мл.10
Осадок ДНК - протеин суспензируют 3 мл 0,5 н. раствора НС 10, нагревают на бане до 70°С и выдерживают при этой температуре 15 мин. Затем охлаждают и центрифугируют при .2°С. Осадок протеина промывают 2 мл 15 холодного 0,5 н. раствора НС 104 при , центрифугируют и промывной центрифугат соединяют с основным экстрактам. Общий объем экстракта доводят 0,5 н. раствором НС104 до 5 мл.20
Раствор ДНК замеряют на спектрофотометре против 0,5 н. раствора НС104. Затем проводят при длине волны 270 и 290 нм.
Расчет количества ДНК (в мг/мл) производят по формуле:2.5
270 Е290 ..,..
, ,------ - 1U,1,
0,19 п где Е ОптичеСкая плотностьГ,
п - вес навески, мг; 30
0,19- постоянный эмпирический выведенный коэффициент;
10,1- постоянный коэффициент для ДНК. Число клеток определяют путем мацерации кусочка ткани хромовой кислотой с последую- 35 щим подсчетом в капле взвеси числа клеток в счетной камере Фукса-Роз под микроскопом. Для каждого объекта подбирают концентрацию хромовой кислотъ и время мацерации, поскольку превышение оптимальных 40 для мацерации условий приводит к разрушению клеток. Для листьев пшеницы достаточно Г0%-ной хромовой кислоты в течение 18 ч.
Количество 1взятой хромовой кислоты зависит от количества мацерируемых кусочков. Для мацерации одного колеоптиля достаточно 1 мл ее. Перед подсчетом следует тщательно потрясти содержимое пробирки, чтобы получилась равномерная взвесь клеток. Если она слишком густая, ее разводят водой. Удобно считать количество клеток в взвеси такой густоты, чтобы в поле зрения (в одном большом квадрате камеры) было 30-50 клеток.
Подсчет проводят в четырех больших квадратах, взятых по диагонали счётной камеры в gj верхней и нижней сетках. После этого камеру прокп.шш, 1Гьй11рШг, заполнягвг и вновь подсчитывают в четырех больших ййадратах в каждой сетке. Эта же ошрация повторяется
и в третий раз. Таким образом, просчитываются по 24 квадрата из каждой пробирки.
Полученные цифры по количеству клеток в одном большом квадрате пересчитьюают на объем всей имеющейся в пробирке взвеси клеток и затем вътчисляют число клеток во взятом отрезке.
Для каждой пробы получают 24 цифры с учетом биологических повторностей, что дает 72 измерения для каждого варианта. Полученные данные подвергают математической обработке.
Установив число клеток на единицу свежего веса образца соответственными подсчетами показателей нуклеиновых кислот в мг % свежего веса, пересчитывают количество ДНК на одну клетку.
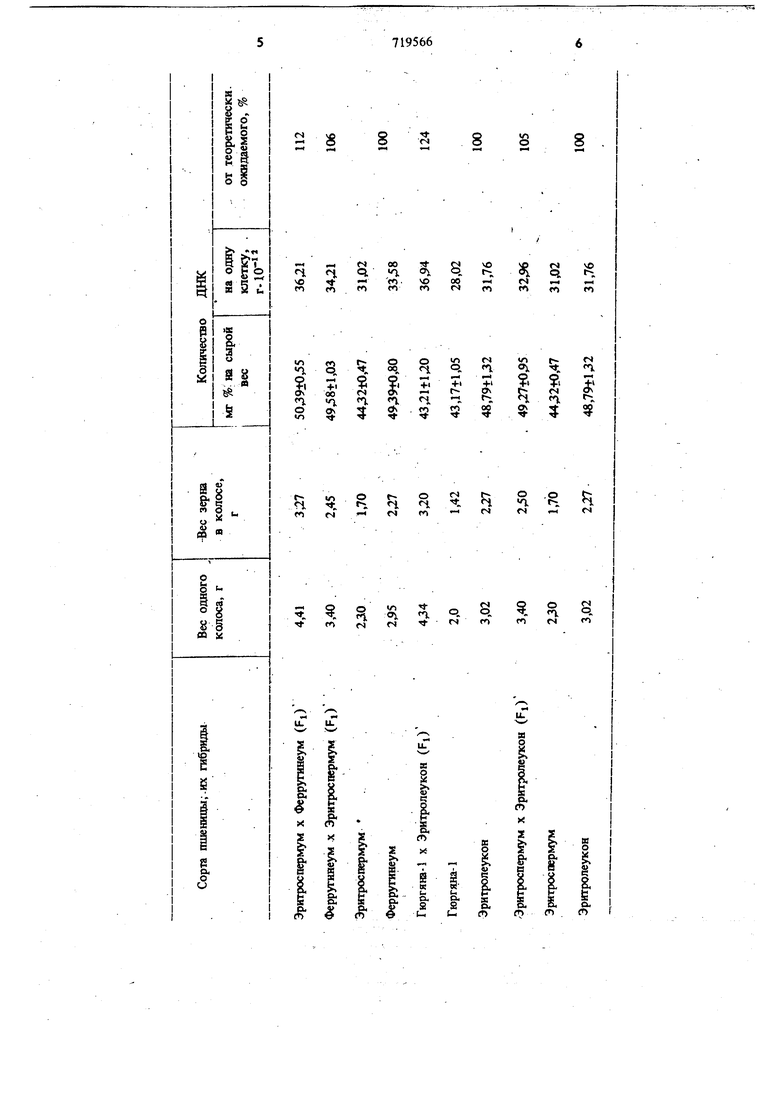
Полученные данные по содержанию ДНК в соматической клетке гибридов пшениц и их родителей приведены .в нижеследующей таблице Показатели, данные в графах 3 и 4 этой табЛИ1Ц)1, характеризуют продуктивность одного растен11я и гетерозисный эффект у гибридов.
Приведенные в таблице данные свидетельствуют об увеличении количества ДНК в соматической клетке проростков гетерозисных гибридов. При этом установлена прямая связь между уровнем гетерозисного эффекта и степенью увеличения ДНК в клетке. Так, например, гибрид Эритроспермум X Ферругинеум (Fj)no весу Одного колоса и по весу зерна в одном колосе резко отличается от своих родителей. У этого гибрида в соматической клетке содержится больше Д11К, чем в клетке родителей; Гибрид Ферругинеум х Эритроспермум попродуктивности не резко отличается от родателей. В соматической клетке этого гибрида количество ДНК увеличивается также не резко.
Таким образом, в соматической клетке гетерозисного гибрида ГюргяНа-1 х Эритролеукон. Отличающегося высокой продуктивностью, содержится больше ДНК, чем в соматической клетке родительских форм, а у гибрида Эритроспермум X Элитролеукон при заметно низком гетерозисном эффекте к6личе(;тво /ШК в соматических клетках увеличивается слабо. Все это доказывает наличие связи между уровнем гетерозисного эффекта у гибридов и степенью увеличения количества ДНК в соматических клетках..
Использование предлагаемого способа определения гетерозисного эффекта у гибридов первого поколения по содержанию ДНК в осмотических клетках гфоростков обеспечивает получение ожидаемого эффекта за очень короткое время, исчисляемое днями, отменяет необходимость в проведении-д;1ительных полевых опыто требующих Месяцы, а иногда и годы.
Ф о р м у л а из о я
Способ определения гетерозисного эффекта у гибридов первого поколения путёКГ определе ШйЩержйния в соматических клётйх гиб- s РИДОВи их родателёй дезоксирибонуклеиновой кислоты, отличающий с я Тгём, чти, с целью сокращения времени определет1я наличия гетерозисного эффекта и исключения закладки полевик опытов, содержаниедез6кс1фибо- Чо нуклеййовой кислоты определяют в калеопгилях трехдневных npopoctkoB ri по увеличению ее количества в клетках гибридов то сравнению
г Вй:йЕ 5 ;г.- - - V
3SSty - -:.nw.-.x --U:.
Р JP родителями судят о наличии гетерозисного эффекта.
Источники информации, принять1е во внимание при экспертизе
N 4. ; - . ..

Авторы
Даты
1980-03-05—Публикация
1978-09-08—Подача