чения, или выделяют в качестве целевого, продукта, или гидролизуют действием кислоты или щелочи для получения соединений формулы 1, где R- водород.
В качестве об -галоидалкилкарбоксилата формулы II предпочтительно используют, хлорметилацетат, пример хлорметилпропионат (или пропионилоксиметилхлорид), хлорметилбутират, хлорметилкапронат, хлорметилкаприлат хлорметиллаурат,хлорметилпальмиат, хлорметилпивалат или хлорметилбензоат.
Реакцию предпочтительно проводят в присутствии связывающего кислоту агента и нормально жидкого полярного растворителя, который инертен по отношению к реакции, но обладает способностью растворять исходные вещества. В общем случае 5-фторурацил и об -галоидалкилкарбоксилат смешиваются или легко растворяются в подоб ном полярном растворителе. Примерами полярного растворителя могут быть такие, как N, N- диалкилкарбоксиламиды, диметилформамид, диметилацетамид, и такие диалкилсульфоксиды, как диметилсульфоксид. В качестве растворителя также можно применять ацетонитрил..
В качестве связывающего кислоту агента используют предпочтительно неорганические основания, такие,как гидроокиси щелочных металлов,гидриды щелочных металлов, карбонаты и бикарбонаты щелочных металлов, и такие органические основания, как алифатические и ароматические третичные амины, .а также гидроокиси тетраалкиламмония. Предпочтительно применяют гидрид натрия, карбонат калия,триэтиламинаи пиридин. Если реагенты растворимы в подобном алифатическом или ароматическом третичном амине, то в этом случае часть или весь,полярный растворитель может быть заменен на такой третичный амин.
Реакцию предпочтительно проводят в температурном интервале от О до , лучше в температуры окружающего воздуха до . Время протекания реакции зависит от выбранной температуры реакции и составляет 120 ч, предпочтительно 2-10 ч.
По окончании реакции конденсации искомое вещество вьвделяют и очищают общеизйестными методами, предпочтительно путем хроматографической обработки . Реакционную жидкость фильтруют с целью выделения нерастворимых веществ, состоящих в основном из неорганической соли или гидрога логенида третичного амина, после чего применяемый растворитель удаляют дистилляцией, предпочтительно в условиях давления ниже атмосферного. Дистилляционный остаток подвергают хроматографической обработке, проводимой в колонке с силикагелем в качестве набивки; в качестве проявительного растворителя служит смесь бензола и этилацетата. Этой обработкой достигается отделе, ние сырого конечного продукта от 3замещенного изомера, образовавшегося в качестве побочного продукта, и от непрореагировавших исходных веществ. Дистилляционный остаток отбирают хлороформом и раствор в хлороформе фильтруют с целью отделения нерастворимого 5-фторурацила, промывают водой и высушивают. После удаления хлороформа дистилляцией получают сырой конечный продукт.в некоторых случаях продуктреакции может быть вылит в воду, в которой растворяется неорганическая соль или гидрогалогенид третичного амина,образовавшийся в ходе реакции конденсации, а водонерастворимые вещества, .включая конечный продукт, высаживаются. Полученный таким образом сырой конечный продукт может быть очищен путем перекристаллизации из бензола,
5 этанола или эфира, или путем растворения сырого продукта в хлороформеи вливания раствора в растворитель,в котором этот продукт не растворяется.
Для гидролиза Nj(, замещенного
0 урацила формулы 1.1 I предпочтительно используют сильную неорганическую кислоту или ее водный раствор, или каустическую щелочь,или ее воднь1й раствор и процесс проводят предпочтительно при температуре от О до в течение 1-10 ч.
Сильная неорганическая кислота, такая, как хлористоводородная или серная, как и их водные растворы,которые могут содержать смешиваемый
с водой органический полярный растворитель, может быть применена как кислота для гидролиза. Сильное неорганическое основание, такое, как едкая щелочь, может быть использована
5 в качестве .щелочи для гидролиз а. Особенно предпочтительно применение водного раствора едкой щелочи, например водного раствора едкого натра, который может содержать смешиваемый с
0 водой органический растворитель, например этанол.
Реакция гидролиза в качестве необязательной обработки обычно производится путем растворения исходного
5 Двузамещенного продукта общей формулы (III) в растворителе, медленного добавления в раствор кислоты или . щелочи или их водного раствора с целью поддержания величины рН жидкости в пределах 10-1,1 и перемешивания
0 смеси до окончания реакции гидролиза обычно при температуре от комнатной до , .в течение 1-8 ч, предпочтительно- 2-5 ч.
После .завершения реакции гидролиза реакционную жидкость концентрируют предпочтительно в условиях пониженного давления и охлаждают, в результате чего высаживается сырой продукт, который затем собирают в ходе фильтрования. Поскольку еврейпродукт содержит примеси, включая многие побочные продукты, например 3-замещенннй изомер, то его выделяют и очищают в соответствии с выше.укащанными способами обработки с использованием хроматографической обработки в колонке. Эта обработка может быть использована для превращения N, М,,-двузамещенного вещества, полученного в виде побочного продукта в первой из указанных реакций конденсации, в конечный продукт
Новые производные урацила формулы I обладают высокой противораковой активностью при слабых побочных эффектах и хорошо растворимы в иньекционной среде, поэтому их можно принимать перорально и в виде иньекций.
Пример 1. В50 мл диметил.ацетамида растворяют 6,50 г(О,05 моль) 5-фторурацила. Затем к раствору добавляют 15,18 г (0,15 моль), хлорметилпропионата. Смеси выдерживают 2 ч, реакционную жидкость оставляют стоять ночь и затем фильтруют для удаления осевшего хлористоводородного триэтиламина. Далее из фильтрата отгоняют диметилацетамид, остаток подвергают обработке в колонке с набивкой из силикагеля и при элюировании смесью бензола и . этилацетата (8:2-1:1) выделяют неочищенный 1-пропионоксиметил 5-фторурадил.Неочищенный продукт перекристаллизовывают из бензола и получают 7,93г чистых белых кристаллов, т.пл. 105Юб С.- Выход 73,1%.
айдено,%: С 44,50; Н 4,03; F 8,39; N 12,92.
CH H,5FN204.
Вычислено,%: С 44,45; Н 4,ZO; F 8,79; N -12,96.
ЯМР-спектр (растворитель JlM-SO d) S 1,05(ЗН, t,l З.СНэ), 2,37(2Н,д, I 8 , СОСН/р) , 5,63(2Н,5,СН20) ,8,-18 (d,l 6,С/-Н) и 12,05{1Н, широкая, NH).
ИК-спектр: 3420, 3200, 3080,2930, 1756, 1725, 1704, 1675, 1472, 1468, 1418, 1382, 1360. 1268, 1204, 1175, 1147, 1090, 1018,, 962, 900, 842, 812, 788 и 715cM-t
Пример2;в80 мл диметилформамида растворяют 10,41 г (0,08 моль) 5-фторурацила. Затем к этому .раствору добавляют 24,29 г (0,24 моль) триэтиламина. Далее к смеси в течение 15 мин по.каплямдобавляют 10,93 г (0,08 моль) хлористого бутирилоксиметила. Смесь выдерживают 5 ч при комнатной температуре и реакционную жидкость фильтруют для удалени
осевшего хлористоводородного триэтиламина. После этого из фильтрата отгоняют растворитель, остаток обрабатывают в колонке с набивкой из силикагеля и элюированием смесью бензол-этилацетат (1:1) выделяют неочищенный 1-бутирилоксиметил-5-фторурацил. Этот неочищенный продукт перекристаллизовывают из бензола и получают чистые белые кристаллы,т.пл. 96-98°С. Выход 86,9%.
0
Найдено,%: С 47,12; Н 4,73; F. 8,08; N 12,82.;
С(Н„ . Вычислено , %: с 46,96; Н 4,82; F 8,25; N 12,17.
5
ЯМР-спектр (растворитель ДMSO-d):
5 0,92 (3H,t,I 8,СНз), 1,60 (2Н, т,СН2), 2,35(2H,t.,l 8 , COCHj) , 5 , 6А (2H,S,OCH2), 8,17(lH,d, I 6,- Cx-H) и 12,02(1Н,широкая, NHj.
ИК-спектр: 34iO, 3290,3080,2970,
0 2920, 2830, 1740 (s), 1665, 1472, 1420, 1380, 1350, 1320, 1268, 1250, 1195, 1180, 1145, 1115, 1095,1040
1000,- 900, 880, 790, 770 и 725 см.
Примерз. В 50 мл диметилфор5мамида растворяют 3,90 г (0,03 моль) 5-фторурацила-. Затем к этому раствору добавляют 3,0 г триэтиламина и к смеси прикапывают 4,73 г(О,0237 моль) хлористого капроилоксиметила. Смесь
0 вьщерживают 3 ч при 50°С. По окончании реакции реакционную жидкость фильтруют для удаления осевшего хлористоводородного триэтиламина и диметилформамид удаляют из.фильтрата от5гонкой. Далее к остатку добавляют 50 мл хлороформа, смесь перемешивают и отфильтровывают для удаления нерастворимого непрореагировавшего 5-фторурацила. Хлороформную фазу
0 промывают водой, а затем сушат.После удаления хлороформа отгонкой получают 3,0 г 1-каприлоксиметил-5-фторурацила в виде белых кристаллов, т.пл. 95-9бс.., Выход 38,7%.
Найдено,%:С. 50,42; Н 5,63;
5 F 7 , 1 7 ; N 1 О , 2 .
С„ H,5F .
Вычислено,%: С 51,16; И 5,85; F 7,36; N 10,85.
ЯМР-спектр (растворитель CDClg);
0 890(3H,t,l 6,СНз). I.SMAJ,-/ .) , 1 ,б2(2Н,т„.СОСН2СН) , 2,it6(2H,t, |6.,-СОСН,г-) , 5,68 (2Н, S,N-CH2-), 7,62(1H,d,I 6,) и 9,85(1Н, широкая, NH).ИК-спектр:
5 3420, 3260, 3065, 2940, 2920,2850, 1720; 1684, 1655, 1463, 1408, 1368, 1255, 1200, 1168, 1137, 1108,972 и 780 см.
Пример4. В смеси 10 мл пиОридина и 10 мл воды растворяют 4р t (0,01 моль) 1 (бензоилоксиметил)-5-фторурацила. К раствору по капле при одновременном перемешивании добавляют 5%-ный водный раствор каустической соды, полдерживая та5
КИМ образом величину рН жидкости 10-11. Смесь выдерживают .в течение 4 ч при 60®С,. в результате чего проходит «елочной гидролиз исходного 1, 3;-бис- (бeнз6йjf:6кcймeтйл) -5-фторурацила. По окончании гидролиза реакционна жидкость концентрируют при понижением давлении и охлахсдают.весь оставшийся непрореагировавший 1j 3-бис(бензоилоксиметил)-5-Фторурацил осаждают и отфильтровывают, после чего фильтрат подвергают хроматографической обработке с использованием колонки, набитой силикагелем.Применяя смесь бензола и этилацетата (3:1) в качбстве элюента, искомый 1-бензоилокси-метил-5-фторурацил выделяют в виде первого компонента элюирования. З-Б-ензоилоксиметил-5-фторурацил, полученный в виде побочного продукта, также выреляют как второй компонент элюирования. Выход 1-бензоилоксиметил-гб-фторурацила и 3-бензоилоксиметил-5-фторурацила составляет соответственно 0,92 (выход 35%) и О ,65 г. После перекристаллизации из бензола получают 1-бензоилоксиметил-5-фторурацил в виде белых кристаллов,т.пл. 179-180°С.
ЯМР-спектр .(растворитель flMSO-d) :1-бензоилоксиметил-5-фторурацила:3 5,87 (2H,S,-Cri2-) , 7, 8 , 1 (5Н ,m ,-©) S,27(IH,d,l 6,) и 12,00 (1Н, широкая, NH).ИК-спектр: 3410,3385, 3365,3255 1730, 1720, 1700, 1659, 1597, 1463, 1449, 1408, 1372, 1272, 1260, 1242, 1200, 1165, 1144, 1106,
1091, 1068, 1041, 1023, 962, 778, 702 см.
Пример 5. В 100 мл диметилацетамида растворяют 19,51 г (0,15 моль) 5-фторурацила и 75,90 г (0,75 моль) триэтиламина. К этой смеси добаЬляют по каплям при комнатной температуре 41,05 г(0,165мол хло{эметиллаурата и смесь выдерживают 20 ч. После реакции триэтилами и диметилацетамид удаляют отгонкой и остаток выливают в 400 мл воды. Смесь перемешивают, профильтровывают, промывают водой и получают кристаллы, которые перекристаллизовывают из 200 мл этанола. Получают 38,06 г 1-лауроилоксиметил-5-фторурацила, т.пл. 113,7-114,. Выход 74,2%.
Найдено,%: С 59,94; Н 8,16; F 5,52; N 8,07.
С,7Н27РМг04.
Вычислено,%: С 59,63; Н 7,95; F 5.55; N8,19.
ЯМР-спектр (растворитель CDClg,): б 0,88 (3H,t,l a.C.Hj) , 1 ,24 (iBH.m, (-СН.)9-) ,2 ,38 (2H,t,l 8, СОСНд) , 5,бЗ(2Н,5,ОСНл) и 7,63(lH,d,l 6, ).
ИК-спектр: 3420,3200,2920 (S), 2850, 1755, 1710(5), 1б72,, 1450, 1372, 1360, 1325. 1267.1205. 1170, (s). 1090, ,1002, 99 980,972, 845, 790 и 720 см.
В табл. 1 приведены результаты синтеза производных урацила общей формулы 1, как описано в примерах 1-3 и 5.
Таблица 1




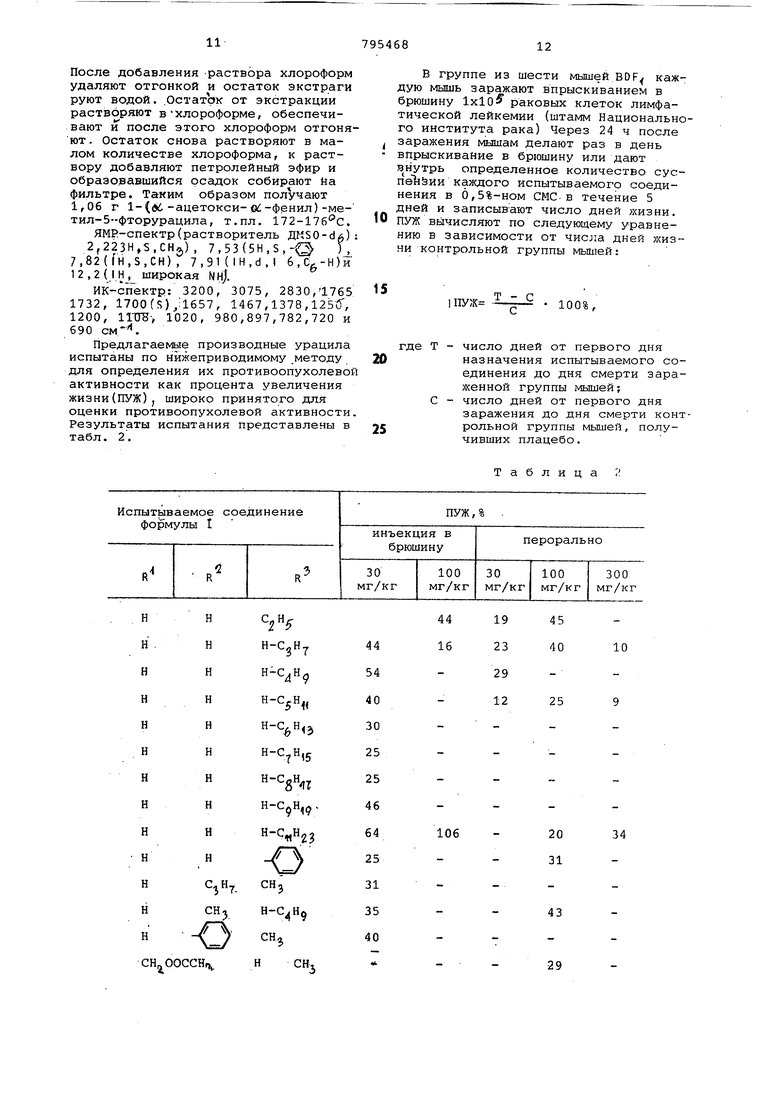
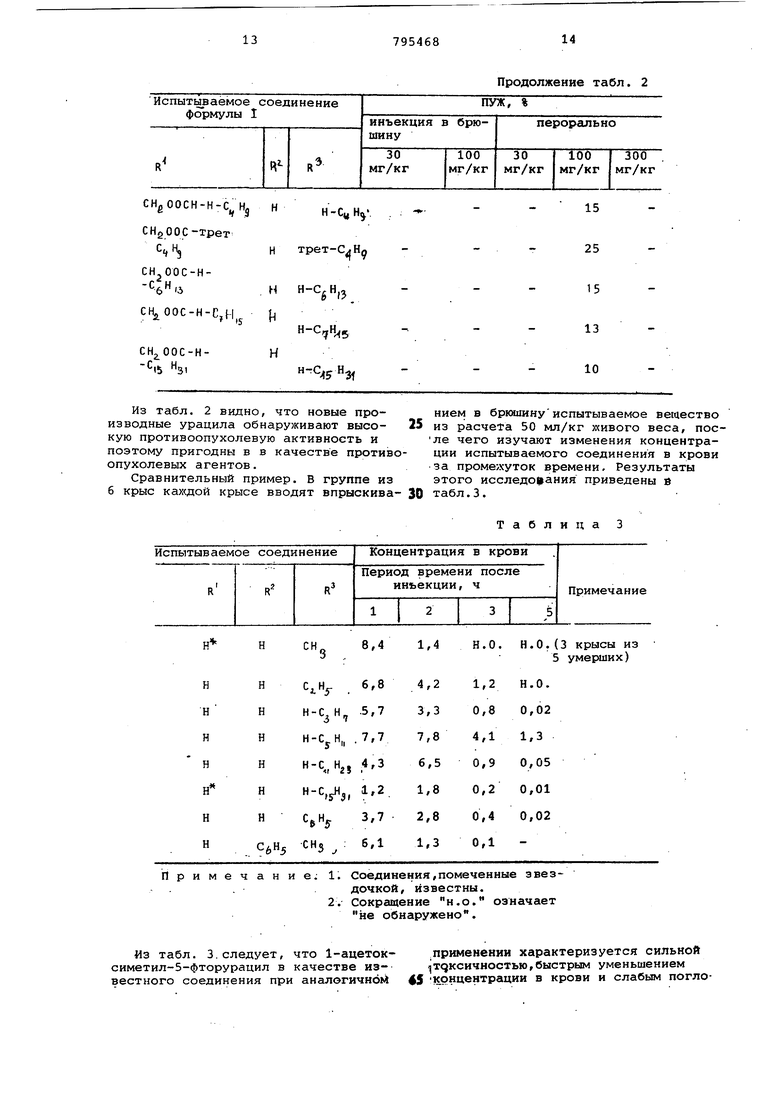


82,8
Н ,,
73,6
Н С-,Н |д
75,8
Н СдН,,
68,0
Н СдИ„ 38,3
CjH СН
12 57,0
сн ,
110 3410,2940,1730(5),1692
1463,1366,1254,1140 и 780
113 3420,2915,1728 (S) , 1693,
1462,1367,1255, 1140(5) И 782
112
3030, 292S, 1730(5) ,1695, 1468, 1372, 1260,1142(5) и 785
3060, 2910, 1720,1693(5) ,
116 1465, 1362, 1260,1140(5) И 780 176
3160, 3040, 1744, 1726, 1695, 1655, 1462, 1373, 1205(5) и 775
3170, 3055, 1739(5X1695,
0 1657, 1460, 1392,1265(5), 1170 и 1088(5)
Пример13, В70мл диметилацетамида растворяют 2,60 г (0,02 моль)-5-фторурацила. Кэтому раствору добавляют 0,96 г(0,02моль) 50%-ного гидрида натрия и затем раствор хлорметилацетата в 10 мл диметилацетамида. Смеси выдерживают 5,5 ч при комнатной температуре.По окончании реакции реакционную жидкость фильтруют для удаления осадка и затем диметилацетамид, применявшийся в качеству растворителя, удаляют из фильтрата отгонкой. Остаток извлекают в 100 мл эфира и эфирный раствор отфильтровывают для удаления нерастворимых продуктов. Эфир удаляют отгонкой и остаток подвергают адсорбционной обработке в колонке с набивкой из силикагеля. Адсорбированное вещество элюируют смесью (1:1)бензола и этилацетата и вьщеляют 180 мг 1,3-бис-(ацетоксиметил)-5-фторурацила с выходом 3,2%. Этот продукт - вязкая жидкость.
ИК-спектр: 3120, 2970, 1755(5), 1704(5), 1690(5), t7B. 1375,1285. 1230(5) , 1170, 1087, 1035(5) , 980, 8k2, 790 и 772см- .
П р и м е р 14. Аналогично примеру 13, но используя вместо хлорме1илацетата 6,10 г (О, О2 моль)хлорметилпальмиата, получают 1,02 г 1,3-бис-(пальмитил+оксиметил)- 5-фторурацила, т.пл. 80-80,, выход 15,2%.
Найдено,%: С -68,10; Н 10,24; F 2 ,65; N ,б9.
СэеНб гмгОбВычислено,%: С.68,43; Н 10,13; F 2,85; N Ц,20.
ЯМР-спектр (растворитель С ОС Ц): :6 0,87(6H,t ,CHg) 1 ,24(52H,m,CH2) , 2,30(,широкая - СОСН), 5,7l(2H, 5,СН20), 6,02(2H,SCH20) И 7,71 (lH,d,l 6, Сх-Н).
ИК-спектр: 2900, 2830, 1740(5), 1690(5), иб, 1355, 1280,. 11.62,956 864, 7бО и 72 .
Пример 15. В 40 мл диметилацетамида растворяют 2,60 г (0,02 моль) 5-фторурацила. Затем к этому раствору добавляют 1,52 г (0,011 моль) порошкового карбоната калия. К смеси прикапывают в течение 1 ч раствор 3,31 г(О,022 моль) хлорметилтриметилуксусной кислоты в 10 мл диметилацетамида.
Смесь вьщерживают 15,5 ч при комнатной температуре. По окончании реакции реакционную жидкость отфильтровывают для удаления осадка и затем диметилацетамид, применявшийся в качестве растворителя,удаляют отгонкой. Остаток извлекают 30 мл эфира и после фильтрации для удаления нерастворимых веществ эфирный- фильтрат концентрируют и получают- 2,52 г кристаллов. Последние перекристаллизовывают из эфира и получают 1,88 г 1,3-бис-(пивалоилоксиметил)-5- фторурацила с выходом 47,8% в виде белых кристаллов,т.пл. 113-114 С.
Найдено,%: С 54,02;н 6,69; 5 F А,99; N 7,72, C|6H23FN20.
Вычислено,%: С 53,62; Н 6,47; F 5,30; N 7.82.
ЯМР-спектр: 8 1,17 (9Н , 5 ,СНз),1.19 0 (9Н,5,). 5.63(2H,5,CHji), 5,83 (TH,5,CHj,) и 7,70(lH,d, 1,6, ).,
ИК-спектр: 3420, 2970, 1737(5), . 1685(5) ,, 470, , 1 366 , 1 268 , 1130(5), 1050, 1035, 980, 927,888,
5 855. 800,77 и 762 см-..
Пример 16. В 100 мл диметилформамида растворяют 7,80 г(0,06моль) 5-фторурацила. Затем к раствору доб,авляют 10,24 г (0,06 моль) хлорметил.. бензоата. К этой смеси прикапывают
медленно раствор 6,07 г (0,06моль) триэтиламина в 10 мл диметилформамида. Смеси дают реагировать в течение 6 ч при комнатной температуре. По окончании реакции реакционную жидкость фильтруют для удаления осевшего хлористоводородного триэтиламина и затем диметилформамид, применявшийся в качестве растворителя, удаляют из фильтрата отгонкой. Остаток
0 растворяют в 100 мл хлороформа и раствор фильтруют для удаления нерастворимых веществ. Фильтрат промывают, сушат и хлороформ удаляют отгонкой. Остаток очищают ь колонке с силикаге5 лем и получают 2,73 г 1-бензоилоксиметил-5-фторурацила, т.пл.178180°С, и 8,43 г 1,3-бис-(бензоилоксиМетил)-5-фторурацила в виде вязкого маслянистого вещества с выходами соответственно 17,1 и 35,4%.
0
ЯМР-спектр (растворитель ДMSO-dg):
S 5,87(2Н,5,- СН/г-), 7,,1 (5Н,т, -О ). 8,27(IH,d,l 6,)и 12,00 (IН, широкая NH.
ИК-спектр: 3410, 3385, 3365,3255, 5 1730, 1720., 1700, 1659, 1597,, 1463, 1449, 1408,-.1372, 1272, 1260,1242,
1200, 1165,- 1144, 1106, 1091,1068, 1041,.1023, 962, 778 и 702 см .
ЯМР-спектр-(растворитель JJM50-d)
0 1,3-бис-(бензоилоксиметил)- 5-фторурацила: S 5,5 А. 6,4 (4Н,т,-СН2-) и 7,4 ,2(nH.m,-O ,-СН-).
И -спектр: 3110, 3078,3000,1768, 1755, 1743, 1707, 1608, 1591, 1462,
5 1381, 1229, 1270, 1190, 1169,1100, 1073, 1055, 1032, 984,770,714 и 692 см-.
Пример 17. В 20 мл хлороформа растворяют 2,74 г (0,01 моль) 2 . -бис (триметилсилил) - 5 -фторурацила и 2,71 г (0,013 моль) бензальдиацетата. К этой смеси медленно доба вляют по каплям раствор 2г четырекхлористого олова в 10 мл хлороформа.
После добавления -раствора хлороформ удаляют отгонкой и остаток экстраги руют водой. .ОстатЬк от экстракции растворяют вХлороформе, обеспечивают к после этого хлороформ отгоняют. Остаток снова растворяют в малом количестве хлороформа, к раствору добавляют петролейный эфир и образовавшийся осадок собирают йа фильтре. Таким образом получают 1,06 г 1-(й -ацетокси-е -фенил)-метил-5 фторурацила, т.пл. 172-17бс.
ЯМЕ-спектр(растворитель flMSO-d): 2,,CH2,) , 7,53(5H,S,© К 7,82(IH,S,CH) , 7,91(IH,d,l 6,)и 1 2 ,2 ( I Н , широкая NH).
ИК-сНектр: 3200, 3075, 2830,1765; 1732, 1700(S),:1657, 1467,1378,1256, 1200, IITIH-, 1020, 980,897,782,720 и 690 см.
Предлагаемые производные урацила испытаны по нижеприводимому методу для определения их противоопухолевой активности как процента увеличения жизни(ПУЖ)у широко принятого для оценки противоопухолевой активности. Результаты испытания представлены в табл. 2.
В группе из шести мышей BDFy каждую мышь заражают впрыскиванием в брюшину 1x10 раковых клеток лимфатической лейкемии (штамм Национального института рака) Через 24 ч после заражения мышам делают раз в день впрыскивание в брюшину или дают в нутрь определенное количество суспеЪйии каждого испытываемого соединения в 6,5%-ном CMC.в течение 5 дней и записыв-ают число дней жизни. ПУЖ вычисляют по следующему уравнению в зависимости от числа дней жизни контрольной группы мышей:
Т - число дней от первого дня
назначения испытываемого соединения до дня смерти зараженной группы мышей; С - число дней от первого дня
заражения до дня смерти контрольной группы мышей, получивших плацебо.
Таблица
,
H-CgH
,.
CH-J
СН,
44 16
19 23 29
45 40
10
12
25
106
34
20 31
43 29
Из табл. 2 видно, что новые производные урацила обнаруживают высо- 25 кую противоопухолевую активность и поэтому пригодны в в качестве противоопухолевых агентов.
Сравнительный пример, В группе из б крыс каждой крысе вводят впрыскива- 30
Примечание; 1. Соединения,помеченные звез2. Сокращение н.о. означает Из табл. 3.следует, что 1-ацетоксиметил-5-фторурацил в качестве известного соединения при аналогичной
Продолжение табл. 2
нием в брюшинуиспытываемое вещество из расчета 50 мл/кг живого веса, после чего изучают изменения концентрации испытываемого соединения в крови за промежуток времени. Результаты этого исследования приведены в табл.3.
Таблица 3 дочкой, известны. не обнаружено. применении характеризуется сильной Т9ксичностью,быстрым уменьшением 45 концентрации в крови и слабым погло
Авторы
Даты
1981-01-07—Публикация
1977-09-06—Подача