(54) СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ БЕЛКА В БИОЛОГИЧЕСКОЙ ТКИДКОСТИ тельно-восстановительный потенаиал находится в пределах рН 6,,7. В процессе восстановления гетерополикислоты происходит постепенная нейт рапизация шепочных компонентов гидроли зукидей смеси кислыми компонентами реактива Фолнна-Чеоколте. При этом в Состав гидролизукхцей смеси входят инградиенты с различным рК- от рК Ю (ед кий натрий) и (рК входясщего в состав реактива карбоната натрия) до 10 (рК карбоната натрия) и, следовательно, в ходе реакции в зависимости от сротношения количеств щелочной гидролизирующай смеси и кислого реактива Фоя0на Чеоколте рН среды может стабил,взйровать ся в широких пределах 13-7-10,2. Это, в свою очередь, может обеспечить неадекватность процесса восстановления фосфомолибдатвояьфрамовой гетерополикиспоты с преимущественным вовлечением в процесс, восстановления фосфомолибдеиовой или фосфовольфрамовой поликислот с соот ветствующим изменением спектральных ха рактеристик получаемых гетерополисиней и, в конечном итоге, к искажению результатов определения количества восстановителя (белка). Следовательно, для того, чтобы обеспечить восстановление только одной из поликислот, входящих в состав реактива- Фоли1ш-Чеоколте, и стабильность спектральных характеристик, peaKJuaio необходимо -вести с таким расчетом, чтобы к концу проведения анализа киспотно щелочное состояние ее стабилизировалось в .определенном пределе это.обеспечит постоянство вовлечения и реакцию одной из.смеси поликислот и устойчивость образующейся гетерополисини. ото достигается эквимоляраой нейтрализацией щелочных.и кислотных компонен.гов гидролизуюшего реактива (смесь карбоната натрия и едкого натрия (1), и раствора Фолина-Чеокояте; диссоциацией в.этих условиях иона НСО j- имекшего рК2 10 рН 10,2, 0,5 мл реактива Фолина-Чеокопте, разведенного до кислотности, в 2,24 раза превышающей щелочность реактива 1), попностыр нейтрализуют едкий натрий с рК iO , входящий в состав 2 мл реактива 1), и карбонат натрия с , В этих условиях рН смеси стабилизируется в пределах 1010,5 за счет диссоциации иона HCOj, что обеспечивает избирательность восстановления фосфомолибдатвольфрамовой геерополикислоты, стабильность спектральых характеристик и оптической плотности образующейся гетерополисини, возможность проведения реакции при eiicoKofi температуре, ускорякадей процесс восстановления. В этих условиях достигается избирательность восстанозпения гетерополикислоты циклическими аминокислотами: цистнн цистеин, в концентрациях 100 мг на 10О млг раствора белка, аскорбиновая кислота и сахароза, в концентрациях 5ОО мг на 100 мл белка заменяют процессу восстановления. В этих услювиях также исключается необходимость связывания белка в биуретановый комплекс, что позволяет исключить из анализа этот этап, а следовательно, упростить проведение реакции. Пример 1.;Реактив Фопина-Чеоколте: 100 г вольфрамовокислого натрия и 25 г молибденовокислого натрия растворяют в 700 мл дистиллированной воды, добавляют 50 мл 8S% фосфорной кислоты и Мл концентрированной соляной кислоты. Смесь кипятят в круглодонной колбе снабженнойм обратным холодильником, течение 10 ч. Полученный реактив оттитровывают по фенолфталеину или под контролем рН- метра реактивом 1. Рабочий раствор готовят путем разведения реактива 2 дистиллированной водой до киспотности, в 2,24 раза превышающей щелочность реактива 1. И солздуемый раствор белка (сыворотка, плазма экстракты органов и тканей, растворы белковых препаратов - разведенные до содержания не более 10 мг бел-, -ка ла 1 мл раствора). Пример 2. ,О,2 м.п исследуемого раствора белка вносят в 2 мл реактива 1, пробы выдерживают 10 мин в кипящей водяной бане, охлаждают и вносят 0,5 МП рабочего раствЬра 2. Лополнительпо выдерживают в кипящей водяной бане 40 с, охяаждают и фотометрируют при 640-74О н в кюветах 3 мм. Найденную оптическую плотность проб , сопоставляют со стандартным графиком зависимости оптической плотности от конпентрашш белка. При проведении анализа данным методом окрашенный комплекс сохраняется в течение 48 ч, разрешающие способности метода- 2 микрограмма бепка в 0,2 мл раствора.
58051464
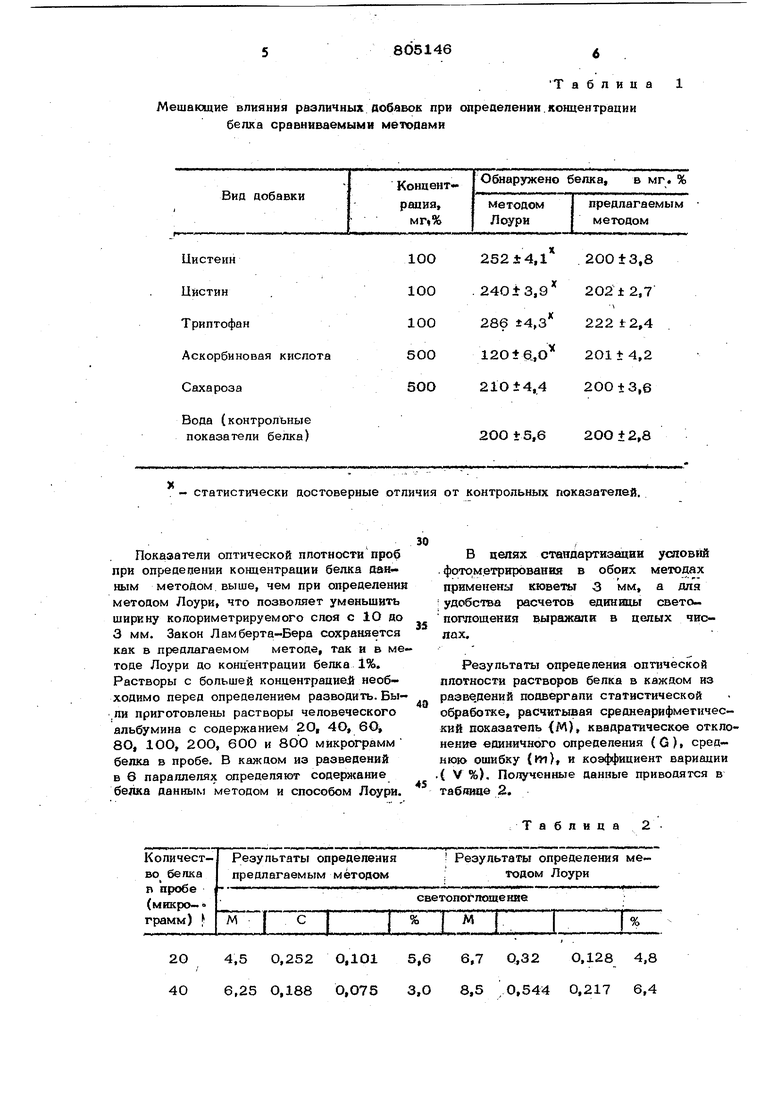
Мешаюцие влияния различных аобавок при опреаеленин.концентрации белка сравниваемыми метоаами
Таблица


| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ БЕЛКА В РАСТВОРАХ | 2004 |
|
RU2267132C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ СТЕПЕНИ ЭНДОГЕННОЙ ИНТОКСИКАЦИИ ОРГАНИЗМА У БОЛЬНЫХ РАСПРОСТРАНЕННЫМИ ХРОНИЧЕСКИМИ ДЕРМАТОЗАМИ | 2006 |
|
RU2333496C1 |
| Способ селекционной диагностики зерна кукурузы на наличие гена Опейк-2 | 1988 |
|
SU1642966A1 |
| СПОСОБ ОЦЕНКИ ТЯЖЕСТИ ОБЩЕГО СОСТОЯНИЯ БОЛЬНОГО С ОСТРЫМ ДЕСТРУКТИВНЫМ ПАНКРЕАТИТОМ И ПРОГНОЗИРОВАНИЯ ИСХОДА ЗАБОЛЕВАНИЯ | 2013 |
|
RU2568601C2 |
| Способ количественного определения истинного белка в кормовых дрожжах | 1986 |
|
SU1401380A1 |
| Способ количественного определения белка | 1984 |
|
SU1383201A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ЛИЗОЦИМНОЙ АКТИВНОСТИ БИОЛОГИЧЕСКИХ ОБЪЕКТОВ | 2005 |
|
RU2294373C2 |
| СПОСОБ ДИАГНОСТИКИ ЭНДОГЕННОЙ ИНТОКСИКАЦИИ ПРИ ОЖОГАХ В ЭКСПЕРИМЕНТЕ | 2002 |
|
RU2217753C2 |
| СПЕКТРОФОТОМЕТРИЧЕСКИЙ СПОСОБ ОПРЕДЕЛЕНИЯ БЕЛКА В БИОЛОГИЧЕСКИХ ЖИДКОСТЯХ | 2015 |
|
RU2593361C1 |
| Фармацевтическая субстанция для лечения инфицированных ран различного генеза | 2018 |
|
RU2687102C1 |

Цистеин
Цистин
Триптофан
Аскорбиновая кислота
Сахароза
Вода (контрольные показатели белка) - статистически достоверные отличия от Показатели оптической ппотности проб при опредепении концентрации белка ttatfrным методом выше, чем при определении методом Лоури, что позволяет уменьшить ширкну колориметрируемого слоя с 1О до 3 мм. Закон Ламберта-Бера сохраняется как в предлагаемом методе, так и в ме тоде Лоури до концентрации белка 1%. Растворы с большей концентрацией необходимо перед определением разводить. Бы,ли приготовлены растворы человеческого альбумина с содержанием 2О, 4О, 6О 8О, 10О, 2ОО, 600 и 8ОО микрограмм белка в пробе. В каждом из разведений в 6 параллелях определяют содержание белка данным методом и способом Лоури. 20 4,5 0,252 0,101 5,6 6,7 40 6,25 0,188 0,075 3,0 8,5
200+ 3,8
252 i 4,1 24Oi-3,9 2О2 ± 2,7
286 ±4,3
222 ±2,4 12О±6.,О
201t 4,2 2 lot 4,4 20О±3,6
2OOt5,620О±2,В контрольных показателей. В целях стандартизации yciiOBiitft . фотометрнрования в обоих методах применены кюветьт 3 мм, а для : удобства расчетов единши 1 светопоглощения выражали в целых числах. Результаты определения оптической плотности растворов белка в каждом из разве.дений подвергали статистической офаботке, расчитывая среднеарифметический показатель (М), квадратическое отклонение единичного определения (G) среднюю ошибку {т}, и коэффициент вариации ( V %). Полученные данные приводятся в табтаов 2. Таблица 2 0,32 0,128 4,8 ,0,544 0,217 6,4
805146 8
Продолжение табл. 2
Авторы
Даты
1981-02-15—Публикация
1978-03-22—Подача