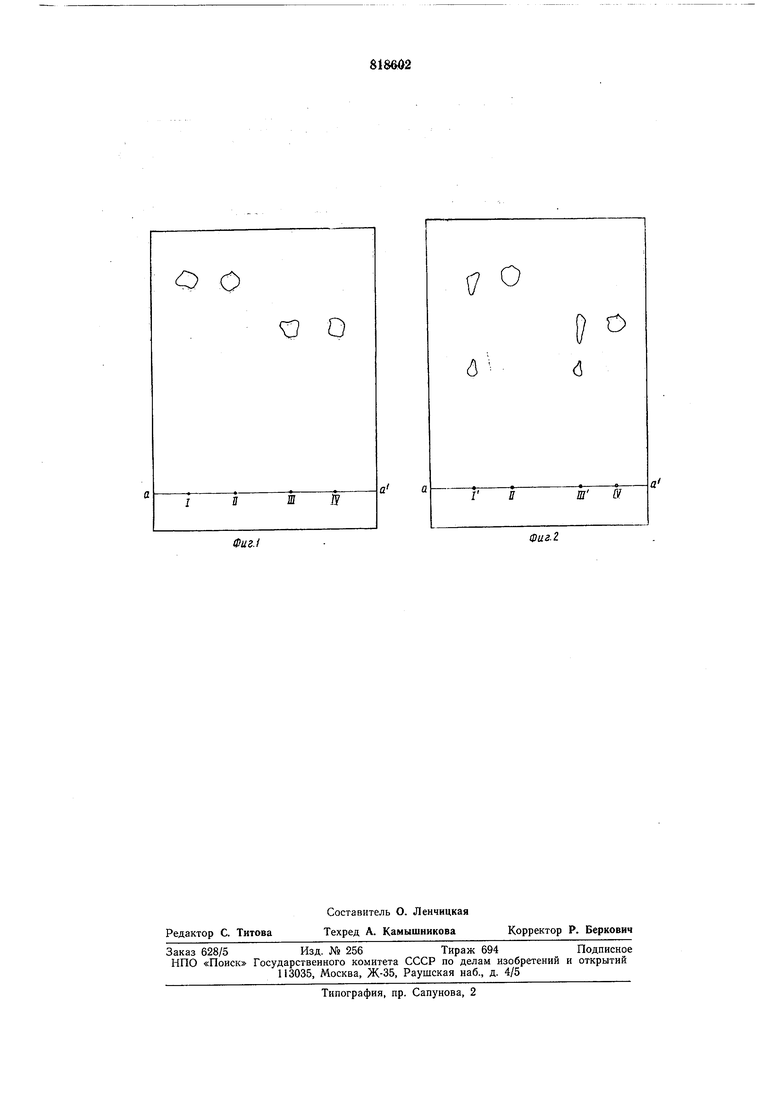
I - холестериловый эфир олеиновой кислоты, предварительно элюированный настоящим составом;
II - химически чистый холестериловый эфир олеиновой кислоты (свидетель);
III- триолеин, предварительно элюированный настоящим составом;
IV- химически чистый триолеин (свидетель) ;
I - холестериловый эфир олеиновой кислоты, предварительно элюированный кислотным растворителем Блайя-Дайера.
ИГ - триолеин, предварительно элюированный кислотным растворителем БлайяДайера.
аа - линия старта, на старт в точки I, П, III, IV, V и П1 нанесено одинаковое количество соответствующих липидов.
Разгонка липидов проводилась на пластине, содержащей люминесцентный индикатор, в малополярной системе растворителей: гептан-метилэтилкетон-ледяная уксусная кислота 42,5 : 7,5 : 0,5 (по объему). Локализация пятен проводилась в УФсвете.
Как следует из фиг. 1, настоящий состав практически не меняет нативности элюируемых липидов (I и III) при сравнении их со взятыми в качестве контроля чистыми липидами - свидетелями (П и IV). В то же время при исследовании липидов (Г и ИГ), элюированных кислотным растворителем Блайя - Дайера (прототип), наблюдаются деструктивные изменения при сравнении с контрольными чистыми липидами (II и IV). Пятна элюированных липидов (Г и ИГ) получаются менее четкими, размытыми. За ними тянутся щлейфы. Возможно появление дополнительных пятен, не свойственных данному соединению, что наблюдается на фиг. 2.
Подобные исследования были проведены с представителями всех основных классов липидов. Результаты были аналогичные. Полученные данные свидетельствуют о том, что кислотный растворитель Блайя-Дайера (прототип), в отличие от предлагаемого состава, не обеспечивает сохранность нативных свойств липидов.
Ввиду отсутствия деструктивного влияния на липиды настоящего состава отпадает необходимость в нейтрализации получаемого элюата.
Пример. Иа пластину для ТСХ, приготовленную по общепринятым правилам, либо стандартную пластину «Silufol, или какую-нибудь другую наносят на старт смесь липидов (общий липидный экстракт изучаемой ткани) до 50 мг.
После разделения смеси в подходящей системе на индивидуальные классы (фосфолипиды, гликолипиды, моноглицериды, стерины, диглицериды, жирные кислоты, триглицериды, эфиры жирных кислот, эфиры стеринов, углеводорбДЫ и др.) локализуют пятна известными в липидологии способами (в УФ-свете, парами йода и др.). Затем сорбент с отмеченных участков соскребают отдельно и переносят без потерь в пробирки с прищлифованными пробками и заливают в каждую по 25 мл смеси: хлороформ - метанол - гептан- ледяная уксусная кислота (20 : 10 : 10 : 1). Состав готовится предварительно простым смешиванием ингредиентов в указанной по объему пропорции. Все операции проводятся при комнатной температуре. Встряхивают пробирки в течение 15 мин
на механической качалке для элюирования с сорбента. Затем пропускают элюаты под небольшим разряжением через фильтр Шотта пористостью 40 в сухие бюксы. Остаток сорбента на фильтре промывают
25 мл вышеуказанной смеси. Фильтраты объединяют.
Общий выход липидов по каждому классу, определенный колориметрически, спектрофотометрически, денситометрически или
гравиметрически, составляет в среднем не менее 99%.
Предлагаемый состав апробирован на различных представителях следующих классов липидов: фосфолипиды, гликолипиды, моноглицериды, диглицериды, стерины, жирные кислоты, триглицериды, эфиры стеринов, углеводороды. Включение высших углеводородов, стеринов и их производных в число липидов объясняется тем, что они обычно связаны с мембранами и содержатся вместе с фосфолипидами и нейтральными липидами в экстрактах, получаемых с помощью растворителей, используемых для извлечения жиров.
Данные испытания состава на химически чистых индивидуальных липидах - свидетелях и их смесях - приведены в таблице.
Полученные описанным способом элюаты прозрачны, бесцветны и не требуют дополнительной обработки нейтрализующими агентами.
В случае необходимости разделения на пластине (пластинах) одновременно более 50 мг липидоБ количество состава должно быть пропорционально увеличено.
Липиды, находясь в элюате, могут сохраняться в холодильнике при-10°С 2-3 месяца. Элюат необходимо заливать в колбу под пробкой и держать в закрытом состоянии. В таких условиях в течение указанного срока не наблюдается деградация липидов.
Использование предлагаемого состава для элюирования липидов с пластин для ТСХ позволяет полностью элюировать одновременно все основные классы липидов, получать липиды в неизменном состоянии, а также исключает необходимость в дополнительной нейтрализации элюата, 56
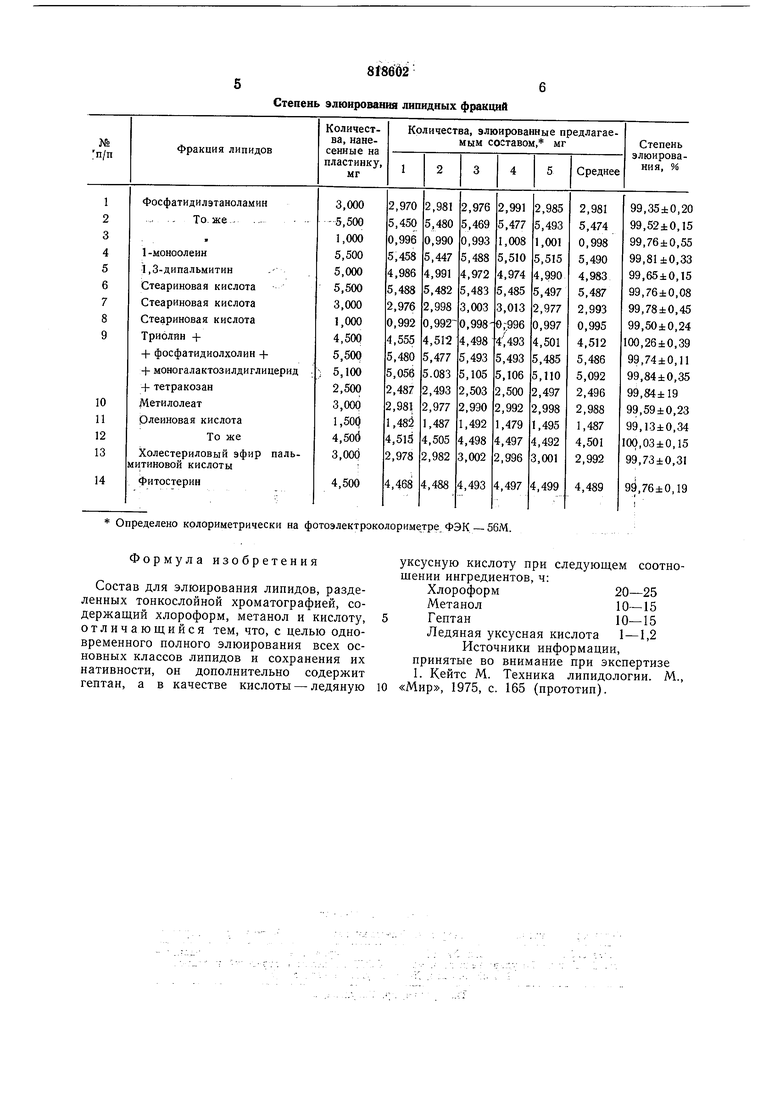
Степень элюирования липидных фракций
818602 

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ разделения липидов рыбьегожиРА HA фРАКции | 1978 |
|
SU824054A1 |
| СПОСОБ ВЫДЕЛЕНИЯ МОНОГАЛАКТОЗИЛДИАЦИЛГЛИЦЕРИНОВ ИЗ РАСТИТЕЛЬНОГО СЫРЬЯ | 2004 |
|
RU2280454C1 |
| Способ разделения липидов и полиэтиленоксидов | 1979 |
|
SU857096A1 |
| Способ определения стероидов в насекомых | 1988 |
|
SU1614774A1 |
| Способ индикации микроколичеств липидов | 1981 |
|
SU991304A1 |
| УСТОЙЧИВЫЕ КРИСТАЛЛИЧЕСКИЕ МОДИФИКАЦИИ ХЛОРИДА DOTAP | 2005 |
|
RU2463291C2 |
| СПОСОБ ПЕРЕРАБОТКИ БУРЫХ ВОДОРОСЛЕЙ | 2008 |
|
RU2360545C1 |
| СПОСОБ ОЦЕНКИ СТЕПЕНИ ЗАВЕРШЕННОСТИ ВОСПАЛИТЕЛЬНОГО ПРОЦЕССА В ВОССТАНОВИТЕЛЬНОМ ПЕРИОДЕ НЕСПЕЦИФИЧЕСКИХ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ ЛЕГКИХ | 1995 |
|
RU2101710C1 |
| ЦЕЛЕВЫЕ ВЕЗИКУЛЯРНЫЕ КОНСТРУКЦИИ ДЛЯ ЗАЩИТЫ КЛЕТКИ И ДЛЯ ЛЕЧЕНИЯ ИНФЕКЦИЙ H. PYLORI | 2000 |
|
RU2207113C2 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ КЛАССОВ ЛИПИДОВ И ПОДКЛАССОВ ФОСФОЛИПИДОВ В БИОЛОГИЧЕСКИХ МАТЕРИАЛАХ | 2011 |
|
RU2517086C2 |

Определено колориметрически на фотоэлектроколориметре ФЭК - 56М.
Формула изобретения
Состав для элюирования липидов, разделенных тонкослойной хроматографией, содержащий хлороформ, метанол и кислоту, отличающийся тем, что, с целью одновременного полного элюирования всех основных классов липидоБ и сохранения их нативности, он дополнительно содержит гептан, а в качестве кислоты - ледяную
уксусную кислоту при следующем соотношении ингредиентов, ч:
Хлороформ20-25
Метанол10-15
Гептан10-15
Ледяная уксусная кислота 1-1,2
Источники информации, принятые во внимание при экспертизе 1. Кейтс М. Техника липидологии. М., «Мир, 1975, с. 165 (прототип).
О о
с о
ш S
Фиг.
о
6
а а
-в-
Ж S
V и
Фиг. 2
Авторы
Даты
1981-04-07—Публикация
1978-07-13—Подача