(54) ПЕРБРОМИДЫ 2,4-ДИНИТРОФЕНИЛГИДРАЗОНОВ АЛИФАТИЧЕСКИХ И ЦИКЛОАЛИФАТИЧЕСКИХ КЕТОНОВ, ОБЛАДАЮЩИЕ ФУНГИЦИДЫЫЛАИ И БАКТЕРИОСТАТИЧЕСКИМИ
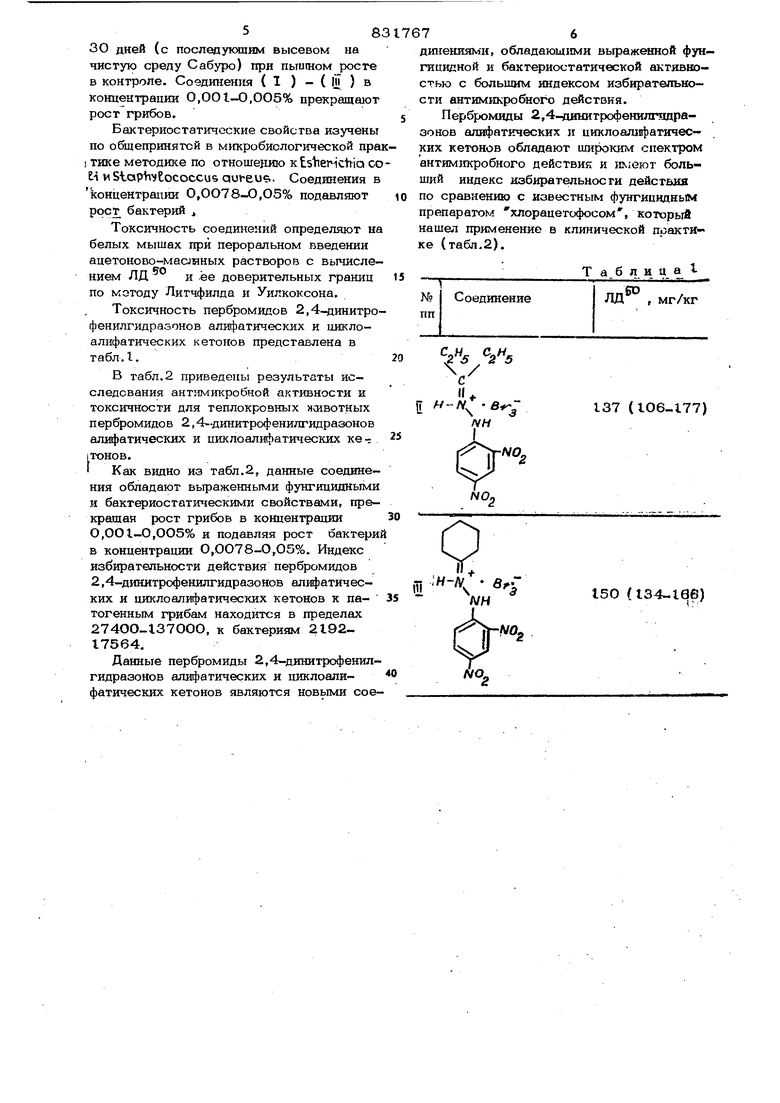
СВОЙСТВАМИ Поставленная цель досгигается применением пербромидов 2,4-динитрофенш1гидразонов алифатических и циклоалифатических кетонов общей формулы (I ). Пербромидьт 2,4-динитрофенилгидра ЗЕШЮВ алифатических и циклоалифатическюс кетонов получают взаимодействием 2,4-йинитрофенилгидразонов соответствующих кетонов с избытттом брома в уксусной кислоте. Пример I. Пербромид 2,4-динитрофенилгидразона ацетона ( 1 ). В суспензию 0,48 г (0,ОО2 г. моль) 2,4-динитрофенилгидразона ацетона в 20 мл ледяной уксусной кислоты добавляют в течение 5 мин при перемешивани раствор 0,58 мл (0,О1 г. моль) брома в 2 мл ледяной уксусной кислоты. Через 15-2О мин отфильтровывают осадоК; промывают уксусной кислотой (ЗхЮ мл) и получают 0,85 г (9О%) желтых кристаллов пербромида ( I ), которые растворимы Б ацетоне и эфире, слабо в спиртах, бензоле, уксусной кислоте и не растворимы в воде. При нагр вании в кристаллах и в растворе пербромид { 1 ) постепенно выделяет бро и превращается в исходное coeдшieниe. Аналитически чистый образец поэтому получают последовательной промывкой кристаллов уксусной кислотой, бензолом и эфиром, УФ-спектр в эталоне, ., 228; 27 363; 428. Найдено, %: В)- 5О,27. N404. ,, Вычислено, %: ВГ 50,10. . П р и м е р 2. Пербромид 2,4-динитрофенилгидразона диэтилкетона (1). В суспенгчию 0,52 г {0,ОО2 2,4-.динитрофенилгидразона диэ тилкетон в 2О мл ледяной уксусной кислоты добавляют при перемешивании в течение 5 мин раствор 0,58 мл (0,О1 г.моль брома в 2 мл ледяной уксусной кислоты и перемешивают еще 15-2О мин при С. Затем отфильтровывают осад и после промывки уксусной кислотой п лучают 0,1 г (92%) оранжево-желтых кристаллов пербромида (Л ), которые растворимы в ацетоне и эфире, слабо растворимы в бензоле, спиртах, не раст воримы в петролейном эфире и воде. При нагревании выше 4О С в кристалл я в растворах пербромид( и ) выделяет б и превращается в исходный гидразоя, по э му аналитически чистый образец получают Последовательной промывкой кристаллов уксусной кислотой, бензолом. немного эфиром и тщательно петролейным эфиром. ИК спектр в вазелине, (NH), 2486 шмР (Н), 1655 Ujvip tuucj (). УФ-спектр в этаноле ,Лллакс (9 f-f): ; 23О (4,23); 266(4,О8); 369 (4,16); 443 ( 3,54). Найдено %: Вг 47,41. 04 Вычислено, %: Вт 47,33. П р и м е р 3. Пербромид 2,4-динитрофенилгидразона циклогексанона (W). В суспензию 0,56 г (0,002 г«моль) 2,4-динитрофенилгидразо на циклогекс анона в 20 мл уксусной кислоты добавляют при перемешивании в течение 5 мин раствор 0,58 мл (0,О1 г.моль) брома в 2мл ледяной уксусной кислоты и перемешивают еще 15-20 мин при 2О-25С. Осадок отфильтровывают, промывают .уксусной кислотой и получают 0,95 г (90%) желтых кристаллов пербромида ( IJ ), которые легко растворяются в ацетоне, эфире, слабо в спиртах, бензоле и не растворимы в воде и петролейном эфире. При нагревании выше 40-50 С в кристаллах и в растворах пербромид ( Ш ) выделяет бром и превращается в исходный гидразон, поэтому аналитический образец получают последовательной промывкой кристаллов уксусной кислотой, бен- золом, немного эфнро: : и тщательно петролейньгм эфиром. ИК спектр в вазелине, см : 32О7 (NH), 255б1 д,р(), 1650 (. |УФ-спектр в эталоне, Л т10|ц( 2Q-E-i ) : 232 (4,23); 265 (4,О4); 37О (4,2О); 445 (3,54) . Найдено, %: Вг 46,01, ВГ Вычислено, %: Вг 46,24. Стабильность пербромидов значительно увеличивается в ряду ( I ) (Ц ) ( а ). Фунгипидные свойства пербромидов i( X ) - ( (ц ) изучены по отношению к грибам - возбудителям дерматомикозов человека и животных: THclioplivton Vub Mjvii,Tr4c1iop1i)ton nievigrag c p1i:jtes, M-icroSpOY-um conis,. грибам-сапрофитам, возбудителям плесневения - Asperg-iEE-os viig-ev, FusQYMUvYi qveir c(, AEternavna sp.Hetm-in-T foSpor-iuYM ep. и к представителю дрожжё подобных грибовCcsndida atticans. Культуры грибов засевают на твердую среду Сабуро, содержащую возрастающие дозы соединения. Критерием противогрибковой активности считают отсутствие роста гриба в течение ЗО дней (с последующим высевом на чистую среду Сабуро) при пьшшом росте в контроле. Соединения (1)-(|1|)в концентрации 0,О01-О,ОО5% прекращают рост грибов, Бактериостатичоские свойства изучены по общепринятой в мтсробиологической пра 1 тике методике по отношению KtslieHctria со Н wStaplivEococcus auireu.. Соединения в koHueHTpanHH 0,ОО78-О,О5% подавляют рост бактерий Токсичность соединений определяют на белых мышах при пероральном введении ацетоново-масляных растворов с вычислением ЛД ° и ее доверительных границ по мотоду Литчфилда и Уилкоксона. Токсичность пербромидов 2,4-динитрофенилгндргззонов алифатических и циклоалифатических кетонов представлена в табл.1. В табл.2 приведены результаты исследования ант21микробной активности и токсичности для теплокровных нжвотных пербромидов 2,4-динитрофенилгидразонов алифатических и циклоалифатических кеiToHOB. Как видно из табл.2, данные соединения обладают вьфаженными фунгицидными и бактериостатическими свойствами, прекращая рост грибов в концентрации О,ОО1-О,ОО5% и подавляя рост бактери в концентрации О,ОО78-О,О5%. Индекс избирательности действия пербромкдов 2,4-динитрофенилгидразонов алифатических и циклоалифатических кетонов к патогенным грибам находится в пределах 274ОО-137ООО, к бактериям 219217564. Данные пербромиды 2,4-динитрофенилгидразонов алифатических и циклоалифатических кетонов являются новьтми сое876 динешими, обладающими вьфаженной фун- гицидной и бактериостатической активностью с большим индексом избирательности антимикробного действия. Пербромиды 2,4-динитрофенилгндразонов алифатических и циклоалифатичес- ких кетонов обладают широким спектром антимикробного действия и имеют больший индекс избирательности действия по сравнению с известным фунгицидным препаратом хлорацетофосом, который нашел применение в клинической практике (табл.2). Таблица t |Г1.37 (1О6-177) 1 «-л; 150 (134-iee)
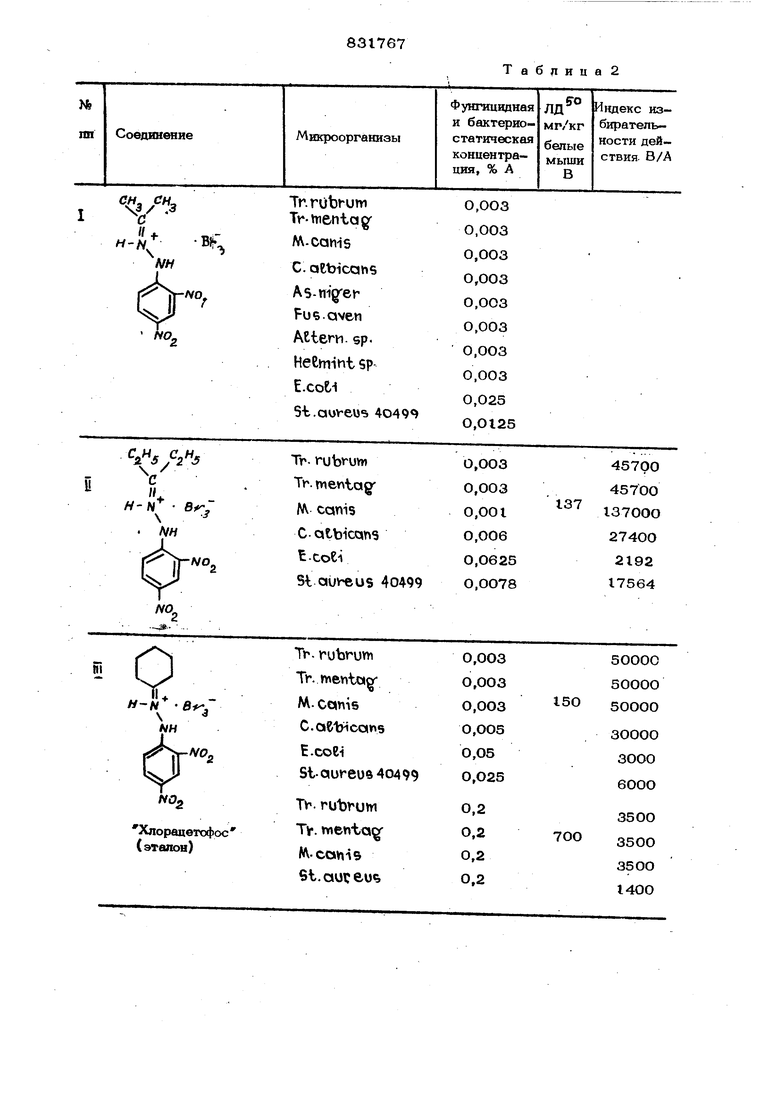
Та6пица2 983 Формула изобретения Пербромид. 2,4-динитрофеШЛгидразонов алифатических и циклоалифатических кетонов общей формулы Я+/7 с / -л/и-() NO 767lO где RH- Rj -СИ,,; С.,Н ; F. + R i t(J /.Эи3. -(СН )g., обладающие фунгицидными и бахтериостатическлми свойствами, Источники информации, принятые во внимание при экспертизе i.F.z-Scott et.ae.,S: hthe3is of aiihf pe -hcie-ide ddducts.. J.cVieni-Soc.Cc,. 1970, p. 2674.




Авторы
Даты
1981-05-23—Публикация
1979-11-29—Подача