C Ilpt f ( НШЧР ( iH Л -t И MO1 1 II 41 1 II
применение n i1 i n .i J ни, ti rai н
КГПН Г ПО iIIIi г и ц - i при p к
ТОП j i i IpClBf HIM
пречар 11
HP P iИ114 fp 1 -maooi I 1
НОПО1 П ( r ГО УЧРНИЯ UHl X Г) ИЛИ
6-я 1мi ) i POMI L ч п чиц с p , 1
хнн i iii тцн ч и I ; ( Ь или эН) , обшдпоLHfHv Ш ( J M 1U
Погтн i и i чл пг достиг at 1с я злЧ ГИТ I I ll 1 1 1 ( r
том, что „j или b-) MI HI in ne IK ч SHMH даяоГ ,1 1| ил 11 нош - f или 5H) н ( i h i in I
r,
III
ni if
гдь. К,- 1, ч,, HI i i г i и i ( , p бен зи i, i и i i i-1 ч ар i i t и ,i ч
си)a i , ,i т и , in
a и ил, ibi t, , u . щ п т pt mи i i i ii, p и i i
ПО 1 4t II ,i V1
цен тр HI ii i
i
КИС ШI ,
в wo1 4 i
O1 HOI 1
Konpet (iii fi
нечгр ни11. гтмi
к тлПс 11 P
ITJI-Q-nj kL I 1 11 (
Jl -Ч10Н 1-17
я) i ipc i j t PO
ifli ci - i i iн нх и . i
XHHP onunoii 1 )|0
, ,4 i 1, If. II i
,1-Ь| и я i гн ( Ь Ь рсн
TJnp in i ii-i (
при °0 ( , HOii и i i i i
бромп i niu HOIi i лчu i TI и1 т ц
lejibHi 11i i i i
балляют 1 , (i HI txi Г ром1„ I
обрЯП 11 1BIUI 1 Tli I 1 nr I OT 1 p
ляют 1 50 M i IP n P чрр -.- , tn i . , 1-b j vim i o
1 ( I 1И 1 1Ы1 lltlHI I 11 )41 ib (ЮГ, UpCiMjii int i i i и i i 10 мл иол ши диет
т
, )
HI I1 I i i S Р I 3
Н Ч1 I I Mlill
-( i ( i гр 1 н Q с i f 0
И -. v 1,1,1,,
I r | , u , I f , Ь
w °
B l ПК ft HO, f U), / ; 1 „ q ,
ir O.O; i ,h
I1i i i( (n) i i 1MHг цазп 2, 1 -Ь j лиьнопинон i- ; hlO
i i ii; (4 M i „ i MI и з i нда t ,1 Ь пи г НПШН i 12 f)H 1 p IP г в О i П II ti iii В Ч Ы I i run H ii
in if i j tiiiii 11 p i 11 i n при
) I I pll IIII l Ц Mi 1 1 I I II II
t iM1iipn 1 U 1i i IM 14 p Kii i i тип при тег нора -
jIIU I I n 1Я )
i t Ьi i i и i n in pic i iI ( ii ( I . 4)
II HiII 1 I 1 f - i 1 I M
I,) J iII ( 1 pi ч j nj n И jT fi I II lH ЗИИ1 , H
IIit1IU i IT л l L 3 МЧН
10 fIII 1 1 r I1(1 OI II ( 1 ГЯ
/
0 i HI и i 11 ( i 11 ш p i in ч j Hi L (. и ни M, шгцшмер,
I1p u i p M t 11 i in 441 ам 1 ч1 ( Ч1Ч 11 i It 1 1 1 U 1 j И ТЫ нч i i ,) i ( Л/ )j пh ill I л
к н , t i , , H .,0; Вт 4,3;
i
S
. , n V;
ii i Ч -rpo iOi it т i i т 1 i ii i jipi,
1 II И I 1 H I , 1 } 1
1i ii l О p 11, ПП 1
HIiji1 U, 1- j Я O4tlH
MlTI p К J V p p jf 1РЛЯПТ
1 /5Ml MI , ) H I di p juKll T3t,iTH i е т п p1 11 j ч i i 90° С до i n in i о (i i ч m ii и J мин Охла
ЧЯ) 1,4I т О1ОМ HTj ОМ, И
бс цпетн зр LT i ii i mm i ii-л pouii-
t HIT ,
lit 01 I ,( 1(
r i ( 1 , i I
ЧЛ 61
1 1
(
. ,1-. ,
i in нчи i i ,,4 1 ;
U( 41
(f} t OH
Пербромид гидробромида получают аналогично примеру 16, но образовавшийся желтый раствор разбавляют 100 мл воды (1:2) „ Выпавшие желтые кристаллы нагревают при перемешивании при 90°С, Полное обесцвечивание наблюдается через 15 мин. Охлаждают до комнатной температуры, нейтрализуют концг аммиаком и фильтруют бес- цветные кристаллы
Выход 2,67 г (81,6%), т„ пл, 261- 262°С (из ДМФА)„
д) Получение 6-метил-9-бромбенз- имидазо 2,1-bJ хиназолинона-12(6Н) при соотношении воды 1:5,
Пербромид гидробромида получают аналогично примеру 16, но образовавшийся желтый раствор разбавляют 250 мл воды (1:5)о Выпавшие желтые кристаллы нагревают при перемешивании до 90°С и выдерживают при этой температуре до полного обесцвечивания комплекса (3 мин) Охлаждают до комнатной температуры, нейтрали- зуют конц аммиаком и отфильтровываю бесцветные кристаллы
Выход 2,88 г (88,1%), . 261- 262°С (из ДМФА),
Таким образом, наиболее оптималь- ным является соотношение реакционной массы и воды 1:(3-3,5), Увеличение или уменьшение количества воды сказывается на выходе искомого продукта и времени продолжительности реакции
Приведенные в таблэ 1 соединения 1а-и, л-о получены аналогично примеру 16 Для получения соединения 1к реакционную массу после обесцвечивания желтого комплекса охлаждают и без последующей обработки основанием отфильтровывают Во всех случаях при уменьшении температуры нагревания на конечной стадии до 80°С время обесцвечивания комплекса увеличивается до 5 мин, что, однако, не влияет на выход искомого продукта о
П р и м е р 2. Взаимодействие соединения III (R - CH-j) с бромом в воде.
2,49 г (0,01 моля) 6-метилбензими ,1-bf хиназолинона-12(6Н) суспензируют в 50 мл воды и при тщательном перемешивании прибавляют 1,6 г (0,01 моля) брома. Несмотря на дли- тельное тщательное перемешивание, бром связывает только половину соединения III, что и наблюдается визуально: в виде осадка в воде находятся
5
5
0
о
0
5
-И
5
оранжевые кристаллы пербромида и бесцветные кристаллы исходного соединения. Их отфильтровывают.
Выход 4,21 г,
ИК-гпектр: 1700, 1685, 1/18 амидные
Пример 3 .Взаимодействие, соединения III (R - СН}) в условиях - предлагаемого способа с бромом без предварительной обработки НВг.
2,49 г (0,01 моля) 6-метилбенз- имидазо{ 2,1-bl хиназолинона-1 2(6Н) растворяют при нагревании в 50 мл ДМФЛ и при тщательном перемешивании при 60-/0°С добавляют 1,6 г (0,01 моля) брома. Полученный оранжевый раствор разбавляют 150 мл воды и выпавшие оранжевые кристаллы отфильтровывают ,
Выход 4,19 г0
ИК-спектр: 16/5, 1685, 1/18 см амидные
На основании данных ИК-спектра видно, что образуется комплекс состава HI (R -С1Ц) и брома 1:2, т,к полосы 1675 и 1718 см-1 являются характерными для пербромида,
Пример 4 Взаимодействие соединения III (R -СН) с бромом в условиях предлагаемого способа, но после добавления воды,
2,49 г (.0,01 моля) 6-метилбенз- имидазо 2, 1-1-Г хиназолинона-1 2(61) растворяют при нагревании в 50 мл ДМФА и при тщательном перемешивании при 80-90°С добавляют 3 мл копц, бромис- товодородной кислоты. Разбавляют 150 мл и при перемешивании на выпавшие бесцветные кристаллы действуют 1,6 г (0,01 моля) брома„ Несмотря на длительное тщательное перемешивание, бром связывает только половину исходного соединения, что и наблюдается визуально: в виде осадка находятся оранжевые кристаллы пербромида и бесцветные кристаллы бензимидазор, 1-bj хиназолинона-1 2(6Н), Их отфильтровывают
Выход 4,21 г
ИК-спектр: 1675, 1685, 1718 см амидные
На основании данных ИК-спектра видно, что образуется комплекс состава III (R -СН3) и брома 1:2, т„к„ полосы 1675 и 1718 являются характерными для пербромида
Пример 5, Встречный синтез Ь-метилбензимидазор, 1 -hf хиназолино-i
716
(6Н) сплавлением 5-бромбензими- дазол-2-сульфокислоты с антраниловой кислотой с последующим алкилирова- нием„
а)Синтез 9-бромбензимидазоГ2,1-bJ хиназолинона-12(6Н) 2,/6 г (0,01 моля) 5-бромбензимидазол-2-сульфокис- лоты сплавляют при 140-160°С с
1,3/ г (0,01 моля) антраниловой кис- лоты в течение 1,5 ч до полного прекращения выделения 50i, Охлаждают, обрабатывают 20 мл 10%-ной НС1, гид- рохлорнд отфильтровывают, нейтрализуют аммиаком Веснветные кристаллы
Выход 2,14 г (68,3%), т„пло 340- 341°С (из ДМФА)с
Найдено,%: С 53,6; И 2,4; Вг 25,3 N 13,4С
Вычислено,%: С 53,5; Н 2,5; Вг 25,5; N 13,4„
б)Метилирование 9-бромбензимида- ,1-Ь хиназолинона-1 2 в условиях межфазного катализас
3,14 г (0,01 моля) 9-бромбензими- дазор, хиназолинона-12(6Н) вносят в раствор 3 г NaOH в 3 мл , добавляют 10 мл ацетона, ТЭБАХ на кончике шпателя и 2,08 г (0,015 моля йодистого метила с Перемешивают при комнатной температуре в течение 1 ч, разбавляют 25 мл холодной воды и фильтруют бесцветные кристаллы
Выход 2,96 г (90,3%), тспл 261- 262° С (из ДМФЛ) ,
Найдено,%: С 54,9; Н 3,0; Вг 24,3; N 12,7.
Вычислено// : С 54,9; Н 3,0; Вг 24,4; N 12,8
Пример 6, Осуществление предлагаемого способа при использовании в качестве исходного соединения 6-аллилбензимидазоЈ2,1-ЬЛ хнназолинона-12(6Н).
2,/5 т (0,01 моля) 6-аллилбенз- имидазо 2,1-bl хиназолинона-12(6Н) растворяют при нагревании в 50 мл ДМФА при 80-90°С, прибавляют 3 мл конц. бромистоводородной кислоты и при тщательном перемешивании при 60-/0°С добавляют 1,6 г (0,01 моля) брома Раствор сначала окрашивается в желтый цвет, но затем обесцвечивается. Разбавляют 150 мл воды. Выпадают бесцветные кристаллы,, Раствор нейтрализуют аммиаком и бесцветные кристаллы Ь-1,2-дибром-3-пропил бенз имидазо 2,1-Ь)хнначолинона-12(6Н) отфильтровывают,
0
5 о
,
0
5
5
Выход 3,28 г (89,3%), т.пл 204- 205аС (из водного ДМФЛ)„
Найдено,%: 46,80; Н 2,91; ВГ 37,01; N 9,62
Вычислено, %: С 46,89; Н 2,98; Вг 36,78; N 9,65
Пример /ь Получение 5-метил- -9-бромбензимидазо 2,1-bl хиназолино- на-12(5Н)0
а)Получение гидробромида пербро- мида 5-метил-9-бромбензимидазо 2,1-bl хиназолинона-12(5Н)„
2,49 г (0,01 моля) 5-метилбензими- ,1-bJхиназолинона-12(5Н) растворяют при нагревании в 50 мл ДМФА, при 90°С прибавляют 3 мл конц„ бромистоводородной кислоты и при тщательном перемешивании при /0°С добавляют 1,6 г (0,01 моля) брома„ В образовавшийся желтый раствор прибавляют 150 мл водыс Выпавшие ярко-желтые кристаллы отфильтровывают, промывают на фильтре 10 мл холодной дист0 воды„
Выход 4,3 г (8/,9%).
Вблизи температуры плавления разлагается на исходные компоненты.
В ИК-спектре 1695 ,
Найдено, %: С 36,6; Н 2,4; Вг 48,9; N 8,6„
С,9Н ,2Br,jN3Oc
Вычислено, %: С 36,/; Н 2,3; Вг 49,0; N 8,6
б)Получение 5-метил-9-бромбенз- имидазо 2,1-Ь хинаэолинона-12(5Н)„
2,49 г (0,01 моля) 5-метилбенз- имидазо 2,1-bj хиназолинона-12(6Н) растворяют при нагревании в 50 мл ДМФА, при 90°С прибавляют 3 мл конц0 бромистоводородной кислоты и при тщательном перемешивании при 70°С добавляют 1,6 г (0,01 моля) брома В образовавшийся желтый раствор прибавляют 150 мл воды, что приводит к выпадению ярко-желтых кристаллов Нагревают при перемешивании полученную суспензию до 90°С и выдерживают при этой температуре 3 мин до обесцвечивания желтого комплекса Охлаждают до комнатной температуры и нейтрализуют основанием, например 10%-ным раствором соды или конц„ аммиаком. Бесцветные кристаллы отфильтровывают
Выход 3,1 г (94,9%), т0плс 263- 264°С (из ДМФА).
Найдено,/,: С 54,9; Н 3,0; Вг 24,3; N 12,7„
Вычислено %: С 54,9; Н 3,0; Вг 24,4; N 12,8.
у16
в)Получение 5-метил-9-бромбенз- имидаэор, 1-ь1хинаэолинона-12(5Н) при соотношении воды 1:3,5.
Пербромид гидробромида получают аналогично примеру 16, но образовавшийся желтый раствор разбавляют 175 мл воды (1:3,5) и нагревают выпавшие желтые кристаллы до 90°С до полного обесцвечивания (3 мин)0 Охлаждают, нейтрализуют конц. аммиаком и бесцветные кристаллы отфильтровывают о
Выход 3,1 г (94,9%), т.пл. 263- 264°С из ДМФА
г)Получение 5-метил-9-бромбенз- имидазоЈ2, 1-Ь хиназолинона-12(5Н) при соотношении воды 1:2„
Пербромид гидробромида получают аналогично примеру 16, но образовавшийся желтый раствор разбавляют 100 мл воды (1:2)о Выпавшие желтые кристаллы нагревают при перемешивании при 90°С. Полное обесцвечивание наблюдается через 15 мин„ Охлаждают до комнатной температуры, нейтрализуют конце аммиаком и фильтруют бесцветные кристаллы.
Выход 2,/6 г (84,1%), т„пл„ 263- 264°С (из ДМФАЬ
д)Получение 5-метил-9-бромбенэ- имидаэо 2,1-Ь|хиназолинона-12(5Н) при соотношении воды 1:5
Пербромид гидробромида получают аналогично примеру 16, но образовавшийся желтый раствор разбавляют 250 мл воды (1:5) Выпавшие желтые кристаллы нагревают при перемешивании до 90°С и выдерживают при этой температуре до полного обесцвечивания комплекса 3 мин„ Охлаждают до комнатной температуры, нейтрализуют концо аммиаком и отфильтровывают бесцветные кристаллы
Выход 2,93 г (89,3%), 263- 264°С (из ДМФА).
Таким образом, наиболее оптимальным является соотношение реакционной массы и воды 1:(3-3,5). Увеличение или уменьшение количества воды оказывается на выходе искомого продукта и времени продолжительности реакции.
Приведенные в табл„2 соединения 1а-з, к-о, получены аналогично примеру 16. Для получения соединения 1и реакционную массу после обесцвечивания желтого комплекса охлаждают и без последующей обработки основанием отфильтровывают, Во всех случаях при
0
5
0
5
0
5
0
5
0
5
уменьшении температуры нагревания на конечной стадии до 80°С время обесцвечивания комплекса увеличивается до 5 мин, что, однако, не влияет на выход искомого продукта
Пример 8„ Взаимодействие соединения IV (R - СП) с бромом в воде о
2,49 г (0,01 моля) 5-метилбенз- имидазо 2,1-bl хиназолннона-12(5Н) суспензируют в 50 мл воды и при тщательном перемешивании прибавляют 1,6 г (0,01 моля) брома. Несмотря на длительное тщательное перемешивание, бром связывает только половину соединения IV, что и наблюдается визуально: в виде осадка в воде находятся оранжевые кристаллы пербромида и бесцветные кристаллы исходного соединения 3 Их отфильтровывают
Выход 4,23 г„
ИК-спектр 1680, 1693, 1/15 см амидные
Пример 9„ Взаимодействие соединения IV (R -CHj) в условиях предлагаемого способа с бромом без предварительной обработки НВг„
2,49 г (0,01 моля) 5-метилбенз- имидаэо 2, 1-bfjхиназолинона-1 2(5Н) растворяют при нагревании в 50 мл ДМФА и при тш,ательном перемешивании при 70 С добавляют 1,6 г (0,01 моля) брома. Полученный оранжевый раствор разбавляют 150 мл воды и выпавшие оранжевые кристаллы отфильтровывают
Выход 4,20 г,
ИК-спектр: 1700, 1693, 1715 см амидные
Па основании данных ИК-спектра видно, что образуется комплекс состава IV (R -СН3) и брома 1:2, полосы 1693 и 1715 являются характерными для пербромида, для которого и характерна оранжевая окраска
Пример 10„ Взаимодействие соединения IV (R -СН) с бромом в условиях предлагаемого способа, но после добавления воды
2,49 г (0,01 моля) 5-метилбенэ- имидазо 2, хиназолинона-1 2(5Н) растворяют при нагревании в 50 мл ДМФА и при тщательном перемешивании при 90°С добавляют 3 мл конц„ бромис- товодородной кислоты Разбавляют 150 мл и при перемешивании на выпавшие бесцветные кристаллы при 70°С действуют 1,6 г (0,01 моля) брома Несмотря на длительное тща-I
16
тельное перемошипание, бром связывает только половину исходного соединения, что и наблюдается визуально: в виде осадка находятся оранжевые кристаллы пербромида и бесцветные кристаллы 5-метилбензимидазо ,1-b | хинаэолинона-1 2 (.5Н) . Их отфильтро- вываютс
Выход 4,2 г
ИК-спектр: 16/5, 1693, 1/15 амидные
На основании данных ИК-спектра видно, что образуется комплекс состава IV (R - CHj) и брома 1:2, т.к. полосы 1693 и 1/15 см являются характерными для пербромида, для которого и характерна оранжевая окраска
Пример 11, Встречный синтез 5-метилбензимидазо 2, иГ|хиназоли- нона-12(5Н) сплавлением 5-бромбенз- имидазол-2-сульфокислоты с антрани- ловой кислотой с последующим алки- лированиеМс
а)Синтез 9-бромбензимидазо 2,1-Ы хиназолинона-1 2 (,6Н) с
2,/6 г (0,01 моля) 5-бромбензими- дазол-2-сульфокислоты сплавляют при 140-160°С с 1,37 г (0,01 моля) антра ниловой кислоты в течение 1,5 ч до полного прекращения выделения Охлаждают, обрабатывают 20 мл 10%- ной НС1, гидрохлорид отфильтровывают нейтрализуют аммиакоме Бесцветные кристалльи
Выход 2,14 г 168,3%), т.пл„ 340- 341°С (из ДМФА),
Найдено,%: С 53,6; Н 2,4; Вг 25,3; N 13,4.
Вычислено, %: С 53,5; Н 2,5; Вг 25,5; N 13,4,
б)Метилирование 9-бромбензимида- ,1-b хиназолинона-12 в ДКФА
3,14 г (0,01 моля) 9-бромбензимида- зо 2,1-bl хиназолинона-12(6Н), 2,08 г (0,015 моля) йодистого метила в 20 мл ДМФА кипятят с обратным холодильником в течение 1,5-2 ч„ Охлаждают, выделившийся гидроиодид от- фильтровывают, суспензируют в 10 мл воды, нейтрализуют аммиаком и бесцветные кристаллы отфильтровывают.
Выход, 2,77 г (84,6%), т.гии 263- 264°С (из ДМФА)с
Найдено, %: С 64,9; Н 3,1; Вг 24,3; N 12, /„
Вычислено, %: С 54,9; II 3,0; Вг 24,4; N 12,8,
Q
5
0 5
0
0
0
5
512
Пример 12. Осуществление предлагаемого способа при использовании в качестве исходного соединения 5-аллилбензимида о Q2, хиназолинона-1 2 (5Н)о
2,/5 г (U,01 моля) 5-аллилбенз- имидазо 2, 1 -b хиназолинона-12 (5Н) растворяют при нагревании в 50 мл ДМФА при 90°С, прибавляют 3 мл конц0 бромистоводородной кислоты и при тщательном перемешивании при /О С добавляют 1,6 г (0,01 моля) брома„ Раствор сначала окрашивается в желтый цвет,но затем обесцвечивается„ Разбавляют 150 мл водыс Выпадают бесцветные кристаллы. Раствор нейтрализуют аммиаком и бесцветные кристаллы 5-(1,2-дибром-З-пропил)бензимидазо- Г2,1-bl хиназолинона-12(5Н) отфильтровывают с
Выход 3,28 г (89,3%), тспл. 209- 210°С (из водного ДМФА).
Найдено, %: С 46,80; Н 2,91; Вг 37,01; N 9,62.
Вычислено, /: С 46,89; Н 2,98; Вг 36,78; N 9,65,
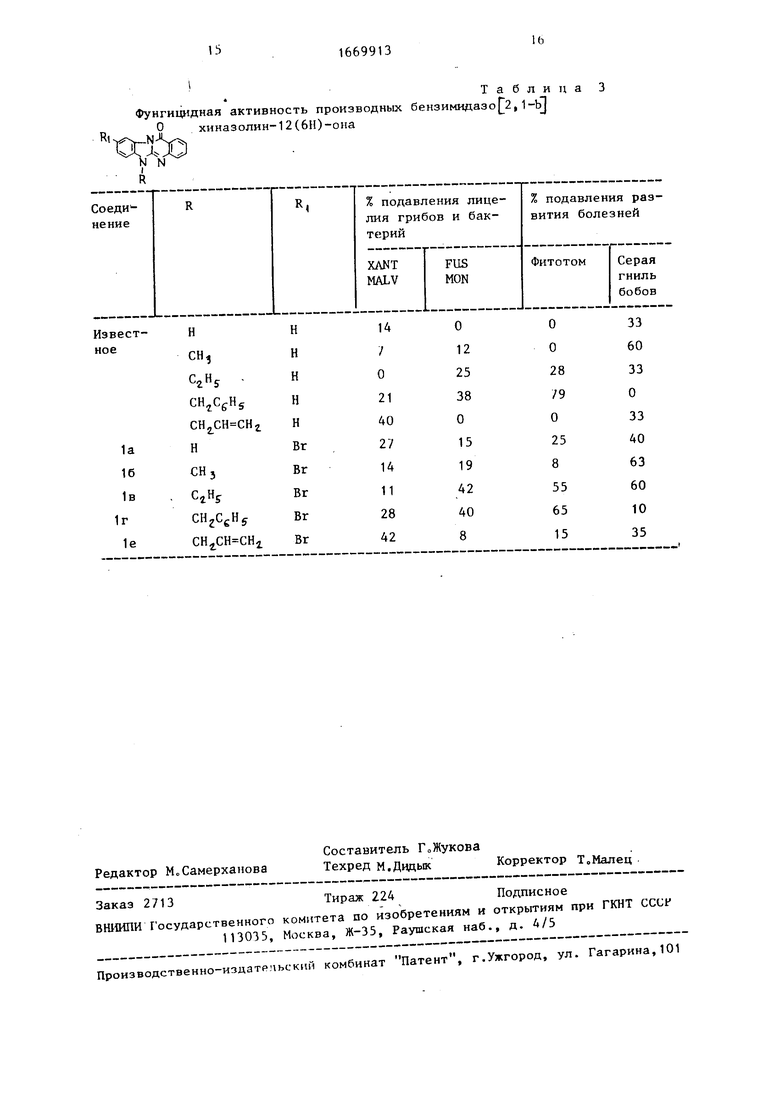
Физико-химические свойства новых соединений приведены в табл0 1 и 2, фунгицидная активность - в табл0 3.
Таким образом, новый способ позволяет получать неописанные ранее 5- или 5-замещенные 9-бромбензимидазо- 2t 1-ьГ хиназолнноны-1 2 (5 или 6Н),с выходом 90-95%„
Формула изобретения
Способ получения 5-или 6-замещен- ных 9-бромбензимидазо 2,1-Ь хиназоли- нонов-12 (6 или 5Н), общей формулы I
или II
О
8г-,
Л N N
R
В г
О
W-N V
чллХ
N N
N I
R
где R - Н, СН5, низший алкил Сг-С, бензил, гидрокси(карбокси,-карбалкок ,
:
СТ
т






Изобретение касается гетероциклических кислот, в частности получения 5-или 6-замещенных 9-бромбензимидазо[2,1-B]хиназолинонов-12(6 или 5H) общей ф-лы I или II: @ , @ , где R - H, CH3, C2 - C4-алкил, бензил, гидрокси(карбокси, -карбалкокси)алкил, фенацил, хлоралкил, цианалкил, ароил, которые могут быть использованы в фармакологии или в качестве полупродуктов для синтеза лекарственных средств. Цель - создание нового способа получения новых веществ указанного класса. Синтез ведут бромированием соответствующего замещенного ф-лы I или II, не содержащего в положении 9 брома, HBR(-кислотой(конц.) в среде диметилформамида при 80 - 90°С с последующим введением брома (в эквимолярном количестве) при 60 - 70°С, разбавлением водой в соотношении 1:(3 - 3,5), нагреванием при 80 - 90°С до обесцвечивания реакционной смеси и нейтрализацией аммиаком или карбонатом натрия. Новые соединения проявляют фунгицидную активность в отношении грибов и бактерий. Новый способ позволяет получать целевые вещества с высоким выходом (90 - 95%). 3 табл.
1) О -
. - -
- Z
Z
Н -, . Со
л -1
- - ЛООЭ - S jsojO- - - .v.
Л-П .
1 Z S J Э J -D
О ОЗОь- -, - -з гл,
- э з о Э;- -ч
:- о о
Г; - о ,
Таблица З
Фунгицидная активность производных бензимидазо 2,1-b Р 0 хиназолин-12(6Н)-она
ССЙО
Ы N R
| Способ получения 5-замещенных бензимидазо @ 2,1- @ хиназолинонов-12 | 1983 |
|
SU1182043A1 |
Авторы
Даты
1991-08-15—Публикация
1989-01-18—Подача