(54) СПОСОБ ПОЛУЧЕНИЯ 1,2,3-ТИАДИАЗОЛ-5-ИЛ-МОЧЕВИН







| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных 1,2,3-тиадиазол-5-илмочевины | 1979 |
|
SU927114A3 |
| Способ получения 5-меркапто-1,2,3-триазолов | 1979 |
|
SU961559A3 |
| Способ получения замещенных 1,4-дигидропиридинов | 1983 |
|
SU1360585A3 |
| Способ получения 1,2,3-тиадиазол-3-ин-5-илиденмочевин | 1978 |
|
SU704454A3 |
| ПРОИЗВОДНЫЕ БЕНЗИМИДАЗОЛА В КАЧЕСТВЕ ИНГИБИТОРОВ ФАКТОРА Ха | 2004 |
|
RU2346944C2 |
| ПРОИЗВОДНЫЕ САХАРИНА ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМАЯ АДДИТИВНАЯ СОЛЬ КИСЛОТЫ ИЛИ ОСНОВАНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ПРОЯВЛЯЮЩАЯ АКТИВНОСТЬ ИНГИБИТОРА ЭЛАСТАЗЫ | 1992 |
|
RU2114835C1 |
| Способ получения производных 1,2,3-тиадиазол-5-ил- мочевины | 1982 |
|
SU1148561A3 |
| СПОСОБ ПОЛУЧЕНИЯ СЛОЖНОГО ЭФИРА СУЛЬФОКСИДА 3-ЭКЗОМЕТИЛЕНЦЕФАМА | 1992 |
|
RU2010795C1 |
| ПОЛИЦИКЛИЧЕСКИЕ СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ РЕСПИРАТОРНО-СИНЦИТИАЛЬНЫХ ВИРУСНЫХ ИНФЕКЦИЙ | 2004 |
|
RU2422444C2 |
| Способ получения производных тиенотриазолодиазепина или их солей | 1978 |
|
SU747429A4 |

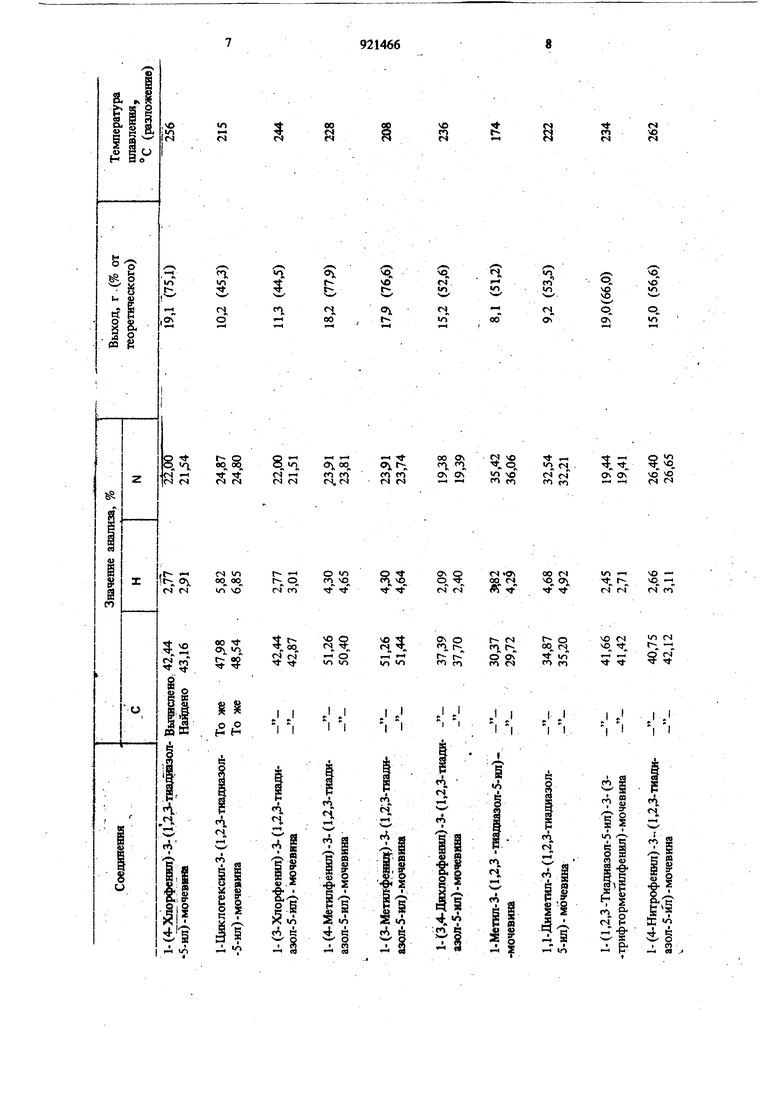
Изобретение относится к способу получения 1,2,3-тиадиазол-5-нл-мочевин общей формулы - N--СНW II II/ N.ci-NHd.oisrc J , Е где R - водород, метил, этил, пропил, бутил. изопропил, изобутил, втор-бутил или аллил; R - метил, этил, аллил, циклопропил, циклогексил, фенил, 2-метш1фенил, 3-метилфеншт, 4-метилфенш1, 2-изопропнлфеннл, 2-хлорфенш1,3-хлорфени . 4-хлорфенил, 3,4-дихлорфенил 2-метоксифенил, 2-нитрофенил, 3-нитрофенил 4-нитрофенил, 2-трифтор ме-. тилфенил, 3-трифторметилфенил,.2-хлор-6-метш1фенил, пиридил, .пирнмндил, 3-метил-2-Пиридил, 4-метил-2-пириднл, 5-метйл-2-пиридил, б-метил-2-пиридил, 4-метил-2-пиримидил или 5-хлор-2-пиридил, или R н R вместе с соседним атомом азота образуют морфолино-, пиперидино- или пирролидино-группу. Известен способ получения 1,2,3-тиадиазол-5ил-мочен ИИ формулы I взаимодействием 5амино-1,2,3-тиадиазола с нзоцнанатамн, анпвдрндами или галоидангидридами соответствующих кислот 1. Недостатком известного способа является .использование малодоступного исходного соединения - 5-амино- 1,3,4-тиадиазола. Цель изобретения - упрощение технология процесса за счет использования более доступного исходного сырья. Поставленная цель достигается способом получения 1,2,3-тиадиазол-5-ил-мочевин общей формулы Г взаимодействием азида 1,2,3-тиадиазол-5-карбоновой кислоты с амином общей формулы 1I HN,,a где R и R имеют укайнные выше значения, в среде растворителя прн ЮО-ИО С. Азид 1,2,3-тиадиазол-5-карбоновой кислоты может быть получен взаимодействием 1,2,3-тиадиазол-5-карбоновой кислбты со сложныл1И эфирамй хлормуравьиной кислоты в инертно. растворителе, в присутствии кислотосвязующих cpeflcrt, с образованием соответствующих смешанных ангидридов, после чего осуществляется реакция с растворами щелочных азидов; или взаимодействием галогенида 1,2,3-тиадиазол-5-карбоновой кислоты в инертном органическом растворителе с водным раствором щелочного азида; или взаимодействием -Гидразида 1,2,3-тиаЯиазол-5-карбоновой кислоты в инертном органическом растворителе с растворами щелочных нитритов или с алкилнитритами в присутствии кислоты с образованием азида 1,2,3, -тиадиазол-5-карбоновой кислоты. Полученный таким образом азид обычно не выделяется из реакционных смесей , а на; против, непосредственно применяется в смесях дня осуществления предлагаемого способа. Таким образом, для осуществления предлагаемого способа требуются легкодоступные исходные материалы. Способ обеспечивает технически простое и неопасное изготовление целевых продуктов. Больщим техническим преимуществом является отсутствие необходимости выделения азида 1,3,5-тиадиазол-5-карбоновой кислоты из использованных для его получения реакцион ных смесей. Весь процесс можно вести в едино сосуде с возможностью непосредственного осуществления реакции этих смесей с аминами по общей формуле 11. Особенным является то обстоятельство, что при таком ведении npoi;ecca образуется требуе мый продукт, а не - как этого можно было ожидать - замещение азидного остатка амином с образованием амида 1,2,3-тиадиазол-5-карбоновой кислоты. Предлагаемьш способ может быть реализова следующим образом. Неочищенный раствор азида., смещанный с эквимолярным количеством амина, капают в инертный растворитель при температуре дефлег мации или можно смешать раствор азида с разбавле1шым растворителем амином при температуре дефлегмации. При интенсивност и дефлегмации можно контролировать спонтанное течение реакции. Азид можно также нагреть в смеси с амином в присутствии инертного растворителя. Температуру желательйо поддерживать от 20 до С,, но предпочтительно от 50 до 120° С. Еще предпочтительней является осущест вление реакции при температуре кипения реакционной смеси. В качестве инертных креагентам растворителей следует упомянуть следующие: алифатические и ароматические углеводороды, например 1иклогексан, гептан, лигроин, бензол, хлорбензол, толуол и ксилол: простые эфиры, как диоксан, тетрагилрофуран,- простой диизоп 9 4 пиловый эфир; сложные эфиры, такие как уксусный и малоновый кетоны, например ацетон, метилизобутилкетон, изофорон и циклогексанон; галоидированные углеводороды, например хлористый метилен, хлороформ и четыреххлористый углерод; нитрилы карбоновой кислоты, например ацетонитрил. По окончании реакции реакционную смесь обрабатывают известным способом, например отгонкой использованного растворителя при нормальном или пот1женном давлении путем осаждения водой,но большей частью путем простого отфильтровывания требуемых продуктов реакции. Таким образом получают 1,2,3-тиадиазол-5-ил-мочевины в превосходно чистой форме при почти количественном выходе и без необходимости (для дальнейшего использования) в каких-либо дополнительных операциях очистки. При этом весьма -благожелательным для процесса является то, что отпадают проблемы разделения, возникающие, например, после реакции 5-амино-1,2,3- тиадиазола с изоцианатами (появление в качестве побочных продуктов симметричных мочевин). Пример 1. Получение 1-фенил-3-( 1,2,3-тиадиазол-З-ил) мочевины из хлорида 1,2,3-тиадиазол-5-карбоновой кислоты. В трехгорлую круглую колбу емкостью , 250 мл, снабженную мешалкой и термометром вливают 9,1 г (0,14 моль) раствора азила натрия в 40 мл воды и 40 мл толуола. Затем в теченйе 15 мин при 15-20° С вливйют каплями (при интенсивном размешива1ши 14,8 г (0,1 моль) раствора хлорида 1,2,3-тиадиазол-5-карбоновой кислоты в 80 мл толуола. Газмеишвание продолжают еще .1,5-2 ч при 15-20° С. 1олуольную фазу отделяют и высушивают над сернокислым магнием. Высуйгенный раствор азида 1,2,3-тиадиазол-5-карботювой кислоты вводят в реакцию при комнатной температуре с 9,14 г (0,1 моль) анилина. Между тем в трехгорлой круглой колбе емкостью 250 мл, снабженной мешалкой, термометром и обратным холодильником, подогревают 80 мл толуола до 110° С. В течение 10 мин сюда вкапывают раствор азида карбоновой кислоты/анилина таким образом, чтобы температура внутри колбы оставалась на уровне 100-110°С. Сразу, при сильном газообразовании, происходит осаждение окрашенных в слабо-желтый цвет кристаллов. Размешивание продолжают с дефлегмацией еще 5 мин, охлаждают до 5° С, кристаллы отфильтровьтают и затем высушивают в вакууме при 40° С до постоянства веса. Выход 19,5 г (88,6% от теоретического) Т. пл. 2J7°C (разложение). DC (хроматографический анализ): растворитель - уксусный эфир, Rf 0,25.;. I 5. 9 Пример 2. Получение 1-фенил-3-(1,2,3 -тиадиазоп-5-ил) мочевины из гидраэида 1,2,3-тиадиазол-5-карбоиовой кислоты. В трехгорлую круглую 500-миллилитровую колбу с термометром и мешалкой помещают 14,4 г (0,1 моль) гидразида 1,2,3-тиадиазол-5-карбоновой кислоты, которые растворяют в 100 мл воды и 12 мл коицентрированной соляной кислоты. Затем в этот раствор вливают 200 мл толуола. В течение 30 мин в эту смесь каплями вливают при температуре 05° С 7,25 г (0,105 моль) раствора нитрита натрия в 20 мл воды. Размешивание продолжают еще 15 мин при той же температуре. Потом отделяют толуольную фазу и сушат над сернокислым магнием. Высушенный раствор азида 1,2,3-тиадиазол-5-карбоновой кислоты вводят при комнатной температуре в реакдию с9,14мл (0,1 моль) анилина. В трехгорлую 500-миллилитровую круглую колбу с мешалкой, термометром и обратным холодальником в это время помешают 50 мл толуола, который подогревают до 110°С. Высушенный раствор азид карбоновой кислоты/ анилина вводят в течение 10 мни с таким рассчетом, чтобы температура оставалась на уровне 100-11 о С. Прн сильном газообразовании немедленно происходат вьшадение .кристаллов, окрашенных в желтоватый цвет. Размешиваше продолжают еще 5 мин с дефлегмацией, охлаждают до 5° С и отсасьшают кристаллы, которые сушат в вакууме при 40° С до постоянства веса. Выход продукта 16,2 г (73,6% от теоретического). Т.,Ш1. 217°С (разложение). DC: растворитель - уксусный эфир, Rf 0,25. Аналогичным образом получают соединения, перечисленные в таблице.
t-
l
ON
o.
:П,
ro 5
H
OO
r
VI
Sw
V-
q.
«4 t
OO Л
- о
§.s ON oq,
f
f
tN
Й 00
O ТЧ
Я «л
vq r rf cT r
r«f. r
О -Г
Tf Tt
M
ii
§ M
§
H о
I /cs с
s
s
«o
41И
rt
Ov OO
я
O. g
.
ч
«J,
n
n
1Л «Л
r t
n
M
O
iss
vO
v
NM
q.
ч
n
4
4 r
o.
о
1Л
A o
0.
a.
-. H.
о
VO tсл
nij.
nro in rf f-;
° . Й
Г4 R
t ro
01
t™H
v
3
r CS ГЯ s N t)
Tt
О
t--, СЛ
tn a00 t
t o
ел
OO S «I «4
чп
«--i
Ч- wo f
M- «Л
«л m
«O O
O «n
rt vo
О
o о
Ov СЛ
о VI
о in
O CT
о г.
rs in m
Ч-Ч Ч V
o t--,
Г т f
ГЛ f
м- ,-1
0 40
T-I t-I in
Tj-i/ 1Л
tn IT)
«n in n in
I I
с (
:
I
I I
& s
4
0g I
Л 5
S
fS
о м
гч
Oi,
0
(
л N.
Г4
о
о
i2
о о с ts
00
оо
7
3
«л
а
1Л1
я
00
vq,
о. л
s
о
fS
ГО
00
Г-
,
п.
ч
п
fS гоС
ON
R
OO S
m Q
S.2;
гОС о
in vj
о о oj, o5
OO O Ч «-;
. J tr
o о S гл гл
(N СЧ г
2: Й
Q о
Г4
fS S fN г)
tN CN
rt гг
00 О
cj
R
in in
r ГЧ
ОО S.
о f
ч ч
l/l OO
ее а
in vO
л,ч. t- so rf
N r
OO OO
s
t, 4
so ЧО in «л
о
..
.
S f
ss
OO CO
Tt СЛ
00 о
l«
CO m
fS vO
Ч, Q.
ЧО OO VO С4
-H O
O 43 n
55 5
СЛ N f CO in in 1Л in
tn n
J I
a
H
Ч (N
а
ffl
«s
Tjо
:;
СЛ N
гч
N
00
rf rоо
л
ч
ЧО
о
1Л
Чи
rjv
ч,
Ч
40
о
«о
СП
00 ю
00 V)
О
ооа
t OS
о
г.-п.
0 00 t.«
п
1
Гсм
M f
СП
N t
f- СЛ, (S CM
SJ ч
ел
(N(-;
(N- Ю Ох ч,
°0,Ч
oo
in л
lOxcTСЛ Г ю чр
t--r
t
ГЛГО
I
I
ш
S
-l lr в г 1792146618 ормула изобретениятш1-2-пиридил, 6-метил-2.пиридил, 4пособ получения 1,2,3-гиадиазол-5-ил-моче-ридил, общей формулы Iили R и R вместе с соседним атомом азота jf-(iH -pi. j образуют морфолино пилеридино- или пнрро ilf nw лидино-группу, Nx.jX- ,из производаого 1,2,3-тиадиаэола, о т л и ч аР Вющийся тем, что, с целью упрощения R - водород, метил, этил, пропил, бутил, технологии процесса, в качестве производного изопропил, изобутил, втор-бутил или to 1,2,3-тиадиазола используют азид 1,2,3-тиадаазопаплил; -5-карбоновой кислоты, которьш подвергают вэ R - метил, этил, аллил, циклопропил,взаимодействию с амином общей формулы 11 циклогексил, фенил, 2-метилфенил,R 3-метилфенил, 4-метилфенил, 2-изопро-HN -il. пилфенил, 2-хлорфенил, 3-хлорфенил, isi 4-хлорфенил, 3,4:дахлорфешш, 2.меток. ™« « ,Тг сифенил, 2-нитрофенш1, 3-нитрофенил, растворителя при 100-110 С. 4-нитрофенил, 2-трифторметилфенил,Источники информации, 3-трифторметилфенил, 2-хлор-6-метил-принятые во внимание при. экспертизе фенил,, пиридил, пиримидил, 3-метил- ло Заявка ФРГ № 2636994, кл. 12 р 9, -2-пиридил, 4-метил-2-пириялл, 5-ме-опублик. 1978 (прототип). -метил-2.11иримидил шга 5-хлор-2-пи
Авторы
Даты
1982-04-15—Публикация
1979-09-20—Подача