М50 СПОСОБ ПОЛУЧЕНИЯ 5-МЕРКАПТО-1 ,2,3изобретение относится к улучшенному способу получения 5-меркапто-1,2,3-триаз6лов, которые являются исходными продуктами в синтезе средст защиты растений,а 1также фармацевтичес ких препаратов. Известен способ получения 5-меркапто-1,2,3-триазола путем обработки бензил-1,2,3-триазола серой в присутствии щелочи с последующим отщеплением бензильной группы РЗ Недостатком способа является сложность процесса, связанная с необходимостью проведения первой стадии процесса при очень низких температурах (-60°с) в атмосфере азота и проведения отщепления бензильной группы под действием натрия в жидком аммиаке. Поэтому процесс не пригоден для получения целевого продукта в промышленном масштабе. Наиболее близким является способ полумения 5-меркапто-1,2,3-триазолов заключающийся в том, что изоцианаты -ТРИАЗОЛОВ подвергают взаимодействию с диаз.ометанами, полученные при этом эфиры 1,2,3-тиадиазолилкарбаминовой кислоты, например 5-феноксикарбониламино,2,3-тиазол, подвергают гидролизу в кислой или щелочной среде при кипя чении реакционной массы с последую- . щим выделением 5-аминотиадиазола, ко тррый подвергают перегруппировке под действием щелочи при кипячении реакционной массы в 5-меркапто-1,2,3-триазол Г 2. Недостатком известного метода является использование токсичных исходных продуктов, а также необходимость выделения промежуточного 5-аминотиадиазола, также являющегося токсичным продуктом. Целью изобретения является упрощением процесса получения 5-меркапто-1,2 3-триазолов. Поставленная цель достигается предлагаемым способом получения 5-мерKanto-1,2,3-триазолов общей фор-k мулы да где R - этой водорода, метил, этил, пропил, бутил, изобутил, втор.-бутил, трет.-бутил, заключающимся в том, что азид 1,2,3 7Тиадиазол-5-карбоновой кислоты общей формулы ., где ( имеет указанные знамения, подвергают взаимодействию со спиртом или фенолом об1цей формулы , , где алкил,-содержащий -k атома .углерода, или фенил, IB инертном органическом растворителе при 90-110®С, полученный при этом Эфир тиадиазолилкарбаминовой кислоты общей формулы |j--тг-Щ N jLwHCOOR ,XW1 где К и R имеют указанные значения подвергают гидролизу при вО-ЮО С с последующей перегруппировкой образова шегося при этом 5-амино-1,2,3-тиадиазола общей формулы. N-rr« iTk IV) N мнг где R имеет указанные значения, в целевой продукт при 80-100 С. ; Согласно предлагаемому способу эфи 0ы тиадиазолилкарбоновой кислоты получают путем взаимодействия азида ; ,2,3-тиадиазол-5-« арбоновой кислоты Ьбщей формулы I со спиртом или фёноJiOM общей формулы III. Предлагаемый способ исключает использование токсичных продуктов, позв ляет проводить процесс получения без Выделения промежуточных продуктов. Например, по одностадийному способу азид карбоновой кислоты формулой можно прямо вводить во взаимодействие со спиртом или фенолом формулы IiI, и применять далее неочищенный сложный Эфир (1,2,3-тиадиазол-5 ил)карбамино вой кислоты формулы IV, а также его 96 йеочищенный раствор или суспензию.Особенно предпочтительно то, что в случае последующего гидролиза карбамата небезопасный (в|:: едный) 5 амино-1,2,3-тиaдиaзoл формулы V как правило образуется только in situ и затем только в растворе и не выделяется отдельно, а самопроизвольно перегруппировывается с помощью щелочи в 5 меркапто-1,2,3-триазол формулы 1. Благодаря соответствующему выбору остатка Дд осуществляется кислотный или щелочной гидролиз карбамата, так как с одной стороны карбаматы формулы 1У образуют с неорганическими осйованиями устойчивые соли, а с другой стороны 5 амино-1,2,3-тиадиазол формулы У неустойчив к действию кислот. Получение 5-меркапто-1,2,3 триазо{юв формулы I. Превращение азида 1,2,3 тиадиазол-5-карбоновой кислоты- формулы Т1., предпочтительно в форме неочищенного раствора, в сложный эфир (1,2,3 -тиадиазрл-5 ил)-карбаминовой кислоты формулы 1У основано на перегруппировке Курциуса через стадию 1,2,3 -тиадиазол-5-ил-изоцианата, который, как правило, не нужно выделять отдельно, он образуется in situ и тотчас реагирует дальше со спиртом или Фенолом формулы Ш. Зта стадия реакции осуществляется. РР 90-110 С, предпочтительнее, однако, при температуре кипения с обратным холодильником реакционной смеси. На практике сырой (неочищенный) раствор азида в смеси с эквимолярным количеством спирта или фенола прикапывают в инертный растворитель-при температуре его кипения с обратным холодильником или же раствор азида добавляют к разбавленному растворителем спирту или фенолу при температуре кипения смеси с обратным холодильником. Интенсивность кипения с обратным холодильником дает возможность контролировать спонтанное течение реакции. Азид также можно нагревать в смеси со спиртом или фенолом в присутствии инертного растворителя. Известное осуществление реакции Курциуса - сначала выпаривание до изоцианата и лишь затем добавка спирта или фенола - не имеет преимущества из-за более незначительного выхода., 5 -. 96 В качестве инертных по отношению к компонентам реакции растворителей можно применять алифатические и ароматические углеводороды, такие как циклогексан, гептан, лигроин, бензол, хлорбензол, толуол и ксилол; простые эфиры, такие как диоксан, тетрагидрофуран и диизопропиловый эфир; сложные эфиры ацетон,
циклогексанон; галоидированные углеводороды - хлористый метилен, хлороформ, четыреххлористый углерод и 1,2-дихлорэтан; нитрилы карбоновых кислот - ацетонитрил. После протекания реакции сырой раствор или сырую суспензию можно непосредственно вводить дальше во взаимодействие или, если желательна следующая стадия очистки, обрабатывать известным обра- 20
зом, например отгонкой использованного растворителя при нормальном или пониженном давлении, осаждением с помощью воды или же одностадийным отфильтровыванием целевого продукта 25 реакции.
Таким образом получают сложный эфир (1 ,2,3 тиадиазол-5-ил)-карбаминовой кислоты в чистой форме и с хорошим количественным выходом. Для даль-зо нейшего его использования не требует ся никакой очистки. Если работают с сырыми (неочищенным) растворами или суспензиями, то для перегруппировки Курциуса применяют растворитель, который ведет себя инертно и в последующих стадиях. Таким растворителем могут быть ароматические углеводороды - бензол, толуол, ксилол, хлорбензол; простые эфиры - тетрагидрофуран и диоксан; галогенированные углеводороды - хлороформ, 1 ,2-дихлорэтан и хлористый . метилен. сложных эфиров (1 ,2,3-т.и - - I - диазол-5 ил -карбаминовых кислот мож но осуществлять и известным образом, выделяя 5 амино-1,2,3 тиадиазолы. Для этого нагревают карбамат формулы 1У, предпочтительно в водной среде, при известных условиях в смеси с органическими растворителями в присутствии кислотных катализаторов. Реакция протекает при 80-ЮО С. Пригодными кислотными катализаторами могут быть сер ная ,соляная, бромистоводородная кислоты, п-толуолсульфокислота. Инертными по отношению к компонентам реакции растворителями являются галоидикатализируемой кислотами омыляемости, что связано с легкой дегидратируемостью третичных спиртов до олефинов.
Толуольный раствор или суспензию сложных трет.-бутиловых эфиров нагревают в присутствии п-толуолсульфокислоты, серной или соляной кислот, причем эти эфиры при отщеплении изобутилена и при декарбоксилировании дают
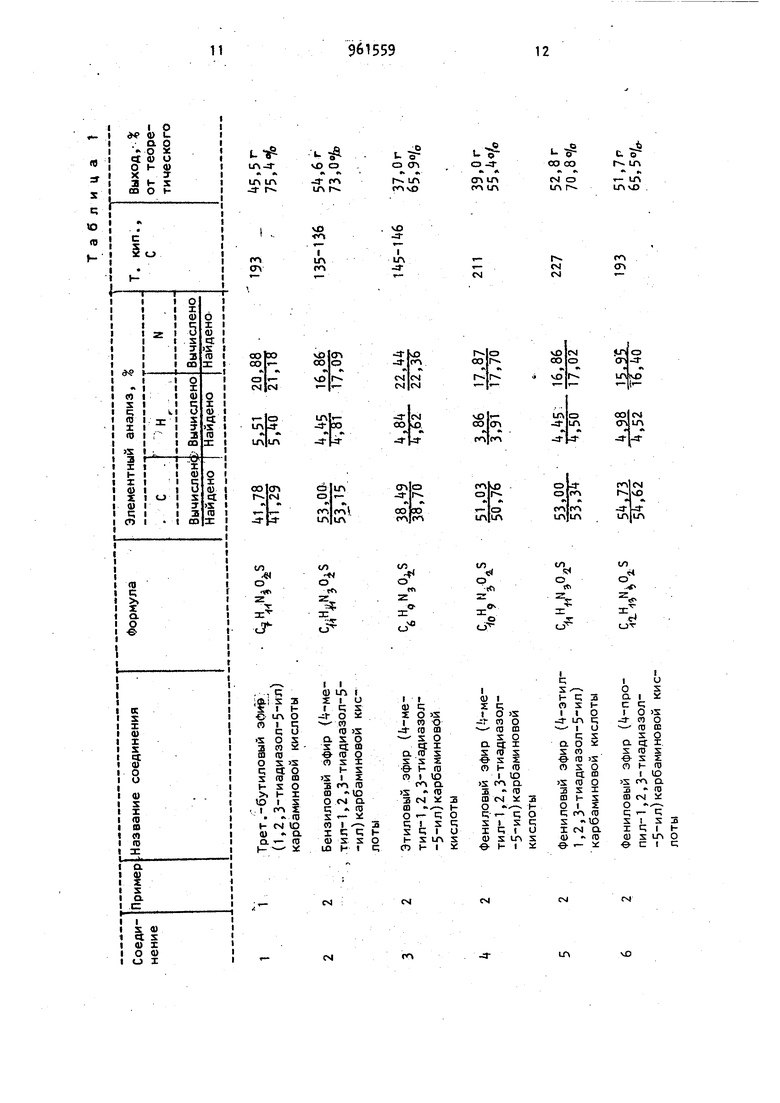
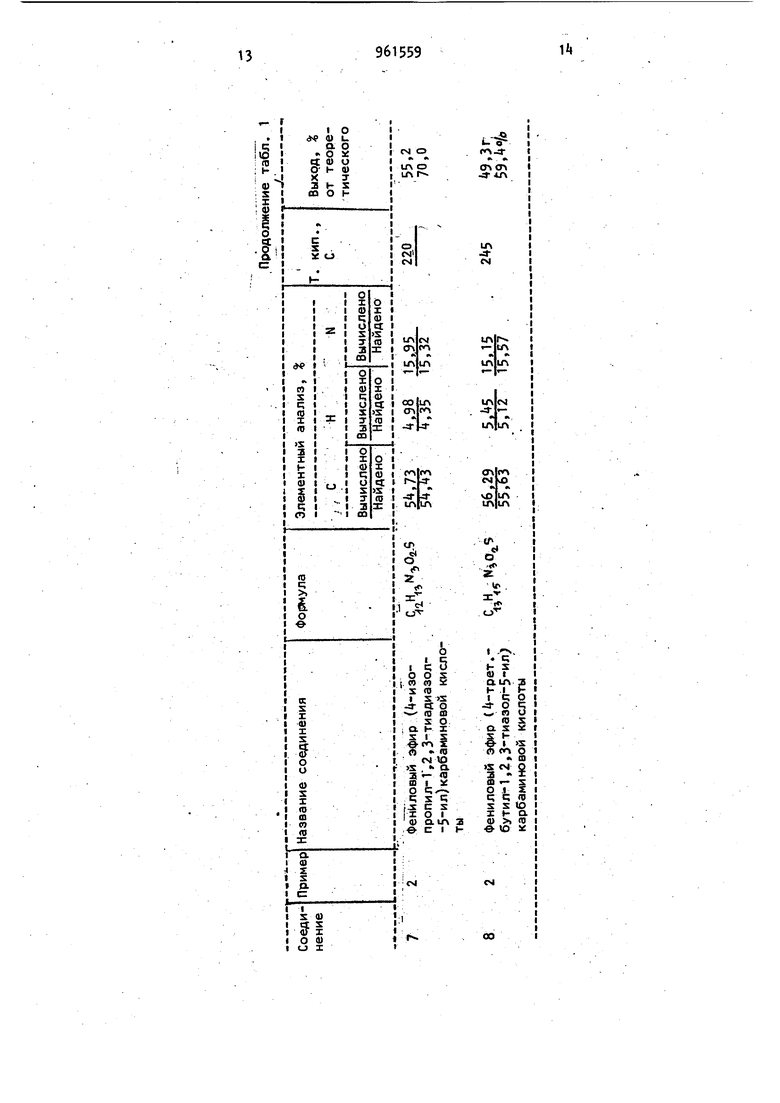
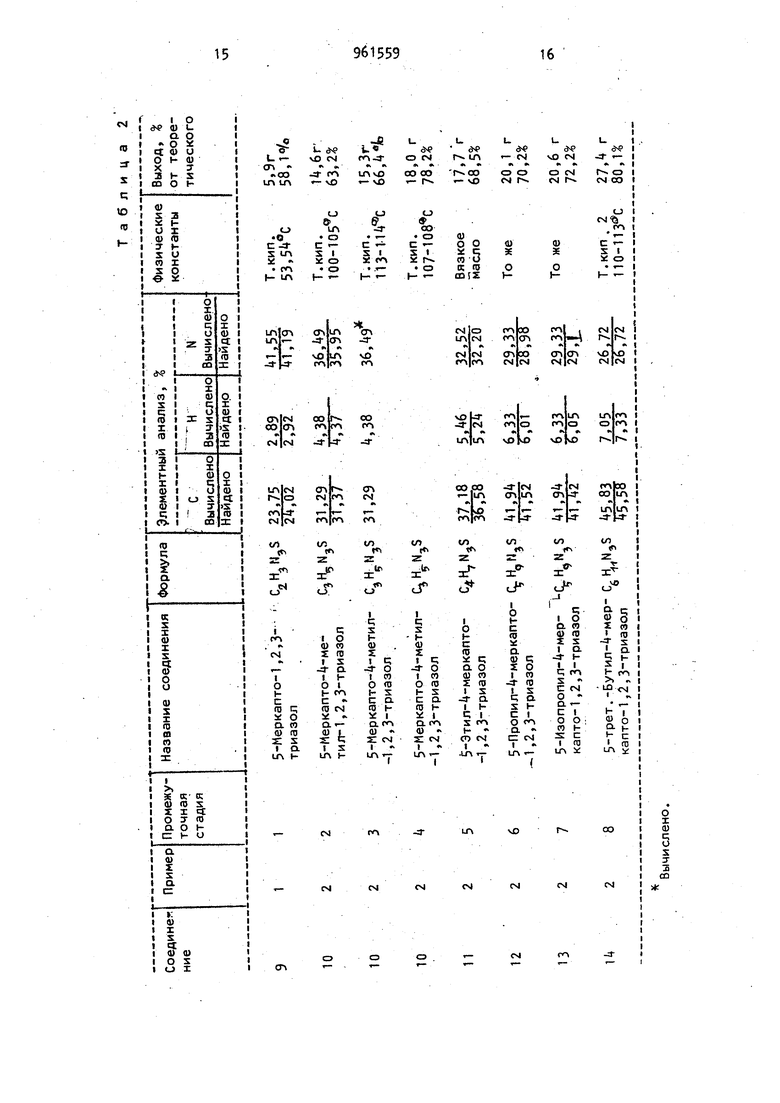
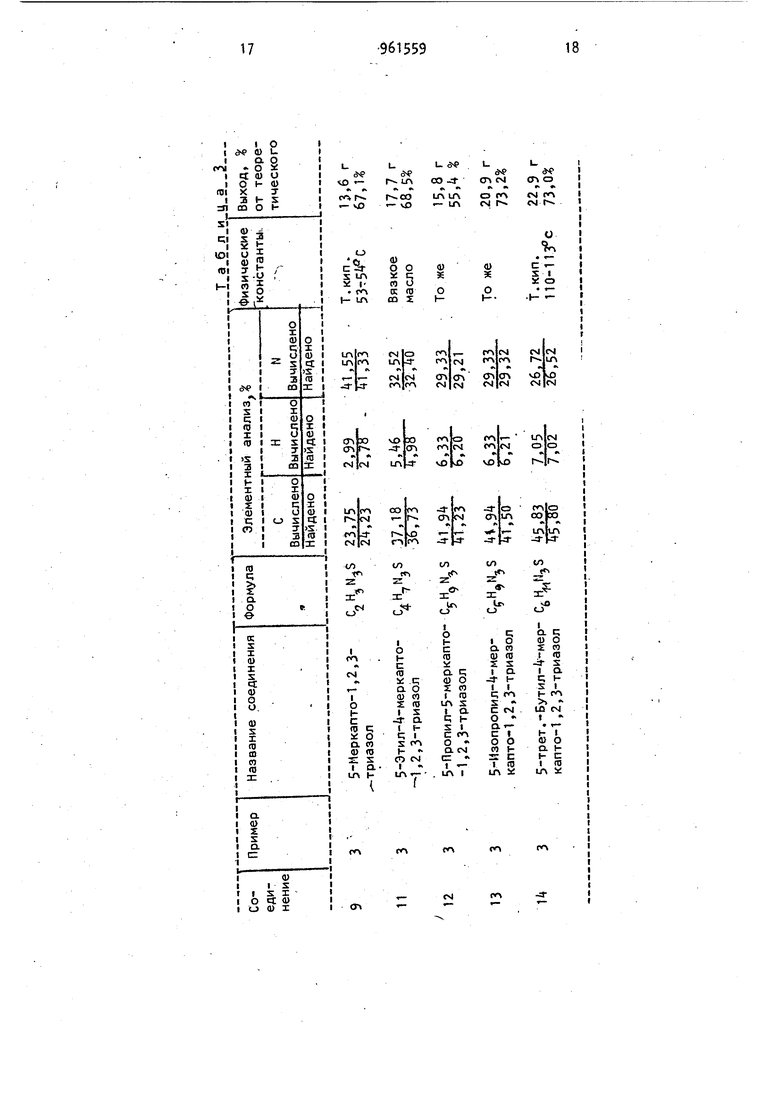
золы формулы у. Образовавшиеся в кислой водной среде и имеющиеся в раст-. . воренном виде 5 змино-1,2,3-тиадиазолы известным образом в присутствии высоких концентраций неорганических оснований, таких как окислы, гидроокиси и карбонаты щелочных или щелЬчноземельных металлов, или же их алкоголяты, можно превращать в 5 меркапто- ,, уксусный и малоновыЯ; кетоны - ЛТрименение карбаматов третичных спирметилизобутилкетон, изофорон,.10 тов предпочтительно из-за их легкой. 9 рованные углеводороды - хлористый метилен, хлороформ, 152-дихлорэтан и четыреххлористый углерод; алифатические и ароматические углеводороды петролейный эфир, пентан, гептан, циклогексан, бензол, толуол, ксилол, хлорбензол, простые эфиры - диэтиловый эфир, тетрагидрофуран и диоксан. соответствующие 5 амино-1,2,3-тиадиа1,2,3-триазол формулы I в процессе перегруппировки Димрота, Благодаря применению большей концентрации основания )меркапто-1,2,3 триазол формулы f имеется в виде соответствующей соли щелочного или щелочноземельного металла, из которой он выделяется благодаря применению соответствующей минеральной кислоты. Целесообразнее использовать основание и 5 амино-1 ,2,3-тиадиазол формулы У в мольном соотношении 2:1. Используемые при протекании реакции органические растворители могут служить одновременно в качестве экстрагирующего средства для 5-меркапто. л fi г -1,2,3-триазолов. После окончания реакции экстракты известным образом обрабатывают, например после соответствующего высушивания - путем отгонки использованного растворителя при нормальном или пониженном давлении. Таким образом получают 5 меркапто-1,2,3 триазол в чистой форме и с очень высоким выходом. Время реакции, в зависимости от температуры реакции, составляет 0,5-5 ч. Омыление сложныхэфиров {1,2,3 -тиадиазол-5 ил)-карбаминовой кисло7 ., 96 ты может происходить и известным образом как щелочное. Карбамат формулы 1У, предпочтительно в виде неочищенного (сырого) раствора или суспензии, нагревают вместе с водным или спиртовым раствором гидроокисей щелочных или щелочноземельных металлов в мольном соотношении карбамат:основание примерно 1:3. Реакция протекает при 80-100 0 . Продолжительность реакции 0, ч, в зависимости от температуры реакции. При таком осуществлении способа невозможно выделить соответствующий 5-амино-1,2,3-тиадиазол, так как сначала получают соли, щелочных или щелоч ноземельных металлов продукта перегруппировки Димрота. 5 Меркапто-1,2,3 тиадиазолы затем выделяются из.-этих солей известным образом. .Пример 1. Получение 5 Меркап то-Ц-метил-1,2,3-триазола. В трехгорлой круглодонной колбе емкостью 2 л с мешалкой, термометром и капельной воронкой kj, г (0,3 мол гидразида -метил-1,2,3 тиадиазол-5 карбоновой кислоты растворяют в 300 мл воды и 36 мл концентрированной соляной кислоты. Раствор затем смешивают с 600 мл толуола. К этойсмеси в течение 30 мин при 0-5°С при капывают раствор 21,75 г (0,315 моль нитрита натрия в 60 мл воды. Перемешивают 15 мин при С, отделяют толуольную фазу, промывают ее 150 мл ледяной воды и высушивают затем над сульфатом магния. В трехгорлой круглодонной колбе емкостью 2 л с мешалкой термометром, обратным холодильником и хлоркальциевой трубкой предварительно нагревают до 150 мл толуола и 31.8 мл (0,33 моль) трет.-бутанола. Высушенный раствор азида карбоновой кислотьГ прикапывают к указанному нагретому раствору в течение 20 мин таким образом, чтобы внутренняя температура под держивалась при 100-110°С. Перемешивают еще 30 мин при 100-110 С, затем „П «. охлаждают до 5 С и отсасывают кристал лы, которые сушат в вакууме при до постоянного веса. Выход 47,1 г, что составляет 73 от теоретического (трет.-бутиловый эфир ( метил-1,2,3 тиaдиaзoл-5 ил)кapбaминoвoй кислоты). Т.пл. 152-153 (разложение). ТХ: элюент уксусный |эфир; значение Rf 0,. Остальные сложные эфиры 1,2,3-тиадиазол-5 ил-карбаминовой кислоты, полученные по способу примера 1, представлены в табл.1. В трехгорлой колбе емкостью 1 л с мешалкой, термометром и обратным холодильником при интенсивном перемешивании нагревают до . 21,5 г (0,1 моль) трет.-бутилового эфира (-метил-1,2,3 Тиадиазол-5-ил)-карбаминовой кислоты в смеси 250 мл толуола 1 200 мл воды и затем в течение 15 мин смешивают с 8 мл концентрированной кислоты. Перемешивают еще 5 мин при 80°С, охлаждают до 20°С, смешивают смесь с раствором 12 г (0,3 моль) гидроокиси натрия в 50 мл воды и-затем нагревают при в течение 5 мин. После этого смесь охлаждают до 20 С, отделяют толуольную фазу и отбрасывают; водную фазу подкисляют 20 мл концентрированной соляной кислоты, смешивают с 75 г поваренной соли и затем экстрагируют уксусным эфиром. Высушенные над сульфатом магния уксусноэфирные экстракты- выпаривают досуха, при 0 С в вакууме. Выход составляет 52,1% от теоретического (5-меркапто- -метил-1 ,2,3-триазол ). Т.пл. 100-105с см. табл. 2 . Пример 2. Получение 5-меркапто-1,2,3-триазола. Аналогичным образом, как в примере 1, получают фениловый эфир (1,2,3 -тиадиазол-5-ил)-карбаминовой кислоты с Т.пл. 21б С ( разложение из гидразида 1,2,3 тиадиазол-5 карбоновой кислоты с выходом 88,1 от теоретического. Остальные сложные эфиры 1 ,2,3-тиадиазол-5-ил карбаминовой кислоты, полученные по способу примера 2, представлены в табл. 1, В трехгорлой круглодонной колбе емкостью 500 мл с мешалкой, термометром и обратным холодильникомбтечение 4 ч нагревают при 95°С и,25 г (0,2 моль) фенилового эфира (1,2,3 . f . .V .. -Тиадиазол-5-ил -карбаминовой кислоты в растворе из 12 г (0,3 моль гидроокиси натрия в 150 (4л воды. Затем раствор охлаждают до 20С и смешивают с 2б, мл концентрированной соляной кислоты. После насыщения 100 г поваренной соли раствор экстрагируют порциями с помощью 150 мл уксусного эфира. Уксусноэфирные экстракты встрякивают с раствором 20 г бикарбоната калия в 75 мл воды. Водную фазу нейт рализуют 17,6 мл концентрированной соляной кислоты и затем снова экстра гируют 150 мл уксусного эфира. ВысуЦенные над сульфатом магния уксусно- эфирные экстракты концентрируют досу ха при в вакууме. Получают окра шенные в слабо-желтоватый цвет кристаллы. Выход 10,7 г, что составляет 52,9% от теоретического (5-меркапто-1,2,3-триазол). Т.пл. 53, (см. табл. 2). . Пример 3. Получение 5 меркапто-Ц-метил-1,2,3 триазола. В трехгорлой круглодонной колбе емкостью 1 л с мешалкой, термометром и капельной воронкой 31,6 г (0,2 моль) гидразида 4-метил-1,2,3-тиадиазол-5 карбоновой кислоты раст воряют в 200 мл воды и 2 мл концент рированной соляной кислоты. Этот фаст вор затем смешивают с (00 мл толуола К этой смеси в течение 15 мин при б-5С прикапывают раствор 14,5 г j|0,/.1 моль) нитрата натрия в tO мл §оды. Перемешивают еще 15 мин при , отделяют толуольную фазу, пройй 1вают ее 100 мл воды и высушивают. над сульфатом магния. В трехгорлой круглодонной колбе емкостью 1 л с мешалкой, термометром обратным холодильником, капельной воронкой и хлоркальциевой («осушительиой) трубкой 18, (0,2 моль) фенола растворяют в 100 «л толуола и предварительно нагрерают до 110 С. Высушенный раствор азида карбоновой кисло ты прикапывают к указанному нагретому раствору в течение 20 мин таким образом, чтобы внутренняя температура поддерживалась равной 100-110 С. Перемешивают еще 15 мин при 100-ПО°С, охлаждают до 90°С, смешивают эту cyc-пензию с раствором 2k г (0,6 моль) гидроокиси натрия в 200 мл воды. Следующие 1,5 ч смесь кипятят с обратным холодильником. Затем смесь охлаждают до , водную фазу отделяют и смешивают с 52,9 мл концентрированной соляной кислоты. После насыщения 70 г поваренной соли смесь экстрагируют 300 мл уксусного эфира (порциями. Уксусноэфирные экстракты потом встряхивают с раствором 22 г бикарбоната калия в 85 мл воды. Водную фазу смешивают с 17,6 мл концентрированной соляной кислоты и I экстрагируют 300 мл уксусного эфира порциями. Высушенные над сульфатом магния уксусноэфирные экстракты выпаривают досуха при k(fC в вакууме. Получают кристаллы белого цвета. Вы|Ход 12,9 г, что составляет 56 от теоретического (5-меркапто-А-метил -1,2,3-триазолК Т.пл. lU-lU C ;(см. табл. 3).. Пример k. Тем же способом, который описан в примерах 1 и 2, получают 5 меркапто-1,2,3-триазолы, представленные в табл. 2, между азидом 1,2,3-тиадиазол-5-карбоновой кислоты или соответствующим галоидангидридом 1,2,3-тиадиазол-5 карбоиовой кислоты или азидом 1,2,3 тиaдиaзoл-5гкapбoнoвoй кислоты и спиртом или фенолом поддерживается то же молярное соотношение.. СоответствуЮ1 4ие сложные эфиры ( ,2,3 тиадиазол-5 ил)-карбаминовой кислоты выделяют, как это описано в примерах 1 и 2, и подвергают катализированной кислотой реакции (пример 1) или реакции, катализированной основанием (пример 2), причем сохраняют то же молярное соотношение, что ,в примерах 1 и.2 (см. табл. 1). Пример S Тем же способом, что и в примере 3, получают следующие 5-меркапто-1,2,3 триазолы, причем поддерживают то же молярное соотноше ие между азидом 1,2,3-тpиaзoл-5-кapбоновой кислоты или соответствующим гидразидЬм 1,2,3-тиадиазол-5- карбоновой кислоты, или галоидангидридом 1,2,3-тиадиазол-5-карбоновой кислоты и фенолом.
- L. VD
о
ff IT, t
vO fO
I
in
rr
e
u
l-
c. o
о cxj CO
LA
k A
«Ч« t
о
en in 1Л
n- u .
Lf r
r«
1 CM m
M
ts





N :
СЧ
CM
tM
tn
vX)
ro
- --
u о ff
.JJ- 4Л
o-«€
i nJ
e to
m
ff
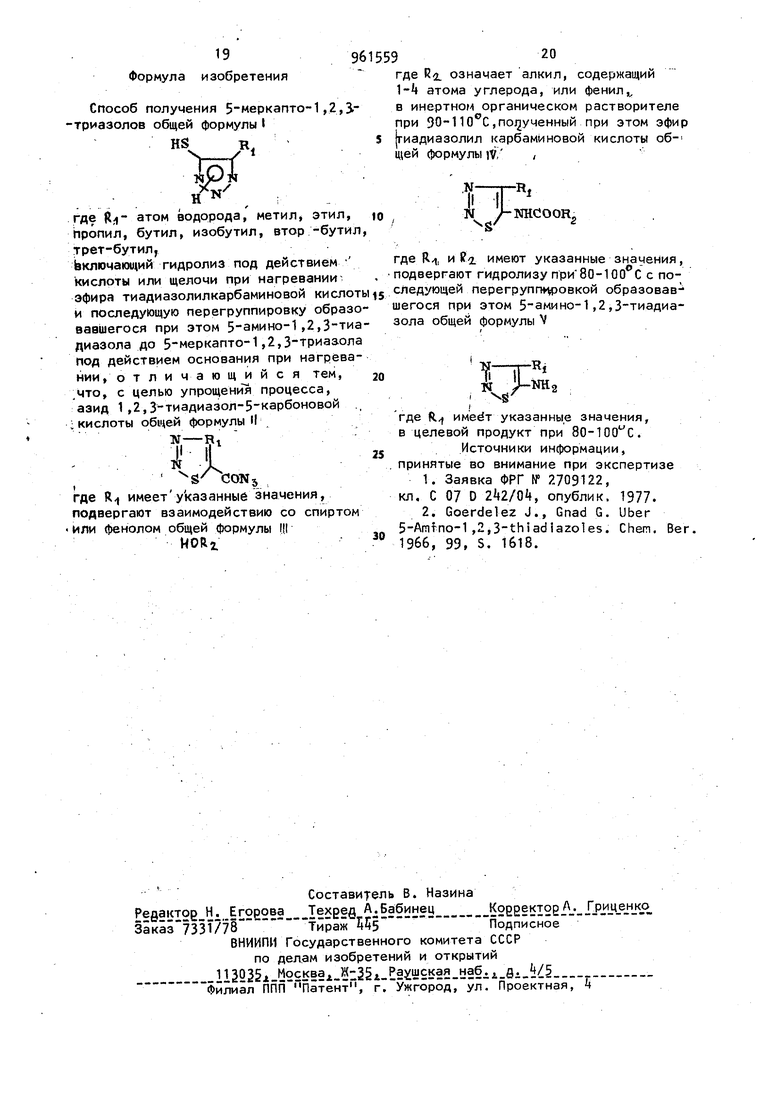
CM 19 Формула изобретения Способ получения 5-меркапто-1,2,i-тpиaзoлoв общей формулы I W ® Н N : где jf атом водорода, метил, этил, Пропил, бутил, изобутил, втор -бутил трет-бутил, Ьключащий гидролиз под действием кислоты или щелочи при нагревании эфира тиадиазолилкарбаминовой кислот и последующую перегруппировку образо вавшегося при этом 5 амино-1,2,3-тиа диазола до 5 меркапто-1,2,3 триааола под действием основания при нагревании , отличающийся тем, что, с целью упрощения процесса, азид 1,2,3-тиадиазол-5-карбоновой . ; кислоты общей формулы II Ж-5 IVItl I g CONj где R имеетуказанныб значения, подвергают взаимодействию со спиртом или фенолом общей формулы 1(1 HORi 96 где R. означает алкил, содержащий 1- атома углерода, или фенил в инертном органическом растворителе при 90-110 C,noj2y4eHHbm при этом эфир гиадиазолил карбаминовой кислоты общей формулы )V, NHCOOR где R и (i имеют указанные значения, подвергают гидролизу при80-100 с с последующей перегруппировкой образовавегося при этом 5 амино-1,2,3-тиадиазола общей формулы V где R/f имеет указанные значения, в целевой продукт при 80-100 0. Источники информации, принятые во внимание при экспертизе 1.Заявка ФРГ № 2709122, кл, С 07 D , опублик. 1977. 2.Goerdelez J., Gnad G. Uber 5-Amfno-1 ,2,3-thiaciiazoles. Chen, Ber, 1966, 99, S. 1618.
Авторы
Даты
1982-09-23—Публикация
1979-11-28—Подача