(54) СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ
/Ь-ЭКЗОТОКСИНА В ИНСЕКТИЦИДНОМ ПРЕПАРАТЕ
12
Изобретение относится к способам анализа инсектицидных препаратов и может быть использовано в сельском хозяйстве, ветеринарии, микробиологической и медицинской поомьпиленности, ПРИ производстве и применении инсектицидных препаратов, содержащих |Ъ -экзотоксин , а также для санитарно-гигиенического контроля внешней среды.
Известен способ количественного определения (Ъ-экзотоксина в инсектич.идных препаратах путем биоиспытаНий на тест-насекомых 1 .
Однако указанный способ требует дополнительного оснащения в виде инсектария или пункта, снабжакяцего исследователя тест-насекомыми. Промежуток времени, нсобходитиый для получения ответной реакции живого объекта, исчисляется -1-2 нед. Погрешность определения 25%. Все это значительно ограничивает применение метода как в практической, так.и в исследователь ной работе.
Известен также способ крличествен.ного определения fb -экзотоксина путем хроматографирования препарата на днионообменной смоле с последующей эмоцией ъ -экзотоксина и УФ-спектрофотометрирования элюата 2.
Существенным недостатком известного метода является суммарное спектрофотометрическое определение мног.:х компонентов, сопутствующих fi -экзотоксину и имеющих максимум поглощения, близкий к максимуму поглощения (i -экзотоксина. В результате этого
10 при спектрофотометрировании определяют поглощение смеси этих компонентов (продуктов деструкции (Ь-экзотоксинов и др.) с (Ъ -экзотоксином, которое принимают за поглоще15ние р -экзотоксина. Количество веществ, сопутствующих р -экзотоксину, зависит от степени его очистки и от методов выделения. Вторым недостатком метода является длитель20ная подготовка исследуемого образца к непосредственному количественному анализу.
Цель изобретения - vБeличeниe точности и чувствительности анализа
25 с одновременным его ускорением.
Поставленная цель достигается тем, что согласно способу количественного определения fi -экзотоксина используют смолу с размером час30тиц 7-15 мкм, а элюцию проводят пр: СКОРОСТИ 15-60 nyi/ч. температуре 20-50С и пои форме градиента кривой элюции У X.. При работе со смолой, диаметр частиц которой меньше 7 мкм, для . достижения скорости элюции 15-60 м .требуется значительное увеличение рабочего давления в.колонке, что пр водит к быстрой потере проницаемост колонки и сокращает cfJOK ее эксплуатации. Уменьшение же скорости элюции нежелательно, поскольку уве личивается продолжительность анали Использование в качестве стационар .ной фазы частиц диаметром более 15 мкм значительно ухудшает качест во разде тени::. Наиболее оптимальной формой градиентной кривой является У х при использовании которой удается достигнуть полного разрешения всех компонентов анализируемых смесей при минимальном ушиоении зон сорбци Поименение линейной формы гради ента с различным наклоном го диентной прямой обеспечивает хорош отделение пика /S -экзотоксина от слабо сорбируе.мых на колонке сое динений, однако ПРИВОДИТ к значительному размывайию зон сорбции ве ществ., иметааих величину времени удерживания более 20 мин, что в 510 раз снижает чувствительность ан лиза.Использование градиентной КРИВОЙ не позволяет достигнуть х рошего разрешения пиков, имеющих не большое различие времен удерживани В частности, в.эт.их условиях ПРОИСХОДИТ частичное перекрывание пиков, соответствутацих /Ь -экз-отокси ну и его лактону. . . Проведение элюции ПРИ комнатной температуре (20°С) ПРИВОДИТ к размыванию зон сорбции, увеличению вре мени удерживания веществ на колонке, ПЛОХОМУ разрешению пиков. Проведение элюции при температуре выше 50°С не желательно вследствие лабильности fb -экзотоксина при тем пературе выше 50°С. Проведение элюции при СКОРОСТИ потока 15 мл/ч нежелательно так какувеличивается-время анализа и происходит размывание зон сорбции Элюирование при скорости потока 60 мл/ч значительно сокращает время анализа. Но ухудшает разрешение пиков, имеющих небольшое различие времен удерживания. Компоненты препарата идентифицируют по их поглощению при 260 нм Количество fb -экзотоксина определяют по величине поглощения в пике с определенным временем удерживания, определяелвлм по калибровочн кривой. Для построения кашибровочной кривой аликвоты стандартного раствора fi -экзотоксина хроматографируйт и определяют площади пиков по формуле .W,, где Н - высота пика, W,,- ширина пика на половине высоты. Величину калибровочного коэффициента определяюТрПО формуле К где К, - калибровочный коэффициент, С - количество р -экзотоксина (рассчитанное), внесенного в колонку, S - площадь пика. Вычисление процента содержания i-экзотоксина проводят по формуле г. S К100 Со/ь где V - объем нанесенного образца, мкл; А - концентрация растворенного . образца, мкг/мкл (мг/глл). Пример 1. Навеску 500 мг инсектицида с неизвестным содержанием fb-экзотоксина растворяют в 5 мл деионизованной воды, осадок отфильтровывают, а раствор в объеме 10 мкл наносят на колонку (1,6 х X 150 мм ), термостатированную при 50®С с анионообменной смолой, диаметр частиц которой 7 мкм, в СГ -форме и разделение осуществляют при скорости потока .15 мп/ч в уело-, ВИЯХ градиентной элюции при форме градиентной кривой двумя раст-. ворами, содержащими НС1 и NaCI в концентрации 0,0025 н. НС1 и 0,005 М NaCI ГП, 0,01 н. НС1 и 0,2 М NaCI С2). Детектирование осуществляют в проточной кювете с объемом 8 мкл при длине волны 260 нм. Время удерживания р -экзотоксина 31 мин. Ошибка измерения ±3%. П р и М е р 2. Раствор образца в объеме 10 мкл, приготовленный аналогично описанному в примере 1 наносят на колонку (1.6 х 150 мм) с анионообменной смолой с размером частиц 15 мкм в Cl - форме и разделение осуществляют в условиях, указанных в примере 1, при скорости элюции 6О,мл/ч. Время удержи- вания Ь-экзотоксина 7 мин. Оитб ка измерения i 3%. Пример 3. Навеску С500 мг) инсектицида с неизвестным содержанием (Ь -экзотоксина растворяют в 5 мл деионизованной воды, осадок отфильуровывгиот, а раствор в объеме 10 мкл наносят на колонку (1;6 х X 150 мм), тер1яостатированную при 2fl°C. q анионообменной сферической
смолой фирьш Hitachi типа 2632 с-оаэмеоом частиц 10 мкм в СГ форме и разделение осуществляют приI скорости потока 18 мл/ч в условиях градиентной эЛюции Гформа градиент ной кривой ) двумя растворами содержащими НС1 и NaCI .в концентрации 0,0025 и. НС1 и 0,005 М NaCI (1). 0,01 н. НС1 и 0,2 М NaCI (21.
Детектирование осутествляют в проточной кювете с объемом 8 «сл при длине волны 260 нм. Время удерживания -экзотоксина 28 мин. Ощиб,ка измерения ±5%.
ПредлагаенШй способ количественного анализа fi-экзотоксина отличается от известного спектрофотометрическозто способа более высо- кой точностью, поскольку в результате хроматографии инсектицидных препаратов в указанных выше уелоВИЯХ происходит полное разделение Уф-пбглощакнцих компонентов, содержащихся в анализиоуемой смеси, и отделение от них fi-экзотоксина, подержание которого далее рассчитывается путем построения соответствующей калибровочной кривой зави1СИМОСТИ концентрации (Ь-экзотоксина от величины площади его пика на хроматогр;амме. При этом величина стандартной ошибки определения не превышает 2,5-3,0%. В случае анализа инсектицидных препаратов известным сПектрофотометрическим способом для очистки препаратов и шлтДедения (ь-экзотоксина используют сорбцию на активированном угле и .неэффективную хроматографию на колонке с сорбентом ДОкех-, что не позволяет получить /Ь -экзотоксин в индивидуальном состоянии. Исследуёмлй спектрофотометрическим способом элюат содержит, наряду с
Р -экзотоксином, значительное количество других УФ-поглощаюадих веществ,
0 образовавшихся в процессе биосинтеза инсектицида. В результате этого по суммарному поглощению растворов нельзя с достаточной точностью судить о содержании в них самого
5
р -экзотоксина.
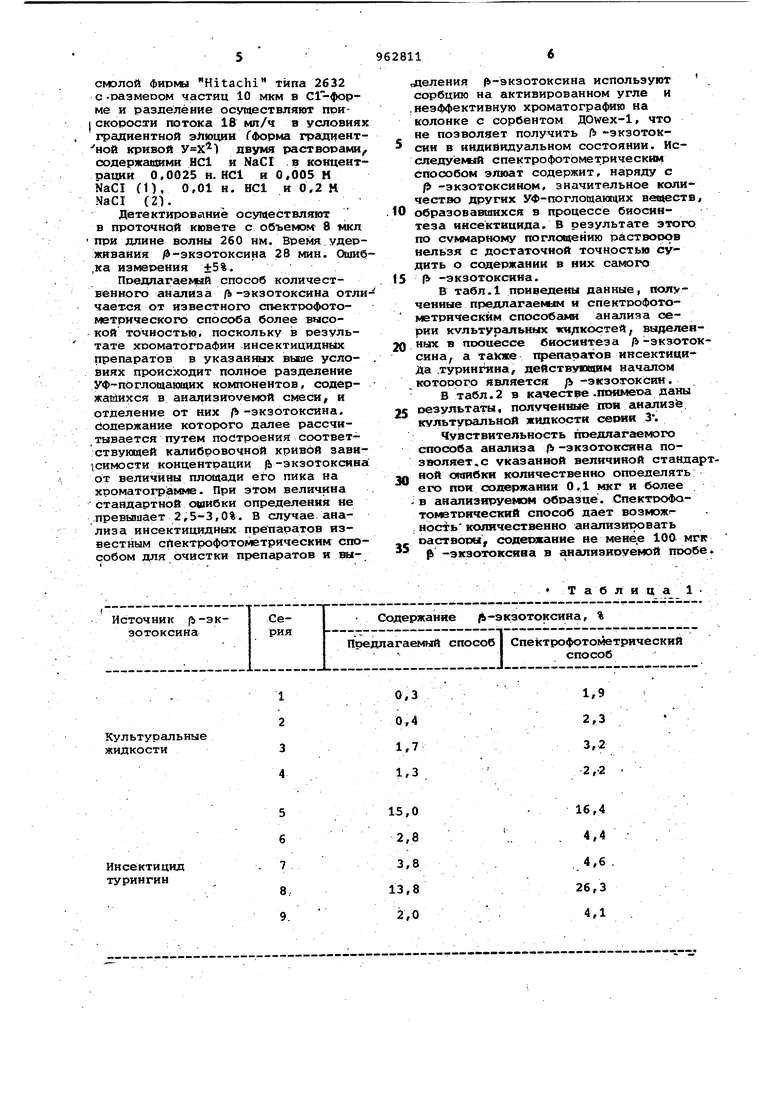
В табл.1 приведены данные, полученные предлагае «1м и спектрофотометрическим способами анализа серии культуральных жидкостей, выделенных в пооиессе биосинтеза /ь-экзоток0сина, а также препаратов инсектицида .турингина, действушщим началом КОТОРОГО является { -экзотоксин.
В табл.2 в качестве .примера даны результаты, полученные пои анализе,
5 культурапьной жидкости серия 3.
Чувствительность поедлагаемого способа анализа (Ь -экзотоксина позволяет с указанной величиной стандарт, ной ошибки количественно определять
0 его пои содержании 0.1 мкг и более в анализируемом образце. СпектроФотометрическяй способ дает возмож. ность количественно анализитэовать оастворы, содетякаиие не менее 10Q мгк
5
-экзотоксина в анализируемой пробе
Т а б л и да 1


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ количественного определения замещенных цефалоспоринов | 1982 |
|
SU1048401A1 |
| Способ определения @ -экзотоксина в инсектицидных биопрепаратах | 1985 |
|
SU1359744A1 |
| Способ количественного определения глицина в биологических лекарственных препаратах методом гидрофильной высокоэффективной жидкостной хроматографии | 2019 |
|
RU2700831C1 |
| Способ очистки нуклеазы из проростков ячменя | 1989 |
|
SU1703688A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПОДЛИННОСТИ И КОЛИЧЕСТВЕННОГО СОДЕРЖАНИЯ БЕНЗЭТОНИЯ ХЛОРИДА В ЛЕКАРСТВЕННЫХ ПРЕПАРАТАХ | 2013 |
|
RU2529814C1 |
| СПОСОБ ХРОМАТОГРАФИЧЕСКОГО РАЗДЕЛЕНИЯ КОМБИНИРОВАННОЙ ТВЕРДОЙ ЛЕКАРСТВЕННОЙ ФОРМЫ, СОДЕРЖАЩЕЙ АМЛОДИПИН И ВАЛСАРТАН | 2015 |
|
RU2603941C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КАРМУАЗИНА В СОКАХ | 2015 |
|
RU2596796C1 |
| Способ прогнозирования течения острого панкреатита | 2016 |
|
RU2637637C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПРОДУКТОВ ХИМИЧЕСКОГО ГИДРОЛИЗА ДЕЗОКСИРИБОНУКЛЕИНОВОЙ КИСЛОТЫ | 2015 |
|
RU2609431C1 |
| Способ количественного определения алоэнина в свежих листьях алоэ древовидного | 2021 |
|
RU2780977C1 |

1 2 3 4
Культуральные жидкости
5
6
7
1,9 2,3 3,2 2,2
16,4
4,4
.4,6
26,3
4,1
6,52 6,85
6,50 6,27 6,19
6,-70
Формула изобретения
Способ количественного определения . |1-экзотоксина в инсектицидном препарате путем хроматограФирования препарата на анионообменной смоле с послехг/юшей элюцией fb-экзотоксина и УФ-спектроботометРИРОвания элюата, отличающийс я тем. что. с целью увеличения точности и чувствительности анализа с одновременным его ускорениТаблица 2
1,84
0,12
ем, ИСПОЛЬЗУЮТ смолу с размером частиц 7-15 мкм, а элюцию ПРОВОДЯТ пои СКОРОСТИ элюнии 15-60 мл/ч, температуре 20-50°С и при Форме градиента КРИВОЙ элюции .
Источники информаи:ии, принятые во внимание ПРИ экспертизе

Авторы
Даты
1982-09-30—Публикация
1980-02-12—Подача