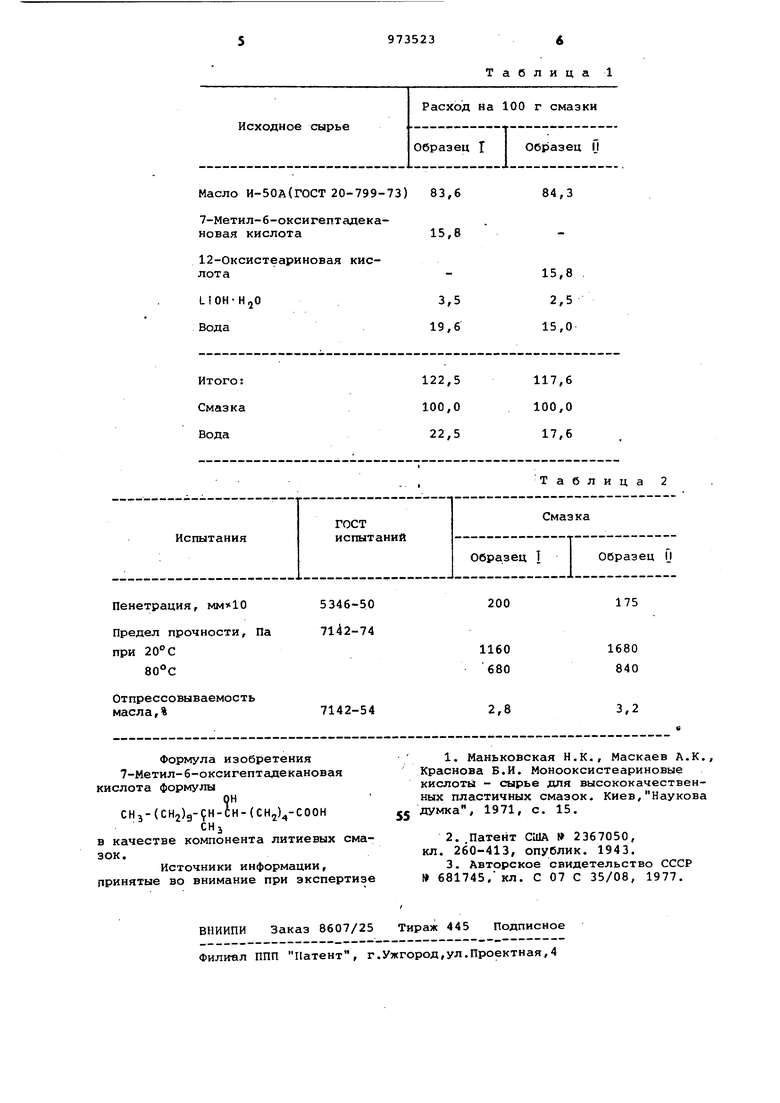
18 мл воды и 8,5 мл серной кислоты ((3 1,84)„ Прибавление хромовой кислоты проводят с скорс тью, чтобы температура реакционной смеси не превышала 15-20С и в течение 20 мин сохранялась характерная оранжевая окраска раствора. После прибавления окислителя смесь перемешивают 1 ч при комнатной температуре, отделяют ацетоновый раствор, остаток экстрагируют эфиром (дважды по 50 мл вытяжки объединяют и растворитель отгоняют. Остаток растворяют в 100 м эфира, промывают 150 мл 5%-ным раст вором бикарбоната натрия и водой до нейтральной реакции. Эфирный слой су шат над безводным сульфатом натрия, отгоняют эфир, и остаток перегоняют в вакууме. Выход 2-изододецилциклоге санона 13,9 г (70,4%, Т.кип. 160 1бЗС/3 мм, n|f 1,4696. Найдено,%: С 79,80; Н 12,56. Вычислено,:С 81,13; Н 12,86. б) Получение 7-метил-6-оксигептадекановой кислоты. К 10,3 г 2-изододецилциклогексанона прибавляют по каплям раствор надуксусн©й кислоты, приготовленный из 17,5 мл 30%-ной перекиси водорода, 11 мл уксусного ангидрида и 2 мл серной кислоты при 30-40С, с такой скоростью, чтобы температура реакционной смеси не пре вышала 60°С. После этого реакционную смесь перемешивают 2 ч при 50-60°С, добавляют 100 мл воды и кипятят 1 ч в колбе, снабженной обратным холодильником. Органический слой отделяю промывают 2-3 раза горячей водой 80 90°С и растворяют в 100 мл 4%-ного раствора едкого натра. Раствор кипятят 1 ч и после охлаждения до комнат ной температуры экстрагируют неомыля мые примеси петролейным эфиром. 2-3 раза -(по 50 мл) свободную оксикислоту выделяют подкислением соляно или серной кислотой до рН 2 фильтру ют, прогнивают на фильтре до нейтральной реакции и сушат в вакууме до постоянного веса. Выход 7,8 г (73,6% ),Т.пл. 91-92°С (из гексана) Найдено,%: С 71,61; Н 11,71; к.ч. 182,8 мг КОН/Г. Нзь ОзВычислено,%:С 71,94, Н 12,07; к.ч. 186,6 мг КОН/Г. п р и м е р- 2. а) Получение 2-из додецилциклогекйанона. К раствору 20 г 2-изододецилциклогексанола в 24 мл ацетона при интенсивном перемешивании, прибавляют по каплям раствор хромовой кислоты, приготовленный из 5,.5 МП хромового ангидрида 16 мл воды и 4,7 МП серной кислоты. с такой скоростью, чтобы температура реакционной смеси не превышала 20°С. Реакционную смесь перемешивают еще 30 мин, добавляют 500 мл воды, органический слой экстрагируют эфиром (З раза по 100 мл). Объединенные эфирные вытяжки промывают 5%-ным раствором натрия и водой, сушат над безводным сульфатом натрия. Эфир отгоняют, остаток перегоняют в вакууме. Выход 2-изододецилциклогексанона 10,1 г (51%), Т.кип. 162-165°С/ /3 мм; 1,4702. б) Получение 7-метил-6-оксигептадекановой кислоты проводят аналогично примеру 1б. Выход 7-метил-6-оксигептадекановой кислоты 7,4 г (70,2%),Т.пл. 90-91°С (из гексана), к.ч. 182,2 мг КОН/г. Пример З..а) Получение 2-изододецилциклогексанона. К эмульсии, приготовленной из 20 г 2-изододецилциклогексанола, 7,5 мл воды и 5,6 мл серной кислоты при перемешивании,прибавляют по каплям раствор 7,8 г бихромата натрия в 30 мл воды и 10,3мл серной кислоты (d-1,84), поддерживая . температуру в пределах 10-20°С. Затем реакционную смесь перемешивают 2 ч при комнатной температуре, органический слой экстрагируют эфиром (трижды по 50 мл). Объединенные эфирные вытяжки промывают водой до нейтральной реакции и сушат над безводным сульфатом натрия. Эфир отгоняют, остаток перегоняют в вакууме. Выход 2-изододецилциклогексанона 12,2 г (82%), Т кип. 165-167°С/Змм п|,° 1,4685. б) 7-Метил-6-оксигептадекановую кислоту получают аналогично примеру 16. Выход 7,2 г (68,5%), Т.пл. 89 91°С (из гексана),к.ч. 184,6 мг КОН/Г. П р и м е р 4. Испытания 7-метил-6-оксигептадекановой кислоты в качестве компонента литиевых смазок. Получают два образца смазок на основе 7-метил-6-оксигептадекановой (образец 1) и 12-оксистеариновой кислоты (образец ij ) Рецептура смазок приведена в табл. 1. Результаты испытаний смазок приведены в табл. 2. Полученные данные свидетельствуют о том, что 7-метил-6-оксигептадекановая кислота пригодна для получения высококачественных (с повышенной прочностью) смазок и может заменить 12-оксистеариновую кислоту, получавшуюся гидрированием касторового масла, в производстве литиевых смазок.

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 2-метилциклопентадеканона | 1977 |
|
SU734186A1 |
| Способ получения 2-метилциклопентадеканона | 1977 |
|
SU734185A1 |
| Способ получения производныхдигидРОбЕНзОпиРАНОКСАНТЕНОНОВ | 1979 |
|
SU818485A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ОКСИ- ИЛИ ТИО-ЭФИРОВ | 1974 |
|
SU440821A1 |
| Способ получения высшего С @ ,С @ или С @ 1-алканола | 1986 |
|
SU1366504A1 |
| Способ получения смеси душистых веществ с запахом амбры | 1980 |
|
SU906995A1 |
| Способ получения производных хиназолина | 1974 |
|
SU523090A1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,2-ДИЗАМЕ1ЦЕННЫХ ЦИКЛОАЛКАН-1,3- | 1973 |
|
SU376933A1 |
| Способ получения стереоизомеров трифтор-п-ментанола-3-7,7,7-трифтор -неоментола и 7,7,7-трифтор- -неозометола | 1974 |
|
SU520343A1 |
| Способ получения производных морфолина | 1974 |
|
SU521844A3 |


Авторы
Даты
1982-11-15—Публикация
1980-12-23—Подача