(54) СПОСОБ ПОЛУЧЕНИЯ АЛКИЛПЮИЗЮДНЫХ АРОМАТИЧЕСКИХ
УГЛЕВОДОРОДОВ



| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОБРАБОТКИ ПОЛИАЛКИЛАРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ | 2020 |
|
RU2818090C2 |
| КАТАЛИТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ АЛКИЛИРОВАНИЯ И/ИЛИ ПЕРЕАЛКИЛИРОВАНИЯ АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ | 1997 |
|
RU2189859C2 |
| СПОСОБ ПОЛУЧЕНИЯ МОНОАЛКИЛИРОВАННЫХ АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ (ВАРИАНТЫ) И СПОСОБ ПЕРЕАЛКИЛИРОВАНИЯ АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ | 1999 |
|
RU2208599C2 |
| СПОСОБ АЛКИЛИРОВАНИЯ АРОМАТИЧЕСКОГО СОЕДИНЕНИЯ | 1991 |
|
RU2014316C1 |
| КАТАЛИТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ АЛКИЛИРОВАНИЯ АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ, СПОСОБЫ ИХ АЛКИЛИРОВАНИЯ И ТРАНСАЛКИЛИРОВАНИЯ | 1995 |
|
RU2147929C1 |
| ПОЛУЧЕНИЕ ЖИДКИХ УГЛЕВОДОРОДОВ ИЗ МЕТАНА | 2005 |
|
RU2405764C2 |
| Способ получения фенола | 1989 |
|
SU1839668A3 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛБЕНЗОЛА | 2004 |
|
RU2298541C2 |
| КАТАЛИТИЧЕСКИЕ КОМПОЗИЦИИ И ИХ ПРИМЕНЕНИЕ В СПОСОБАХ АЛКИЛИРОВАНИЯ АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ | 2018 |
|
RU2763741C2 |
| КАТАЛИТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ТРАНСАЛКИЛИРОВАНИЯ АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ | 2003 |
|
RU2351393C2 |

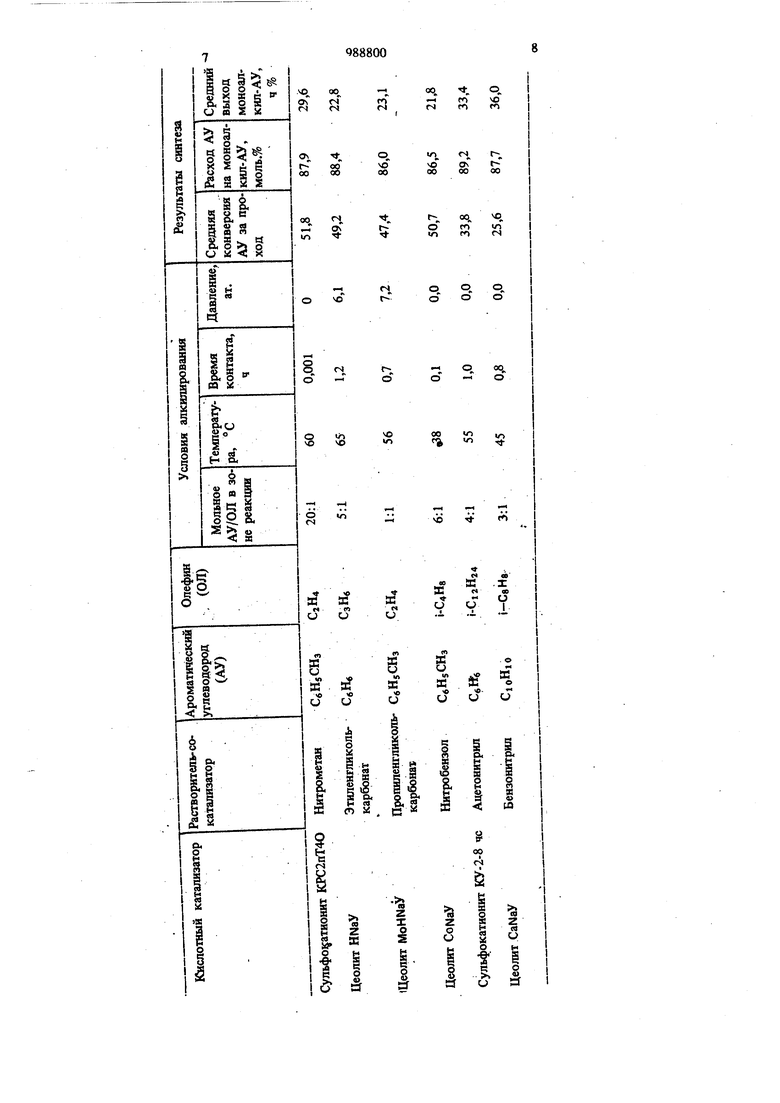
Изобретение относится к нефтехимической промышленности, точнее к получению алкнлпроизводных ароматических углеводородов, преимущественно этилбензола, кумола, диизопропилбеназола, этил- или третбутнлтолуола, додецилбензола, нафталина, алкилированием бензола, толуола или нафталина олефинами C2-Ci2. Указанные соединения применяются в качестве промежуточных продуктов производства винилароматических мономеров, фенилов, поверхностно-активных соединений, в качестве компонентов высокооктанового ПОторного топлива или смазочных масел. Ароматические утлеводороды (АУ) алкилируют олефинами (ОП) в жидкой фазе в при сутствии сильных кислот Лыоиса. Например без водного хлорида алюминия в виде комплекса с хлористым водородом. или его комплекса с нитрометаном или нитробензолом при 25- 80С, мольном соотношении ароматического углеводорода к олефнну,равном 1,5-5:1. ftuход алкилароматических углеводородов 25- 41% при конверсии аооматических углеводородов 40-50% 2. Одаако из-за значительной растворимости кислот Льюиса в катализате и их быстрой де- . зактивадии кислород-, азот-, серусодержашими примесями сырья, катализат приходится очищать от кислоты и: суспензии дезактивированного катализатора, что сопряжено с расходом 15-20 кг катализатора на 1 т продута,; образованием сточных вод, загрязненных сипь ными ядами биоочистки, усложнением технологической схемы и заметной коррозией аппаратуры. В качестве кислотных катализаторов можно применять также сильные кислоты Бренстеда - 88-98%-ная серная кнслота при температуре 30-40°С,АУ/ОЛ 4-6:1 (по моляМ), углеводороды: H2SQ4 1:1 (по обьему), давлении 1012 ат., времени коитакта около 1 ч. При конверсии АУ 55%, целевые продукты получают с селективностью около 80% 3. Однако непрореагировавшие ДУ и алкнл; производные, содержащие менее, чем необходимо, алкильных групп, возвращают в зону реакции. Деалкилпроизводные получают в условиях получения моноалкилпроизводных, но при увеличении времени контакта, при этом процесс сопряжен с большим расходом кислоты - до 200 кг/т продукта, образованием сточных вод, загрязненных ядами биоочистки, значительной коррозией аппаратуры, большим выходом побочных, загрязнением алкилтата ядами (сернистыми, фторидами) де гидирования. Недостатки устраняются использованием твердых кислотных кГатализаторов. Наиболее близким к изобретению по технической сущности и достигаемому резуль тату является способ получения алкилпроизводных ароматических углеводородов путем контактирования в жидкой фазе при повышенной температуре ароматического углеводорода, с олефшюм С2-Cj2 в присутствии синтетического твердого кислотного катализатора. В известном способе используют высококремнеземный синтетический цеолит,содержащий алюмосиликатный катализатор с мольным соотношением А1з.Оз к ЗЮг 8,8-50, причем содержание цеолита составляет 1-89% (например 2:SM-2I, ZSM 35, ZSM 38) и проводят процесс при температуре 30-600°С, давлении 0,18-56 ат., времени контакта 0,2-2,0 ч. При конверсии АУ до 15%, селективность по моноалкилпроизводному около 83%. С той же, примерно, селективностью по лучают диалкилпроизводные при конверсии моноалкилпроизводных до 10% 4. Недостатками способа являются сяощюсть производства за счет больших рециклов сырь и, как результат, малая конверсия и селективность. Цель изобретения - увеличение выхода целевого продукта. Поставленная цель достигается согласно способу получения алкилпроизводных ароматического углеводорода путем контактирования в жидкой фазе при температуре 38- 200° С ароматического углеводорода с олефином C2-Ci2 в присутствии твердого синтети ческого кислотного катализатора и 10-60 об растворителя, выбранного из группы, содержа щей сульфолан, Р, 7-ДИметилтетраметш1енсульфон, / -метилтетраметиленсульфон, нитрометан, ншробензол, ацетонитрил, бензонитрил, этилен- или пропиленгликолькарбонаг,их смесь. Технология предлагаемого синтеза состоит в следующем. Моноалкилирование проводят при повышен ной температуре АУ/ОЛ 1-20/1-3 (по молям давлении 0-20 ат., времени контакта 2 ч в статическом или проточном реакторе, подавая смесь углеводородов совместно с растворителем со cfcopocтью 0,5-1000 ч. В качестве катализатора используют цеолитсо94 держашие (типа У) алюмосиликаты. Собирают целевой продукт. Непрореагиронавший АУ вместе с растворителем возвращают в зону реакции. КЬн версия АУ за проход составляет 40-60% при селективности по моно-ААУ 86-88% (выход моно-ААУ в среднем составляет 21,5-25,8% ч). Синтез диалкилпроизводных проводят в тех же условиях, увеличив время контакта сырья с катализатором на 0,5-4 ч, возвращая моно- и полиалкилароматические углеводороды в зону реакции. При зтом конверсия за проход АУ составляет 72-88%, его расход на целевые продукты 40-55%, на сумму монои диалкил-АУ - 88-95%. При использовании в качестве сырья моноалкил-АУ при конверсии за проход 40-60% селективность по диалкил-АУ составляет 87-91%. Пример 1. Получение кумола. В термостатируемый при 200° С стальной реактор емкостью 59 мл помещают 9,0 г цеолита CctV фракции 0,25 мм, 15 мл осушенного сульфолана и 35 мл (30,8 г) бензола. Через суспензию барботируют пропилен со скоростью 12 г/ч под давлением 4 ат. в течение 1ч.. Мольное соотношение бензол:пропилен в жидкости устанавливается 20:1. Время койтакта пропилена с бензолом в среднем около 2,2 с. Реактор охлаждают до комнатной температуры. Собирают верхний углеводородный слой. Растворенный в сульфолане бензол и продукты его алкилирования экстрагируют 25 мл гексана. Экстракт объединяют с верхним слоем. В реактор снова заливают 35 мл бензола и проводят алкилирование, как указано выше. Эти операции повторяют еще 68 раз. Объединенную смесь продуктов и экстрактов подвергают разгонке. Кроме гексана и сульфолана получают 1401 г непрореагировавшего бензола; 1022,0 г кумола и в сумме 191,5 г ди- и триизопропилензолов (ПИБ). Средняя конверсия бензола 35% при селективности по кумолу 88%. Материал реактора не корродирует. Анализы: кумол: t° „ 152°С; 1,4916; 0,8631. Найдено, %: углерод 90,00; водород 10,00. Рассчитано, %: углерод 89,93; водород 10,07. ПИБ (смесь 4 продуктов) t, 203215°С. Молекулярная масса (криоскопия) Пример 2. Получение этилбензола. В термостатируемый при 70° С стальной автоклав емкостью 300 мл загружают 25,0 г сульфокатионита КУ-2-8 чс фракции 0,2- 0,4 мм, 40 мл ,7- диметилтетраметиленсульфона и 160 мл бензола. Поддерживают давление этилена i 8 . ат. 10 с. Стравливают давление и автоклав охлаждают до комнатной температуры. Собирают верхний углеводород ный слой. Остатки катализатора и сульфонового раствора экстрагируют 50 мл гексайа, который затем отгоняют из экстракта. Послед ний объединяют с верхним споем. Катализах (по данным ГЖХ) состоит из бензола, 42,6% этилбензола и, в сумме 7,9% диэтилбен золов с примесью триэтилбензолов. Катализат разгоняют. Выход этилбензола 36,8% на загру женный бензол при селективности ВТ,5%. Анализы: этилбензол: 1,, 136°С . 1,4958, 0,8648, совпадение временя удерживания с таковым для стандартного э1н бензола (ГЖХ, неподвижная фаза - полиди.этиленгликольсукцинат на кирпиче, газ-носительазот), диэтилбензолы (1:1,2-0,1 орто, параи Atera-изомеров) с примесью 1,5% тризтилбензолов; , 181-184С, молекулярная масса (криоскопия, нафталин) 135,6, совпадение хроматографических времен удерживания со стандартами. Пример 3. Получение диизопрошшбензолов. Синтез проводят в условиях приме ра 1, при атмосферном давлении в течение 3 ч, заменив сульфолан на смесь 1:1 (по объему) /,7-f диметилтетраметиленсульфона с пропиленгликолькарбонатом. Катализат содержит ,мас.%: непрореагировавший бензол 16,5; кумол 21,7; о-диизопропилбензол 26,0; и-диизопропилбензол 22,0; м-диизопропилбензол 0,6. и триизопропилбензолы в сумме 13,2. Катализат разгоняют. Смесь из 8,3 г непрореагировавшего бензола и 11,0 г кумола снова помещают в .реактор и подвергают изопропилированию, как указано вьнпе. Суммарный выход днизопропилбензолов 58,6% на загруженный бензол. Анализ: диизопропилбензолы (смесь 1,00: :0,85: 0,02 орто-, пара-, А егд-изомеров) t°j, 204-2П°С, молекулярная масса (криоскопии, нафталин) 162,0. Найдено, %: углерод 88,72; водород 1,22. Рассчитано, %: углерод 88,79; водород 11,21. Пример 4. Получение диэтилбензолов. Синтезируют диэтнлбензолы в условиях примера 2, увеличив время выдерживания автоклава под давлением до- 30 мин и заменив |3-метилтетраметш1енсульфон на смесь (2:1 по объему) 1штрометана с адетонитрилом. Катализат разгоняют без предварительной экстракции продуктов из растворителя-сокатализатора. Получают, кроме растворителя, 17,1 г непрореашровавшего бензола, 93,5 г этилбензола, 86,0 г дизтилбензолов и 13,0 г тризтилбензолов. Смесь непрореагировавшего бензола с этилбензолом возвращают в зону реакшш. В итоге 2,1 г непрореагировав- шего бензола, 48,6 г зтилбензола, 71,9 г диэтилбензолов и в сумме 12,7 г триэтилбензолов. Средняя конверсия бензола 83,6%, его расход в дизтилбензолы - 40,0%, в сумму этил- и диэтилбензолов 95%. Анализы: диэтилбензолы (смесь 25:28-1 орто, пара- и иего-изомеров): ,„ 181- 183 С, молекулярная масса (криоскопия, нафталин) 134,5. Найдено, мас.%: углерод 89,52; водород 10,48. Рассчитано, мае. %: углерод 89,49; водород 10,51. Результаты моноалкилирования бензола, толуола и нафталина этиленом, пропиленбм, изобутиленом, диизобутиленом и триизобутиленами в условиях примера 1 или 2 приведены в таблице. Как следует из таблицы, прн конверсии ароматического углеводорода 25,6-51,8% его расход на моноалкиппронзводное не ниже 86%.
Формула изоёретення
Способ полученкя алкклпрояэводных ароматических углеводородов путем контактарования в жидкой фазе при повышшной температуре ароматического углеводорода с олефином €}- 2 в присутствии сиитетического твердого кислотного катализатора, отличающийся тем, что, с целью увеличения выхода целевого продукта, процесс проводят яри температуре 3&-2(XfC и я присутствии 10-60 о6.% растворителя, выбранного из группы, содержащей сул1 фолаи 0 м гтилтетраметилеисульфон, 0, - диметилтстраметилеисульфон, иитрометан, нитробензол, ацетонигрил, бензоиитрил, этилен- или прошшенгликолькарбонат, их смесь. Источники информации, принятые во внимание щт экспертизе

Авторы
Даты
1983-01-15—Публикация
1980-08-19—Подача