Изобретение относится к способам алкилирования ароматического соединения в присутствии синтетического пористого кристаллического цеолита в качестве катализатора алкилирования.
Известен способ алкилирования ароматических соединений/ включающий контактирование его с алкилирующим агентом в присутствии катализатора/ представляющего собой синтетический пористый кристаллический цеолит со следующей картиной дифракции рентгеновских лучей (1/2).
Межплоскостные Относительная интен-
расстояния сивность
d(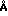 )
)
11,9 Сл - С
10/2 Сл
7/2 Сл
5/9 Сл
4/2 ОС
3/9 ОС
3/6 Сл
2/85 Сл
Изобретение относится к способам алкилирования ароматического соединения/ включающим контактирование ароматического соединения с по крайней мере одним алкилирующим агентом в присутствии алкилирующего катализатора/ включающего синтетический пористый кристаллический цеолит/ имеющий дифрактограмму/ включающую значения/ в основном представленные в табл. 1 описания.
Термин "ароматический" относительно алкилируемых соединений включает замещенные и незамещенные моно- и полиядерные соединения. Соединения ароматического характера/ которые обладают гетероатомом/ также употребительны при условии/ что они не действуют в качестве каталитических ядов при выбранных условиях протекания реакции. Замещенные ароматические соединения / которые могут здесь алкилироваться/ должны обладать по крайней мере одним водородным атомом/ непосредственно связанным с ароматическим ядром. Ароматические кольца могут быть замещены одним или более алкилом/ арилом/ алкарилом/ алкокси/ арилокси/ гидрокси/ циклоалкилом/ галоидом/ и/или другими группами/ которые не мешают реакции алкилирования.
Приемлемые ароматические углеводороды включают бензол/ толуол/ ксилол/ нафталин/ антрацен/ нафтацен/ перилен/ коронен и фенантрен.
Приемлемые алкилзамещенные ароматические соединения включают толуол/ ксилол/ изопропилбензол/ нормальный пропилбензол/ альфа-метилнафталин/ этилбензол/ кумол/ мезитилен/ дурол/ п-кумол/ бутилбензол/ псевдокумол/ о-диэтилбензол/ м-диэтилбензол/ п-диэтилбензол/ изоамилбензол/ изогексилбензол/ пентаэтилбензол/ пентаметилбензол; 1/2/4-тетраэтилбензол; 1/2/3/5-тетраметилбензол; 1/2/4-триэтилбензол; 1/2/3-триметилбензол/ м-бутилтолуол; п-бутилтолуол; м-пропилтолуол; 4-этил-м-ксилол; диметилнафталины; этилнафталин; 2/3-диметилантрацен; 9-этилантрацен; 2-метилантрацен; о-метилантрацен; 9/10-диметилфанантрен; и 3-метилфенантрен. Высокомолекулярные алкилароматические углеводороды могут быть использованы в качестве исходных материалов и включают ароматические углеводороды такие/ которые получают путем алкилирования ароматических углеводородов олефиновыми олигомерами. Такие продукты часто называют в данной области техники алкилатами и они включают гексилбензол/ нонилбензол/ додецилбензол/ пентадецилбензол/ гексилтолуол/ нонилтолуол/ додецилтолуол и пентадецилтолуол.
Приемлемые алкилируемые фенольные соединения включают метилфенолы (крезолы); диметилфенолы (ксиленолы); (этил/ пропил и бутилфенолы; галоидфенолы (например/ хлор и бром); алкилгалоидфенолы; алкоксифенолы; дигидроксибензолы (например/ гидрохинон катехол/ резорцин); и гидроксилированные конденсированные кольцевые системы/ например/ нафтолы/ антранолы и фенантранолы.
В своей прокаленной форме пористый кристаллический цеолит/ используемый в качестве катализатора в способе алкилирования данного изобретения/ имеет дифракционную картину/ включающую линии/ перечисленные в табл.1. Более определенно линии пересчислены в табл.2. И еще более определенно линии перечислены в таблице 3.
Наиболее точно/ прокаленный цеолит имеет дифракционную картину рассеяния рентгеновских лучей/ которая включает линии/ перечисленные в табл.4:
Эти значения определяют по стандартным методикам. Было использовано излучение К-альфа дублет меди и дифрактометр/ снабженный сцинтилляционным счетчиком и соединенный с компьютером. Высоты пиков/ l/ и положения пиков как функция 2 тэта/ где тэта угол Брегга/ определяли/ используя алгоритмы компьютера/ связанного с дифрактометром. Из этих относительных интенсивностей/ 100 l/lo/ где lo есть интенсивность самой сильной линии или пика и d (набл.) межплоскостное расстояние в Ангстремах (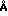 ), соответствующих записываемых линий/ определяли. В табл. 1-4 относительные интенсивности даны в терминах символов Сл=слабая/ Ср=средняя/ С=сильная и ОС= очень сильная. В терминах интенсивностей они могут означать следующее:
), соответствующих записываемых линий/ определяли. В табл. 1-4 относительные интенсивности даны в терминах символов Сл=слабая/ Ср=средняя/ С=сильная и ОС= очень сильная. В терминах интенсивностей они могут означать следующее:
Сл = 0-20 С = 40-60
Ср = 20-40 Ос = 60-100
Эти картины дифракции рентгеновских лучей характерны для всех разновидностей цеолитов. Натриевая форма/ также как и другие катионные формы/ обнаруживают в основм ту же самую картину с некоторыми небольшими сдвигами в межплоскостном расстоянии и изменение относительной интенсивности.Другие незначительные изменения могут происходить в зависимости от молярного отношения Y к X/ например кремния к алюминию/ данного образца/ также как от степени его термической обработки.
Синтетический пористый кристаллический цеолит/ используемый в качестве катализатора в одном способе алкилирования/ имеет в большинстве случаев состав/ включающий молярное отношение:
Х2О3:(n)YO2, где X есть трехвалентный элемент/ такой как алюминий/ бор/ железо и/или галий/ предпочтительно алюминий/ Y есть четырехвалентный элемент/ такой как кремний или германий/ предпочтительно кремний/ и n есть по крайней мере 10/ обычно от10 до 150/ более обычно от 10 до 60/ и еще более предпочтительно от 20 до 40. В синтезируемой таким образом форме цеолит имеет формулу в безводном состоянии и единицах молей оксида на n молей YO2/ как следует ниже:
(0/005-0/1) Na2O : (1-4)R : X2O3: nYO2 где R есть органический компонент/ Na и R компоненты ассоциированы с цеолитом в результате их присутствия во время кристаллизации и легко удаляются путем методов пост-кристаллизации/ описанными более детально ниже.
Цеолит/ используемый здесь/ термически стабилен и демонстрирует большую площадь поверхности (более чем 400 м2/г/ измеренную методом БЭТ (Bruenauer, Emmet and Teler) испытания) и необычно большую сорбционную емкость по сравнению со сходными кристаллическими структурами. В частности цеолит демонстрирует равновесные сорбционные емкости более/ чем 4/5 мас.%/ обычно более/ чем 7 мас.% для паров циклогексана и более/ чем 10 мас.% для паров н-гексана и обычно более/ чем 10мас.% для паров воды. Данный цеолит синтезируют почти свободным от катионов Na. Поэтому его можно использовать в качестве катализатора алкилирования с кислотной активностью без стадии обмена. При желании однако исходные катионы натрия синтезированного таким образом материала могут быть замещены в соответствии с методиками/ известными в данной области по крайней мере частично путем ионного обмена другими катионами. Предпочтительно замещающие катионы включают ионы металла/ ионы водорода/ предшественник водорода/ например аммоний/ ионы и смеси их. Особенно предпочтительными являются катионы/ которые специально подобраны/ чтобы быть активным катализатором алкилирования. Они включают водород/ редко-земельные металлы и металлы групп IIa. IIIA, IVA, IB, IIB, IIIB, IVB и VIII Периодической таблицы элементов. До его использования в качестве катализатора алкилирования/ цеолит следует подвергать термической обработке для удаления части или всех любых органических составляющих/ присутствующих в нем.
Цеолитный катализатор алкилирования. используемый здесь/ может быть также использован в хорошо известном сочетании с гидрирующим компонентом/ таким как фольфрам/ ванадий/ молибден/ никель/ кобальт/ хром/ марганец или благородный металл/ такой как платина или палладий/ где должна осуществляться функция гидрирования-дегидрирования. Такой компонент может быть введен в состав катализатора путем сокристаллизации/ может быть обменен в композиции в пределах элемента группы IIIA/ например/ алюминий/ находится в структуре/ пропитанной им или хорошо физически смешанной с ним. Такой компонент может импрегнироваться внутрь или снаружи цеолита/ так как например/ в случае платины путем обработки цеолита раствором/ содержащим платину в виде иона/ содержащего платину. Таким образом/ подходящие для этой цели платиновые соединения включают хлорплатиновую кислоту/ двуххлористую платину и различные соединения/ содержащие платиновый аминный комплекс.
До своего использования в способе алкилирования этого изобретения данные кристаллы цеолита следует дегидрировать по крайней мере частично. Это может быть сделано нагреванием цеолита до температуры в пределах от 200 до 595°С в такой атмосфере/ как воздух/ азот и т.д. и при атмосферном/ субатмосферном или высоких давлениях в течение периода от 30 мин до 48 ч. Дегидратация может осуществляться при комнатной температуре/ просто помещая кристаллический материал в вакуум/ но требуется более длительное время для того/ чтобы получить достаточную степень дегидратации.
Цеолит/ используемый в данном способе/ можно получить из реакционной смеси/ содержащей источники щелочных или щелочно-земельных мателлов (М)/ например натрий или калий/ катион/ оксид трехвалентного элемента Х/ например/ алюминий/оксид четырехвалентного элемента Y/ например кремний/ органический (R) направляющий агент/ гексаметиленимин/ и вода/ указанная реакционная смесь имеет состав/ в единицах мольных отношений оксидов/ внутри следующих пределов:
Реагенты Используемые Предпочтительные
YO2/X2O3 10-60 10-40
H2O/YO2 5-100 10-50
OH-/YO2 0,01-1,0 0,1-0,5
M/YO2 0,01-2,0 0,1-1,0
P/YO2 0,05-1,0 0,1-0,5
В предпочтительном способе синтеза/ YO2 реагент содержит значительное количество твердого YO2, например по крайней мере около 30 мас.% твердого YO2. Когда YO2 представляет собой диоксид кремния/ использование источника диоксида кремния/ содержащего по крайней мере/ около 30 мас.% твердого диоксида кремния/ например/ Ultrasil (осажденный/ высушенный распылением диоксид кремния/ содержащий 90 мас.% диоксида кремния) или Hisil (осажденный гидратированный SiO2, содержащий 87 мас.% диоксида кремния/ 6 мас.% свободной Н2О и 4/5 мас.% связанной Н2О гидратации и имеющий размер частиц 0/02 мкм) благоприятствует образованию кристалла из упомянутой смеси. Если используют другой источник оксида кремния/ например Q-Brand (силикат натрия/ включающий 28/8 мас. % SiO2, 8,9 мас.% Na2O и 62.3 мас.% H2O/ то кристаллизация может проходить незначительно/ если вообще имееет место для требуемого цеолита/ и могут получиться примесные фазы других кристаллических структур/ например ZCM-12. Предпочтительно поэтому/ чтобы YO2источник/ например/ диоксид кремния содержал по крайней мере 30 мас.% YO2/ например диоксида кремния/ и более предпочтительно по крайней мере 40 мас.% YO2/ например диоксида кремния.
Кристаллизацию требуемого цеолита можно проводить либо в статических условиях либо при перемешивании в подходящем реакционном сосуде/ таком как/ например полипропиленовые сосуды или автоклавы/ облицованные тефлоном или из нержавеющей стали. Кристаллизацию обычно проводят при температуре от 80 до 225°С в течение от 25 ч до 60 дней. После кристаллизации/ кристаллы отделяют от жидкости и выделяют.
Кристаллизация облегчается присутствием по крайней мере 0/01 %/ предпочтительно 0/10 % и еще более предпочтительно 1%/ затравочных кристаллов в расчете на общий вес кристаллического продукта.
До использования в способе изобретения/ полученный цеолит предпочтительно соединяют с другим материалом/ который устойчив к температурам и другим условиям/ используемым в способе алкилирования. Такие материалы включают активные и неактивные материалы и синтетические или имеющиеся природные цеолиты/ также как и неорганические материалы/ такие как глины/ диоксид кремния и/или оксиды металла/ такие как окись алюминия. Последняя может быть либо природного происхождения/ либо в форме желатинированных осадков или гелей/ включающих смеси диоксида кремния и оксидов металла. Использование материала в сочетании с цеолитом в момент его получения / т.е./ соединенным тотчас или с присутствующим во время его синтеза/ который сам по себе является каталитически активным/ может изменить конверсию и/или селективность катализатора. Пригодные неактивные материалы служат в качестве разбавителей для контроля глубины конверсии/ так что продукты алкилирования могут быть получены экономично и аккуратно без применения других средств для контроля скорости реакции. Эти материалы могут включаться в имеющиеся природные глины/ например бентонит и каолин/ чтобы улучшить прочность на разрушение катализатора в условиях алкилирования при коммерческой эксплуатации. Указанные материалы/ т.е. глины/ оксиды и т.д. функционируют как связующие для катализатора. Желательно разработать катализатор/ имеющий хорошую прочность на разрушение/ так как при коммерческом использовании желательно предотвратить катализатор от разрушения в порошокподобные материалы. Эти глинистые связующие используются обычно только для цели улучшения прочности на разрушение катализатора.
Встречающиеся в природе глины/ которые могут быть комбинированными с момента их образования включают семейство монтмориллонита и каолина/ и эти семейства включают суббентониты/ и каолины обычно известные как Dixie, McNamee, Georgia и Horida глины или другие/ в которых основным минеральным составляющим является галлуазит/ каолинит/ дикит/ накрит или анауксит. Такие глины моугт использоваться в неочищенном виде как первоначально добытые или в начальной стадии подвергнутые обжигу/ кислотной обработке или химической модификации. Связующие/ полезные для составления с цеолитом/ также включают неорганические оксиды/ облагороженные оксидом алюминия.
В дополнение к приведенным материалам данный цеолит может быть составлен с пористым матричным материалом/ таким как диоксид кремния-оксид алюминия/диоксид кремния - оксид магния/ диоксид кремния-диоксид циркония/ диоксид кремния-оксид тория/ диоксид кремния-оксид бериллия/ диоксид кремния-диоксид титана/ также как и тройные композиции/
такие как диоксид кремния-оксид алюминия-диоксид циркония/ диоксид кремния-оксид алюминия-оксид тория/ диоксид кремния-оксид алюминия-оксид магния и диоксид кремния - оксид магния-диоксид циркония. Представляется полезным разработать/ по крайней мере/ часть вышеприведенных матричных материалов в коллоидной форме/ так чтобы облегчить экструзию связанных каталитических(ого) компонента(ов).
Относительные пропорции цеолита и неорганической оксидной матрицы варьируются широко/ причем содержание цеолита колеблется от 1 до 90 мас.% и более обычно/ в частности/ когда композит приготавливают в форме шариков в пределах от 2 до 8 мас.% композита.
Стабильность катализатора алкилирования/ использованного в данном способе/ может быть увеличена путем обработки паром/ которую обычно осуществляют путем контактирования цеолита с 5-100 % паром при температуре по крайней мере 300°С (предпочтительно 300-650°С) в течение по крайней мере 1 ч (предпочтительно 1-200 ч) при давлении 101-2/500 кПа. В более конкретном варианте осуществления катализатор может быть изготовлен/ претерпевая обработку 75-100 % паром при 315-540°С и атмосферном давлении в течение 1-25 ч.
Способ алкилирования по данному изобретению обычно проводят при температуре от 0 до 500°С/ предпочтительно от 50 до 400°С/ и наиболее предпочтительно от 100 до 350°С; давлении от 20 до 25350 кПа (0/2 до 250 атмосфер)/ предпочтительно от 100 до 2550 кПа (1 до 25 атмосфер): молярное отношение алкилируемого ароматического соединения к алкилирующему агенту от 0/1: 1 до 50:1/ предпочтительно 0/5:1 до 10:1/ и исходная объемная скорость (WHSY) от 0/1 до 500/ и предпочтительно от 0/5 до 100/ причем последняя WHSY берется в расчете на общий вес активного катализатора (и связующего/ если присутствует).
Способ алкилирования по изобретению можно выполнять как периодическим процессом/ полунепрерывным или непрерывным процессом/ используя неподвижный/ псевдоожиженный или движущийся слой каталитической системы.
В дальнейшем изобретении поясняется более подробно на примерах и фиг.1 - 10.
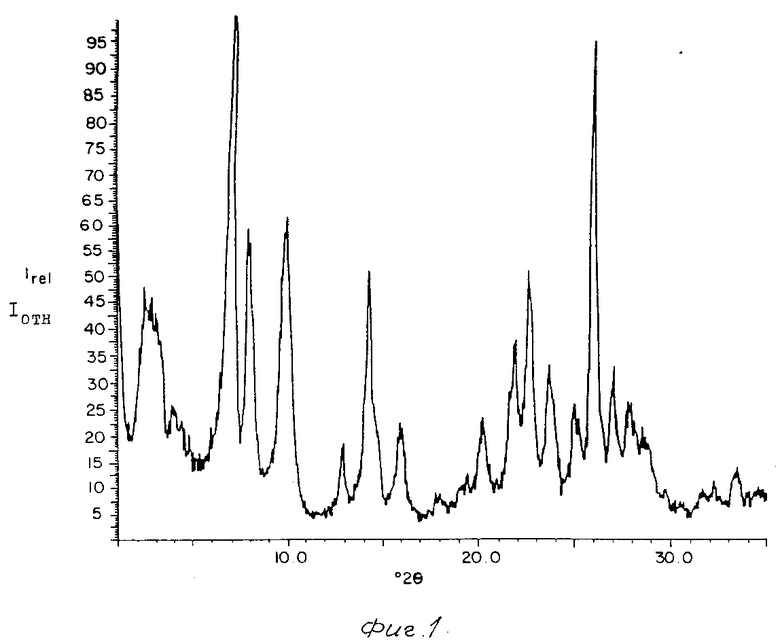
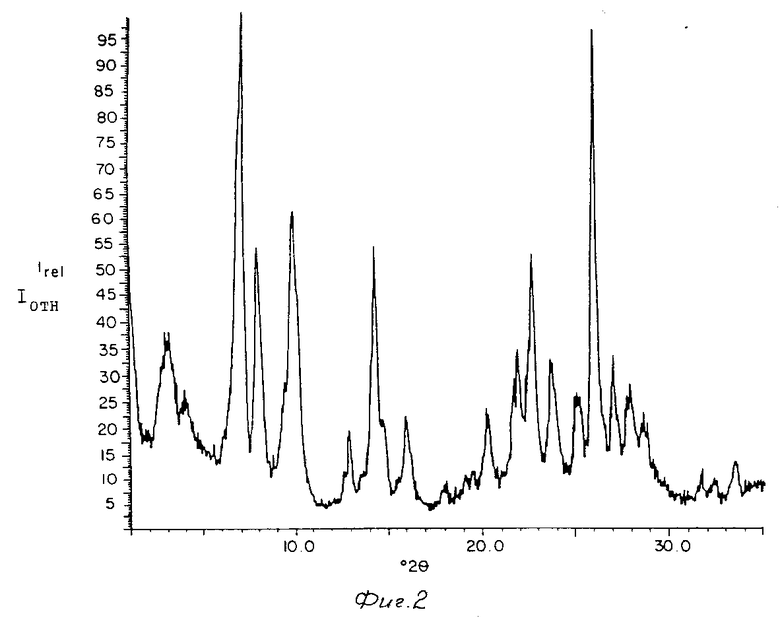
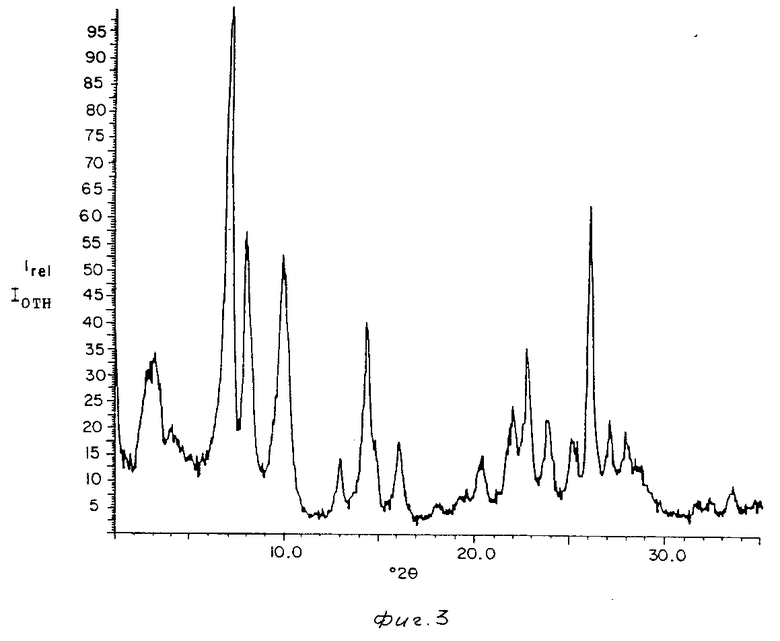
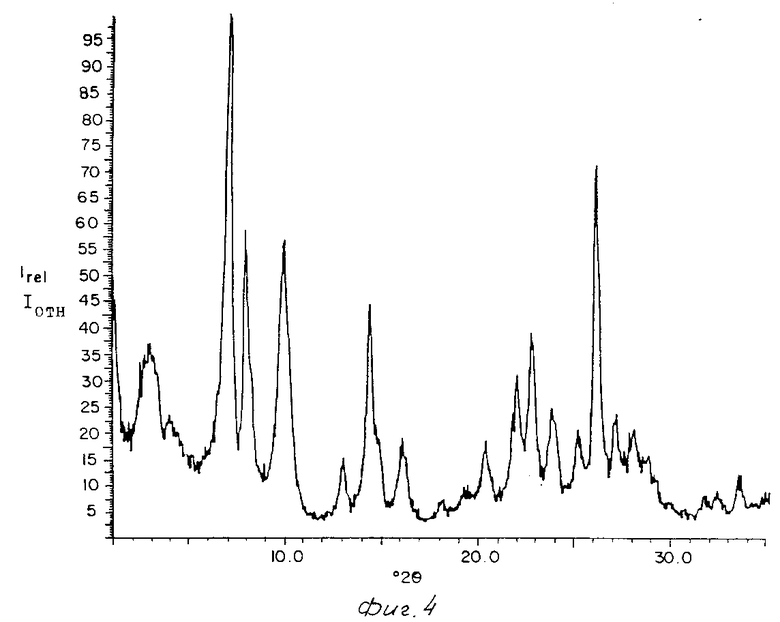
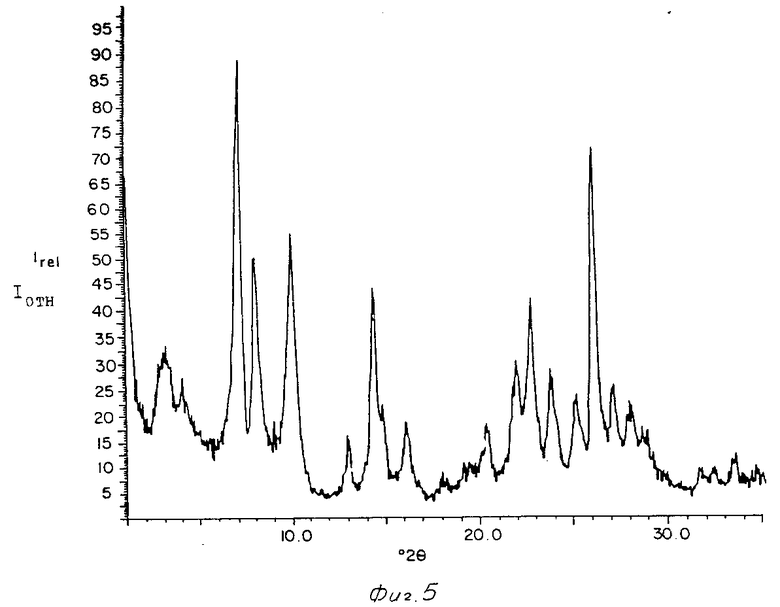
На фиг.1-5 представлены картины дифракции ренгеновских лучей продуктов прокаленных кристаллических материалов примеров 1/3/4/5 и 7/ представленных ниже;
на фиг. 6-10 гграфические изображения данных режима работы способа/ относящихся к примеру 15.
В примерах/ всякий раз когда представлены данные по сорбции для сравнения сорбционных емкостей по воде/ циклогексану и/или н-гексану они являются значениями равновесной сорбции/ определенной следующим образом.
Взвешенный образец прокаленного адсорбента приводят в контакт с желаемым чистым паром адсорбента в адсорбционной камере/ откачивают до менее/ чем 1 мм Hg и приводят в контакт с 1/6 кПа (12 торр) паров воды или 5/3 кПа (40 торр) н-гексана или 5/3 кПа (40 торр) паров циклогексана/ давления/ менее/ чем равновесное давление пар-жидкость соответствующего адсорбата при 90°С. Давление поддерживают постоянным (с точностью около ± 0/5 мм Hg) путем добавления паров адсорбата/ контролируемым маностатом во время периода адсорбции/ который не превышает 8 ч. По мере того как адсорбат адсорбировался цеолитом/ уменьшение давления заставляло маностат открывать кран/ который впускал больше паров адсорбата в камеру/ чтобы восстановить упомянутые контрольные давления. Сорбцию завершали/ когда изменение давления было недостаточным/ чтобы активировать маностат. Увеличение в массе вычисляют как сорбционную емкость образца в г/100 г прокаленного адсорбента. Цеолит/ используемый в способе изобретения/ всегда показывает значения равновесной сорбции больше/ чем 4/5 мас.% обычно большие/ чем 7 мас.% для паров циклогексана/ и большие/ чем 10 мас.% для паров н-гексана и обычно большие/ чем 10 мас.% для паров воды.
Когда рассматривают Значение Альфа/ отмечают/ что Альфа значение есть приблизительное указание каталитической крекирующей активности катализатора по сравнению со стандартным катализатором/ и оно дает константу относительной скорости (скорость)/ обычной конверсии гексана на объем катализатора на единицу времени. Оно базируется на активности высокоактивного крекирующего катализатора диоксид кремния-оксиь алюминия/ принимаемой как Альфа/ равная l (Константа скорости - 0/016с-1). Альфа Тест/ который используется здесь/ описан в l. Catalysis, 61, pp.390-396 (1980).
Пример 1. 1 ч. алюмината натрия (43,5 % Al2O3, 32,2 % Na2O, 25,6 % H2O) растворяют в растворе/ содержащем 1 ч 50 % -ного NaOH раствора и 103/13 частей H2O. К этому добавляют 4/50 ч. гексаметиленимина. Полученный раствор добавляют к 8/55 ч. Ultrasil/ осажденный/ высушенный распылением диоксид кремния (около 90 % SiO2).
Реакционная смесь имеет следующий состав/ в молярном отношении:
SiO2/Al2O3= 30,0
OH-/SiO2= 0.18
H2O/SiO2= 44.9
Na/SiO2= 0.18
R/SiO2= 0.35 где R есть гексаметиленимин.
Смесь кристаллизуют в реакторе из нержавеющей стали с перемешиванием при 150°С в течение 7 дней. Кристаллический продукт отфильтровывают/ промывают водой и сушат при 120°C. После 20 ч прокаливания при 538°C,дифракционная картина рассеивания ренгеновских лучей содержит основные линии/ представленные в табл. 5. Фиг.1 показывает/ дифракционную картину рассеивания ренгеновских лучей прокаленного продукта. Сорбционные емкости прокаленного материала/ как измерено/ составляют:
H2O 15,2 %
Циклогексан 14/6 %
н-гексан 16/7 % Площадь поверхности прокаленного кристаллического материала/ как измерено/ составляет 494 м2/г.
Химический состав непрокаленного материала/ как определено/ был следующим:
Компонент/ мас.%:
SiO2 66,9
Al2O3 5,40
Na 0,03
N 2,27
Ash 76,3 SiO2/Al2O3, молярное отношение - 21/1.
Пример 2. Часть прокаленного кристаллического продукта примера 1 испытывают в Альфе тесте и находят/ что Альфа значение равно 224.
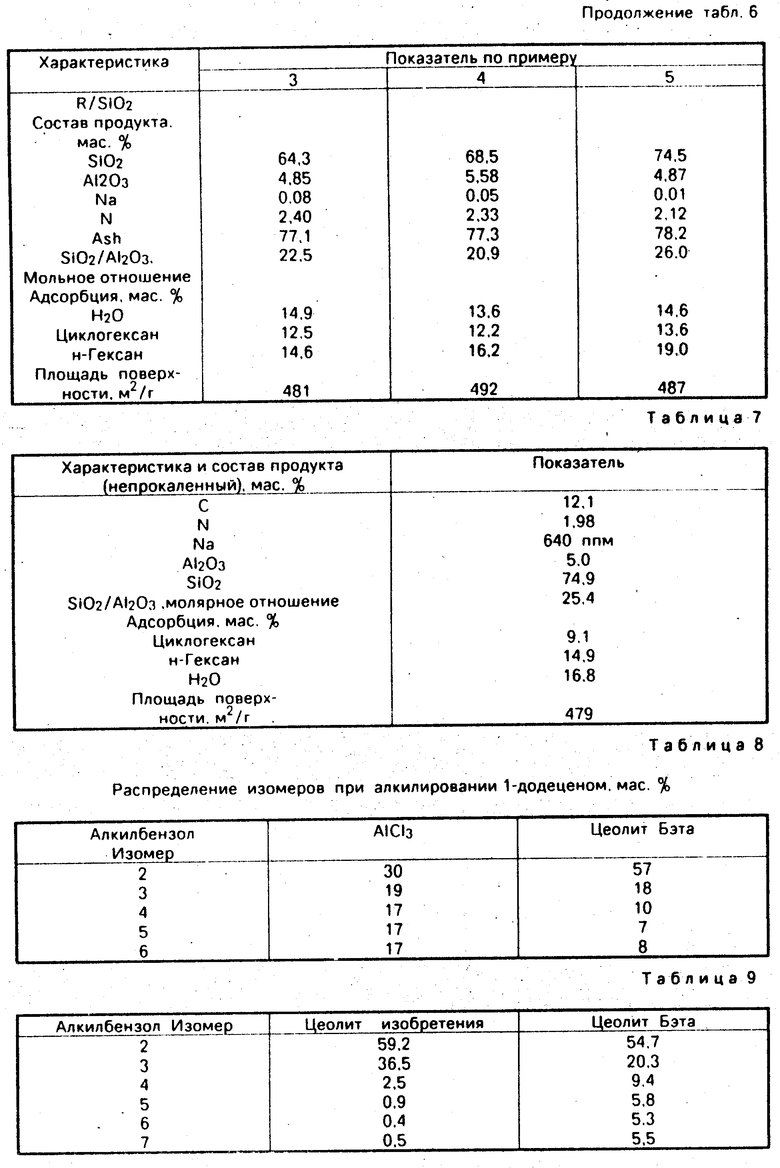
Примеры 3-5. Получают три раздельные синтетические реакционные смеси с составами/ указанными в таблице 6. Смеси получают с алюминатом натрия/ гидроксидом натрия/ Ultrasil/ гексаметиленимином (R) и водой. Смеси выдерживают при 150/ 143 и 150°С соответственно в течение 7/8 и 6 дней соответственно в автоклавах из нержавеющей стали при аутогенном давлении. Твердые вещества отделяют от непрореагировавших компонентов фильтрацией и затем промывают водой с последующей сушкой при 120°С. Кристаллы продукта исследуют методом ренгеноструктурного анализа/ определяют сорбцию/ площадь поверхности и химически анализируют. Результаты сорбции/ площади поверхности и химического анализа представлены в табл.6 и картины рентгеновской дифракции представлены на фиг.2/3 и 4 соответственно. Измерения сорбции и площади поверхности проводили для прокаленного продукта.
Пример 6. Количества прокаленных (538°С в течение 3 ч) кристаллических силикатных продуктов примеров 3/4 и 5 испытывают в Альфа Тесте и находят/ что Альфа значения равны 227/ 180 и 187/ соответственно.
Пример 7. Чтобы продемонстрировать дальнейшее получение данного цеолита/ 4/49 ч. гексаметиленимина добавляют к раствору/ содержащему 1 ч/ алюмината натрия/ 1ч. 50 % NaOH раствора и 44/19 ч. воды. К объединенному раствору добавляют 8/54 ч. Ultrasil диоксида кремния. Смесь кристаллизуют при перемешивании при 145°С в течение 59 ч и полученный продукт промывают водой и сушат при 120°С.
Картина дифракции ренгеновских лучей кристаллов высушенного продукта представлена на фиг.5 и демонстрирует/ что продукт является кристаллическим материалом данного изобретения. Химический состав продукта/ площадь поверхности и результаты анализа адсорбции представлены в таблице 7.
Пример 8. 25 г твердого кристаллического продукта из примера 7 прокаливают в токе азота при 538°С в течение 5 ч. с последующей продувкой газом с 5 % содержанием кислорода (баланс N2) в течение последующих 16 ч при 538°С.
По 3 г образцов прокаленного материала подвергают ионному обмену с 100 мл 0/1N, TEABr/ и NaCl3(TEA - ТЭА - триэтаноломин; ТРА = ТФК - терефталевая кислота) раствором соответственно. Каждую процедуру выполняют при комнатной температуре в течение 24 ч и повторяют три раза. Продукты обмена собирают фильтрацией/ промывают водой от свободных галогенидов и сушат. Составы обменных образцов представлены ниже/ демонстрируя обменную емкость данного кристаллического силиката для различных ионов.
Обменные ионы/ ионный состав/ мас.% ТЕА ТРА La
Na 0,095 0,089 0,063
N 0,30 0,38 0,03
C 2,89 3,63 -
La - - 1,04
Пример 9. La-обменный образец из примера 8 просеивают через сита от 14 до 25 меш и затем прокаливают на воздухе при 538°С в течение 3 ч. Прокаленный материал имеет Альфа значение 173.
Пример 10. Прокаленный материал Lа-обменного образца из примера 9 обрабатывают водяным паром при 649°С в 100 % паре в течение 2 ч. Отпаренный образец имеет Альфа значение 22/ что демонстрирует/ что цеолит имеет очень хорошую стабильность при жесткой гидротермической обработке.
Пример 11. Этот пример иллюстрирует приготовление данного цеолита/ где Х в общей формуле/ supra/ есть бор. Борную кислоту/ 2/59 ч. добавляют к раствору/ содержащему 1ч. 45 % КОН раствора и 42/96 ч. H2O. К этому добавляют 8/56 частей Ultrasil диоксида кремния/ и смесь тшательно гомогенизируют.Гексаметиленимин в количестве 3/88 ч. добавляют к смеси.
реакционная смесь имеет следующий состав в молярных отношениях:
SiO2/B2O3= 6.1 OH-/SiO2= 0.06
H2O/SiO2= 19.0
K/SiO2= 0.06
R/SiO2= 0.30 где R есть гексаметиленимин.
Смесь кристаллизуют в реакторе из нержавеющей стали/ при перемешивании при 150°С в течение 8 ч. Кристаллический продукт отфильтровывают/ промывают водой и сушат при 120°С. Часть продукта прокаливают в течение 6 ч при 540°С и устанавливают/ что он имеет следующие сорбционные емкости: H2O (12 торр) 11,7 % циклогексан (40 торр) 7/5 %
н-гексан (40 торр) 11/4 % Площадь поверхности прокаленного кристаллического материала/ как измерено (БЭТ)/ составляет 405 м2/г.
Химический состав непрокаленного вещества/ как определено/ является следующим:
N 1,94 мас.%
Na 175 ppm
K 0,60 мас.%
Бор 1/04 мас.%
Al2O3 920 ppm
SiO2 75,9 мас.%
Ash 74,11 мас.%
SiO2/Al2O3
молярное отношение = 1406
SiO2/(Al+B)2O3
молярное отношение = 25/8
Пример 12. Часть прокаленного кристаллического продукта примера 2 обрабатывают NH4Cl и снова прокаливают. Конечный кристаллический продукт испытывают в Альфа Тесте и находят/ что Альфа значение равно 1.
Пример 13. Этот пример иллюстрирует другое получение цеолита/ в котором Х в общей формуле/ ранее/ является бором/ 2/23 ч. борной кислоты добавляют к раствору одной части 50 % NaOH раствора и 73/89 ч. H2O. К этому раствору добавляют 15/29 ч. HiSiI диоксида кремния с последующим добавлением 6/69 ч. гексаметиленимина. Реакционная смесь имеет следующий состав вмольных отношениях:
SiO2/B2O3= 12.3 OH-/SiO2= 0.056
H2O/SiO2= 18.6
K/SiO2= 0.056
R/SiO2= 0.30 где R является гексаметиленимин.
Смесь кристаллизуют в реакторе из нержавеющей стали/ при перемешивании/ при 300°С в течение 9 дней. Кристаллический продукт отфильтровывают/ промывают водой и сушат при 120°С. Измеряют сорбционные емкости прокаленного вещества (6 ч при 540°С): H2O (12 торр) 14,4 мас.% циклогексан (40 торр) 4/6 мас.%
н-гексан (40 торр) 14/0 мас.% Площадь поверхности прокаленного кристаллического вещества/ как измерено составляет 438 м2/г.
Химический состав непрокаленного вещества/ как определено/ является следующим:
Компонент/ мас.% N 2,48 Na 0/06
Бор 0/83
Al2O3 0/50
SiO2 73,4
SiO2/Al2O3/
молярное отношение = 249
SiO2/(Al+B)2O3,
молярное отношение = 28.2
Пример 14. Часть прокаленного кристаллического продукта примера 13 испытывают в Альфа Тесте и находят/ что значение Альфа равно 5.
Пример 15. Сравнительные опыты по старению катализатора для алкилирования бензола пропиленом выполянют предложенным способом с цеолитом и с ZSM-12 при объемной скорости бензола WHSY 17 ч-1/ мольном отношении бензола к пропилену 3 кI/ и 2170 кПа (300 фунт/дюйм2изб).
Цеолит готовят добавлением 4/49 ч. гексаметиленимина к смеси/ содержащей 1/00 ч. алюмината натрия/ 1.00 ч 50 % NaOH, 8,54 ч. Ultrasil YN3 и 44.19 частей дионизованной H2O. Реакционную смесь нагревают до 143°С (290°F) и перемешивают в автоклаве при этой температуре во время кристаллизации. После достижение полной кристаллизации большую часть гексаметиленимина удаляют из автоклава контролируемой дистилляцией и кристаллы цеолита отделяют от оставшейся жидкости фильтрацией/ промывают дионизированной водой и сушат.
Часть кристаллов цеолита объединяют с Al2O3 с образованием смеси состоящей из 65 ч по массе цеолита и 35 ч. Al2O3. Добавляют воду к этой смеси/ чтобы позволить полученному катализатору сформироваться в экструдаты. Катализатор активируют прокаливанием в атмосфере азота при 540°С (1000°F) с последующим обменом водным раствором нитрата аммония и прокаливанием на воздухе при 540°С (1000°F).
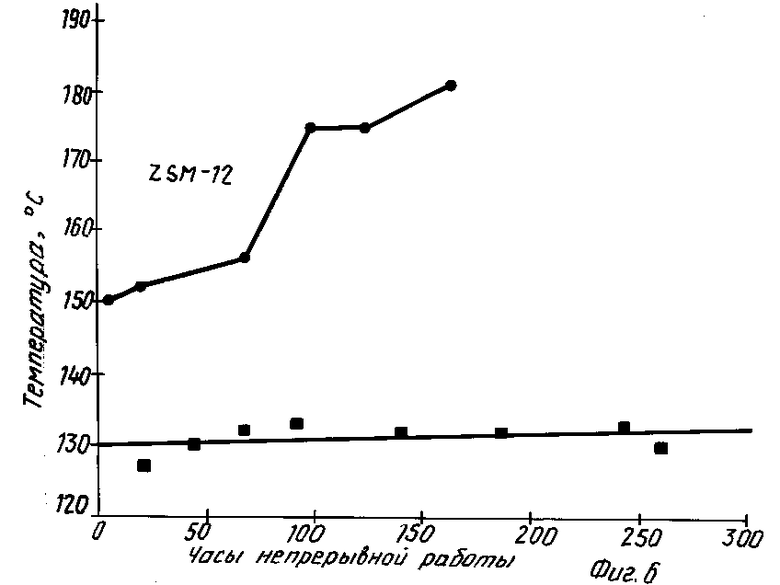
Фиг. 6 показывает температуру/ требуемую для поддержания полноты конверсии пропилена. При 130°С данный цеолит не стареет в течение 270-часовой непрерывной работы в изотермических условиях проведения реакции.
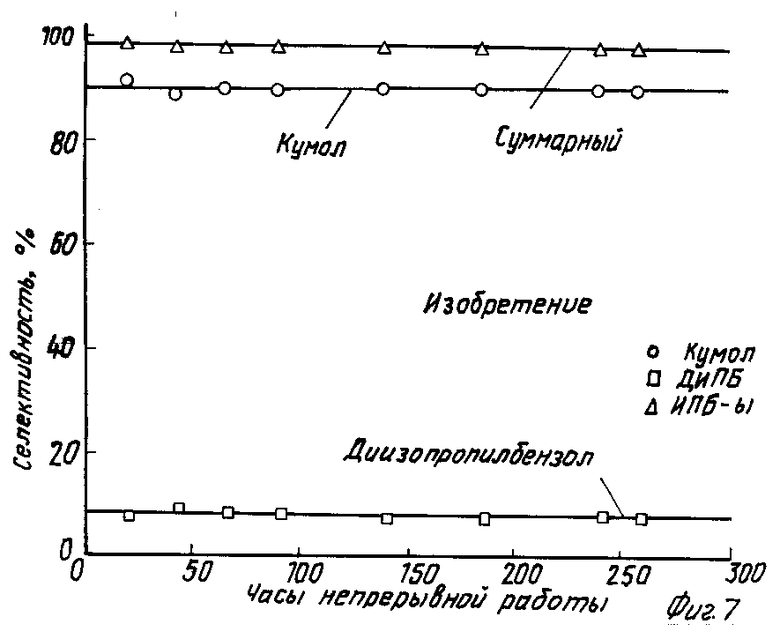
Селективность по изопропилбензолам (ИПБ-ов) для цеолита и для ZSM-12 показана на фиг. 7 и 8/ соответственно. Используя данный цеолит/ общая селективность по ИПБ составляет приблизительно 100 % по сравнению с 90 % в случае использования ZSM-12 в условиях полной конверсии пропилена. Эти данные хроматографии указывают на то/ что пропилен олигомеризуется на ZSM-12/ приводя к более низкой селективности по ИПБ.
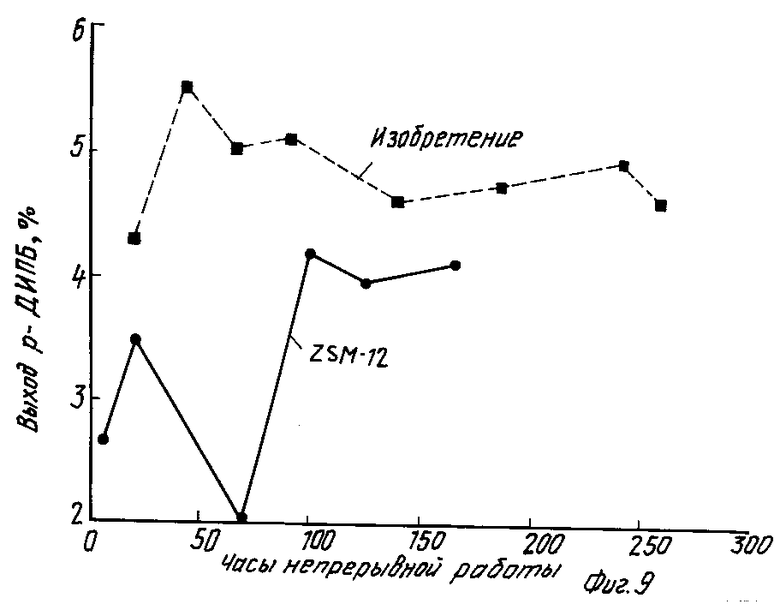
Данные представленные на фиг.9 показывают/ что цеолит является более активным для образования диизопропилбензолов (ДИПБ-ов)/ чем ZSM-12. Таким образом/ при алкилировании бензола пропиленом/ 10 % продуктов на данном цеолите представляют собой ДИПБ/ главным образом/ мета- и пара-изомеры. Фиг. 9 показывает/ что выход пара-ДИПБ выше в случае данного цеолита (Около 5 мас.% от общего углеводородного продукта)/ чем в случае ZSM-12 (около 4 % ) ДИПБ являются промежуточными продуктами для получения дигидроксибензолов/ таких как гидрохинон (п-) и резорцин (м-)/ каждый из которых имеет важное промышленное использование.
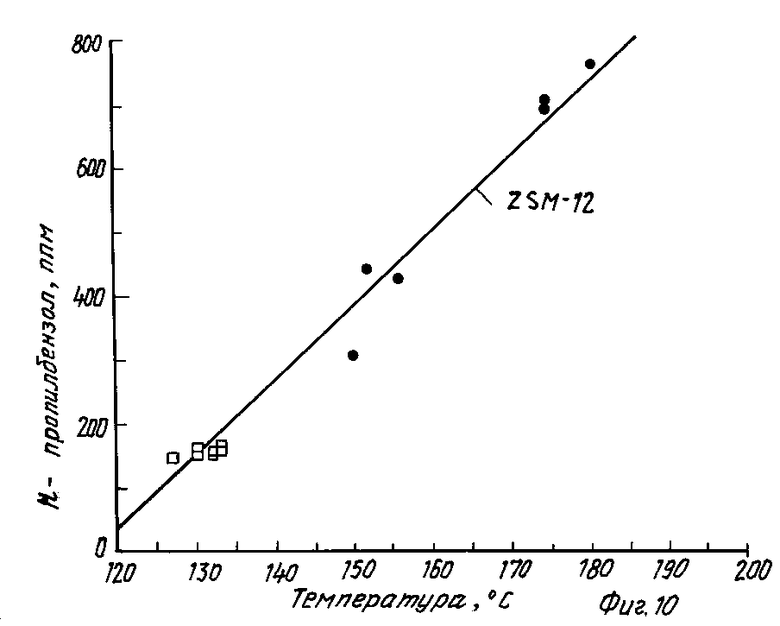
Фиг. 10 показывает/ как меняется отношение н-пропилбензола к кумолу в реакционных продуктах в присутствии ZSM-12 и данного цеолита в зависимости от температуры реакции/ В течение 270 ч реакции в присутствии данного цеолита отношение н-пропилбензола к кумолу остается приблизительно постоянным при 160 ppm. Это сравнимо с уровнем 700 ppm для ZSM-12 при том же самом условии 98% + конверсс пропилена/ но при более высокой температуре.
Пример 16. Этот пример иллюстрирует алкилирование кумола пропиленом в присутствии данного цеолита с получением диизопропилбензолов (ДИПБ-ов). Условия реакции алкилирования являются следующими: 2170 кПа (300 фунт/дюйм2изб. )/ 150°С и 1:1 молярное отношение кумола к пропилену. Достигается 81 % превращения кумола в алкилат. ДИПБ включают 84 % этого алкилированного продукта/ причем оставшаяся часть представляет собой триизопропилбензол (ТИПБ). ДИПБ представляют собой пара-(65 %)/ мета-(34%) и орто (1% ).
Пример 17. Этот пример демонстрирует алкилирование фенола альфа -С14 олефином в присутствии данного цеолита с получением смеси алкилированных фенолов. Алкилирование проводят в 1-литровом автоклаве/ используя 400 г (2.02 моля) олефина/ 95 г (1.01 моля) фенола и 38 г катализатора/ 65 мас. % МСМ-22/35 мас. % Al2O3 связующее. Время реакции составляет 6 ч при 177°С (350°F) при 2860 кПа (400 фунт/дюйм2) азота.
Анализ продукта указывает на присутствие моно-/ди- и тритетрадецилфенолов.
Пример 18. Этот пример показывает алкилирование бензола 1-додеценом/ используя каждый из двух известных катализаторов алкилирования/ а именно/ кислота Льюиса AlCl3 и цеолит Бэта/ раскрытый в Пат.США N 4301316. Распределение изомеров представлено в табл.8 следующим образом:
Состав смеси додецилбензолов до некоторой степени зависит от используемого кислотного катализатора. Как указано/ серная кислота приводит к 41 мас. % додецилбензола/ в то время как в случае HF получают только 20 мас.%. Подобные результаты могут быть показаны для других случаев алкилирования/ включая относительно длинные/ т.е. С6+, алкилирующие агенты.
Пример 19. Этот пример показывает алкилирование бензола альфа- С14 олефином (Shell's Neodene - 14) на цеолите (полученному согласно примеру 15) и отдельно на цеолите Бэта. Алкилирование проводят в 1-литровом автоклаве/ используя 400 г (2/02 моля) олефина/ 79 г (1/01 моля)бензола и 38 г катализатора. Время реакции составляет 6 ч при 204°C (400°F) при 2860 кПа (400 фунт/дюйм2) азота. Распределение изомеров представлено в табл.9:
Распределение изомеров при алкилировании/ мас. %
Данные примеров 18 и 19 показывают/ что использование цеолита в соответствии с данным изобретением в качестве катализатора алкилирования приводит к значительно более высокому процентному содержанию 2- и 3-алкил изомеров алкилированного продукта/ чем в случае известных катализаторов алкилирования кислоты Льюиса или цеолита Бэта в идентичных или аналогичных условиях.
Алкилированные продукты/ обладающие алькильными боковыми цепями с приблизительно от 8 до 16 углеродными атомами/ особенно полезны в качестве интермедиатов для производства синтетических детергентов - линейных алкилбензолсульфонатов.
Пример 20. Два различных цеолитных катализатора/ цеолит (по изобретению)/ полученный согласно примеру 15/ и цеолит Бэта/ используют в раздельных опытах алкилирования/ А и В/ проводимых/ в основном в индентичных условиях с получением основного маслянистого сырья. Композиция каждого катализатора содержит 65 % цеолита/ связанного с 35 мас.% оксида алюминия.
Реакцию алкилирования для каждого опыта проводят в 1-литровом автоклаве/ используя 400 г (2/02 моля) альфа -С14 олефина (Shell Neodene- 14)/ 79 г (1/01 моля) бензола (5:1 молярное отношение бензола к олефину) с 38 г катализатора при 204°С (400°F) в течение 6 ч при давлении азота 2860 кПа (400 фунт/дюйм2).
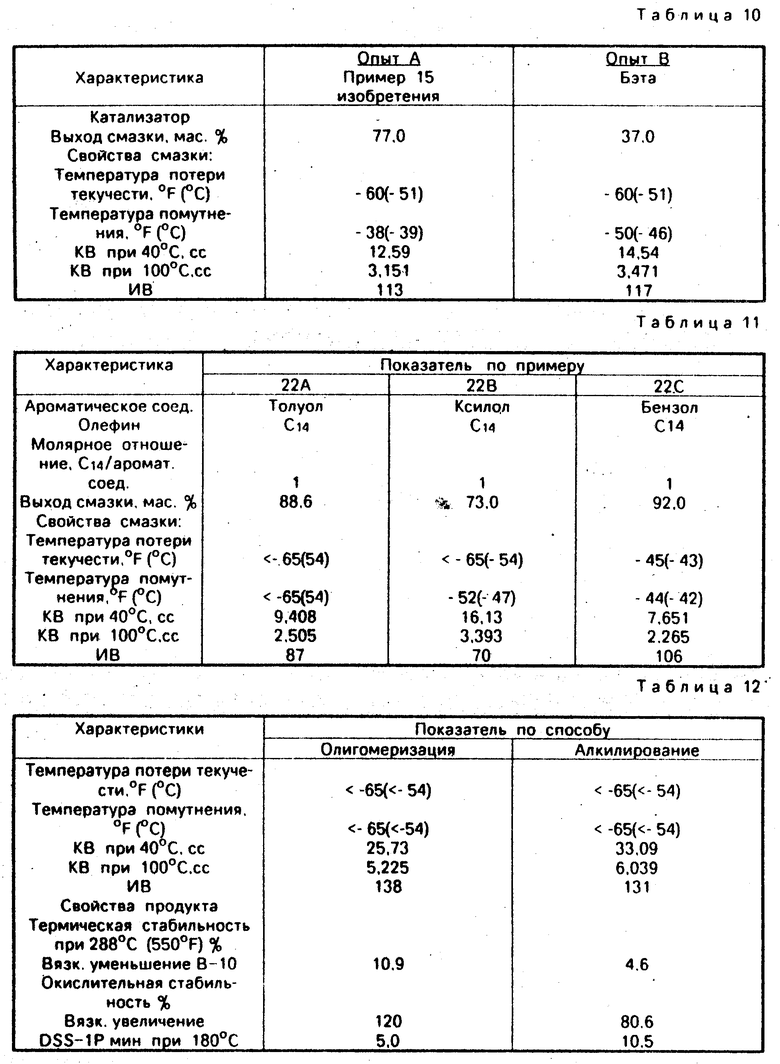
Табл. 10 представляет выход и свойства продуктов/ получающихся при алкилировании/ проводимых в присутствии с каждым из приведенных цеолитов.
Газохроматографический анализ и ионизационный масс-спектрометрический анализ с полевой эмиссией указывают/ что синтетическая смазка/ полученная в присутствии катализатора по изобретению/ содержит смесь моно- и диалкил бензольных соединений/ 67 и 33 мас.%/ соответственно. Другой катализатор/ т. е. цеолит Бэта промотирует не только алкилирование с образованием моно- и диалкил бензолов/ то также С14 олигомеризацию с образованием С28 олефинов. В дополнение к показанной (проявлению) уникальной селективности при алкилировании/ катализатор по изобретению является значительно более активным и продуцирует основной маслянистый продукт алкилированного бензола с очень низкой температурой потери текучести и низкой температурой помутнения по сравнению с продуктами/ полученными в присутствии цеолита Бэта.
Пример 21. Этот пример сравнивает активность катализатора по изобретению с активностью цеолита Бэта при алкилировании нафталина альфа С14 олефином. Реакцию осуществляют в условиях способа/ аналогичных условиям примера 20/ используя 0/5:1 молярное отношение альфа-олефина к нафталину/ Выход маслянистого продукта/ алкилированного нафталина составляет около 94 мас.% и преимущественно содержат смесь моно-/ ди- и триалкил нафталины и имеют следующие свойства:
Катализатор Цеолит по изобретению
Выход смазки/ мас.% 94
Свойства смазки:
Температура потери текучести.
°F(°C) < -65(<-54)
КВ при 40°С/ сс 37/27
КВ при 100°С/ сс 5,894
ИВ 100
Пример 22. Это пример также иллюстрирует превосходящую активность и селективность данного цеолитного катализатора для алкилирования альфа С14 олефина другими ароматическими соединениями/ такими как толуол (пример 22А) и ксилол (пример 22В) по сравнению с бензолом (пример 22 С) в аналогичных условиях способа (табл.11):
Пример 23. Этот пример иллюстрирует способ алкилирования в соответствии с данным изобретением/ который использует сырьевую смазку/ полученную при олигомеризации 1 -децена/ использующей пропанолпромотируемый BF3 катализатор. Используемый катализатор представляет собой цеолит/ полученный/ как в примере 15/ исключая соединение со связующим Al2O3 и превращение в водородную форму.
1-Децен/ BF3 и пропанол вводят в реактор для олигомеризации 1-децена/ Продукт олигомеризации промывают сначала гидроксидом натрия и затем водой до отделения легких продуктов оттуда в вакуумной дистиляционной установке/ 250 г олигомеров 1-децена/ содержащих 33 мас.% С30 олефина/ 52 мас.% С40 олефина и 15 мас.% С50 олефина/ затем используют для алкилирования 78 г бензола/ используя 22 г цеолита изобретения в качестве катализатора. Реакцию проводят при 2860 кПа (400 фунт/дюйм2) азота и 204°С (400°F) в течение 6 ч.
После декантации катализатора и отгонки непрореагировавшего бензола/ выход смазки составляет 88 мас. %/ указывая на то/ что 12 мас.% бензола проалкировано и включено в структуру основной цепи олигомеров децена. Это в дальнейшем подтверждается анализом инфракрасной спектроскопии. Свойства олигомеров до и после алкилирования бензола представлены следующим образом (Таблица 12):
Результаты указывают/ что стадия алкилирования дает бензолсодержащий синтетический компонент смазки с превосходными свойствами продукта/ такими как очень низкие температуры потери текучести и помутнения/ высокий коэффициент вязкости наряду с улучшенными характеристиками растворяющей способности присадки/ также как и повышенной термической и окислительной стабильностью.
Пример 24. Этот пример иллюстрирует способ алкилирования/ проводимый с олигомерным продуктом 1-децена/ полученным в присутствии Cr/SiO2 катализатора.
Таким образом/ 1-децен и Cr/SiO2 вводят в реактор для олигомеризации/ причем продукт оттуда удаляют вакуумом/ после чего его вводят в реактор для алкилирования вместе с бензолом.
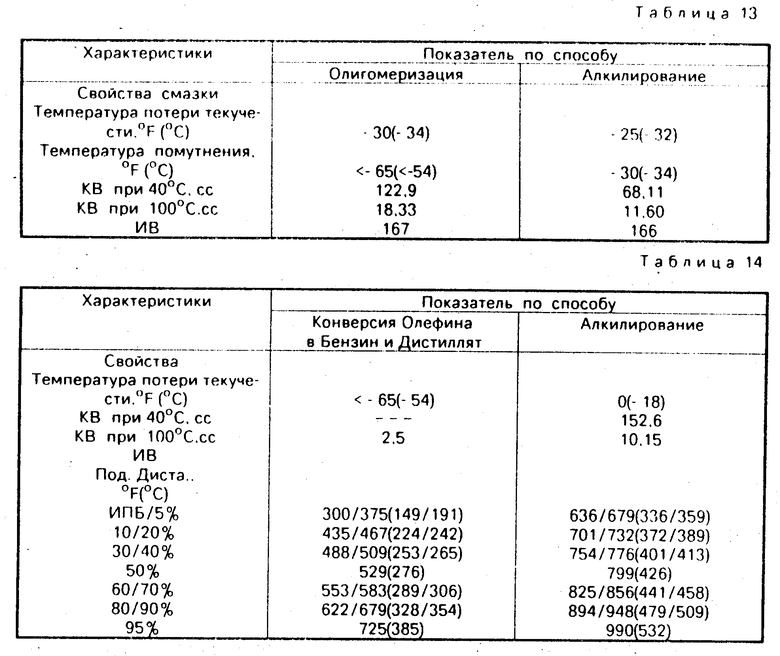
Реакцию алкилирования осуществляют в условиях способа/ идентичных условиям в примере 23/ но используя 500 г единомеров децена и 95 г бензола с 36 г цеолита (по изобретению) в качестве катализатора. Свойства олигомеров децена до и после алкилирования бензола представлены следующим образом (табл. 13):
Пример 25. До известной степени аналогично примеру 23/ 400 г 200-371°С (400-700°С) дистиллята (78 мас.%)/ полученного олигомеризацией легких олефинов на ZSM-5/ алкилируют с 115 г нафталина (12 мас.%) на катализаторе изобретения. Выход полученной 370°С+(700°F+) смазки составляет 54 мас.%. Таблица 14 иллюстрирует свойства базового компонента смазки алкилированного нафталина.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ КАТАЛИТИЧЕСКОЙ КОНВЕРСИИ УГЛЕВОДОРОДНОГО СЫРЬЯ, ВКЛЮЧАЮЩЕГО ПО КРАЙНЕЙ МЕРЕ ОДНО АРОМАТИЧЕСКОЕ СОЕДИНЕНИЕ, СОДЕРЖАЩЕЕ ПО КРАЙНЕЙ МЕРЕ 9 АТОМОВ УГЛЕРОДА, В ПРОДУКТ, СОДЕРЖАЩИЙ C-C-АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ | 1991 |
|
RU2011650C1 |
| СПОСОБ АЛКИЛИРОВАНИЯ ИЗОПАРАФИНА ОЛЕФИНОМ | 1991 |
|
RU2031900C1 |
| СИНТЕТИЧЕСКИЙ СЛОИСТЫЙ МАТЕРИАЛ МСМ-56, ЕГО ПОЛУЧЕНИЕ И ИСПОЛЬЗОВАНИЕ | 1994 |
|
RU2140962C1 |
| ФОРМОСЕЛЕКТИВНЫЙ ЦЕОЛИТОВЫЙ КАТАЛИЗАТОР И СПОСОБ КОНВЕРСИИ АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ | 1996 |
|
RU2163506C2 |
| СИНТЕЗ ЦЕОЛИТОВ ZSM-5 И ZSM-11 | 2000 |
|
RU2243156C2 |
| СПОСОБ ГИДРООБЕССЕРИВАНИЯ И СПОСОБ ПОВЫШЕНИЯ КАЧЕСТВА УГЛЕВОДОРОДНОГО СЫРЬЯ | 1998 |
|
RU2186831C2 |
| СПОСОБ КОНВЕРТИРОВАНИЯ АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ | 1996 |
|
RU2148573C1 |
| Способ получения ароматических углеводородов | 1975 |
|
SU1091850A3 |
| УЛУЧШЕННЫЙ СПОСОБ ЖИДКОФАЗНОГО АЛКИЛИРОВАНИЯ | 2012 |
|
RU2602160C2 |
| СПОСОБ ПОВЫШЕНИЯ КАЧЕСТВА СЕРОСОДЕРЖАЩЕЙ ФРАКЦИИ СЫРЬЯ (ВАРИАНТЫ) | 1998 |
|
RU2186830C2 |


Сущность изобретения: алкилирование ароматического соединения включает его контактирование с алкилирующим агентом в присутствии катализатора-синтетического пористого кристаллического цеолита, имеющего следующую дифракцию рентгеновских лучей: межплоскостные расстояния 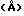 1/12,36+-0,4; 2/11,03+-0,02; 3/8,83+-0,14; 4/ 6,18+-0,12; 5/ 6,0+-0,10; 6/ 4,06+-0,07; 7/ 3,91 +-0,07; 8/ 3,42+-0,06. Относительная интенсивность, 1/1 100 1/С - 0, 2/ С - С, 3/С - 0, 4/ С- 0, 5/ С - С, 6/ С-С, 7/ С- 0, 8/0. Цеолит содержит X2O3 и YO2 в молярном соотношении (10 - 30) : 1, где X - алюминий, бор, железо и/или галлий; Y-кремний и/или германий. Процесс ведут при 0 - 500°С и давлении 0,2 - 250 атм и молярном отношении алкилируемого ароматического соединения к алкилирующему агенту от 0,1 : 1 до 50 : 1. 2 з.п. ф-лы, 14 табл., 10 ил.
1/12,36+-0,4; 2/11,03+-0,02; 3/8,83+-0,14; 4/ 6,18+-0,12; 5/ 6,0+-0,10; 6/ 4,06+-0,07; 7/ 3,91 +-0,07; 8/ 3,42+-0,06. Относительная интенсивность, 1/1 100 1/С - 0, 2/ С - С, 3/С - 0, 4/ С- 0, 5/ С - С, 6/ С-С, 7/ С- 0, 8/0. Цеолит содержит X2O3 и YO2 в молярном соотношении (10 - 30) : 1, где X - алюминий, бор, железо и/или галлий; Y-кремний и/или германий. Процесс ведут при 0 - 500°С и давлении 0,2 - 250 атм и молярном отношении алкилируемого ароматического соединения к алкилирующему агенту от 0,1 : 1 до 50 : 1. 2 з.п. ф-лы, 14 табл., 10 ил.
Межплоскостные расстояния d(А) Относительная интенсивность, I/I0 · 100
12,36 ± 0,4 Ср - Ос
11,03 ± 0,2 Ср - С
8,83 ± 0,14 Ср - Ос
6,18 ± 0,12 Ср - Ос
6,00 ± 0,10 Сл - Ср
4,06 ± 0,07 Сл - С
3,91 ± 0,07 Ср - Ос
3,42 ± 0,06 Ос
2. Способ по п.1, отличающийся тем, что используют цеолит, содержащий X2O3 и YO2 в молярном соотношении 10 - 30 : 1, где X - алюминий, бор, железо и/или галлий, Y - кремний и/или германий.
Авторы
Даты
1994-06-15—Публикация
1991-09-24—Подача