Изобретение относится к химическим средствам борьбы с насекомыми на основе производных 2-арилпропилового эфира.
Известна инсектицидная композиция, содержащая в качестве активного ингредиента соединение формулы
Cl- 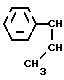 -
- -O-CH
-O-CH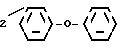 растворитель и диспергатор. Однако она недостаточно активна.
растворитель и диспергатор. Однако она недостаточно активна.
Целью изобретения является усиление инсектицидной активности композиции на основе 2-арилпропилового эфира.
Нижеследующие примеры иллюстрируют арсенал активных веществ используемых в композиции, способ их получения примеры приготовления композиций и их биологическое действие.
Пример синтеза 1 (А способ этерификации).
Полученные 3-(4-метоксифенокси)бензил-2-(4-метилфенил)- 2-метилпропилового эфира.
К 20 мл сухого ацетонитрила добавляют 0,90 г гидрида натрия (60% в масле) и к смеси по каплям добавляют раствор 2,5 г 2-(4-метилфенил)-2-метилпропилового спирта в 10 мл ацетонитрила при 50оС.
Эту смесь кипятят с обратным холодильником в течение 30 мин и к реакционной смеси в течение 10 мин по каплям добавляют раствор 5,3 г 3-(4-метоксифенокси)бензилбромида. Смесь дополнительно кипятят с обратным холодильником в течение 1 ч, смесь охлаждают до комнатной температуры, выливают ее в воду и экстрагируют смесь толуолом. Толуольный экстракт промывают насыщенным водным раствором хлористого натрия и высушивают над сульфатом натрия, выпаривают при пониженном давлении и полученный неочищенный эфир очищают на хроматографической колонке со 150 г силикагеля (в качестве элюента применяют смешанный растворитель (1: 1) из толуола и н-гексана), получая 3,4 г целевого эфира (выход 50% из теории).
nD20 1,5750; Dмакс см-1 (в пленке): 1590, 1510, 1490, 1345, 1215, 1105, 1040, 815.
δССl4 млн. д. : 1,30 (с, 6Н), 2,28 (с, 3Н), 3,35 (с. 2Н), 3,75 (с, 3Н), 4,38 (с, 2Н), 6,7-7,3 (м, 12Н) [C-синглет, М-мультиплет] .
Данные элементного анализа для С25Н28O3:
Вычислено, % : С 79,75, Н 7,50.
Найдено, % : С 79,99, Н 7,48.
Пример синтеза 2 (Б способ этерификации).
Полученные 3-(4-фторфенокси)бензил-2-(3,4-дихлорфенил)-2-метилпропилового эфира.
К 20 мл толуола добавляют 0,63 г гидрида натрия (60% в масле) и смесь кипятят с обратным холодильником, к этой смеси в течение 15 мин по каплям добавляют раствор 2,3 г 2-(3,4-дихлорфенил)-2-метил- пропилового спирта в 10 мл 25% диметилформамида в толуоле. Смесь перемешивают в течение 15 мин и добавляют к ней в течение 20 мин по каплям раствор 3,5 г бромистого 3-(4-фторфенокси)бензила в 10 мл толуола. Затем смесь кипятят в течение 1 ч с обратным холодильником и охлаждают до комнатной температуры, выливают воду. Органический слой отделяют, промывают водой, высушивают над сульфатом натрия и выпаривают при пониженном давлении, полученный неочищенный эфир очищают на хроматографической колонке со 100 г силикагеля (в качестве элюента применяют смешанный растворитель (1: 1) из толуола и н-гексана), получают 3,1 г целевого эфира (выход составил 74% от теории).
nD20 1,5732; Dмакс см-1 (в пленке), 1590, 1505, 1490, 1265, 1205, 1100, 1035, 695. δCCl4, м. д. : 1,30, (с, 6Н), 3,34 (с, 2Н), 4,38 (с, 2Н), 5,7-7,4 (м, 11Н).
Данные элементного анализа для С23Н21Сl2FO2,
Вычислено, % : С 69,09, Н 5,29, Сl 8,87, F 4,75.
Найдено, % : С 68,88, Н 5,34, Сl 8,75, F 4,57.
Пример синтеза 3 (В способ этирификации).
Получение 3-(4-метилфенокси)бензил-2-(4-хлорфенил)-2-метилпропилового эфира.
К 15 г 50% -ного водного раствора NaOH добавляют 6,0 г 2-(4-хлорфенил)-3-метилпропилового спирта, 8,1 г 3-(4-метилфенокси)-бензилхлорида и 1,1 г бромистого тетрабутиламмония, и смесь перемешивают 1 ч при 80оС. Смесь охлаждают до комнатной температуры и добавляют воду, смесь экстрагируют толуолом, толуоловый экстракт промывают водой и высушивают над сульфатом натрия, выпаривают при пониженном давлении, полученный неочищенный эфир очищают на хроматографической колонке с 250 г силикагеля (в качестве элюента используют смешанный растворитель (1: 1) толуол: н-гексан), получая 9,9 г целевого эфира (выход составляет 80% от теоретического).
n D20 1,5741, Dмакс, см-1 (в плане): 1595, 1510, 1455, 1260, 1215, 1110, 1015, 830, 695.
δCCl4, м. д. , 1,29 (с. 6Н), 2,31 (с, 3Н), 3,32 (с. 2Н), 4,35 (с, 2Н), 6,7-7,3 (м, 12Н).
Данные элементного анализа для С24Н25Сl02,
Вычислено, % : С 75,68, Н 6,61, Сl 9,31.
Найдено, % : С 75,86е, Н 6,42, Сl 9,22.
Пример синтеза 4 (Г способ этерификации).
Получение 3-(4-фторфенокси)бензил-2-(4-фторфенил)-2-метилбутилового эфира.
К 20 мл толуола добавляют 2 мл концентрированной серной кислоты, 2,7 г 3-(4-фторфенокси)бензилового спирта и 2,3 г 2-(4-фторфенил)-2-метилбутилового спирта, и смесь кипятят в течение 6 ч с обратным холодильником (образовавшуюся в реакции воду удаляют). Смесь охлаждают до комнатной температуры и к смеси добавляют воду, отделяют толуольный слой, промывают водой, высушивают и выпаривают при пониженном давлении, полученный неочищенный эфир очищают на хроматографической колонке со 100 г силикагеля (в качестве элюента используют смешанный растворитель (1: 1) - толуол: н-гексан), получая 2,2 г целевого эфира (выход составляет 46% от теоретического).
nD20 1,5478.
Dмакс, см-1 (в пленке): 1585, 1505, 1230, 1950 1165, 110, 830, 780, 690.
δCCl4, м. д. : 0,65, [T-триплет] J = 7,5 Гц, 3Н), 1,28 (с, 3Н), 1,5-1,9 (м. 2Н), 3,37 (с, 2Н), 4,35 (с, 2Н). 6,7-7,3 (м, 12Н).
Элементный анализ для С24Н24F2O2:
Вычислено, % : С 75,37 Н 6,32, F 9,94.
Найдено, % : С 75,54, Н 6,21, F 10,01.
Пример синтеза 5 (D способ этерификации).
Получение 3-феноксибензил-2-(4-дифторметоксифенил)-2-метилпропилового эфира.
Перемешивают при 50оС в течение 2 ч 2,0 г 2,4-дифторметоксифенил-2-метилпропилового спирта, 2,0 г м-феноксибензилхлорида, 20 г 50% -ного NaOH и 0,3 г триэтилбензил аммоний бромида. Затем в реакционную смесь добавляют воду и бензол, смесь тщательно перемешивают, бензольный слой отделяют, промывают водой, сушат над сульфатом натрия и выпаривают при пониженном давлении, и полученный неочищенный эфир очищают на хроматографической колонке со 130 г силикагеля (в качестве элюента используют смешанный растворитель (2: 3)-толуол-гексан), получая 3,0 г целевого эфира (выход составляет 81% от теоретического).
n D20,5 1,5490.
Dмакс см-1 (пленка): 1590, 1485, 1380, 1250, 1215, 1130, 1040, 690.
δCCl4, м. д. : 1,32 (с, 6Н), 3,36 (с, 2Н), 4,21 (с, 2Н), 6,38 (с, 1Н), J = 7,5 Гц), 6,8-7,4 (м, 13Н).
Пример синтеза 6.
Получение 3-(4-бромфенокси)бензил-2-(4-фторфенил)-2-этилпропилового эфира.
К 20 мл толуола добавляют 0,60 г гидрида натрия (60% в масле) и смесь кипятят с обратным холодильником, к этой смеси в течение 20 мин по каплям добавляют раствор 2,0 г 2-(4-фторфенил)-2-метилбутилового спирта в 10 мл 40% диметилформамида в толуоле. Смесь перемешивают в течение 10 мин и добавляют к смеси по каплям в течение 10 мин раствор 4,0 г 3-(4-фромфенокси)-бензилбромида и 10 мл толуола. Смесь дополнительно нагревают и кипятят с обратным холодильником в течение 1 ч, охлаждают до комнатной температуры и выливают в воду. Отделяют толуольный слой, промывают водой, высушивают над сульфатом натрия, выпаривают при пониженном давлении и полученный сырой эфир очищают на хроматографической колонке со 100 г силикагеля (в качестве элюента используют смешанный растворитель (1: 1) толуол-гексан), получая 3,7 г целевого эфира.
nD20,2 1,5778.
Dмакс, см-1 (пленка), 1605, 1580, 1510, 1485, 1250, 1165, 1100, 1070, 1010, 830.
δCCl4, м. д. , 0,67 (т. 3Н, J= 7,2 Гц), 1,30 (с. 3Н), 1,5-1,9 (м, 2Н), 3,39 (с, 2Н), 4,39 (с, 2Н), 6,7-7,5 (м, 12Н).
Пример синтеза 7.
3-феноксибензил 2-(3,4-метилендиоксифенил)-2-метилпропиловый эфир синтезируют по методике, описанной в примере синтеза 2, применяя 0,4 г 2-(3,4-метилендиоксифенил)-2-метилпропиловый спирт.
nD20,7 1,5839.
Dмакс, см-1 (пленка): 1590, 1490, 1255, 1105, 1045, 940, δССl4, м. д. 1,28 (с, 6Н), 3,32 (с, 2Н), 4,41 (с, 2Н), 5,82 (с, 2Н), 6,5-7,4 (м, 12Н).
Пример синтеза 8 (Е способ этирификации).
Получение 3-(4-метоксифенокси)бензил-2-(3,4-дихлорфенил)-2-метилпропилово- го эфира.
Смесь 9,98 г хлористого 3,4-дихлорнеофила, 9,67 г 4-метоксифеноксибензилового спирта, 3,9 г 45% гидроокиси натрия и 48 г диметилсульфоксида нагревают и перемешивают при 140оС в течение 3 ч, дополнительно добавляют 1,8 г 45% гидроокиси натрия, выдерживают при той же температуре в течение 4 ч, выливают в воду и экстрагируют бензолом. Бензольный экстракт промывают водой, высушивают над сульфатом натрия, выпаривают при пониженном давлении и полученный сырой эфир очищают на хроматографической колонке с 250 г силикагеля (в качестве элюента применяют смешанный растворитель (1: 1) толуол: н-гексан), получая 3,34 г целевого эфира (выход составляет 78% от теоретического, в расчете на превращенный хлористый, 3,4-дихлорнеофил).
nD20 1,5830.
Dмакс, см-1 (пленка): 1590, 1510, 1490, 1250, 1220, 1110, 1040, 840.
δCCl4, м. д. : 1,30 (с. 6Н), 3,34 (с, 2Н), 3,76 (с, 3Н), 4,38 (с, 2Н), 6,6-7,5 (м, 11Н).
Пример синтеза 9.
Получение 3-феноксибензил-2-(4-фтормилфенил)-2-метилпропилового эфира.
К 30 мл сухого диэтилового эфира добавляют 0,70 г литий-алюминий гидрида и к этой смеси по каплям добавляют за 15 мин при 0оС 1,63 г этилацетата. Смесь выдерживают в течение 30 мин при 0оС. Затем к этой смеси по каплям добавляют раствор 6,0 г 3-феноксибензил 2-(4-цианофенил)-2-метилпропилового эфира в 10 мл сухого эфира, и полученную смесь перемешивают в течение 1 ч при 0оС. Затем к смеси добавляют 20 мл 4 н. серной кислоты, и образовавшуюся смесь перемешивают в течение 30 мин. Отделяют эфирный слой, промывают его водой, высушивают над сульфатом натрия и выпаривают. Затем 6,4 г остатка очищают на хроматографической колонке со 130 г силикагеля (в качестве элюента используют бензол) получают 2,9 г исходного 3-феноксибензил 2-(4-цианофенил)-2-метилпропилового эфира и 2,3 г целевого 3-феноксибензил-2-(4-фтормилфенил)-2-метилпропилового эфира.
nD20 1,5858
Dмакс, см-1 (пленка): 1720, 1615, 1590, 1500, 1260, 1225, 1105, 835, 700.
δCCl4 (от ТМС), м. д. : 1,37 (с, 6Н), 3,40 (с, 2Н), 4,37 (с, 2Н) 6,7-7,7 (м, 13Н), 9,82 (с, 1Н).
Пример синтеза 9.
3-феноксибензил 2-(4-этоксиметоксифенил)2-метилпропиловый эфир синтезирован по следующей методике.
1) В 20 мл влажного хлороформа растворяют 1,2 г 3-феноксибензил 2-(4-формилфенил)-2-метилпропилового эфира и 0,70 г м-хлорбензойной кислоты добавляют к раствору, смесь выдерживают 4 сут при комнатной температуре. Образовавшийся осадок удаляют фильтрацией, хлороформный слой промывают разбавленной щелочью, затем водой, высушивают над сульфатом натрия и выпаривают при пониженном давлении, получая 1,0 г целевого эфира. Затем 1,0 г эфира растворяют в 30 мл 5% -ного раствора КОН в метаноле и раствор нагревают в течение 3 ч при 50оС, чтобы вызвать гидролиз.
Метанол удаляется перегонкой при пониженном давлении, к остатку добавляют воду и бензол, значение рН смеси понижают ниже 4, добавляя концентрированную хлористоводородную кислоту, смесь перемешивают. Смесь еще выдерживают, отделяют бензольный слой, промывают водой, высушивают над сульфатом натрия и выпаривают при пониженном давлении, получая 0,90 г неочищенного эфира. Сырой эфир очищают на хроматографической колонке с 20 г силикагеля (в качестве элюента используют смешанный растворитель (20: 1) бензол-диэтиловый эфир), получая 0,60 г 3-феноксибензил 2-(4-оксифенил-2-метилпропилового эфира.
δCCl4 (от ТМС), м. д. : 1,26 (с. 6Н), 3,33 (с, 2Н), 4,34 (с, 2Н) 5,76 (с, 1Н), 6,4-7,4 (м, 13Н).
2) К 50 мл сухого тетрагидрофурана добавляют 1,0 г гидрида натрия (60% в масле) и затем к этой смеси при кипячении с обратным холодильником по каплям за 30 мин добавляют 5,0 г 3-феноксибензил 2-(4-оксифенил)-2-метилпропилового эфира в 15 мл сухого тетрагидрофурана. Смесь дополнительно кипятят в течение 10 мин и к смеси в течение 30 мин по каплям добавляют 5,0 мл этилхлорметилового эфира. Полученную смесь дополнительно кипятят с обратным холодильником в течение 10 мин, охлаждают до комнатной температуры, выливают в воду и экстрагируют бензолом. Бензольный экстракт промывают водой, высушивают над сульфатом натрия и выпаривают, получая маслянистый остаток, который после очистки на хроматографической колонке со 150 г силикагеля (в качестве элюента используют смешанный растворитель (20: 1) бензол и диэтиловый эфир, дает 5,0г 3-феноксибензил 2-(4-этоксиметоксифенил)-2-метилпропилового эфира.
nD20 1,5330.
νмакс, см-1 (пленка): 1580, 1510, 1485, 1230, 1225, 1215, 1105, 1080, 1005, 830, 685.
δССl4 (от ТМС), м. д. 1,20 (т. 3Н), J = 7,2 Гц), 1,30 (с, 6Н), 3,33 (с, 2Н), 3,65 (квадруплет К), 2Н, J = 7,2 Гц), 4,38 (с, 2Н), 5,08 (с, 2Н) 6,5-7,4 (м, 13Н).
Пример синтеза 11.
3-феноксибензил 2-(4-карбэтоксифенил)-2-метилпропиловый эфир синтезируют по следующей методике.
1) Смесь 3,5 г 3-феноксибензил 2-(4-цианофенил)-2-метилпропилового эфира, 7,0 г гидроокиси калия, 7,0 г воды и 20 мл этиленгликоля перемешивают при 130оС в течение 4 ч. Смесь охлаждают до комнатной температуры, добавляют в нее воду и подкисляют, добавляя хлористоводородную кислоту. Затем смесь экстрагируют эфиром, эфирный экстракт промывают водой, высушивают над сульфатом натрия и выпаривают, получая 3,1 г 3-феноксибензил-2-(карбоксифенил)-2-метилпропилового эфира, т. пл. 98,5 - 102, 5оС.
2) Смесь 1,0 г 3-феноксибензил-2-(4-карбоксифенил)-2-метилпропилового эфира, 0,6 г пятихлористого фосфора и 15 мл бензола нагревают при 70-80оС в течение 30 мин и растворитель удаляют перегонкой при пониженном давлении. Полученный неочищенный хлорангидрид кислоты растворяют в 10 мл бензола, этот раствор по каплям добавляют к смешанному раствору 5 мл этанола, 1 мл пиридина и 30 мл бензола при комнатной температуре. Смесь выдерживают в течение 30 мин, промывают водой, высушивают над сульфатом натрия, выпаривают при пониженном давлении, получая 1,3 г неочищенного эфира. Полученный неочищенный эфир очищают на хроматографической колонке с 40 г силикагеля (в качестве элюента используют бензол), получая 0,9 г 3-феноксибензил-2-(4-карбэтоксифенил)-2-метилпропиловый эфир.
Dмакс см-1 (пленка): 1735, 1620, 1595, 1500, 1380, 1285, 1260, 1225, 1120.
δССl4 (от ТМС), м. д. 1,24-1,47 (м, 9Н), 3,38 (с, 2Н), 4,15-4,41 (м, 4Н), 6,7-8,0 (м, 13Н).
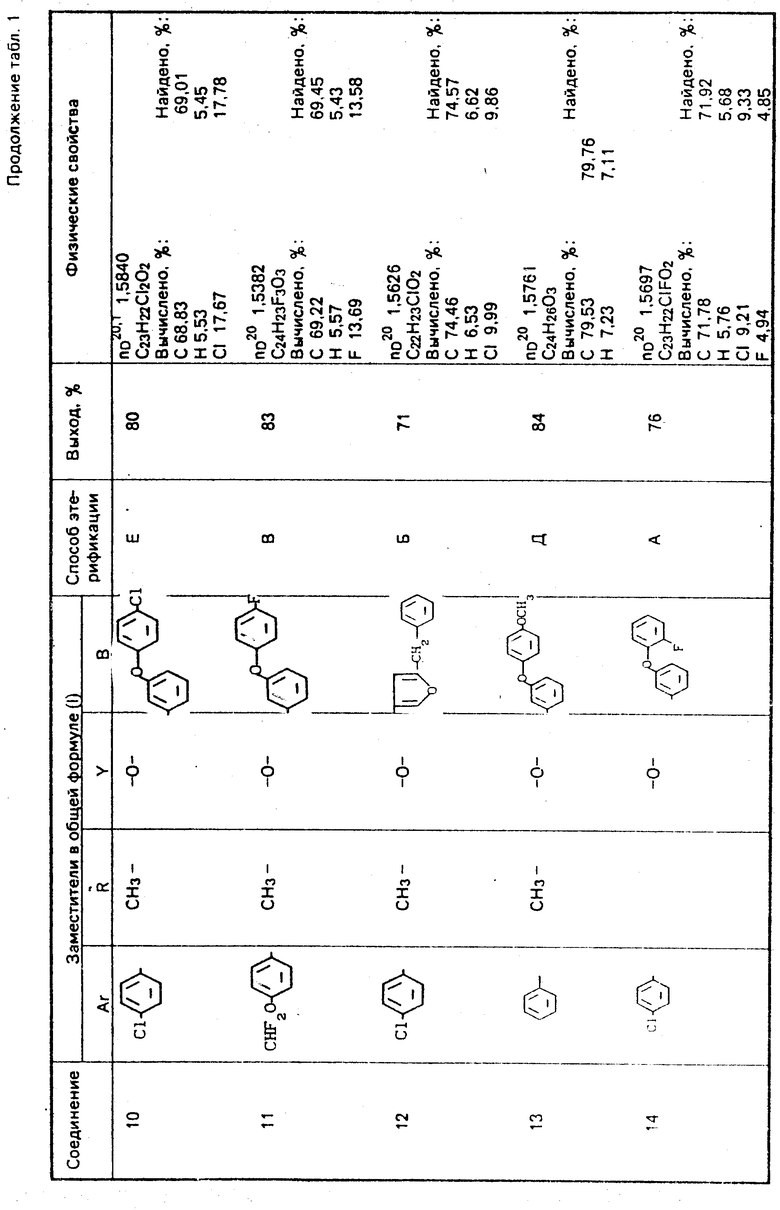
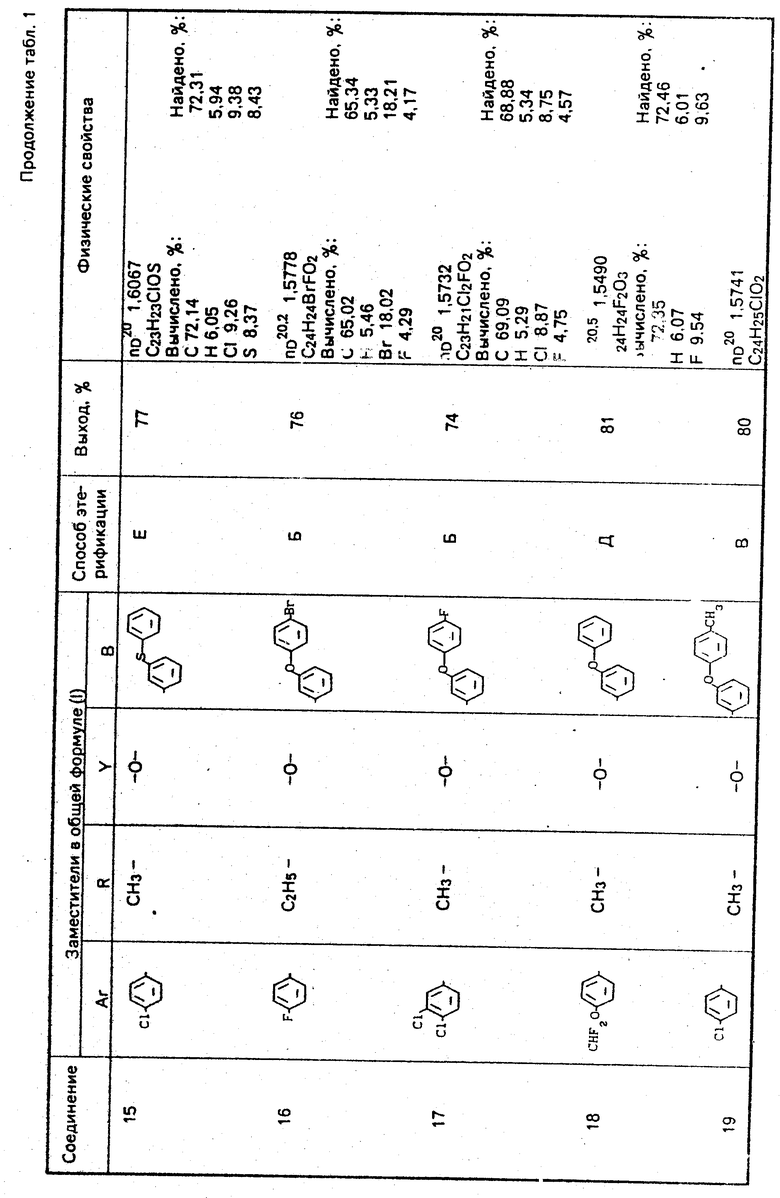
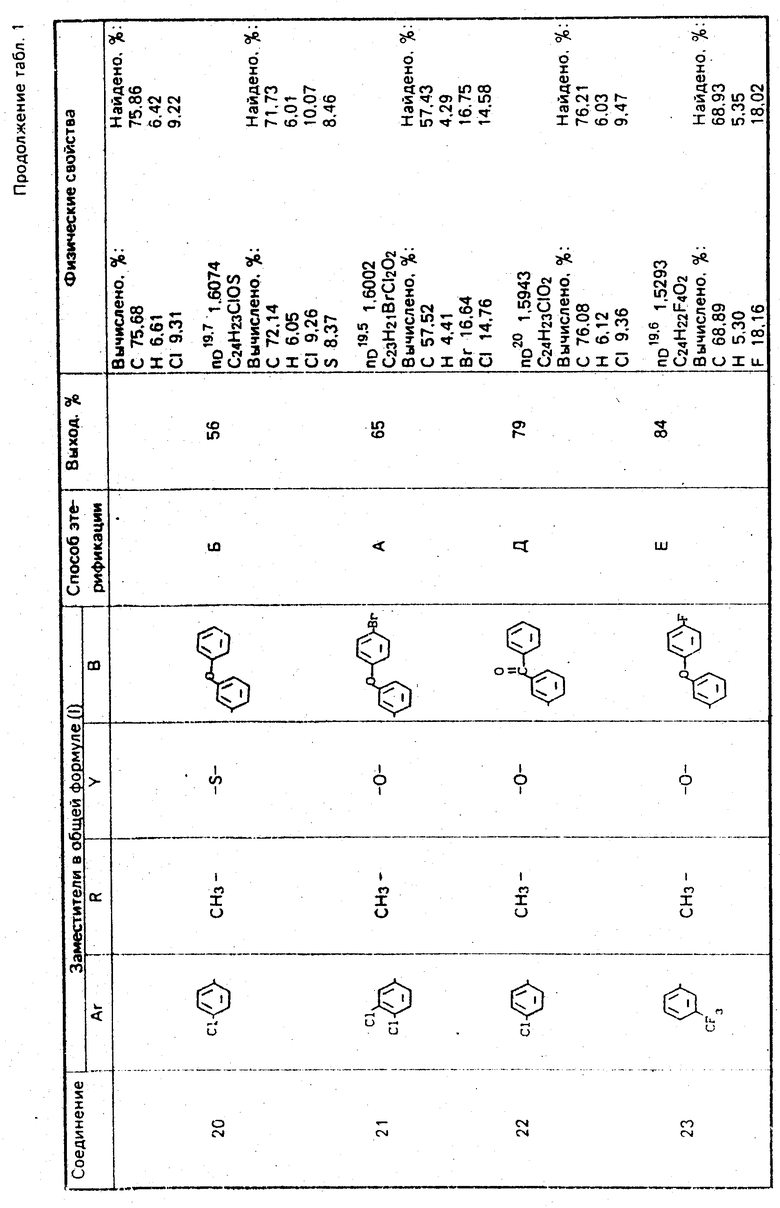
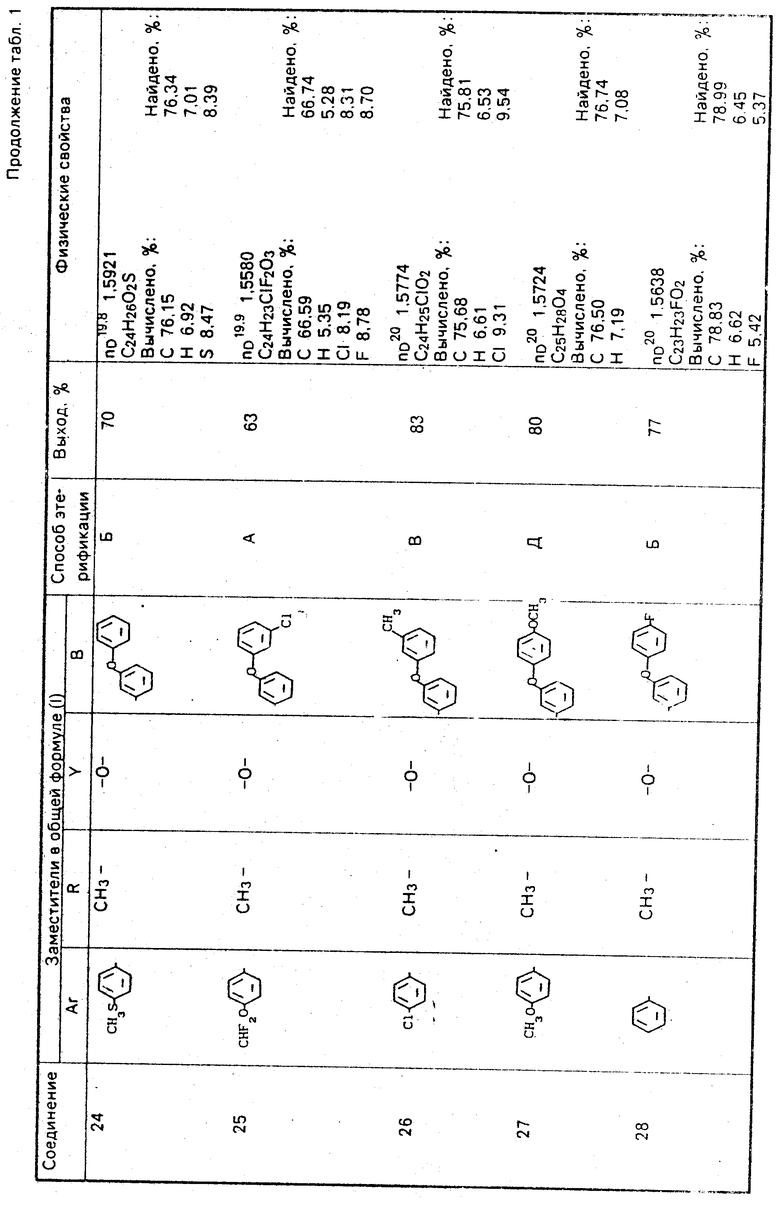
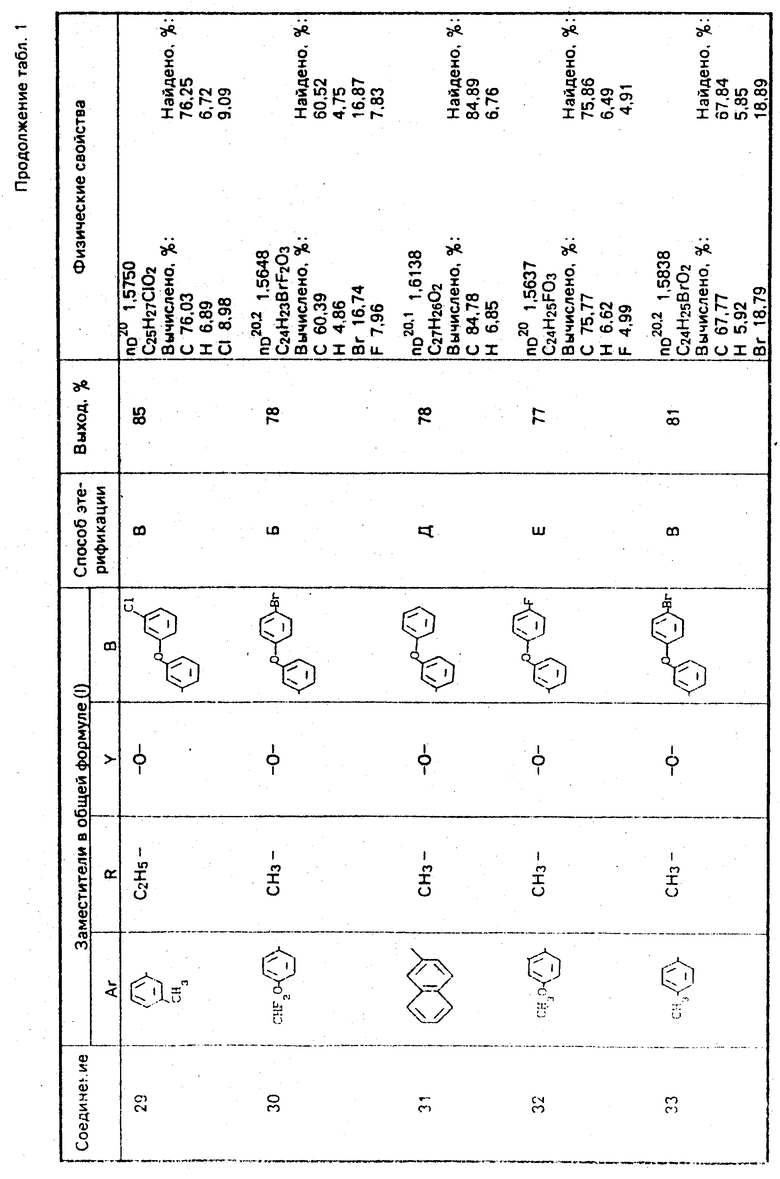
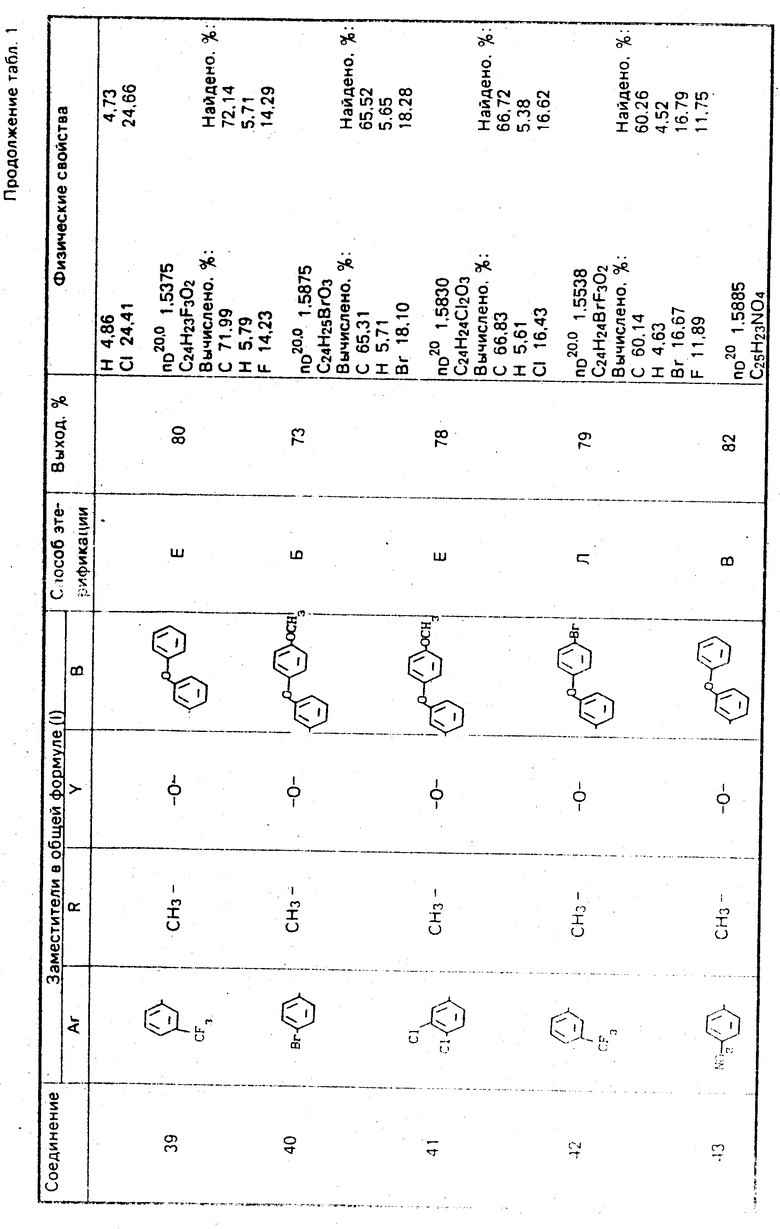
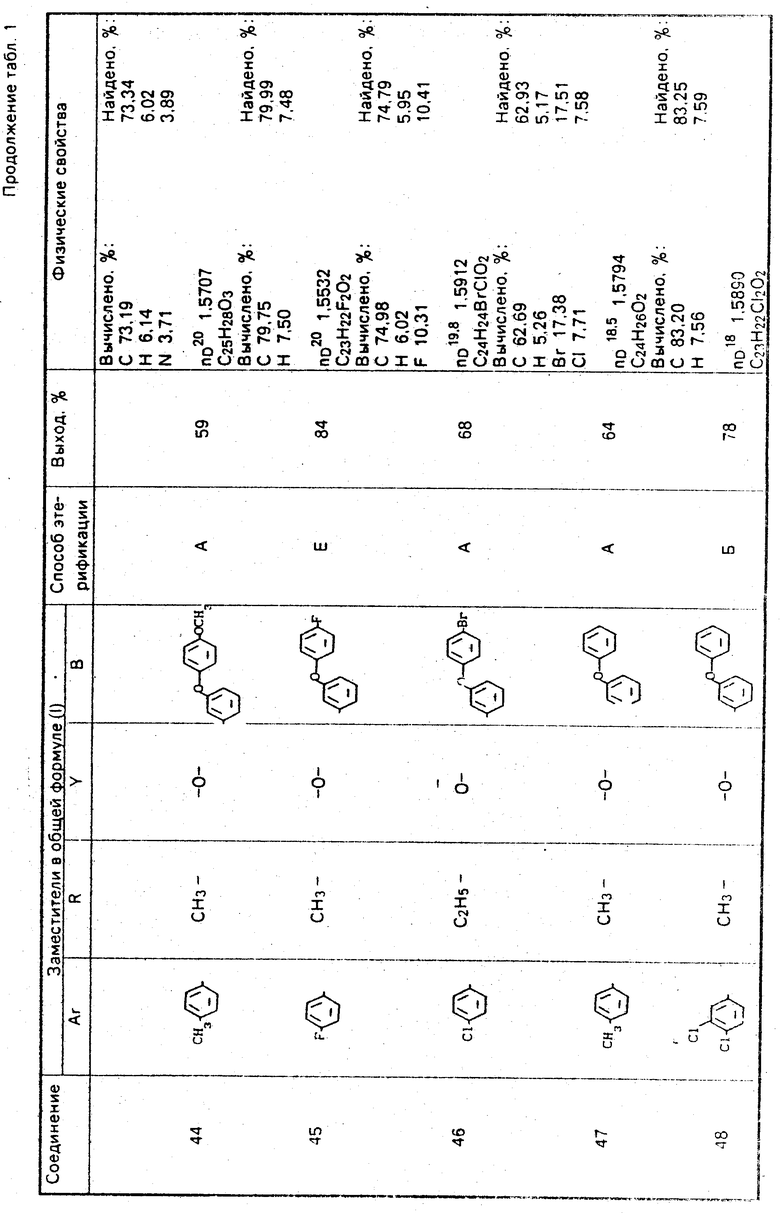
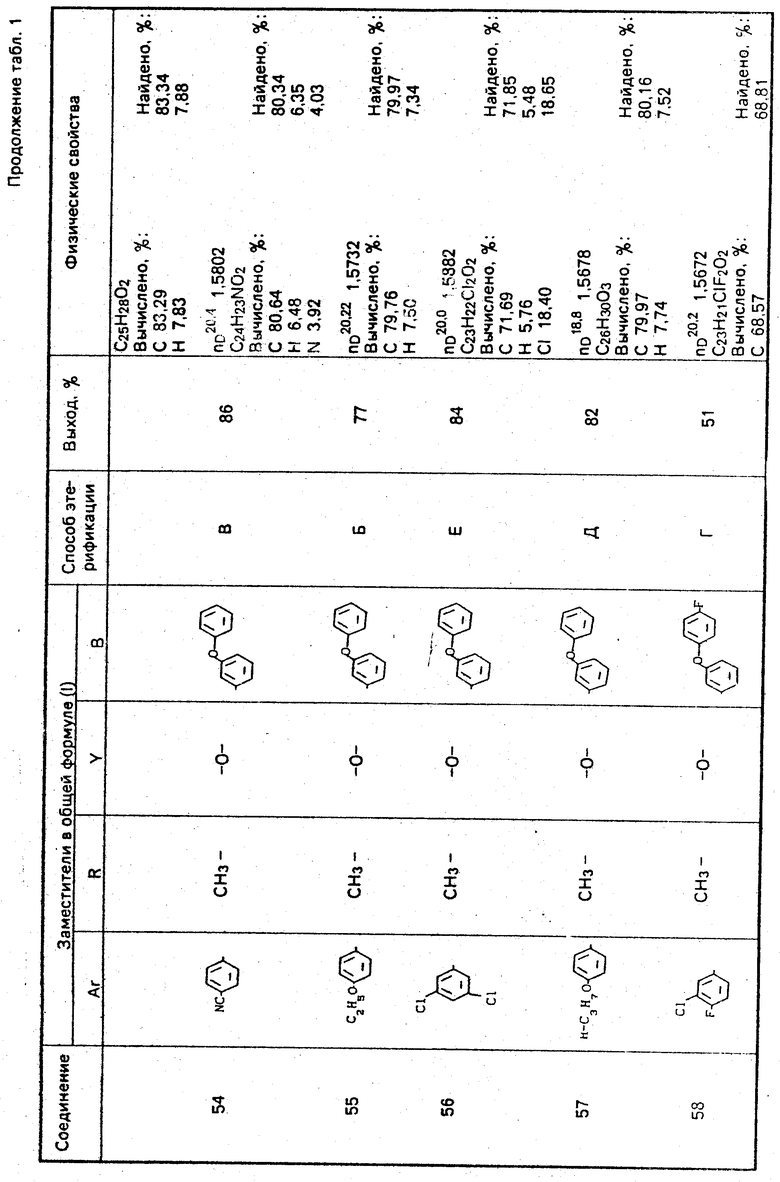
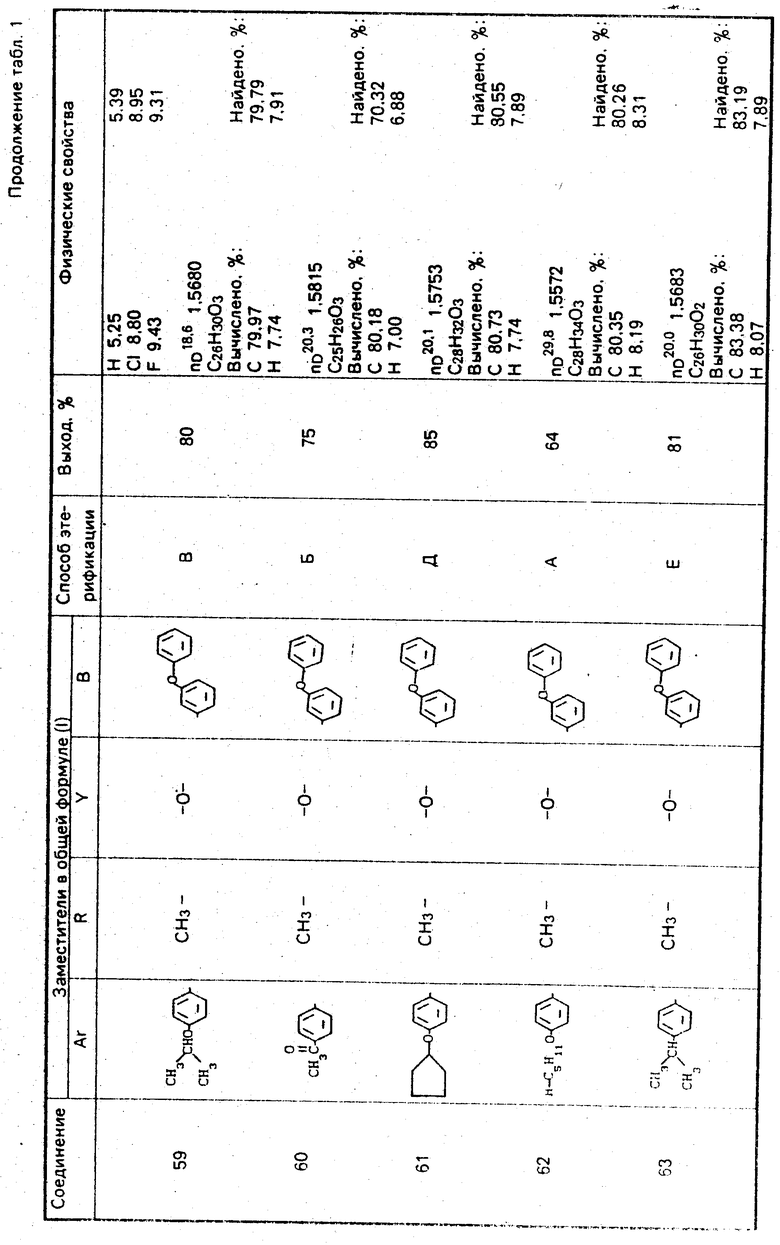
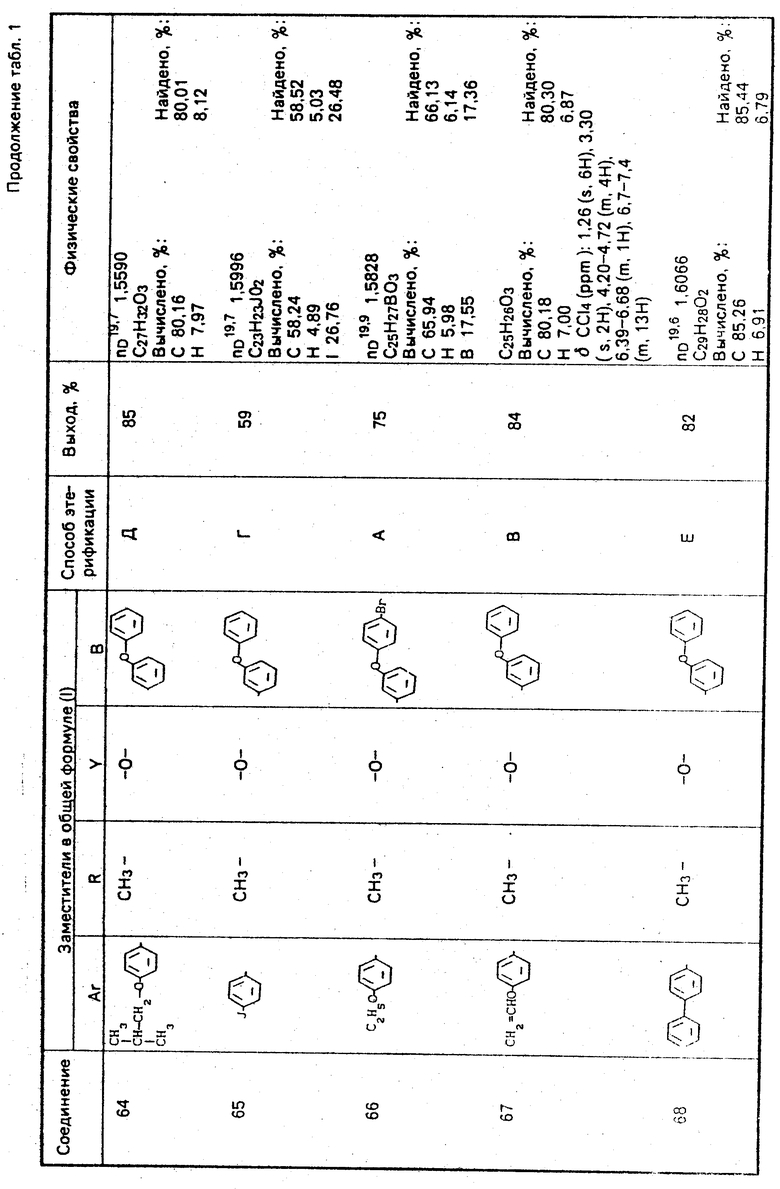
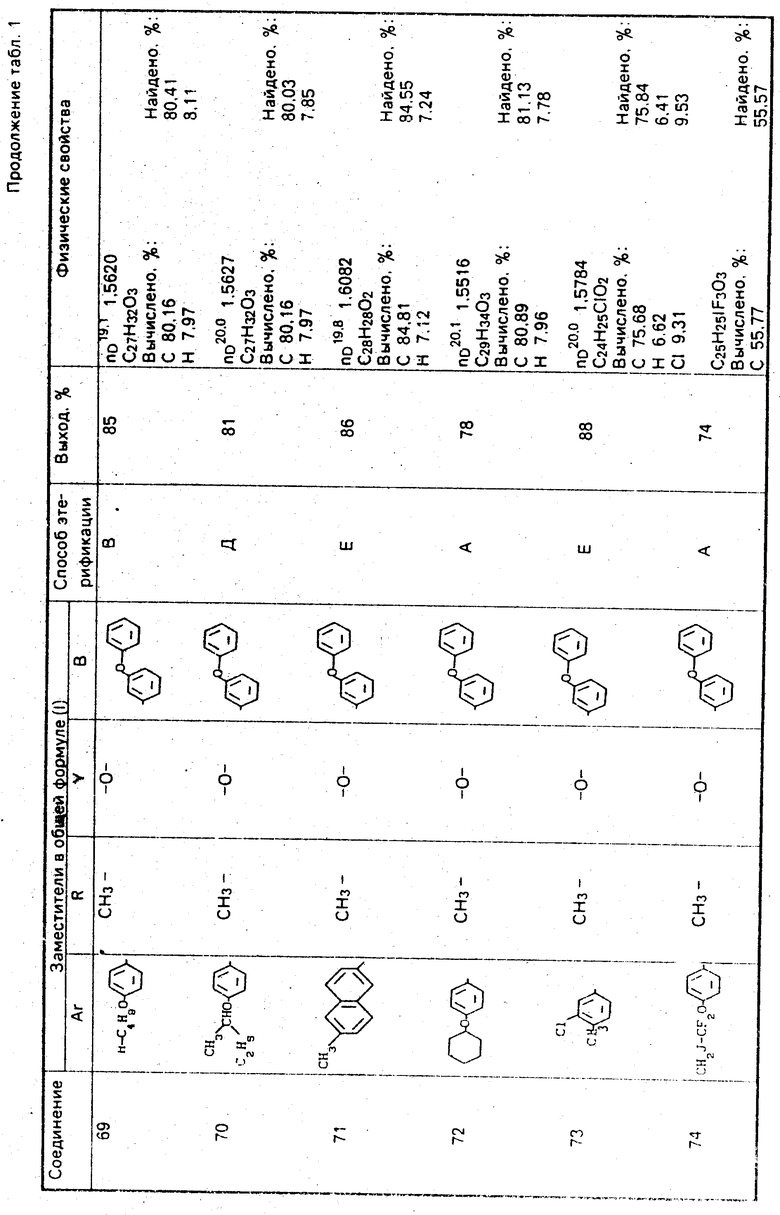
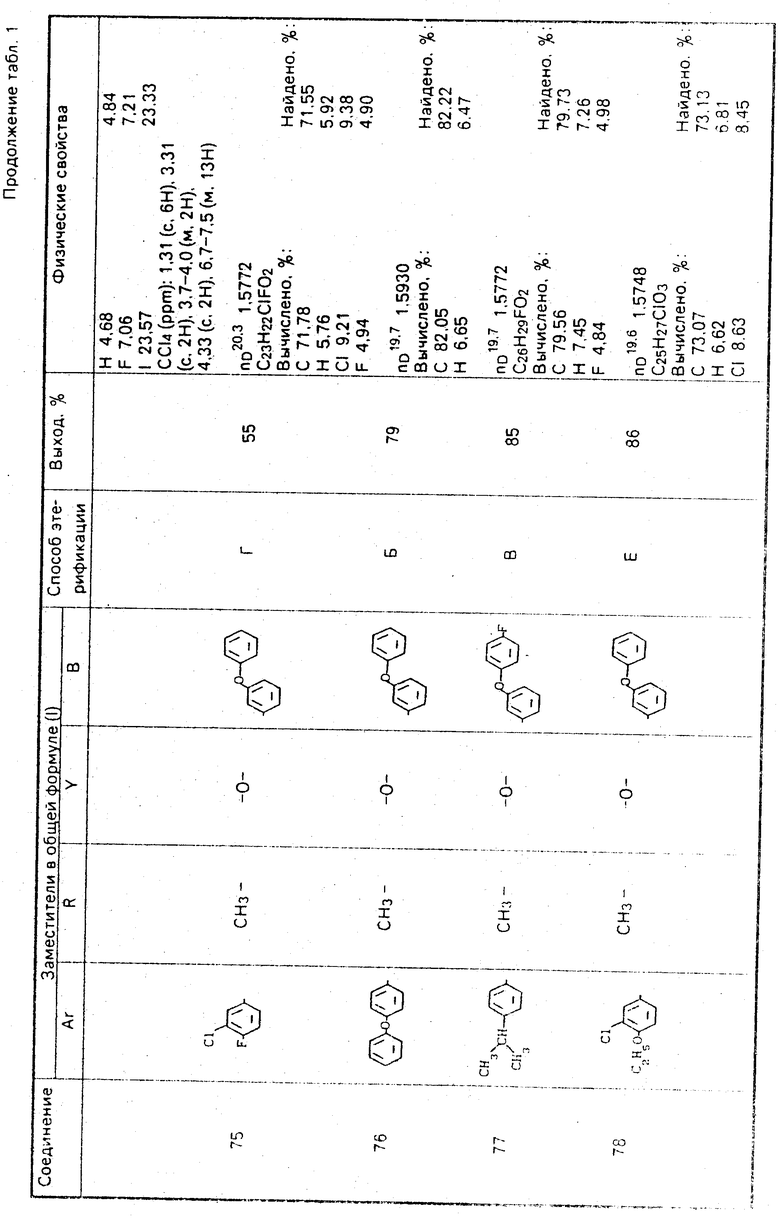
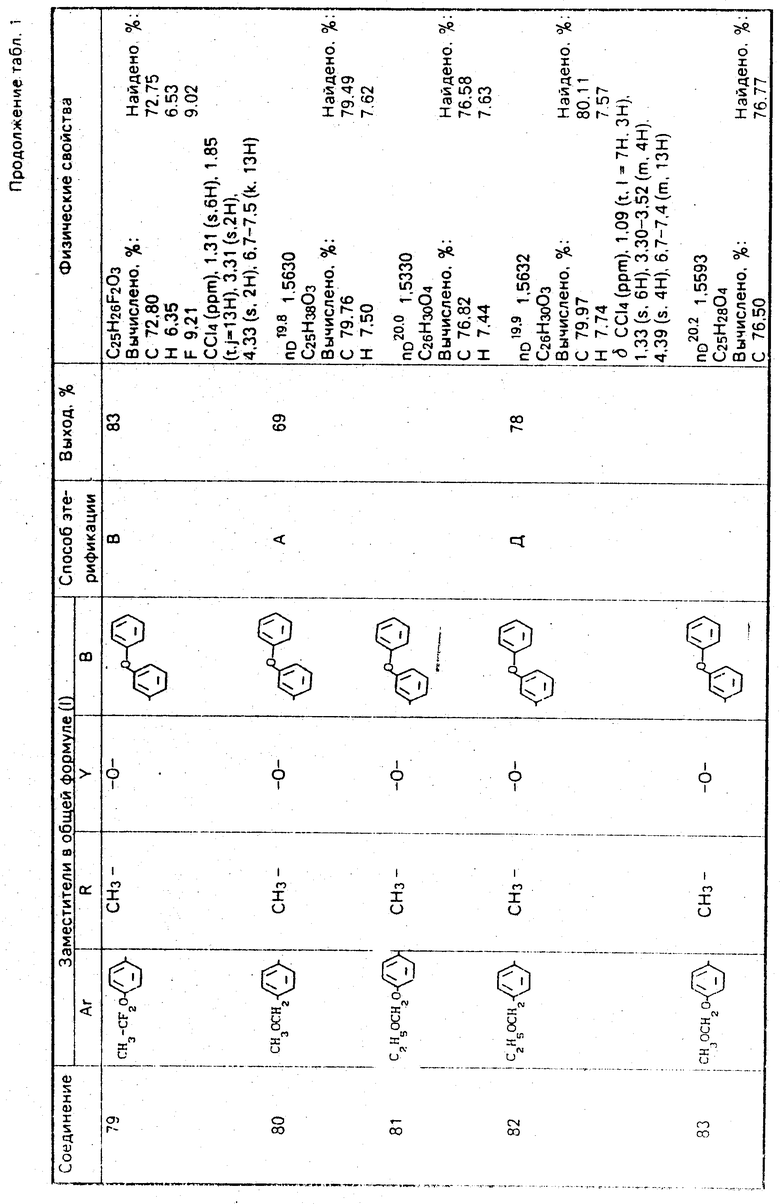
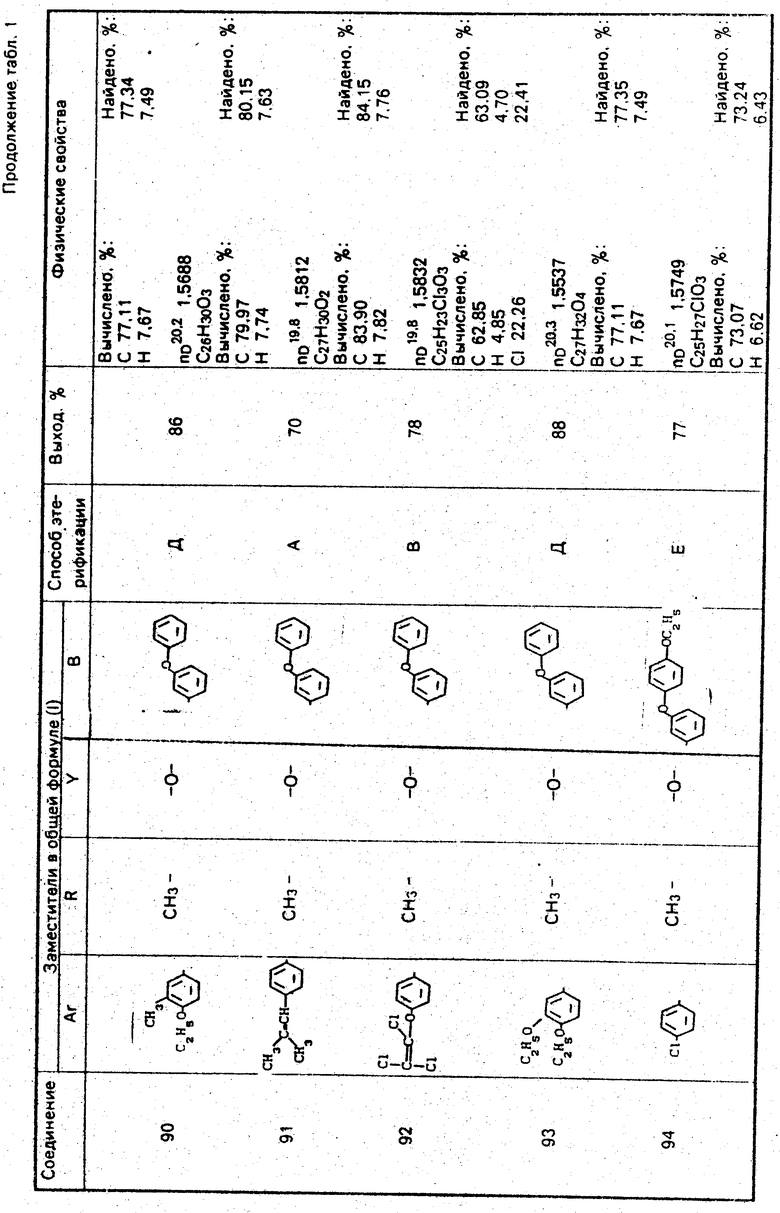
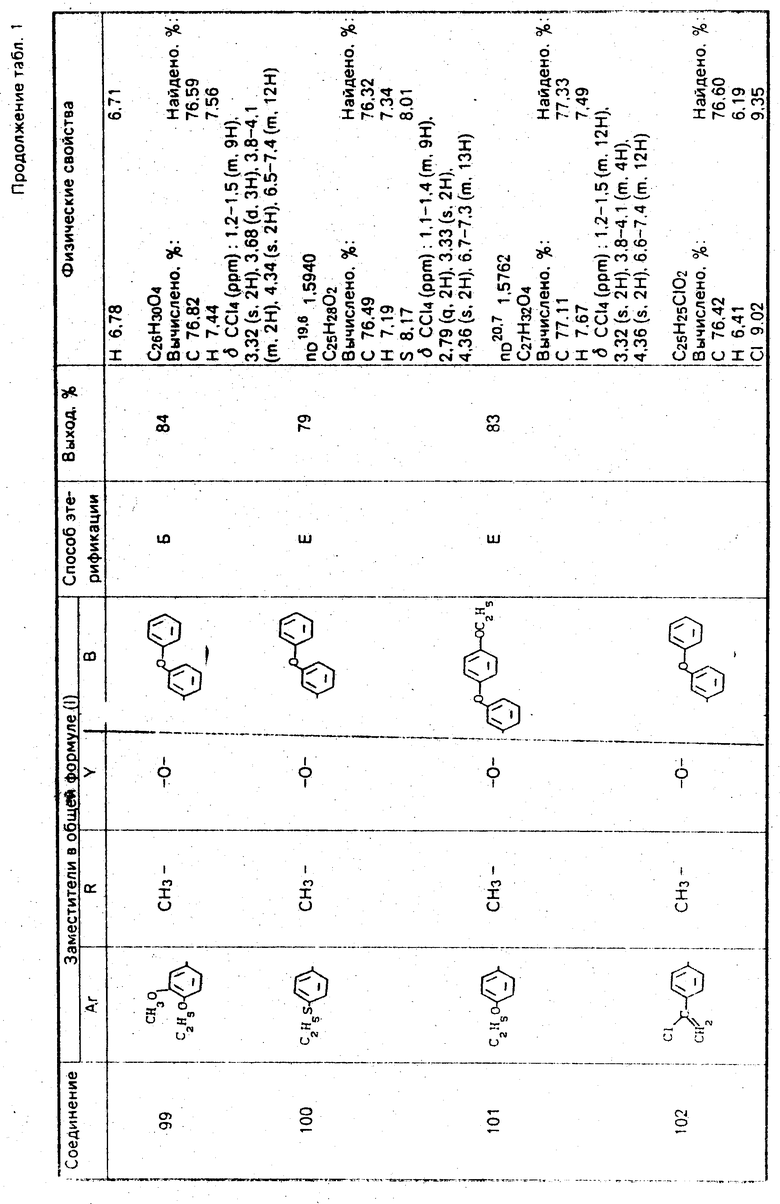
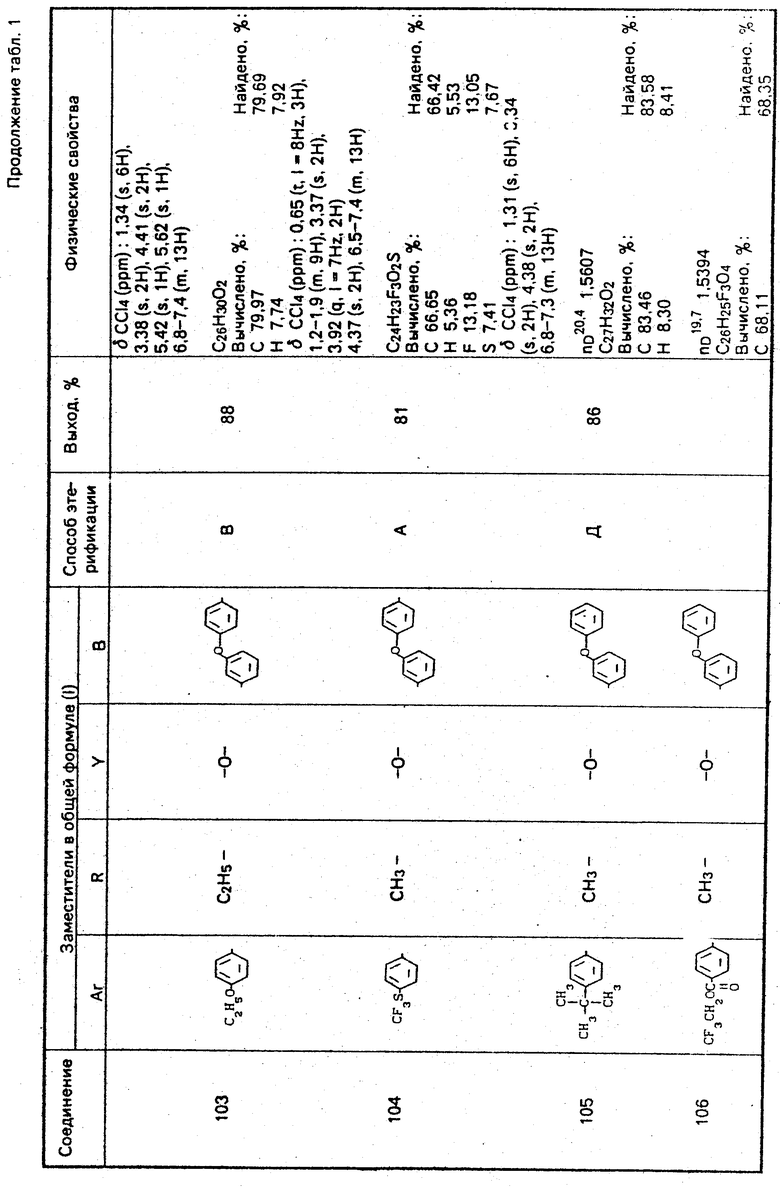
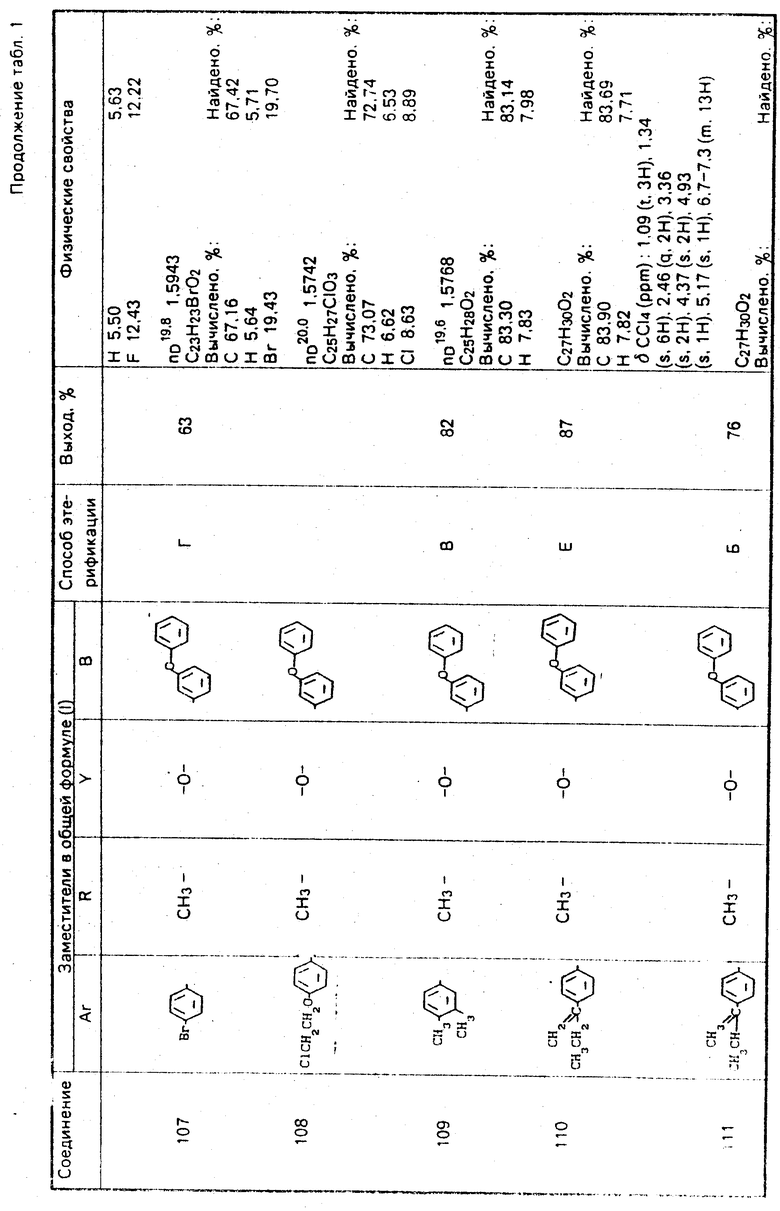
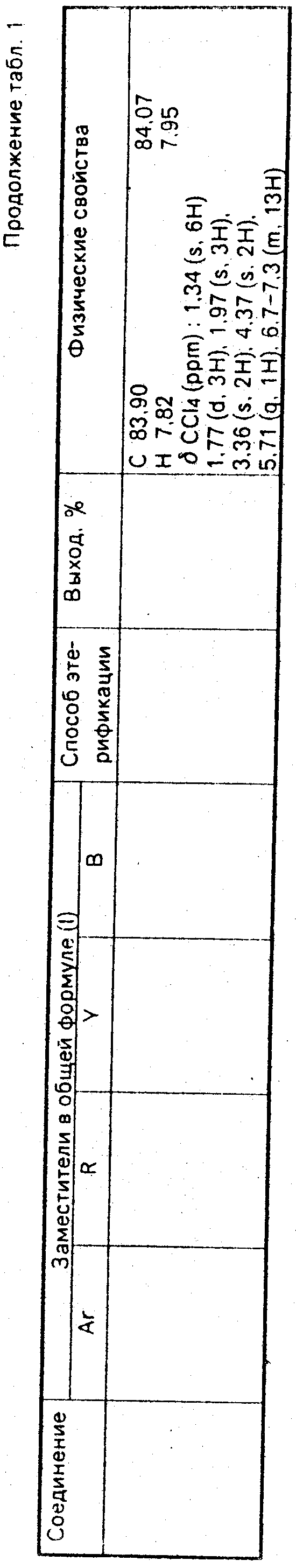
Используемые в композиции активные вещества представлены в табл. 1.
Пример композиции 1.
Раствор, образованный смешением 0,4 ч соединения настоящего изобретения и 2,0 ч пиперонилбутоксида с 6 ч. ксилола и 7,6 ч. дезодорированного керосина, помещают в аэрозольный баллон и через клапанную часть под давлением вводят 84 ч. диспергатора (сжиженный нефтяной газ) и получают аэрозоль (А).
Пример композиции 2.
Аэрозоли получают аналогично примеру композиции 1.
Синергист: пиперонилбутоксид
Неактивное масло: керосин, диспергатор; жидкий нефтяной газ.
Пример композиции 3.
Аэрозоли получают аналогично примеру композиции 1.
Синергист: октахлордипропиловый эфир (S-421)
Неактивное масло: ксилол
Диспергатор: сжиженный нефтяной газ
Пример композиции 4.
Аэрозоли получали аналогично примеру композиции 1.
Синергист: пиперонилбутоксид
Диспергатор: сжиженный нефтяной газ
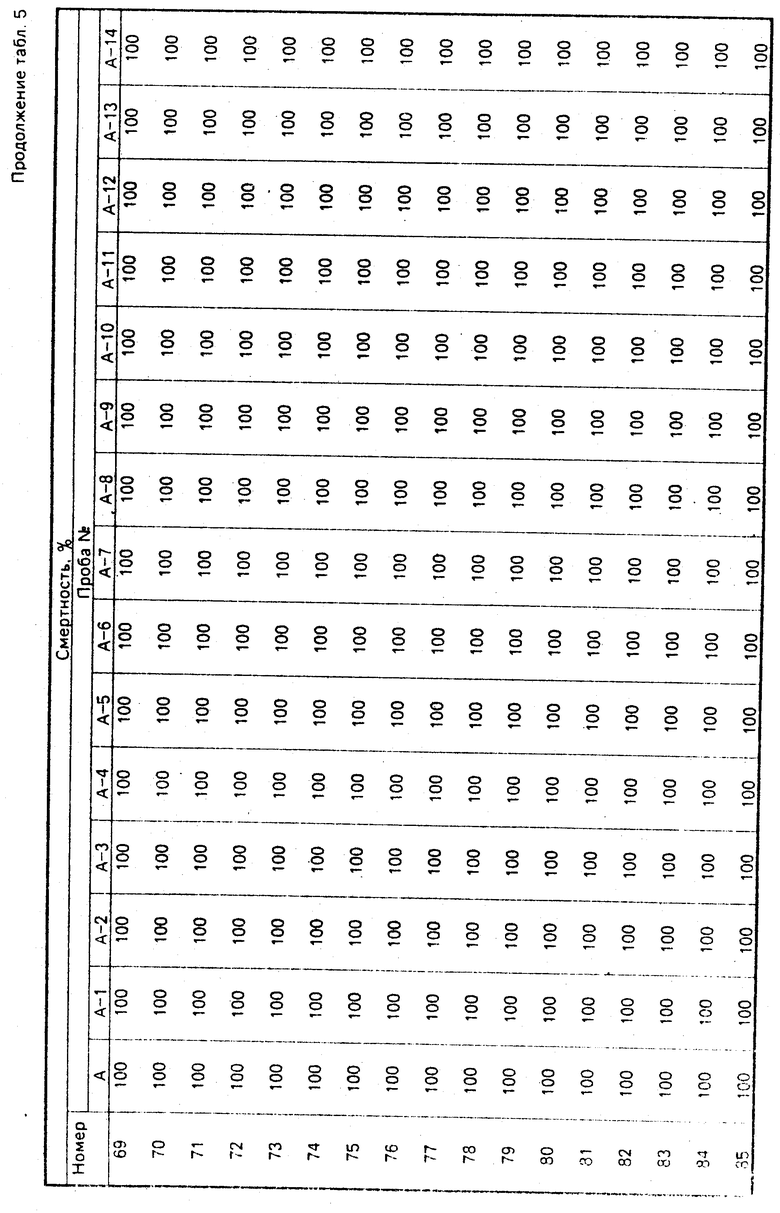
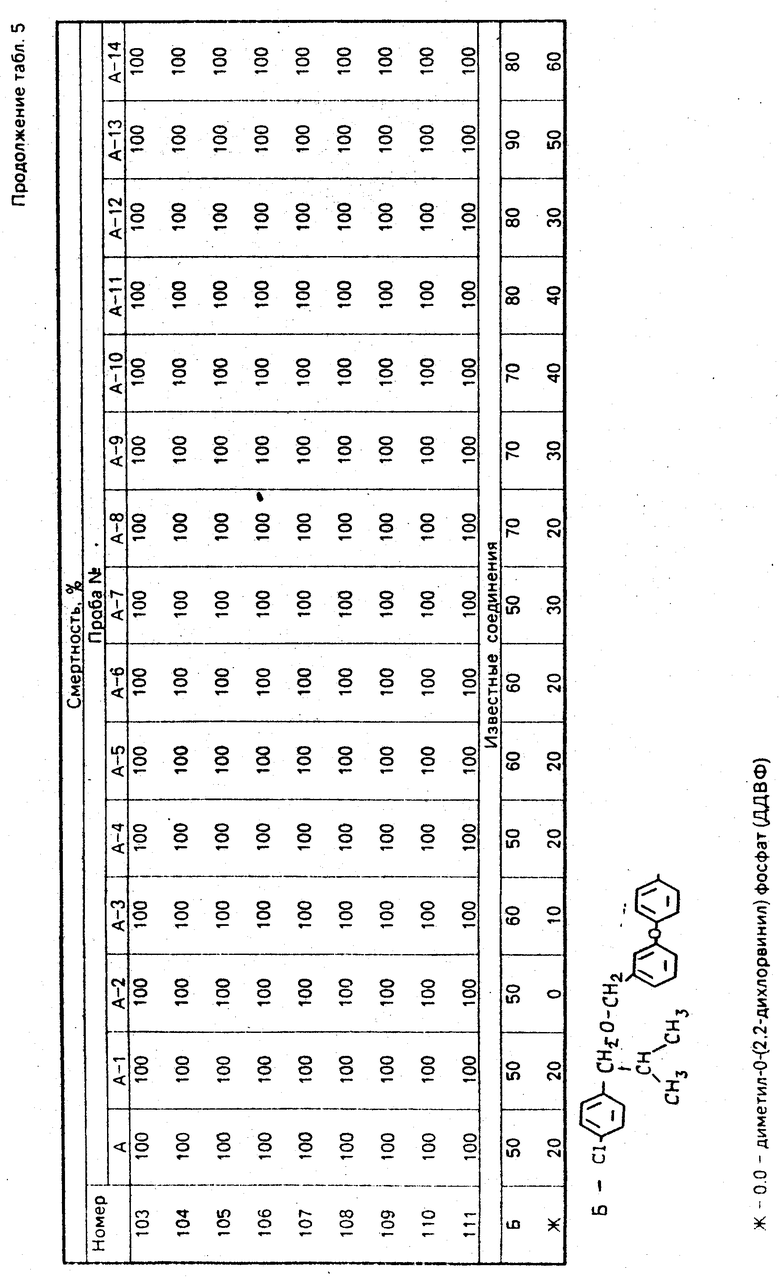
Тест 1. 10 женских особей взрослых мух комнатных сажают свободно в чашку Петри (диаметр 9 см, высота 5 см), затем чашку накрывают металлической сеткой (меш 16). На стеклянную пластину (25х25х0,5 см) помещают стеклянный цилиндр (диаметр 20 см, высота 43 см). Указанную чашку устанавливают вниз стеклянного цилиндра и на этот стеклянный цилиндр помещают стеклянную пластину с отверстием (диаметр 1 см) в середине для покрытия. Аэрозоль, приготовленный по способу, описанному в примере композиции 1, вносят в течение 5 с в каждом случае соединений. После закрытия отверстия аэрозоль не вносят. Через 10 мин упавших мух переносят в полиэтиленовую чашку (диаметр 10 см, высота 5 см). Кусок ваты пропитывают 5% -ным водным раствором сахара и питают им мух в чашке. Данную полиэтиленовую чашку закрывают. Через 2 сут подсчитывают число погибших и живых мух и вычисляют смертность. Полученный результат приведен в табл. 5.
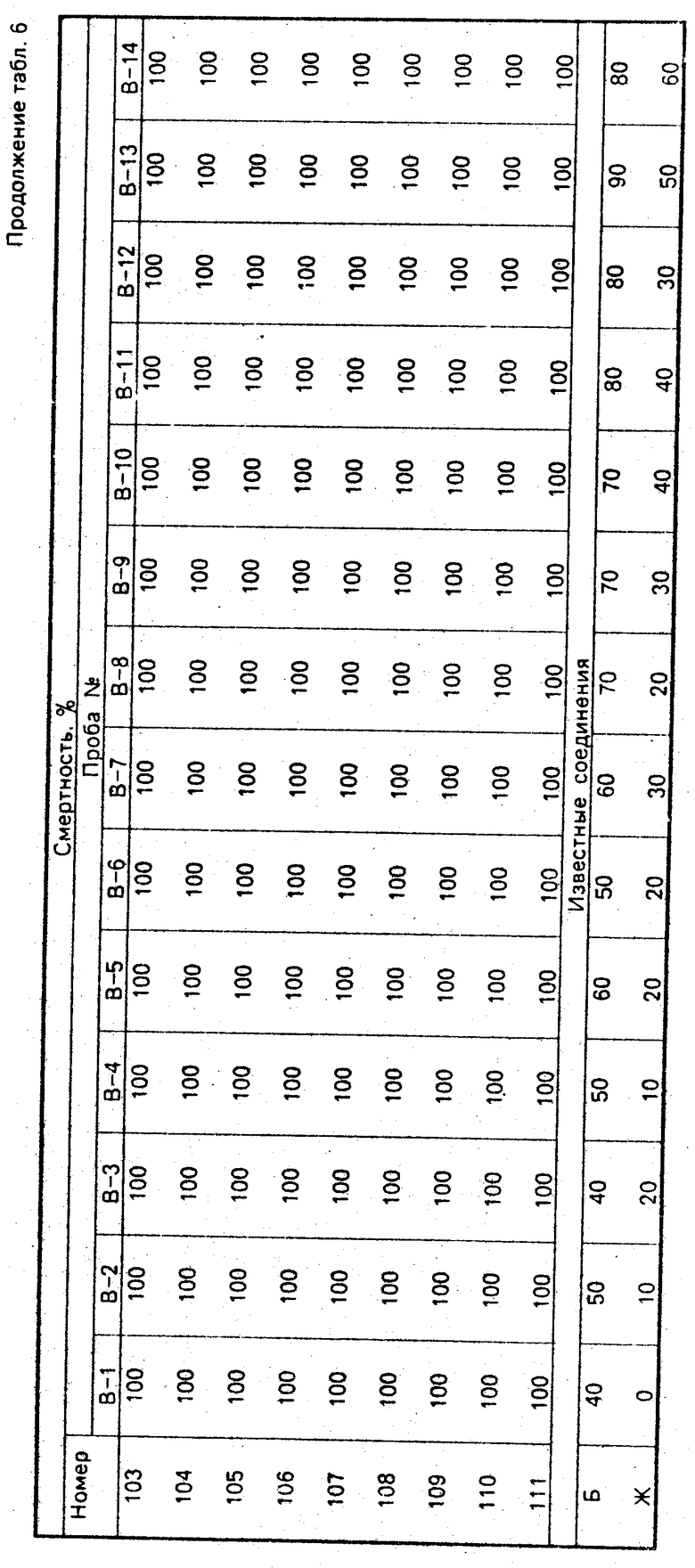
Тест 2. Все аэрозоли, полученные по способу, описанному в примере композиции 2, проверили аналогично тесту 1. Полученный результат показан в табл. 6.
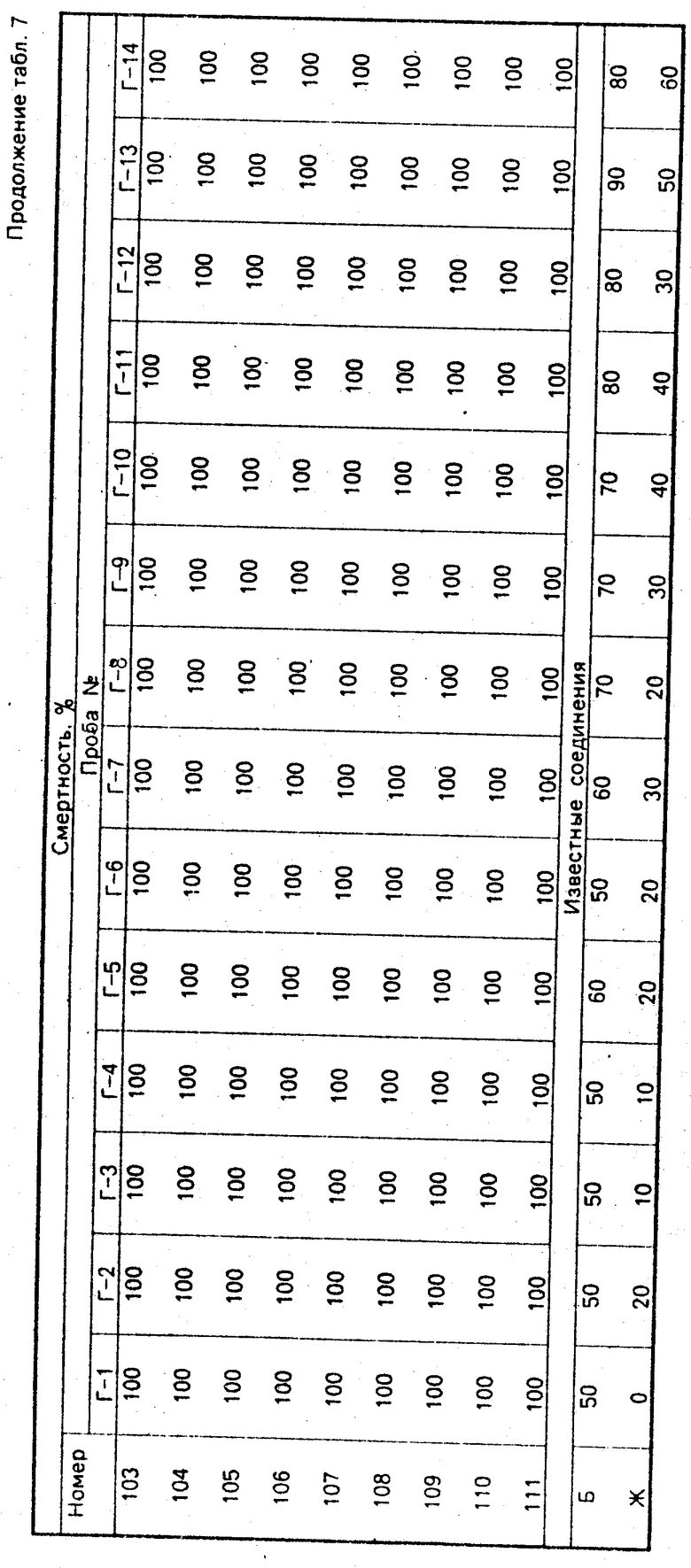
Тест 3. Все аэрозоли, полученные по способу, описанному в примере композиции 3, проверили аналогично тесту 1. Полученный результат приведен в табл. 7.
Тест 4. Все аэрозоли, полученные по способу, описанному в примере композиции 4, проверили аналогично тесту 1. Полученный результат приведен в табл. 5. (56) Патент США N 4073812, кл. 260-613, опубл. 1978.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ 2-АРИЛПРОПИЛОВЫХ ЭФИРОВ | 1992 |
|
RU2045511C1 |
| Инсектоакарицидная композиция (ее варианты) | 1981 |
|
SU1477230A3 |
| Способ получения производных 2-арилпропилового эфира или тиоэфира | 1981 |
|
SU1416052A3 |
| Способ получения производных 2-арилпропилового эфира или тиоэфира | 1982 |
|
SU1442067A3 |
| Способ получения производных ароматических алканов | 1984 |
|
SU1524808A3 |
| Способ получения производных феноксибензил-2-(4-алкоксифенил)-2-метилпропилового эфира | 1983 |
|
SU1447275A3 |
| Инсектицидная композиция (ее варианты) | 1983 |
|
SU1837764A3 |
| ХИНОНОВЫЕ ПРОИЗВОДНЫЕ | 1992 |
|
RU2054412C1 |
| ПРОИЗВОДНОЕ 2-АЛКЕНИЛ-3-АМИНОТИОФЕНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2007 |
|
RU2403248C2 |
| ЖИДКАЯ ПЕСТИЦИДНАЯ КОМПОЗИЦИЯ | 1987 |
|
RU2067831C1 |
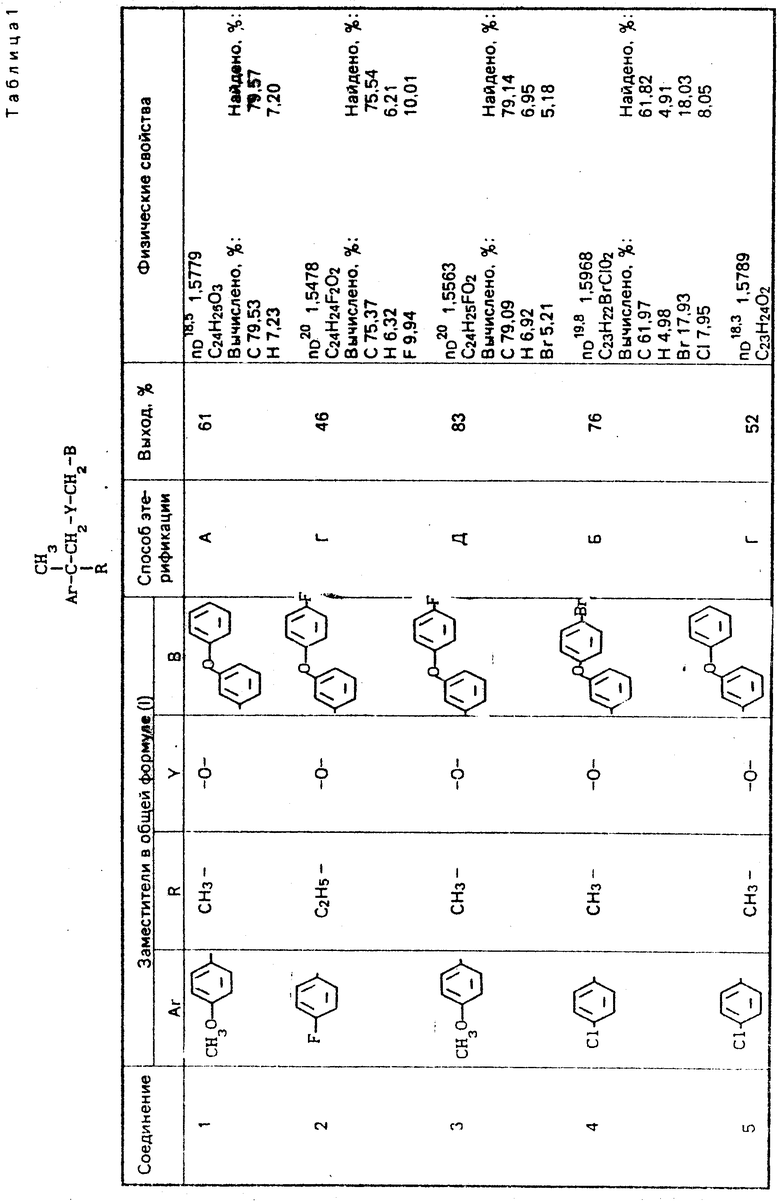
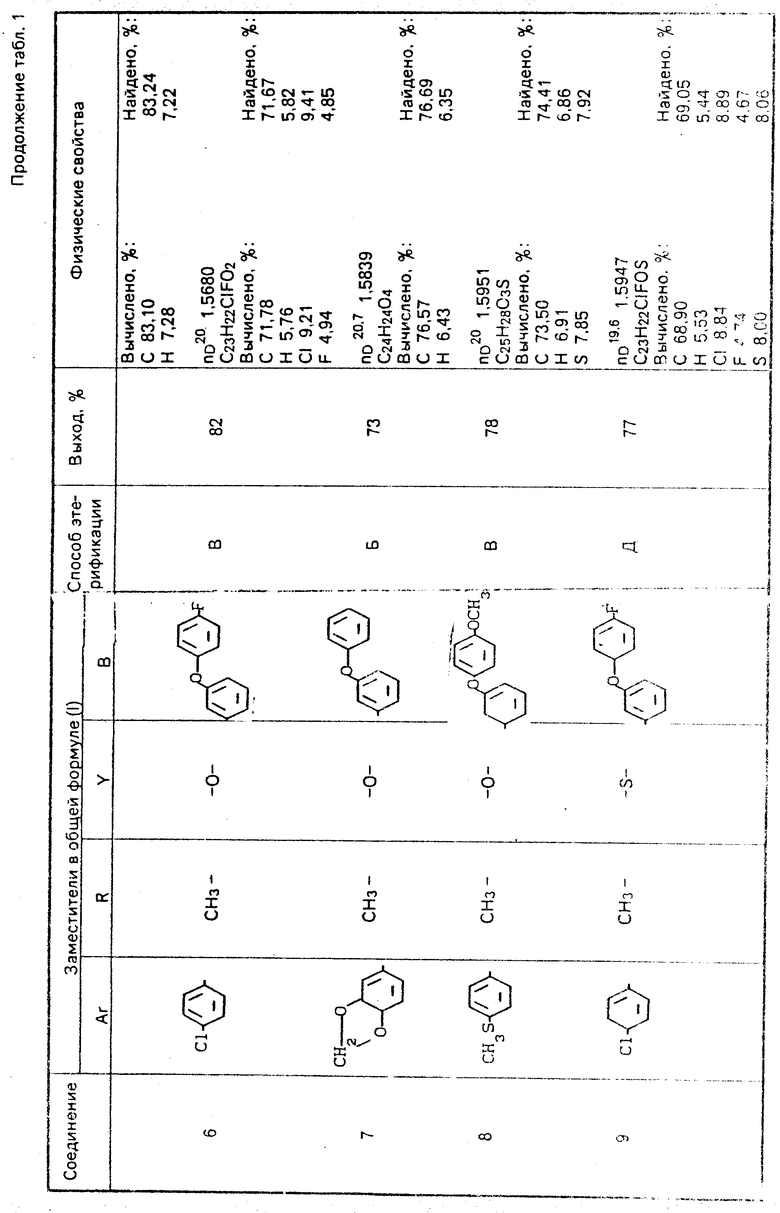























Использование: сельское хозяйство, химические средства защиты растений. Сущность изобретения: композиция в форме аэрозоля содержит, мас. % : : активное начало - соединение формулы Ar-C(CH3)R-CH2-Y-CH2B, где Ar - фенил, фенил, монозамещенный алкилом, имеющим 1, 3 или 4 атома углерода, алкокси, имеющий 1-5 атомов углерода, алкилтио, имеющий 1-2 атома углерода, циклоалкокси, имеющий 5-6 атомов углерода, фенилом, трифторметилтио, винилокси, 1-метилвинилом, 2, 2-диметилвинилом, 1-хлорвинилом, 1-этилвинилом, 1, 2, 2-трихлорвинилокси, 1-метил-1-пропенилом, этинилом, 2-пропинилокси, трифторметилом, дифторметокси, 2-иод-1, 1-дифторэтокси, 1, 1-дифторэтокси, 2-хлорэтокси, метоксиметилом, этоксиметилом, 1-этоксиэтилом, 1-метоксиэтилом, этоксиметокси, метоксиметокси, этоксиэтокси, ацетилом, этоксикарбонилом, 2, 2, 2-трифторэтоксикарбонилом, нитро, нитрилом, 3, 4-метилендиокси, фенокси или атомом галогена, или фенильную группу, дизамещенную атомами хлора или фтора или метилом, метокси или этоксигруппами, или 3, 5-диметил-4-этоксифенил, нафтил или 7-метилнафтил, R - метил, этил; Y - кислород или сера; B - группа формулы 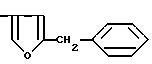 или
или  Z - кислород, сера, карбонильная или метиленовая группа, R1 - водород, хлор, бром, фтор, метил, метокси, этокси в количестве 0,1-0,5, растворитель - керосин, ксилол или смесь керосина и ксилола 5-25, синергист - октахлордипропиловый эфир или пиперонилбутоксид 0,05-8,00, диспергатор - сжиженный нефтяной газ - остальное. 7 табл.
Z - кислород, сера, карбонильная или метиленовая группа, R1 - водород, хлор, бром, фтор, метил, метокси, этокси в количестве 0,1-0,5, растворитель - керосин, ксилол или смесь керосина и ксилола 5-25, синергист - октахлордипропиловый эфир или пиперонилбутоксид 0,05-8,00, диспергатор - сжиженный нефтяной газ - остальное. 7 табл.
ИНСЕКТИЦИДНАЯ АЭРОЗОЛЬНАЯ КОМПОЗИЦИЯ, включающая активный ингредиент - производное 2-арилпропилового эфира, растворитель и диспергатор, отличающаяся тем, что, с целью усиления инсектицидной активности, в качестве производного 2-арилпропилового эфира она содержит соединения общей формулы
Ar-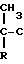 H2-Y-CH2-B
H2-Y-CH2-B
где Ar - фенил, или фенил, монозамещенный алкилгруппой, имеющей 1,3 и 4 атомов углерода, C1 - C5-алкоксигруппой, C1 - C2-алкилтиогруппой, C5 - C6-циклоалкоксигруппой, фенилом, трифторметилтио, винилокси, 1 - метилвинилом, 2,2 - диметилвинилом, 1 - хлорвинилом, 1 - этилвинилом, 1,2,2 - трихлорвинилокси, 1 - метил - 1 - пропенилом, этинилом, 2 - пропинилокси, трифторметилом, дифторметокси, 2 - иод - 1,1 - дифторэтокси, 1,1 - дифторэтокси, 2 - хлорэтокси, метоксиметилом, этоксиметилом, 1 - этоксиэтилом, 1 - метоксиэтилом, этоксиметокси, метоксиметокси, этоксиэтокси, ацетилом, этоксикарбонилом, 2,2,2 - трифторэтоксикарбонилом, нитро, нитрилом, 3,4 - метилендиокси или феноксигруппой или атомом галогена, или фенил, дизамещенный атомами хлора или фтора или метилом, метокси или этоксигруппами, или 3,5 - диметил - 4 - этоксифенил или нафтил, или 7 - метилнафтил;
R-метил или этил;
Y - кислород или сера;
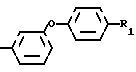
B - группа, представленная формулой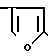
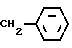
или общей формулой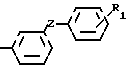
где Z - кислород, или сера, или карбонил, или метиленовая группа, R1 - водород, хлор, бром, фтор или метил, метокси или этоксигруппа,
в качестве растворителя содержит керосин, или ксилол, или смесь керосина и ксилола, в качестве диспергатора - сжиженный нефтяной газ и дополнительно содержит синергист - октахлордипропиловый эфир или пиперонилбутоксид при следующем соотношении, мас. % :
Активный ингредиент 0,1 - 5,0
Синергист 0,05 - 8,00
Указанный растворитель 5 - 25
Указанный диспергатор Остальное
Приоритет по признакам:
02.05.80 при Ar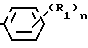
R1 - галоген, алкил, содержащий 1,3 или 4 атома углерода;
n= 1 или 2;
Y - кислород;
B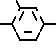 O
O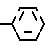
R - метил, этил.
Авторы
Даты
1994-04-15—Публикация
1989-05-30—Подача