Изобретение относится к медицине, а именно к биологически активным веществам, обладающим бактериостатическими и цитотоксическими свойствами.
Известные противоопухолевые препараты класса фосфорсодержащих алкилирующих агентов, к которым относится динодбензо-ТиоТЭФ (см. авт. св. СССР N 431878, кл. A 61 K 31/66, 1975), замещенный фосфонитрил (авт. св. N 325756, кл. A 61 B 31/15, 1970), замещенные фосфемы сложного строения (авт. св. N 761474, кл. C 07 F 9/24, 1980). Все указанные препараты являются биологически активными веществами, обладают цитоксическим и цитостатическим действиями.
Однако большинство биологически активных веществ при введении в организм не только оказывает избирательное действие на патологически измененные клетки, ткани и органы, но и негативно влияют на здоровые системы организма. Это вызвано присущей биоактивным веществам токсичностью. Если в соотношении к патологически измененным клеткам токсичность биоактивных веществ является положительным свойством, то для здоровых клеток токсичность противопоказана. С другой стороны для получения положительного химиотерапевтического эффекта необходимо создавать высокие концентрации химического соединения, что отрицательно сказывается на общем состоянии организма, т.к. химиопрепарат, в данном случае трехфункциональный алкилирующий агент, распределяется по всему организму более менее равномерно. Это свойство биологически активных веществ ограничивает возможности их применения из-за их негативного побочного влияния на организм.
Подобными недостатками обладает и противоопухолевое соединение ТиоТЭФ (тиофосфамид), применяющееся при лечении рака молочной железы, рака легких, рака желудка (Информационное письмо по противоопухолевым препаратам, Киев ГПУ, 1982 г., N 2, с.38-39), выбранное в качестве прототипа, как наиболее близкое по технической сущности.
Механизм его противоопухолевого действия остается неясным. В малых дозах он оказывает мутагенный эффект, в больших - цитостатический и цитотоксический эффект. Однако при нарушении дозировки отмечается депрессивное действие на костномозговое творение: лейкопоэз, тромбоцитопоэз. При передозировке или повышении чувствительности к препарату может развиваться редкая лейкопения и тромбоцитопения с явлениями иморрагического диатеза, тошнота, рвота, понижение активности.
Следовательно, одной из острых проблем в применении цитоксических веществ является исключение негативного влияния на здоровые клетки за счет постепенного, строго дозированного введения противоопухолевого препарата в живой организм.
Целью изобретения является устранение указанных недостатков, то есть ослабление токсичного воздействия на здоровые ткани, обеспечение возможности усиления действия противоопухолевого препарата, повышение эффективности воздействия при уменьшении дозы.
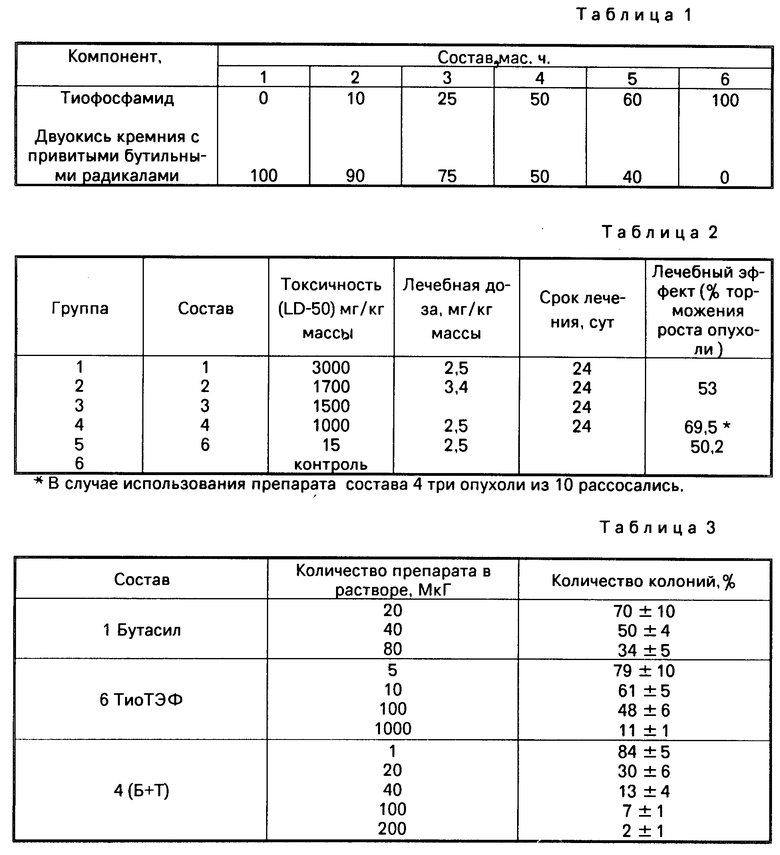
Поставленная цель достигается тем, что противоопухолевый препарат, содержащий биологически активное вещество, например тиофосфамид, согласно изобретению, состоит из тиофосфамида и высокодисперсной двуокиси кремния с привитыми спиртовыми радикалами при следующем соотношении компонентов, мас. ч.: Тиофосфамид 10-50
Двуокись кремния с
привитыми спиртовыми радикалами 50-90
Предпочтительным является вариант использования высокодисперсной двуокиси кремния с привитыми радикалами бутилового спирта. При смешивании противоопухолевого препарата с двуокисью кремния, частицы которого имеют на поверхности бутильные радикалы, происходит связывание молекул за счет физического взаимодействия.
Соотношение компонентов, входящих в состав заявляемого препарата, обусловлено именно этим взаимодействием их молекул. При наличии менее чем 10 мас. ч. тиофосфамида в составе, частично остается свободной поверхность частиц двуокиси кремнезема, а при содержании более 50 мас.ч. тиофосфамида на частицах двуокиси кремния образуется слой свободного тиофосфамида. Поэтому не достигается эффект пролонгации, так как имеет место вступления в действие свободного тиофосфамида, что затрудняет его дозирование при введении в ткани организма.
Существенность отличий предлагаемого решения подтверждается тем, что модифицированный кремнезем сам по себе не обладает противоопухолевым действием, поэтому усиление цитостатического эффекта, тиофосфамида при смешении его с модифицированным кремнеземом носит неожиданный характер.
Сущность заявляемого технического решения в дальнейшем поясняется методикой приготовления состава, табл.1 рецептур и конкретными примерами проверки микробиологических и цитотоксических свойств заявляемого препарата.
Методика.
Для приготовления противоопухолевого препарата в качестве наполнителя используют высокодисперсный кремнезем с привитыми на его поверхности бутильными радикалами, так называемый бутасил (выпускается Калушским опытно-экспер. заводом ИХП АН УССР).
Тиофосфамид (выпускаемый объединением "Олайнфар", Рига) дважды перекристаллизованный.
Для проверки цитотоксического эффекта полученного противоопухолевого препарата его испытывали на белых мышах для лечения рака (подкожная опухоль - солидная опухоль). Препараты, приготовленные согласно составам 1,2,3,4,6, применяли на 4 день после прививки опухоли.
Животные были разбиты соответственно на 5 групп по 9-10 мышей в каждой. Шестая группа - контрольная. Животным при лечении вводили препарат в дозе 2,5 мг/кг массы (внутрибрюшинно). Учет и контроль эффективности лечения оценивали на 25-й день лечения (табл.2).
Следует отметить, что эффективность торможения опухоли при введении препарата, приготовленного согласно заявляемому составу, практически на 3-19,3% выше, чем в случае использования тиофосфамида, причем концентрация тиофосфамида при этом (см. группу 6) в 2 раза больше, чем для группы 4 в 10 раз больше, чем для группы 2. Следовательно, снижая дозу активного противоопухолевого препарата, удалось повысить эффективность лечения раковой опухоли, токсичность препарата снижается соответственно.
Для проверки усиления действия бактерицидных свойств заявляемого препарата проведены эксперименты с использованием штамма Escherichia coli K-12 по следующей методике:
Высевают штамм E.coli в LB-среду.
Состав среды: Триптон 10 г Дрож. экстракт 5 г NaCl 5 г глюкоза 1 г 1 н. NaOH 1 мл вода 1000 мл Суточную культуру E.coli разливают по пробиркам по 1 мл и добавляют в определенных концентрациях препараты составов 1, 4, 6. Для лучшего диспергирования обрабатывают водные растворы препаратов ультразвуком (установка УЗДН 22 кГц, 150 Вт).
Инкубацию культуры E.coli с препаратом проводят при постоянном встряхивании при 37оС.
После инкубации с помощью 0,14 М физ. раствора разводят суспензию в пробирках в 2000 раз.
Отбирают из каждой пробирки по 10 мл смеси, наносят ее на чашки Петри, залитые агаризованной питательной средой, и растирают с помощью шпателя.
Состав агаризованной среды: Триптон 10 г Дрож. экстракт 5 г NaCl 5 г глюкоза 1 г 1 н. NaOH 1 мл агар 5 г вода 1000 мл
Жизнеспособность клеток определяли по количеству колоний, выросших через 24 ч при 37оС.
Результаты исследований представлены в табл.3.
Преимущества заявляемого состава противоопухолевого препарата по сравнению с прототипом заключаются в следующем.
Введение в состав препарата двуокиси кремнезема с привитыми бутанольными радикалами дает возможность регулировать количество введения активного компонента - тиофосфамида, что сводит к минимуму негативный побочный эффект, т.е. влияние тиофосфамида на здоровые ткани.
Возможность оптимального выбора параметров состава препарата позволяет повышать эффективность состава, уменьшив при этом его дозу.
В перспективе возможно введение в состав препарата биологически активных веществ противоопухолевого действия, которые ранее вообще невозможно было использовать для лечебных целей.
| название | год | авторы | номер документа |
|---|---|---|---|
| ВЕЩЕСТВО "СИЛЛАРД", ОБЛАДАЮЩЕЕ АДАПТОГЕННОЙ АКТИВНОСТЬЮ | 1992 |
|
RU2038085C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОЛОГИЧЕСКИ АКТИВНОГО СРЕДСТВА НА ОСНОВЕ БЕРЕЗОВОГО СОКА | 1991 |
|
RU2019184C1 |
| ПРОТИВООПУХОЛЕВОЕ СРЕДСТВО ДЛЯ МЕСТНОГО ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ | 1992 |
|
RU2077885C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПЛЕКСОВ НА ОСНОВЕ АЦИКЛИЧЕСКИХ АМИНОВ, ОБЛАДАЮЩИХ РАДИОПРОТЕКТОРНЫМИ СВОЙСТВАМИ | 1991 |
|
RU2032660C1 |
| ИЗОТИУРОНИОАЗИНЫ, ПРОЯВЛЯЮЩИЕ ПРОТИВООПУХОЛЕВУЮ АКТИВНОСТЬ | 1991 |
|
RU2032676C1 |
| ТЕТРАЭТИЛ-2-(2,2,6,6-ТЕТРАМЕТИЛПИПЕРИДИН-4-ИЛАМИНО)-ЭТИЛЕН-1,1-БИСФОСФОНАТ, ОБЛАДАЮЩИЙ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2013 |
|
RU2506085C1 |
| МОДИФИКАТОР ДЛЯ ПРОТИВООПУХОЛЕВОЙ ТЕРАПИИ | 1995 |
|
RU2111750C1 |
| СПОСОБ ЛЕЧЕНИЯ ГНОЙНЫХ ЗАБОЛЕВАНИЙ ЛЕГКИХ И ПЛЕВРЫ | 1992 |
|
RU2064799C1 |
| БРОМИД 1-ГЕКСАДЕЦИЛ-R-(-)-3-ОКСИ-1-АЗОНИАБИЦИКЛО[2.2.2]ОКТАНА - ИММУНОМОДУЛЯТОР С ПРОТИВООПУХОЛЕВЫМИ, БАКТЕРИОСТАТИЧЕСКИМИ И АНТИАГРЕГАНТНЫМИ СВОЙСТВАМИ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2005 |
|
RU2296761C2 |
| СПОСОБ ЛЕЧЕНИЯ ГНОЙНОГО МЕДИАСТЕНИТА | 1992 |
|
RU2064798C1 |
Изобретение относится к медицине, в частности к биологически активным веществам, обладающим бактериостатическими и цитотоксическими свойствами. Цель - повышение эффективности действия при уменьшении дозы и ослабление токсического воздействия на здоровые ткани. Предлагаемое вещество, обладающее противоопухолевым действием, содержит тиофосфамид и диоксид кремния с привитыми спиртовыми радикалами при следующем соотношении компонентов, мас. ч. : тиофосфамид 10 - 50; двуокись кремния с привитыми спиртовыми радикалами 50 - 90. 3 табл.
ВЕЩЕСТВО, ОБЛАДАЮЩЕЕ ПРОТИВООПУХОЛЕВЫМ ДЕЙСТВИЕМ, содержащее тиофосфамид, отличающееся тем, что, с целью повышения эффективности действия при уменьшении дозы и ослабления токсического воздействия на здоровые ткани, оно дополнительно содержит высокодисперсный диоксид кремния с привитыми спиртовыми радикалами при следующем соотношении компонентов, мас.ч.:
Тиофосфамид 10 - 50
Диоксид кремния с привитыми спиртовыми радикалами 50 - 90
| Информационное письмо по противоопухолевым препаратам | |||
| Киев, ТПУ, 1982, N 2, с.38-39. |
Авторы
Даты
1994-10-30—Публикация
1987-11-30—Подача