Изобретение относится к области органической химии, конкретно к производным β -аминоизомасляной кислоты - высшим N-ацил-N,N1,N2- трифенил- β -аминоизобутириламидиний хлоридам (гидрохлоридам высших N-ацил-N, N1, N2-трифенил- β -аминоизобутириламидинов) общей ф-лы I, обладающим противовирусной активностью в отношении вируса гриппа А(Н3N2).
P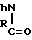 -CH
-CH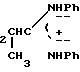
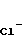 (I) (I)
(I) (I)
Заявляемые соединения формулы (I) могут найти применение в медицине в качестве антивирусного препарата, а также в биологии для изучения механизма противовирусного действия.
Соединения формулы (I) и их биологические свойства в литературе не описаны.
Известен лекарственный препарат ремантадин, применяющийся в медицинской практике для лечения гриппа [1].
Известно, что ряд природных ацилированных по β -аминогруппе β -аланинамидинов, таких как амидиномицин (II) [2,3]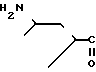
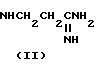 и ноформицин (III) [2,4,5],
и ноформицин (III) [2,4,5],
H2N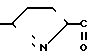 NH
NH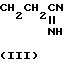 H2 обладает противовирусной активностью в отношении вирусов парагриппа тип 3, гриппа свиней, полиомиелита SК, человеческого риновируса N 2, риновируса лошадей, некоторых причинных вирусов животных. Однако информации об антивирусной активности соединений (II), (III) в отношении вирусов гриппа человека А(Н3N2) не имеется.
H2 обладает противовирусной активностью в отношении вирусов парагриппа тип 3, гриппа свиней, полиомиелита SК, человеческого риновируса N 2, риновируса лошадей, некоторых причинных вирусов животных. Однако информации об антивирусной активности соединений (II), (III) в отношении вирусов гриппа человека А(Н3N2) не имеется.
Наиболее близким по структуре к заявляемым соединениям (I) являются N-стеароил- β -аланинамидин (IV) [6]
C17H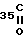 N
N CH
CH H2 и N-бензоил- β-аланинамидиний хлорид (V) [7].
H2 и N-бензоил- β-аланинамидиний хлорид (V) [7].
Ph 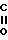 NHCH2CH
NHCH2CH
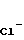 Сравнительно близким по структуре к заявляемым веществам (I) является и N-бензоил-N,N1,N2-трифенилглицинамидиний хлорид (VI) [8] .
Сравнительно близким по структуре к заявляемым веществам (I) является и N-бензоил-N,N1,N2-трифенилглицинамидиний хлорид (VI) [8] .
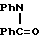 CH2C
CH2C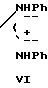

Однако об антивирусной активности соединений (IV)-(VI) сведений не имеется.
Задачей изобретения является синтез производных амидинов β -аминокислот, обладающих высокой антивирусной активностью в отношении вирусов гриппа А(Н3N2).
Поставленная задача достигается высшими N-ацил-N,N1,N2-трифенил- β -аминоизобутириламидиний хлоридами формулы (I), которые обладают эффективным противовирусным действием.
Заявляемые соединения формулы (I) получают ацилированием N1,N2- дифенил- β-N-фениламиноизобутириламидина хлорангидридами высших карбоновых кислот.
П р и м е р 1. N-пеларгоноил-N,N1,N2-трифенил- β -аминоизобутириламидиний хлорид (Iа, R=C8H17).
К раствору 2,0 г (0,006 моль) N1,N2-дифенил- β -N- фениламиноизобутириламидина в 30 мл безводного серного эфира при перемешивании прибавляют 1,07 г (0,006 моля) пеларгоноилхлорида в 20 мл безводного эфира. На следующий день отфильтровывают осадок аналитически чистого продукта, выход - 2,5 г (81% ), т. пл. 159-160оС. ИК-спектр (в вазелиновом масле), ν, см-1: 1496, 1576, 1597 (С=С) аром., 1615 (N 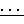
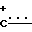 N) , 1661(С=О), 2400-2800 (
N) , 1661(С=О), 2400-2800 (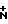 -Н). УФ-спектр (в МеОН), λмакс., нм (lg ε ):263,5 (4,20). Спектр ПМР (CDCl3), δ, м. д. (J, Гц): 0,82 т (3Н,
-Н). УФ-спектр (в МеОН), λмакс., нм (lg ε ):263,5 (4,20). Спектр ПМР (CDCl3), δ, м. д. (J, Гц): 0,82 т (3Н, 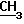 СН2, 5); 1,13 ш.с. (12Н, (СН2)6); 1,47 д (3Н,
СН2, 5); 1,13 ш.с. (12Н, (СН2)6); 1,47 д (3Н,  СН, 6); 1,93 кв (2Н, СН2С(О),7) 3,33-3,97 м (2Н, СН2СН); 4,58-5,23 м (1Н, СН), 6,77 ш. с. (10Н, 2Рh); 7,25 ш.с. (5Н, Ph); 12,13 ш.с. (2Н, 2
СН, 6); 1,93 кв (2Н, СН2С(О),7) 3,33-3,97 м (2Н, СН2СН); 4,58-5,23 м (1Н, СН), 6,77 ш. с. (10Н, 2Рh); 7,25 ш.с. (5Н, Ph); 12,13 ш.с. (2Н, 2 H). Найдено,%: С 73,98; Н 8,07; Сl 7,28; N 8,44.
H). Найдено,%: С 73,98; Н 8,07; Сl 7,28; N 8,44.
С31Н40ClN3O.
Вычислено, %: С 73,59; Н 7,91; Сl 7,02; N 8,31.
П р и м е р 2. N-ундеканоил-N,N1,N2-трифенил- β - аминоизобутириламидиний хлорид (Iб, R=С10Н21) получают аналогично примеру 1 из 2,1 г (0,0063 моль) N1,N2-дифенил- β -N- фениламиноизобутириламидина и 1,3 г (0,0063 моль) ундеканоилхлорида, выход 94%, т.пл. 166-168o С.
ИК-спектр (в вазелиновом масле), ν, см-1: 1497, 1574, 1597 (С=С) аром., 1613 (N 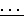
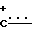 N), 1662 (С=О), 2400-2800 (
N), 1662 (С=О), 2400-2800 (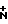 -Н). УФ-спектр (в МеОН), λмакс., нм (lg ε):263,5 (4,19).
-Н). УФ-спектр (в МеОН), λмакс., нм (lg ε):263,5 (4,19).
Спектр ПМР (CDCl3) δ, м.д. ( J, Гц): 0,84 т (3Н,  СН2, 5); 1,15 ш.с. (16Н, (СН2)8); 1,48д (3Н,
СН2, 5); 1,15 ш.с. (16Н, (СН2)8); 1,48д (3Н,  СН, 6); 1,92 кв (2Н, СН2С(О),7); 3,33-3,95 м (2Н, СН2СН); 4,58-5,23 м (1Н, СН); 6,72 ш.с. (10Н, 2Ph); 7,25 ш.с (5Н, Ph); 12,15 ш.с. (2Н, 2
СН, 6); 1,92 кв (2Н, СН2С(О),7); 3,33-3,95 м (2Н, СН2СН); 4,58-5,23 м (1Н, СН); 6,72 ш.с. (10Н, 2Ph); 7,25 ш.с (5Н, Ph); 12,15 ш.с. (2Н, 2 Н).
Н).
Найдено, %: С 74,23; Н 8,47; Cl 7,01; N 8,28.
С33Н44ClN3O.
Вычислено, %: С 74,23; Н 8,25; Cl 6,65; N 7,87.
Заявляемые соединения (I) представляют собой мелкокристаллические вещества, малорастворимые в воде, хорошо растворимые в спиртах, диполярных апротонных растворителях, хлороформе.
Изучение антивирусной активности
Исследование антивирусных свойств соединений проводили по способности подавлять репродукцию вируса гриппа А/Ленинград 34/72 (Н3N2). Эксперименты проводили на переживающих фрагментах хорионаллантоисной оболочки куриного эмбриона (ХАО КЭ).
Для определения токсичности соединений для клеток ХАО навески последовательно разводили с коэффициентом -2 в растворе Хенкса, разливали по 0,5 мл в лунки пластиковой панели и вносили фрагменты ХАО. Состояние клеток определяли через 48 ч инкубации при 37оС. Минимальной токсической дозой (МТД) считали минимальную концентрацию, вызывающую гибель клеток в трех и более лунках.
В работе использовали аллантоисный вирус, прошедший пассаж на 10-11-суточных куриных эмбрионах, титр вируса на куриных эмбрионах составил 10-8, на клетках ХАО -10-6, титр гемаглютинина вируса равнялся 1:2048.
Клетки заражали 1, 10 и 100 дозами вируса. Затем вносили различные разведения соединений, меньшие МТД, для клеток ХАО. Через 48 ч инкубации при 37оС определяли наличие жизнеспособных клеток и титр вируса в культуральной среде (раствор Хенкса) реакцией гемаглютинации с 1%-ной взвесью эритроцитов кур.
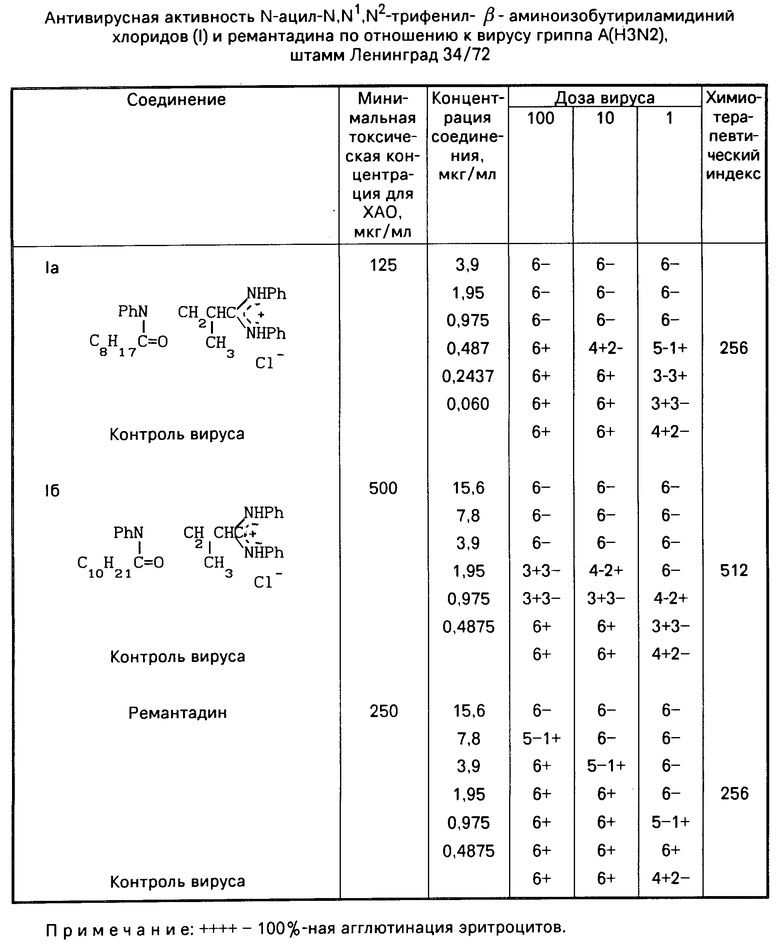
Проведенные исследования показали, что соединение Iа обладало минимальной токсичностью для клеток ХАО, равной 125 мкг/мл. В концентрации 0,487 мкг/мл задерживало репродукцию 1 дозы вируса гриппа, при заражении 100 дозами этот эффект наблюдался при внесении в среду 0,975 мкг/мл. Химиотерапевтический индекс соединения равнялся 256 (таблица). МТД для клеток ХАО соединения Iб равнялась 500 мкг/мл. Соединение задерживало размножение вируса при заражении клеток 100 дозами в концентрации 3,9 мкг/мл, при заражении 1 дозой в концентрации 0,975 мкг/мл (таблица). В качестве эталонного объекта использовали препарат ремантадин, используемый в терапии и профилактике гриппозной инфекции. МТД ремантадина для клеток ХАО равнялась 250 мкг/мл. Содержание Iб было в 2 раза менее токсичным для клеток и проявляло выраженный эффект, в 2 раза превышающий активность базового препарата. Антивирусная активность соединения Iа была аналогичной активности ремантадина (таблица).
| название | год | авторы | номер документа |
|---|---|---|---|
| ВЫСШИЕ N-АЦИЛ-N, N -ТРИФЕНИЛ- β - АМИНОИЗОБУТИРИЛАМИДИНИЙ ХЛОРИДЫ, ОБЛАДАЮЩИЕ СПОСОБНОСТЬЮ ИНГИБИРОВАТЬ ХИМИЧЕСКУЮ КОРРОЗИЮ МЕТАЛЛА В СЕРОВОДОРОДСОДЕРЖАЩИХ МИНЕРАЛИЗОВАННЫХ СРЕДАХ | 1992 |
|
RU2024499C1 |
| 3-Азидо-4-окси-1(6)-эпоксиэтилциклогексан,ОблАдАющий пРОТиВОВиРуСНыМ дЕйСТВиЕМ | 1978 |
|
SU738334A1 |
| Способ получения N-(1-цианобензил)-амидофосфита или -фосфонита общей формулы | 1983 |
|
SU1143041A1 |
| ГЛУТАМАТ ГИДРАЗИДА N-АМИНОМЕТИЛБЕНЗОЙНОЙ КИСЛОТЫ, ОБЛАДАЮЩИЙ ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ ВИРУСА ГРИППА СЕРОТИПОВ А И В | 1988 |
|
SU1531420A1 |
| ИМИНОПРОИЗВОДНЫЕ КАМФОРЫ - ЭФФЕКТИВНЫЕ ИНГИБИТОРЫ РЕПРОДУКЦИИ ВИРУСА ГРИППА (штамм A/California/07/09 (H1N1)pdm09) | 2014 |
|
RU2554934C1 |
| ПРИМЕНЕНИЕ (1S,3aR,4R,7aS)-N-(2,2,4,7a-ТЕТРАМЕТИЛОКТАГИДРО-1,4-ЭТАНОИНДЕН-3а-ИЛ)-АЦЕТАМИДА В КАЧЕСТВЕ ИНГИБИТОРА РЕПРОДУКЦИИ ВИРУСА ГРИППА | 2016 |
|
RU2616255C1 |
| N'-{N-[3-ОКСО-20(29)-ЛУПЕН-28-ОИЛ]-9-АМИНОНОНАНОИЛ}-3-АМИНО-3-ФЕНИЛПРОПИО НОВАЯ КИСЛОТА, ОБЛАДАЮЩАЯ ИММУНОСТИМУЛИРУЮЩЕЙ И ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ | 2002 |
|
RU2211843C1 |
| ПРОИЗВОДНЫЕ 5H-ПИРАНО[2,3-D:6,5-D']ДИПИРИМИДИНА, ОБЛАДАЮЩИЕ АНТИМИКРОБНЫМ, ПРОТИВОВИРУСНЫМ И ИММУНОМОДУЛИРУЮЩИМ ДЕЙСТВИЕМ | 1997 |
|
RU2188201C2 |
| ВЕЩЕСТВО С ПРОТИВОВИРУСНОЙ И АНТИБАКТЕРИАЛЬНОЙ АКТИВНОСТЬЮ НА ОСНОВЕ ПРОИЗВОДНЫХ 2,8-ДИТИОКСО-1H-ПИРАНО[2,3-D, 6,5-D`] ДИПИРИМИДИНА И ИХ 10-АЗА-АНАЛОГОВ | 2003 |
|
RU2246496C1 |
| 3-Бутилтио-1-(бета-D-2-дезоксирибофуранозил)-5-фенил-(4Н)-1,2,4-триазол, синтез, противогерпесвирусное действие | 2023 |
|
RU2815137C1 |
Использование: в медицине, в качестве противовирусного средства. Сущность изобретения - продукты ф-лы PhN(C(R)=O)CH2C(CH3)H-CNHPh(+NHPh)Cl- . БФ C31H40ClN30 ; т.пл. 159-160°С. БФ C33H44ClN30 ; т.пл. 166-168°С. Реагент 1: ацилхлориды. Реагент 2: N, N1 , N2 -трифенил- β - амминоизобутириламидин. Условия реакции: безводный серный эфир. 1 табл.
Высшие N -ацил- N, N1, N2 - трифенил- β -аминоизобутириламидиний хлориды общей формулы
P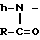 CH
CH


где R = C8H17, C10H21,
обладающие противовирусной активностью.
| Коршин Э.Е., Соболева Г.И., Левин Я.А., Захарова Л.Г., Литвинов И.А., Наумов В.А., Подвальный Е.А., Ефремов Ю.Я., - Ж.орган.химии Рег | |||
| Приспособление с иглой для прочистки кухонь типа "Примус" | 1923 |
|
SU40A1 |
Авторы
Даты
1994-12-15—Публикация
1992-03-17—Подача