(54) 3-АЗИДО-4-О ОБЛАДАЮЩИМИ Изобретение относится к новым х мическим биологически активным соединениям, в частности к 3-азидо -4-ОКСИ-1(6)-эпоксиэтилциклогексан формулы СН-СН2 Такое соединение обладает противовирусной активностью и может быть использовано в качестве противовирусного средства для лечения и профилактики гриппа. Наиболее близким по структуре к предлагаемому соединению является фенила3ид, обладающий жаропонижающими свойствами. Однако такое соединение не проявляет противовирусных свойств. Цель изобретения - расширение ассортимента соединений, воздейству щих на живой организм, путем получе ния 3-азидо-4-окси-1(6)-эпоксиэтилциклогексана, обладающего антивирус ными свойствами. Это достигается тем, что соединение получают взаимодейтсвием моноокиси винилциклогексена с азидом 6}-ЭПОКСИЭТИЛЦИКЛОГЕКей -, ОВИРУСНЫМ ДЕЙСТВИЕМ }В П Т Б -nsTR ог 11:рТПГ ФУПЙ ;UyaLrrjt , натрия с последующим эпоксидированием продукта реакции . или взаимодействием диокиси винилциклогексена с азидом натрия в мягких условиях по известному способу. Получают 3-азидо-4-окси-1(6)-эпоксидиклогексан и испытывают его биологические свойства следующим образом. Пример 1. З-азидо-4-окси-1(6)-эпоксиэтилциклогексан. а) 3-азидо-4-окси-1(6)-винилциклогексан. К 10 г (0,08 моля) моноокиси винилциклогексена добавляют 8 г (0,12 моля) NaNj в 50 мл воды. Смесь перемешивают 5 ч при 100°С, затем экстрагируют эфиром. После обработки получают 6 г (45%) -. . ., (0,08 мм) ; продукта с т.кип, .О, , j20 ,5051, ,0834, ИК-спектр ( сГ, см-): 2100 (); 1640 () 3400 (ОН). Спектр ПМР (сГ , м.д.): 3,53 (Н при C-N), 4,85-6,03 (винильные протоны), Найдено %: С 57,55; Н 7,93; N 24,57. вычислено, % С 57,47, Н 7,84; N 25,12. б) 3-аэидо-4-окси-1(6)-эпоксиэтил циклогексан. К 3,3 г (О,-О2 моля) 3-азидо-4-окси-.1 (6) -винилциклогексана, растворенному в 8 мл абсолютного серного эфира (0,5 л эфира на вещества), приливают 4 tin (0,023 моля) 50,5%-ной гил.роперекиси ацетила. После двухнедельного стояния при кон натной температуре реакционную смесь обрабатывают 7%-ньм раствором едкого кали, промывают водой и сушат над сульфатом магния. После раз гонки получают 2,23 г (45%) продукта с т.кип. 94-95 с (0,05 мм): п| 1,5103; d2°I,1930o ИК-спектр () civf 2100 (WSN), 3050 (эпокси- CHgl , (ОН), Спектр ПМР ( , м,ц,): 2,41-2,76 (эпокси-СНо), 3,51 к 3,60 (Н при C-N и Н прн ). Найдено, %г С 53,06 Н 7,28; N 22,60 С 52р44; Н 7,15; Вычислено, N 22,92 Пример 2 3-азидо-4 окс.и--1(6)-эпоксиэтилциклогексан, К 14„г (Qfl моля) диокиси ВКНИЛЦ логексана добавляют 8,5 г (0,1.3 мол NaN в 25 мл воды. перемеитивают 6 ч при 0-10°Cf затем экстраги руют эфиром„ После обычной обработни и разгонки получают 7,4 г(50%) непрореагировавшей диокиси и 4 г (22%) продукта с т,кип, 93 94с (0,05 мм); 11 3 15100,- ,193G, ИКспектр, (л г см): 2100 (N S Iv) , 305 (апокси-СН) 3400 (ОН), Спектр ПйР (cf , м.д,); 2,38-2,75 (эпокси-СНа) , 3,53 и 3,60 (Н при C--N и Н при СНайдено, %; С 53,02; Н 7,12 N 22,78. Вычислено, %5 С 52,44; Н 7,15; N 22,92. Испытания противовирусной активн ти проводят в отношении вируса гриппа АЗ. (wTaMJvi Ленинград 34/74), полученного из всесоюзного НИР гри.п Репродукцию вируса гриппа и испытания противовирусной активности проводят на переживающих фрагментах хорионаллантоисной оболочки (ХА.О) куриного эмбр.иона, . Испытания проводят с концентрациями соединений меньшими , чем минимальная токсическая доза Испыта ния ведут с 1,10,. 100 дозами зирус Наличие вируса определяют по реакц гемагглютинации 1%-ной взвеси кури эритроцитов, Титрование рабочей дозы вирусаГотовят ряд разведений вируса с (коэффициентом 10 на растззоре Хэнкс В лунки панели разливают по 0,5 мл раствора Хэнкса и в каждую лункустерильно вносят по одному фрагмен ХАО. По 0,2 мл каждого разведения лантоисного вируса вносят в 6 луно панели. Панели закрьшают стерильны теклянными пластинами д.)Я герметичости заслеивают лейкопластырем и омешают при 37®С в термостат. Через 8 V. инкуб.ации проверяю ; состояние AOs У переживаюш.их кусочков ХлО чет-о обозначены блестнщке кровег осные ос;уды„ Раствор Хэнксе прозрачен и озового цвета, Валкчье вируса з ультуре определяют пс реакции геаплютинации с 1%-ноз взвесью кури-ых зритроцитов, Наибольшее азведение вируса , ;г:де наблюдается емагглютинация в т-рех к более лунах, считают 1 дозой вируса.., I доза 3HPVca в наших опытах была в разведв - Т НИИ 10 ,Определение токсичности для клеток Для определения токсичности для клеток ХАО соединение растворяют Б Т1-шенгликоле,- исходна.я концентрация этой кокцег1трацин на састЕоре Хэнкса раэве.пенил соединения, содержащие мкг/глпг 250, 25 62,5, 31,5, 15,6, 7,8„ ,цое разведение соединения по 0,5 д-ш разливают в 6 .гунок, в котсрЬЗ вносят по кусочку ХАО, Этиленгликоль токси-Еек для ХАО в кОнцентраЦии 50000 мкг/чл Через 48 ч инкубации гфовериют состояние ободочек , Минима.льной токсической дозол (МТД) счтнают ту наименьшую концентрацию, которая вызывает гибель клеток ХАО в трех и более лукках. Испытания противовирусной активности проводят с концектрацияки соединений, меньшими МТД„ Противовирусная активность соединакия гюдтзерхпается в повторных опытах Каждую к он цен-.грацию соединения разливают Го 0,5 мл Б b лунок, куда йО, Через 1 ч вносят по 1 фраг1 1еиту контакта пр-и комна: н-o теклературе дoбaвляЮlT в объеме О, MJ-I разведеН1у1 1--г вируса 10-,- 10 Калсдым ра-3веде.ни-эы вируса заражают кусочки ХАО в шести лунках,. Через 48 ч инкубации прн ЗТ-С .ч.ки ХАО вынимг1ют и npocThiaTpHBaicTr Реакцию г-емагглютинд1дии с--гавя-г с 1%-ной взвесьБЭ куриных эри-троцитов, которую добавляют по 0,5 мл Б каждуЮ яунку В -rex же условия.х ста:зят контрольные опыты с ремантадином,. Соединения бы,аи . токсичны для клеток Х-АО в к он центра ци.я,:-: 500 мкг/мл (-СМ „ табЛс) .. Исс.педованное соединение задерживает репродукцию вируса при заражении 100 дозами вируса клеток ХАО куриного эмбриона при концентрации 125 мкг/кш и одной дозой при концентрации 15,6 мк.г/,мл (ск, таб.л.) Минимальная концентрация- задерживающая репродукцию вируса при заражении 1 дозой, была в 32 раза -меньше минимальной токсической ,дозы, т,е„ терапевтический нидекс равен 32,
В качестве стандарта был. взят ремантадин, который используется в медицинской практике для профилактики гриппа.
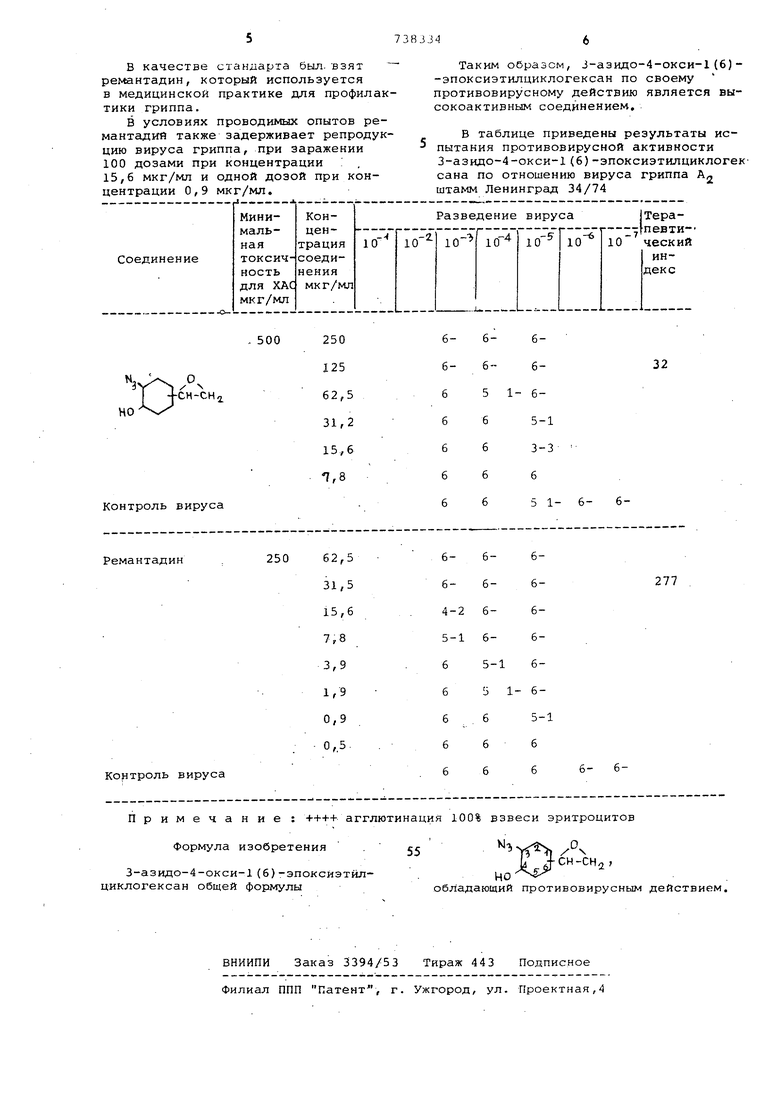
В условиях проводимых опытов ремантадий также задерживает репродукцию вируса гриппа, при заражении 100 дозами при концентрации 15,6 мкг/мл и одной дозой при концентрации 0,9 мкг/мл.
Таким образом, 3-азидо-4-окси-1(6)-эпоксиэтилциклогексан по своему противовирусному действию является высокоактивным соединением,
В таблице приведены результаты испытания противовирусной активности 3-азидо-4-окси-1(6)-эпоксиэтнлциклогексана по отношению вируса гриппа А„ штамм Ленинград 34/74

| название | год | авторы | номер документа |
|---|---|---|---|
| ВЫСШИЕ N-АЦИЛ-N, N -ТРИФЕНИЛ- β -АМИНОИЗОБУТИРИЛАМИДИНИЙ ХЛОРИДЫ, ОБЛАДАЮЩИЕ ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ | 1992 |
|
RU2024500C1 |
| Способ получения N-(1-цианобензил)-амидофосфита или -фосфонита общей формулы | 1983 |
|
SU1143041A1 |
| ПРОТИВОВИРУСНОЕ, ИММУНОМОДУЛИРУЮЩЕЕ СРЕДСТВО | 2001 |
|
RU2202547C2 |
| НАТРИЕВАЯ СОЛЬ 5-МЕТИЛ-6-НИТРО-1,2,4,-ТРИАЗОЛО[1,5-a]ПИРИМИДИН-7-ОНА ДИГИДРАТ | 2006 |
|
RU2330036C1 |
| ГЛУТАМАТ ЭТИЛОВОГО ЭФИРА АМБЕНА, ОБЛАДАЮЩИЙ ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ ВИРУСОВ ГРИППА СЕРОТИПОВ A И B | 1990 |
|
RU2030393C1 |
| 3,3-Ди-трет-бутил-6-метил-5-оксо-2,3,4,5-тетра-гидро-1,2,4,3- @ -триазафосфориний хлорид, обладающий противовирусной активностью в отношении вируса везикулярного стоматита | 1986 |
|
SU1433004A1 |
| 3-ЗАМЕЩЕННЫЕ 6-(МЕТОКСИКАРБОНИЛ)УМБЕЛЛИФЕРОНЫ, ОБЛАДАЮЩИЕ ИНГИБИРУЮЩЕЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ ВИРУСА ГРИППА A/Н1N1 | 2024 |
|
RU2838462C1 |
| ГЛУТАМАТ ГИДРАЗИДА N-АМИНОМЕТИЛБЕНЗОЙНОЙ КИСЛОТЫ, ОБЛАДАЮЩИЙ ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ ВИРУСА ГРИППА СЕРОТИПОВ А И В | 1988 |
|
SU1531420A1 |
| Йодметилат 3е-ацетокси-1е, за-диметил-6ео-бензилоксифенил-4-пиперидон, проявляющий противовирусную активность | 1975 |
|
SU536676A1 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОВИРУСНЫМ ДЕЙСТВИЕМ И СОДЕРЖАЩЕЕ 2-МЕТИЛТИО-5-МЕТИЛ-6-НИТРО-1,2,4-ТРИАЗОЛО[1,5-a]ПИРИМИДИН-7(3Н)-ОН | 2007 |
|
RU2365591C2 |


Авторы
Даты
1981-06-07—Публикация
1978-11-28—Подача