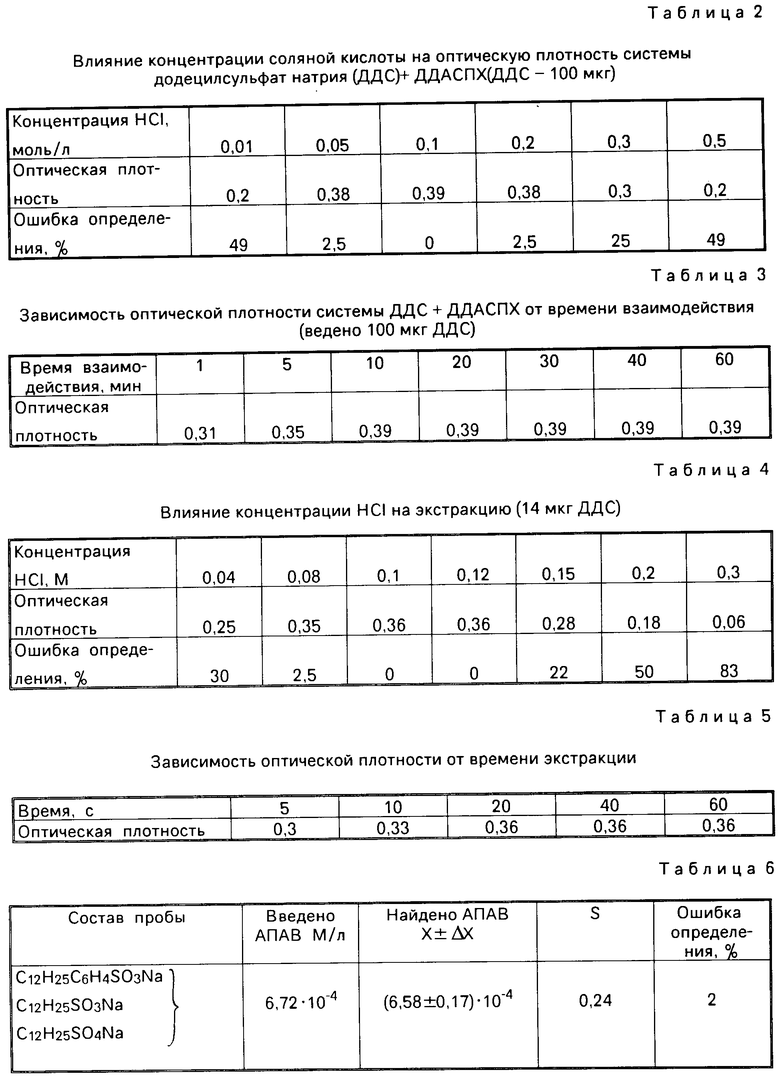
Изобретение относится к аналитической химии, конкретно к новому химическому соединению 2,6-дифенил-4-(4-диметиламиностирил)пирилия хлориду формулы I
Cl-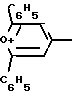 CH= CH
CH= CH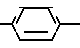 N(CH3)2 используемого в качестве органического реагента для количественного фотометрического определения анионных поверхностно-активных веществ (АПАВ).
N(CH3)2 используемого в качестве органического реагента для количественного фотометрического определения анионных поверхностно-активных веществ (АПАВ).
Соединение формулы I может найти применение при определении больших и малых количеств АПАВ в различных технических и природных материалах и объектах (сточных водах, промышленных ПАВ, биологических материалах).
Заявляемое соединение получено впервые и в литературе не описано.
Известны соединения различных классов, используемые в качестве реагентов для фотометрического определения АПАВ [1,2]: тиазиновые красители (метиленовый синий, Азур А), трифенилметановые красители (метиловый зеленый, бриллиантовый зеленый), соединения, содержащие положительно заряженный четвертичный атом азота (аммонийные, пиридиниевые, индолиниевые соединения) и другие.
Все известные реагенты, в основном, использованы для определения додецилсульфата натрия и додецилбензолсульфоната натрия в природных и сточных водах.
Наиболее часто для определения анионных ПАВ используется метиленовый синий.
Известен наиболее близкий по структуре реагент - 2,6-дифенил-4-(4-диметиламиностирил)тиопирилия хлорид (/"бирюзовый") формулы
Cl-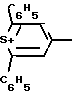 CH= CH
CH= CH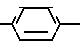 N(CH3)2 применяемый для фотометрического определения суммы алкилсульфатов в минерализованных водах [4].
N(CH3)2 применяемый для фотометрического определения суммы алкилсульфатов в минерализованных водах [4].
Недостатком данного реагента является низкая чувствительность реакции ( ε= 3 ˙104) и то, что круг определяемых ПАВ ограничен только алкилсульфатами.
В качестве базового объекта выбран метиленовый синий [2,5].
Недостатками указанного реагента являются невысокая избирательность - на экстракцию влияет значительное число органических и неорганических ионов и веществ; низкая степень экстракции (84%); необходимость проведения трехкратной экстракции, что увеличивает трудоемкость и время анализа; необходимость применения нейтрального и кислого растворов реагента (6-кратная экстракция), что еще больше усложняет анализ.
Цель изобретения - упрощение и ускорение анализа, повышение его избирательности, расширение круга определяемых АПАВ, диапазона определяемых концентраций.
Поставленная цель достигается использованием нового соединения 2,6-дифенил-4-(4-диметиламиностирил)пирилия хлорида в качестве реагента для количественного фотометрического определения анионных поверхностно-активных веществ.
П р и м е р 1. Синтез 2,6-дифенил-4-(4-диметиламиностирил)пирилия хлорида.
В круглодонной колбе, снабженной обратным холодильником, смесь 0,31 г (0,0011 моля) 4-метил-2,6-дифенилпирилий хлорида [3] и 0,23 г (0,0016 моля) п-диметиламинобензальдегида в среде уксусного ангидрида (3,8 мл) нагревают при 106-110оС в течение 35 ч. Затем реакционную смесь выдерживают при комнатной температуре 2 сут.
После этого выливают в 30 мл сухого эфира. Выпавший осадок отфильтровывают, очищают путем переосаждения эфиром из хлороформа. Выход составляет 4,5 г (90% от теоретического). Кристаллы темно-синего цвета. Т.пл. 228оС (разложение).
Найдено,%: С 78,18; Н 5,75; Cl 8,32; N 3,45.
C27H24СlO.
Вычислено,%: C 78,36; H 5,80; Cl 8,60; N 3,39.
Электронный спектр в этаноле:
λ1= 400 нм, ε1 = 6,6˙103.
λ2= 637 нм , ε2= 3,03 ˙104.
П р и м е р 2. Выявление оптимальных условий взаимодействия.
Установлено, что взаимодействие 2,6-дифенил-4(4-диметиламиностирил)пирилия хлорида (ДДАСПХ) с АПАВ происходит как в водной среде, так и при экстракции толуолом, что позволило разработать безэкстракционный способ для определения больших количеств АПАВ и экстракционный для определения микроколичеств АПАВ. Найдены оптимальные условия для обоих вариантов. Для установления оптимальных условий выбран один из представителей АПАВ-додецилсульфат натрия (ДДС). В табл.1,2,3 (безэкстракционный вариант) приведены данные для безэкстракционного способа. При взаимодействии ДДАСПХ с АПАВ образуются крупные частицы, для удержания которых необходим стабилизатор. Из табл.1 видно, что лучшим стабилизатором является поливиниловый спирт.
Для создания необходимой кислотности среды применялась соляная кислота.
Оптимальная кислотность среды 0,1 М, допустимый предел достаточно широк 0,05-0,2М HCl, что позволяет строго не выдерживать концентрацию HCl на уровне 0,1М.
Таким образом окраска развивается 10 минут и остается стабильной в течение 1 час.
В водной среде абсорбционная кривая ассоциата имеет два максимума поглощения, λ1 = 570 нм и λ2= 725 нм, в органическом растворителе λ1= 590 нм и λ2 = 640-650 нм.
Из табл.1,2,3 видно, что для безэкстракционного варианта выбраны следующие оптимальные условия:
кислотность среды 0,1М HCl (допустимые пределы 0,05-0,2М)
стабилизатор - 40%-ный раствор поливинилового спирта
время взаимодействия 10 мин
Экстракционный вариант.
При подборе оптимальных условиях для экстракционного способа варьировались следующие параметры: соотношение водной и органической фаз, время экстракции возможность экстракции различными растворителями, кислотность среды. Данные представлены в табл.4.5.
Оптимальная концентрация cоляной киcлоты 0,08-0,12М.
Изучение влияния объема водной фазы на экстракцию ассоциатов показало, что прямолинейность градуировочной характеристики в пределах 3-30 мкг ДДС в 10 мл экстракта наблюдается при любом объеме водной фазы от 10 до 500 мл.
Ассоциат практически полностью переходит в экстракт в течение 20 с.
Выбор органического растворителя проводился из четырех опробованных реагентов (толуол, хлороформ, изоамиловый спирт, четыреххлористый углерод). Лучшим оказался толуол.
Таким образом, для экстракционного способа выбраны следующие оптимальные условия:
Кислотность среды 0,08-0,12М HCl (лучше 0,1М)
Экстрагент - толуол
Время экстракции 0,5-1 мин
Объем водной фазы 10-500 мл
П р и м е р 3. Определение различных видов анионных поверхностно-активных веществ.
Готовят 5˙10-5 М растворы различных видов анионных ПАВ:
Децилсульфат натрия C10H21SO4Na
Додецилсульфат натрия C12H25SO4Na
Тридецилсульфат натрия C13H27SO4Na
Тетрадецилсульфат натрия C14H29SO4Na
Гексадецилсульфат натрия C16H33CO4Na
Додецилсульфонат натрия C12H25SO3Na
Додецилбензолсульфонат натрия C12H25C6H4SO3Na
Додециловый эфир сульфоянтарной кислоты, динатриевая соль CH3-(CH2)11-COO-CH2-CH-SO3Na
|
COONa
Построение градуировочной характеристики.
В делительную воронку помещают 20 мл 0,1М соляной кислоты, 0; 0,25; 0,5; 0,75; 1,0; 1,25; 1,5; 1,75 мл любого из вышеуказанного 5 ˙10-5М раствора АПАВ; 0,5 мл 10-3М спиртового раствора ДДАСПХ, 10 мл толуола и экстрагируют 1 минуту, толуольный экстракт фотометрируют на КФК-2 при λ= 590 нм, l = 2 см. По полученным данным оптической плотности строят градуировочный график. Для всех вышеперечисленных соединений прямолинейность градуировочного графика соблюдается в интервале (1,5-9) ˙10-8М АПАВ в 10 мл экстракта. Тангенсы углов наклона близки между собой, что делает возможным определение как каждого индивидуального вещества, так и суммы анионных ПАВ по эталонному образцу (чаще всего по додецилсульфату натрия). Определение АПАВ проводят как при построении градуировочной характеристики. Вводят аликвоту пробы 1-5 мл. В табл.6 приведены результаты определения суммы различных видов АПАВ.
П р и м е р 4. Определение малых количеств анионных ПАВ в водных растворах и пластовых водах.
В делительную воронку помещают 50-200 мл анализируемой пробы, добавляют 2,5-10 мл 2М соляной кислоты, так чтобы ее концентрация в конечном объеме была ≈0,1М, 0,5 мл 10-3М спиртового раствора ДДАСПХ, перемешивают, добавляют 10 мл толуола, экстрагируют в течение 1 минуты. Органическую фазу фотометрируют в кювете с толщиной поглощающего слоя l = 2 см на фотоколориметре КФК-2 при λ = 590 нм. Количество АПАВ в растворе определяют по градуировочному графику, построенному по стандартному раствору определяемого АПАВ (додецилсульфат натрия, додецилбензолсульфат натрия и др.) в аналогичных условиях. Подчинение закону Бера сохраняется в пределах 5-1000 мкг/л (0,005-1 мкг/мл) АПАВ в пробе. Продолжительность анализа трех параллельных проб 0,5 ч, ошибка определения не превышает 10%. Относительное стандартное отклонение при концентрации 0,20 мг/л составляет 0,06.
П р и м е р 5. Определение больших количеств АПАВ безэкстракционным способом. Определение содержания основного вещества в промышленном образце сульфонола марки А (основа сульфонола - додецилбензолсульфонат натрия, ДДБС).
Построение градуировочной характеристики.
В мерные колбы емкостью 25 мл помещают 15 мл 0,1М соляной кислоты, 0; 20; 40; 60; 80; 100; 120; 140 мкг стандартного раствора додецилбензолсульфоната натрия (ДДБС), 3 мл 4%-ного раствора поливинилового спирта, 0,7 мл 10-3М спиртового раствора ДДАСПХ, доводят до метки соляной кислотой, выдерживают в течение 10 мин и измеряют оптическую плотность полученных растворов на КФК-2 при λ= 540 нм в кюветах с толщиной поглощающего слоя l = 2 см относительно раствора сравнения, не содержащего ДДБС. Прямолинейная зависимость наблюдается в интервале 20-140 мкг ДДБС в 25 мл раствора.
Определение содержания сульфонола в промышленном образце.
Навеску сульфонола 0,05 г помещают в мерную колбу емкостью 250 мл растворяют в дистиллированной воде. Аликвотную часть 1-3 мл помещают в колбу емкостью 25 мл и далее поступают как при построении градуировочной характеристики. Содержание ДДБС в сульфоноле рассчитывают по формуле
Q. % = 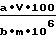 где а - количество мкг ДДБС, найденное по градуировочной характеристике;
где а - количество мкг ДДБС, найденное по градуировочной характеристике;
V - разведение, мл;
b - аликвота, мл;
m - навеска, г.
Правильность полученных результатов определяют титрованием цетилтриметиламмоний бромидом с индикаторами 2,7-дихлорфлуоресцеином (ДХФ) и метиленовым синим (двухфазное титрование в системе вода:хлороформ). Надо отметить, что при титровании наблюдается затянутый трудноразличимый переход окраски. Двухфазное титрование - сложный длительный способ.
Данные представлены в табл.8. Сравнение результатов по F и t-критериям показало их полную совместимость.
П р и м е р 6. Определение мешающего влияния посторонних ионов и веществ.
Определение проводят аналогично примеру 4 для экстракционного варианта и примеру 5 для безэкстракционного с добавлением в исследуемый раствор посторонних веществ, наиболее часто сопутствующих ПАВ в анализируемых объектах. Данные по селективности приведены в табл.9. Для сравнения приведены данные мешающего влияния при использовании метиленового синего и "бирюзового". В табл.9 указаны кратные массовые количества посторонних веществ, на мешающие определению 20 мкг додецилсульфата натрия.
П р и м е р 7. Определение свободного додецилсульфата натрия в тканях млекопитающих.
Анионные ПАВ - один из самых распространенных загрязнителей окружающей среды. Исследование движения ПАВ по биологической цепи и выяснение их влияния на организм человека и животных невозможно без надежных методов контроля токсикантов в различных биологических объектах.
Разработка надежного фотометрического способа определения АПАВ является важной задачей. В настоящее время фотометрические методы контроля за содержанием ПАВ в биологических объектах практически отсутствуют.
При разработке методики основным препятствием явилось плохое разделение фаз после экстракции ассоциата толуолом вследствие стабилизации эмульсии белками и другими органическими соединениями препаратов тканей.
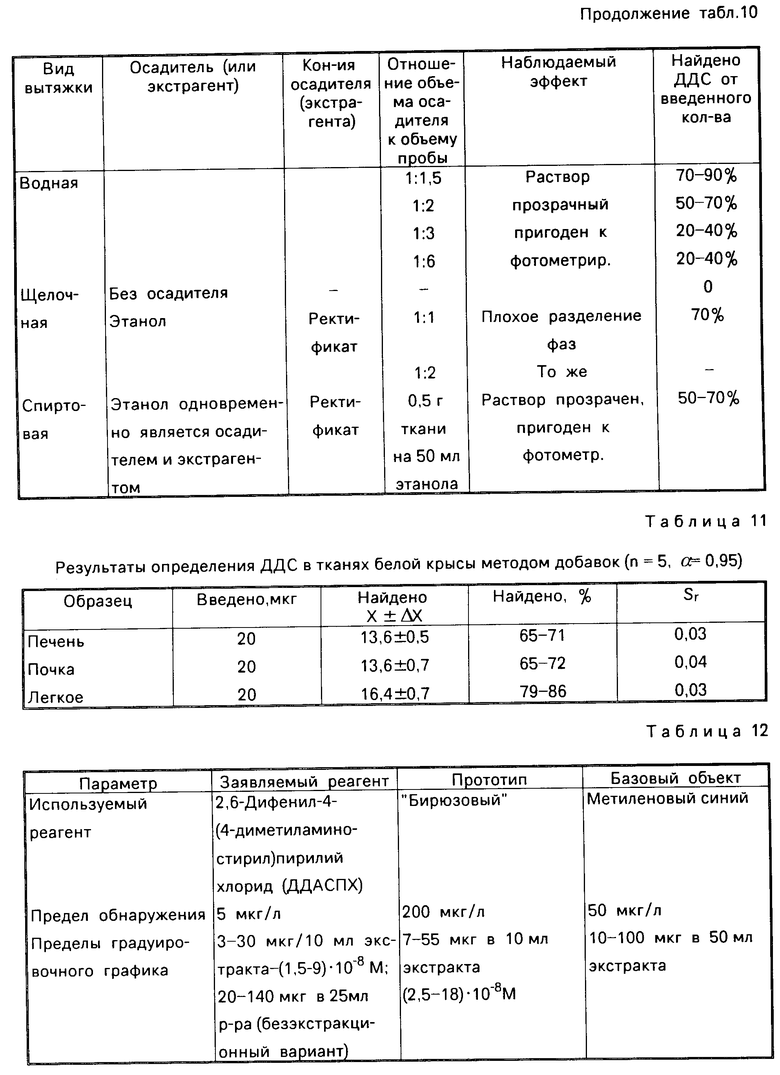
Для устранения мешающего действия белков в биохимии применяют различные методы их осаждения [6]. При разработке способа использовались водные, спиртовые, щелочные вытяжки из гомогенизированных препаратов печени, почек и легкого белой лабораторной крысы, использовались различные осадители. Данные приведены в табл.10.
Анализ полученных данных позволил выбрать наилучший вариант, позволяющий определить 70-90% введенного ДДС, который предусматривает приготовление водной вытяжки препарата с применением в качестве осадителя этанола при соотношении проба: этанол = 1,5:1.
Для определения свободного додецилсульфата натрия в тканях млекопитающих навеску органа (печень, почка, легкое) 0,1-0,5 г помещают в фарфоровую ступку и растирают до однородного состояния, смешивают содержимое ступки с водой и количественно переносят в мерную колбу емкостью 50 мл, доводят до метки дистиллированной водой и перемешивают.
В центрифужную пробирку помещают 2-5 мл пробы и дистиллированную воду до общего объема 5 мл. Приливают 3 мл этанола, помещают пробирку в центрифугу и центрифугируют 10 мин со скоростью 3000 об/мин. Содержимое центрифужной пробирки переливают в делительную воронку, прибавляют 8 мл 0,2н. HCl, 0,5 мл 10-3 М раствора ДДАСПХ и 15 мл толуола. Экстрагируют 1 мин. Толуольный слой сливают в кювету через вату и фотометрируют на фотоколориметре КФК-2 при λ= 590 нм. Раствор сравнения готовят аналогичным образом без ДДС, используя вместо пробы дистиллированную воду.
Содержание ДДС определяют по градуировочному графику. Для построения градуировочного графика используют раствор ДДС с концентрацией 10 мкг/мл, который готовят разбавлением исходного раствора с концентрацией 1 мг/кг.
В делительную воронку помещают 0,5; 1,0; 2,0; 3,0; 5,0 мл (5,10,20,30, 50 мкг) раствора ДДС с концентрацией 10 мкг/мл и приливают дистиллированную воду до общего объема 5 мл. Прибавляют 3 мл этанола, 8 мл 0,2 н. раствора соляной кислоты, 0,5 мл 10-3М раствора ДДАСПХ, 15 мл толуола. Экстрагируют 1 мин, полученный экстракт фотометрируют при 590 нм на фотоэлектроколориметре КФК-2, по полученным данным строят градуировочный график.
В оптимальных условиях были установлены метрологические характеристики способа (правильность и воспроизводимость) на различных тканях. Результаты приведены в табл.11, из которой видно, что заявляемый способ позволяет определить 65-85% вводимого количества ПАВ, воспроизводимость способа для различных тканей достаточно высока. Определение проводят сразу после введения ДДС в препарат ткани (в течение ≈10 мин).
Неполное извлечение ДДС из препаратов объясняется связыванием ПАВ белками в очень прочные ассоциаты, что подтверждается данными литературы. Таким образом, данный способ позволяет определять свободный (остаточный) ДДС.
Попытка определения ДДС в тканях животного с помощью метиленового синего не дала положительного результата. Хлороформный экстракт имеет ярко-синюю окраску, даже в отсутствие ДДС, по-видимому метиленовый синий взаимодействует с белками пробы и применение этого реагента для анализа биологических образцов невозможно.
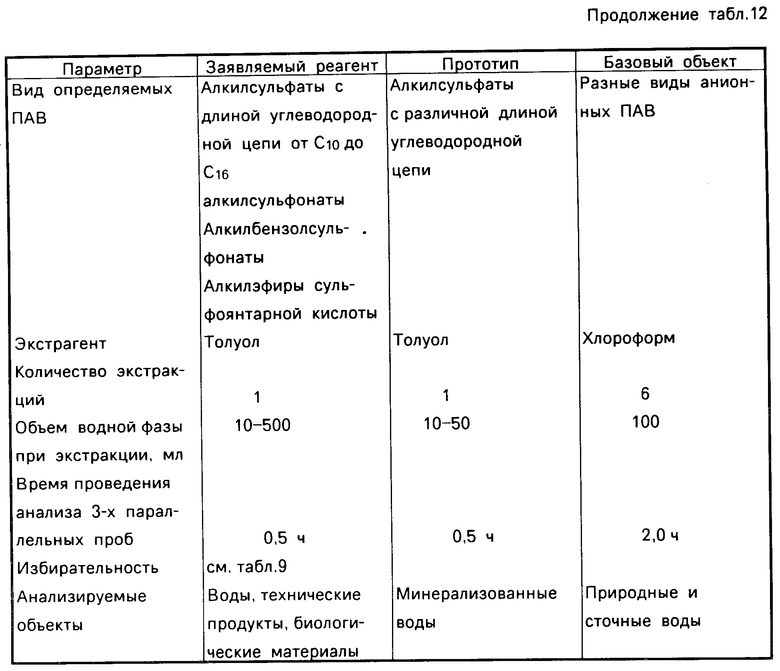
В табл. 12 приведены сравнительные данные основных параметров известных и заявляемого реагентов для фотометрического определения анионных ПАВ.
Таким образом, синтезированный новый реагент имеет следующие преимущества перед известными:
позволяет проводить как экстракционное, так и безэкстракционное определение АПАВ;
чувствительность экстракционного определения повышается в связи с возможностью экстракции из большого объема раствора;
расширяется круг определяемых видов АПАВ;
сокращается количество экстракций и время анализа (по сравнению с базовым объектом).
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения алкилсульфатов в водных растворах | 1989 |
|
SU1675746A1 |
| Реагент для фотометрического определения висмута ( @ ) | 1983 |
|
SU1161873A1 |
| Способ фотометрического определения оксиэтилированных алкилфенолов в минерализованных водах | 1989 |
|
SU1659802A1 |
| Реагент для фотометрического определения анионных синтетических поверхностно-активных веществ | 1981 |
|
SU1008652A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ НИТРИТ-ИОНОВ | 2019 |
|
RU2727879C1 |
| Реагент для фотометрического определения палладия | 1983 |
|
SU1096580A1 |
| Способ количественного определения сульфаниламидных препаратов | 1991 |
|
SU1817008A1 |
| Ионоселективный электрод | 1990 |
|
SU1809374A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ НЕИНОГЕННЫХ ПАВ В ИХ СУЛЬФАТИРОВАННЫХ ПРОИЗВОДНЫХ | 2007 |
|
RU2329497C1 |
| Способ количественного определения 0-, м-, п-фенилендиаминов | 1991 |
|
SU1800331A1 |

Использование: в аналитической химии в качестве реагента для количественного фотометрического определения анионных поверхностно-активных веществ (АПАВ). Сущность изобретения: продукт 2,6-дифенил-4-(4-диметиламиностирил)-пирилий хлорид. Б.Ф. C27H24ClO 228°С (разложение). Реагент 1:4-метил-2,6-дифенилпирилий хлорид. Реагент 2: n-диметиламинобензальдегид. Условия процесса: в среде уксусного ангидрида при 106-110°С в течение 35 ч с последующей выдержкой при комнатной температуре 2сут. Позволяет повысить чувствительность определения АПАВ, расширить круг определяемых АПАВ и проводить как экстракционное, так и безэкстракционное определение АПАВ. 12 табл.
2,6-ДИФЕНИЛ-4-(4-ДИМЕТИЛАМИНОСТИРИЛ)ПИРИЛИЯ-ХЛОРИД В КАЧЕСТВЕ АНАЛИТИЧЕСКОГО РЕАГЕНТА ДЛЯ КОЛИЧЕСТВЕННОГО ФОТОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ АНИОННЫХ ПОВЕРХНОСТНО-АКТИВНЫХ ВЕЩЕСТВ.
2,6-Дифенил-4-(диметиламиностирил)-пирилия хлорид формулы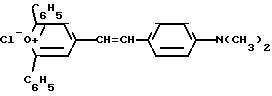
в качестве аналитического реагента для количественного определения анионных поверхностно-активных веществ.
| Руководство к лабораторным занятиям по биологической химии, М.: Медицина, 1976 г, с.294. |
Авторы
Даты
1995-03-10—Публикация
1992-02-17—Подача