Изобретение относится к ионообменной технологии и может найти применение в процессах водоподготовки, извлечения ценных компонентов из растворов и т.д.
Обычно целевые операции извлечения электролита из раствора проводятся в условиях, когда извлекаемый ион сорбируется сильнее, чем тот, который первоначально содержался в ионите. При деминерализации вод ионы Na, Ca, Mg сорбируются сильнее, чем Н+-ион ионита. Регенерацию же приходится вести при обратном соотношении сорбируемостей. Поэтому для достижения достаточно высоких степеней регенерации используют большой избыток регенеранта.
Получающиеся в результате регенерации растворы, как правило, содержат избыток достаточно концентрированного регенеранта и являются основным источником загрязнения окружающей среды.
Известен способ регенерации сильнокислотных катионитов обработкой соляной кислотой в колонне с неподвижным слоем [1]. Скорость раствора 5 м/ч. В качестве оптимальной концентрации для регенерации КУ-2х8 указана 2н НСl. При избытке кислоты по сравнению с полной обменной емкостью в 1,8; 3,8 и 8,75 раз достигалась соответственно 75, 90 и 99%-ная степень регенерации.
Наиболее близким к предлагаемому по технической сущности и достигаемому результату является способ регенерации сильнокислотного катионита в противоточным контакторе Хиггинса ≈2 н. раствором НNO3. Расход кислоты по сравнению с регенерацией в неподвижном слое сокращается в 1,7 раз [2].
Однако степень регенерации ионита в этом случае не превышает 75%.
Цель изобретения - повышение степени регенерации ионита.
Для этого регенерацию сульфокатионита в Са- и смешанной Са, Мg, Na-форме проводят в противоточной ионообменной колонне, выполненной в форме расширяющегося к верху усеченного конуса, 4-6 н. раствором соляной кислоты при непрерывной ее подаче сверху вниз, а ионита - снизу вверх, при соотношении потоков кислоты и ионита (в эквивалентах) 1:(1,1-1,05).
Использование конической колонны с подачей раствора в широкую часть позволяет завершать регенерацию при меньших скоростях раствора, облегчает перемещение ионита навстречу раствору (набухаемость ионита увеличивается при переходе из Са-формы в водородную). Кроме того, направление подачи регенерирующего раствора в колонне сверху вниз позволяет уменьшить размывание фронта десорбции в результате стабилизирующего действия естественной конвекции.
Обычно в процессах водоподготовки сильнокислотный катионит КУ-2х8 получают в смешанной Са, Мg, Nа-форме. Затраты регенеранта определяются равновесными характеристиками обмена регенерирующего иона на наиболее сильно удерживаемый ион, содержащийся в ионите. Из указанных ионов наиболее сильно удерживается ион кальция.
Изучение равновесия обмена Са2+-Н+ на катионите КУ-2х8 показало, что при концентрациях кислоты больших 4 н. ионы Н+ удерживаются катионитом сильнее, чем ионы Са2+. Кроме того, увеличение концентрации регенерирующей кислоты приводит к уменьшению объема раствора, содержащего регенерированные вещества, что упрощает утилизацию отходов. Ограничение концентрации соляной кислоты 6 н. связано с пределом растворимости NaCl и МgCl2 и опасностью выпадения их кристаллов в колонне.
Поддержание соотношения потоков кислоты и ионита (в эквивалентах) 1: (1,1-1,05) связано с необходимостью удерживания сорбционного фронта неподвижно относительно стенок колонны.
Все это позволяет добиться степени регенерации катионита 90-93% при 100%-ном использовании регенерирующего вещества (НСl) и получить в качестве продукта регенерации концентрированный раствор СаСl2, МgCl2, NaCl, не содержащий кислоты.
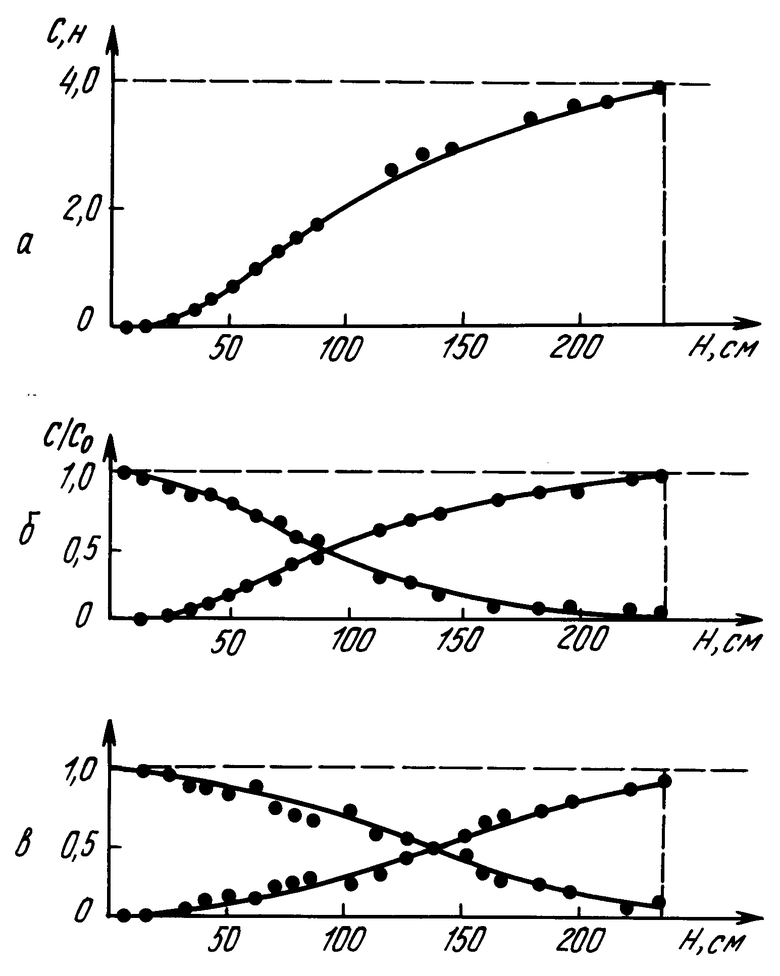
На чертеже изображены кривые зависимостей при регенерации Са-формы катионита КУ-2х8 4 н. раствором НСl в противоточной колонне:
а) кривая распределения концентрации по высоте Н колонны;
б) распределение отношения концентраций в растворе: О - Са2+,  - Н+ по высоте колонны;
- Н+ по высоте колонны;
в) распределение отношения концентраций тех же катионов в ионите по высоте колонны, где С0 - исходная концентрация кислоты;
С - текущая концентрация кислоты.
П р и м е р 1. Регенерацию Са-формы катионита КУ-2х8 проводят в противоточной ионообменной колонне непрерывного действия, имеющей форму усеченного конуса, расширяющегося кверху. Размеры колонны: Н = 236 см; Dнижн = 4 см; Dверхн = = 15,5 см.
4 н. раствор НСl пропускают сверху вниз со скоростью 100 мл/мин. Ионит, насыщенный ионами Са2+, подают снизу вверх со скоростью 220 мл/мин. Соотношение потоков раствора и ионита в эквивалентах 1:1,1. Отрегенерированный катионит выгружают сверху. Из пробоотборников, установленных по высоте колонны, через определенные промежутки времени отбирают пробы раствора для анализа. По результатам анализа строят кривые распределения концентраций ионов Са2+ и Н+ по высоте колонны. После того, как отрегенерировано 25 л ионита, опыт заканчивают.
Достигаемая при стационарном режиме степень регенерации катионита составляет 90 ± 2% . Выходящий раствор содержит 4 н. СаСl2. Кислоты в нем не было обнаружено.
П р и м е р 2. Регенерацию Са-формы катионита КУ-2х8 проводят 6 н. раствором НСl в колонне по методике, описанной в примере 1. Раствор подают сверху со скоростью 100 мл/мин, ионит - снизу вверх со скоростью 315 мл/мин. Соотношение потоков раствора и ионита в эквивалентах 1:1,05. Было отрегенерировано 25 л катионита.
При стационарном режиме из колонны выводят отрегенерированный на 93 ± 2% ионит и ≈6 н. раствор СаСl2, не содержащий кислоты.
П р и м е р 3. Проводят регенерацию смешанной Са, Мg, Na-формы катионита КУ-2х3, полностью отработанного в процессе деминерализации раствора, содержащего 0,16 н. NaCl; 0,03 н. МgSO4 и 0,03 н. СаSO4. Регенерацию ведут 4 н. раствором соляной кислоты.
Установка и методика описаны в примерах 1 и 2.
В стационарном режиме из колонны выводят ионит, отрегенерированный на 90 ± 2%, и 4 н. раствор, содержащий NaCl, CaCl2 и МgCl2.
Таким образом, предложенный способ позволяет повысить степень регенерации смешанной Са, Мg, Na-формы сульфокатионита до 90-93% при 100%-ном использовании регенерирующего вещества (НСl) и получать в качестве продукта регенерации концентрированный раствор СаСl2, МgCl2, NaCl, не содержащий регенерирующего вещества (НСl).
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ отмывки ионитов от растворов | 1991 |
|
SU1787946A1 |
| Способ извлечения стронция из высокоминерализованных растворов, содержащих натрий и кальций | 1988 |
|
SU1590441A1 |
| СПОСОБ ПОЛУЧЕНИЯ МИНЕРАЛЬНЫХ ВЕЩЕСТВ ИЗ МОРСКОЙ ВОДЫ | 1992 |
|
RU2006476C1 |
| СПОСОБ ИОНООБМЕННОГО УМЯГЧЕНИЯ СОКА II САТУРАЦИИ СВЕКЛОСАХАРНОГО ПРОИЗВОДСТВА | 1993 |
|
RU2056942C1 |
| Способ извлечения стронция из высокоминерализованных растворов, содержащих натрий и кальций | 1988 |
|
SU1606460A1 |
| Способ извлечения цезия и/или рубидия из смесей щелочных элементов | 1990 |
|
SU1781313A1 |
| СПОСОБ РАЗДЕЛЕНИЯ РАСТВОРОВ ЭЛЕКТРОЛИТОВ С ОДНОИМЕННЫМИ ИОНАМИ | 1993 |
|
RU2056899C1 |
| Способ очистки амнинокислот от минеральных солей | 1975 |
|
SU535291A1 |
| СПОСОБ КОМПЛЕКСНОЙ ПЕРЕРАБОТКИ КАЛЬЦИЙ- И СУЛЬФАТСОДЕРЖАЩИХ ПРИРОДНЫХ И ТЕХНОГЕННЫХ ВОД | 2024 |
|
RU2837737C1 |
| Способ извлечения стронция из высокоминерализованных растворов с рН 7-10 | 1987 |
|
SU1473835A1 |
Использование: ионообменной технологии в процессах водоподготовки, извлечения ценных компонентов из растворов. Сущность:регенерацию сульфокатионита из Ca- или смешанной Ca, Mg, Na- формы в водородную проводят в противоточной ионообменной колонне, выполненной в форме расширяющегося к верху усеченного конуса, 4 - 6 н.раствором соляной кислоты при непрерывной ее подаче сверху вниз, а ионита - снизу вверх, при соотношении потоков кислоты и ионита (в эквивалентах) 1:(1,1 - 1,05). При этом из колонны сверху выводят отрегенерированный до 93 ± 2% сульфокатионит, а снизу - раствор, содержащий только регенирированное вещество без примеси регенерирующего. Предлагаемый способ позволяет повысить степень регенерации смешанной Ca, Mg, Na- формы сульфокатионита до 90 -93% при 100%-ном использовании регенерирующего вещества (HCl) и получить в качестве продукта регенерации концентрированный раствор CaCl2, MgCl2, NaCl, не содержащий регенерирующего вещества (HCl). 1 ил.
СПОСОБ РЕГЕНЕРАЦИИ СУЛЬФОКАТИОНИТА из Са- или смешанной Ca, Mg, Na-формы в водородную путем его обработки минеральной кислотой в противоточной ионообменной колонне, отличающийся тем, что обработку ведут в колонне в форме расширяющегося к верху усеченного конуса 4-6 н.раствором соляной кислоты при соотношении эквивалентов кислоты и ионита 1 : (1,05 - 1,1).
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Higgins J.R., Chopra K.C., Jntern | |||
| Conference on Jon Ekchange in the Process Industries | |||
| Iuly, 1969 | |||
| London, Preprints | |||
| Способ отопления гретым воздухом | 1922 |
|
SU340A1 |
Авторы
Даты
1995-03-27—Публикация
1991-09-17—Подача