Изобретение относится к сорбентам для хроматографии на основе диоксида циркония и может использоваться в различных видах хроматографии, в том числе в высокоэффективной жидкостной хроматографии (ВЭЖХ) и газовой хроматографии.
Жидкостная хроматография является одним из наиболее интенсивно развивающихся инструментальных методов исследования и анализа сложных смесей органических и биологически активных соединений. Для решения ряда сложных задач в хроматографии, особенно в варианте ВЭЖХ, к адсорбентам и носителям предъявляются определенные требования к физико-химическим свойствам: форме гранул и размеру частиц, пористой структуре (удельная поверхность, размер пор и сорбционный объем пор), механической прочности гранул, гидролитической устойчивости. С одной стороны, это микросферическая форма гранул с однородным размером и достаточно высокой механической прочностью. Например, у коммерческих адсорбентов и носителей на основе силикагелей гранулы сферической формы с размером 3-50 мкм. С другой стороны, материал должен обладать определенной пористой структурой, обеспечивающей эффективное разделение органических веществ с большими молекулярными массами. К достоинствам неорганических носителей относятся достаточно высокая прочность гранул и ненабухаемость матрицы. Широко используются в хроматографии стационарные фазы на основе силикагеля, однако они не могут использоваться в течение длительного времени при рН растворов более 8 вследствие низкой гидролитической устойчивости силоксановой матрицы [1,2]
Гидролитическую стабильность носителей, например освоенных промышленностью пористых силикагелей, можно повысить путем покрытия поверхности стабильными в щелочных средах оксидами, такими как диоксиды титана или циркония [3,4] Этот прием позволил в отдельных случаях поднять предел применимости таких хроматографических материалов только до значения рН 10, что ограничивает их использование в более щелочных средах.
Известно использование в качестве хроматографических материалов индивидуальных диоксидов циркония или титана, которые обладают достаточно высокой гидролитической устойчивостью в области рН от 0 до 14. Наряду с гидролитической устойчивостью приводятся и другие характеристики материала: удельная поверхность 30-62 м2/г; диаметр пор 9,5-15 нм; форма гранул сферическая и размер гранул 5-50 мкм [5]
Недостатком индивидуального диоксида циркония как хроматографического материала является то, что при получении заданной пористой структуры при термо- и гидротермальном модифицировании интенсивно идут различные фазовые переходы, что приводит к потере механической прочности и разупрочнению гранул.
Наиболее близким к предложенному способу является способ получения гидратированного диоксида циркония, по которому водный раствор хлорида циркония подвергают электролизу с получением золя, переводят золь в сферогель, промывают его и термообрабатывают [6]
Задачей изобретения является получение хроматографического материала на основе диоксида циркония, обладающего повышенной пористостью и механической прочностью.
Указанная задача решается предлагаемым сферическим хроматографическим материалом на основе диоксида циркония, представляющего собой твердый раствор с тетрагональной или кубической решеткой общей формулы
МеxZr1-xO2-0,5. nH2O, где X 0,02-0,40;
Ме металла III группы Периодической системы;
n 0,01-0,8, и имеет средний диаметр пор 3-100 нм, сорбционный объем пор 0,04-0,6 см3/г, средний диаметр гранул 3-600 мкм. Параметры элементарной ячейки твердых растворов заявленного состава не изменяются при термообработке в области 400-1100оС. Высокая термическая устойчивость твердого раствора ZrO2-Me2O3 с тетрагональной или кубической решеткой обеспечивает стабильность прочностных характеристик и позволяет в широких пределах регулировать параметры пористой структуры сорбента.
Введение в хроматографический материал стабилизирующей добавки по М3+ в количестве менее 0,02 молярных долей приводит к образованию моноклинной модификации диоксида циркония с малой механической прочностью гранул. Кроме того в процессе термообработки при фазовом переходе моноклинная 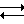 тетрагональная происходит дробление гранул из-за резкого изменения параметров элементарной ячейки. При введении стабилизирующей добавки по М3+ в количестве более 0,40 молярных долей образуется двухфазная система, состоящая из твердого раствора и самостоятельной фазы стабилизатора. Это приводит к снижению механической прочности и нарушает однородность сорбента.
тетрагональная происходит дробление гранул из-за резкого изменения параметров элементарной ячейки. При введении стабилизирующей добавки по М3+ в количестве более 0,40 молярных долей образуется двухфазная система, состоящая из твердого раствора и самостоятельной фазы стабилизатора. Это приводит к снижению механической прочности и нарушает однородность сорбента.
Поставленная задача решается также способом получения материала, согласно которому хроматографический материал предложенного состава и пористой структуры с тетрагональной или кубической решеткой получают золь-гель методом. Готовят водный раствор, содержащий хлорид циркония и по меньшей мере один хлорид металла из III группы Периодической системы Д.И.Менделеева при их молярном соотношении Zr:Me= (0,60-0,98):(0-40-0,02). Электролиз смешанного раствора ведут при 40-100оС до рН 1,6-2,2. Электролизу подвергают растворы с общей концентрацией названных хлоридов металлов от 0,8 моль/л и вплоть до насыщения.
Полученный золь диспергируют в гелирующей среде в зависимости от желаемого фракционного состава материала. В качестве последней для получения гранул размером 100-600 мкм и более, преимущественно используемых в газовой хроматографии, применяют жидкую гелирующую среду водный раствор аммиака. Для получения более мелких сфер (диаметром менее 100 мкм) диспергирование золя проводят в газовой среде с подогревом при 100-1000оС методом распылительной сушки, используя в качестве технического средства, например, форсунку, а в качестве газа воздух, азот, углекислый газ и др. Диспергирование золя осуществляют путем вибрационного распыления при частоте колебаний 20-500 кГц. Образовавшиеся сферические частицы отмывают водой и подвергают термообработке при 400-1000оС.
В состав заявленного материала, кроме указанных трехвалентных редкоземельных металлов, могут входить и лантаноиды с переменной валентностью. Например, СеО2, образующийся при прокалке на воздухе или в какой-либо окислительной атмосфере, может присутствовать самостоятельно либо в смеси с Се2О3 в зависимости от условий окисления и термообработки.
Для экспериментальной проверки хроматографического материала заявляемого состава пористой структуры с тетрагональной или кубической решеткой были получены 24 образца (табл.1-4), 14 из которых показали оптимальные результаты по механической прочности гранул.
П р и м е р ы 1-5. Водный раствор хлоридов циркония и алюминия, содержащий 0,01, 0,02, 0,20, 0,40, 0,45 мол. по Al и 0,99, 0,98, 0,80, 0,60 и 0,55 мол. по Zr с суммарной концентрацией по металлам 1,5 мол/л заливали в однокамерный электролизер, в котором в качестве электродов использовали: анода платину, катода титан. Электролиз проводили при 75оС при катодной плотности тока 450 А/м2. В результате электролиза получали устойчивые во времени золи с рН 1,8-2,0. Выход по току продукта в процессе электролиза составил 85-90%
Полученные золи диспергировали в 12%-ный водный раствор аммиака. Диспергирование проводили с помощью ультразвукового источника путем вибрационного распыления с частотой колебаний 44 кГц. Гель-сферы отмывали от электролитов дистиллированной водой и сушили при 150оС, а затем проводили термообработку при 800оС в течение 6 ч. Полученные гранулы сорбента имели форму, близкую к сферической, и диаметр преимущественно 3-50 мкм.
Рентгенофазовый анализ (РФА) образцов проводили на дифрактометре марки ДРОН-2 при комнатной температуре с использованием CuKα -излучения. Сокращенное наименование фаз: А аморфная, Т тетрагональная, К кубическая. Параметры пористой структуры образцов находили следующим образом: удельную поверхность (SN2) определяли по изотермам адсорбции азота методом БЭТ; удельный сорбционный объем VS пор и средний диаметр dn пор определяли по полным изотермам адсорбции-десорбции паров бензола. Механическую прочность Pm гранул определяли по максимальному усилию при раздавливании гранулы как упруго-хрупкого тела между двумя жесткими опорами. Среднее значение Pm вычисляли по результатам испытаний 20 гранул. Величина относительной погрешности измерений составила 18-28% при доверительной вероятности 0,95.Размер частиц сорбента измеряли на микроскопе МБИ-11 с точностью определения ±0,001 мм.
Экспериментальные данные для системы AlxZr1-xO2-0,5x.nH2O приведены в табл. 1, из которой следует, что состав сорбента соответствует формуле AlxZr1-xO2-0,5x.nH2O, где Х 0,02-0,04;
n 0,06, и представляет собой твердый раствор с тетрагональной решеткой.
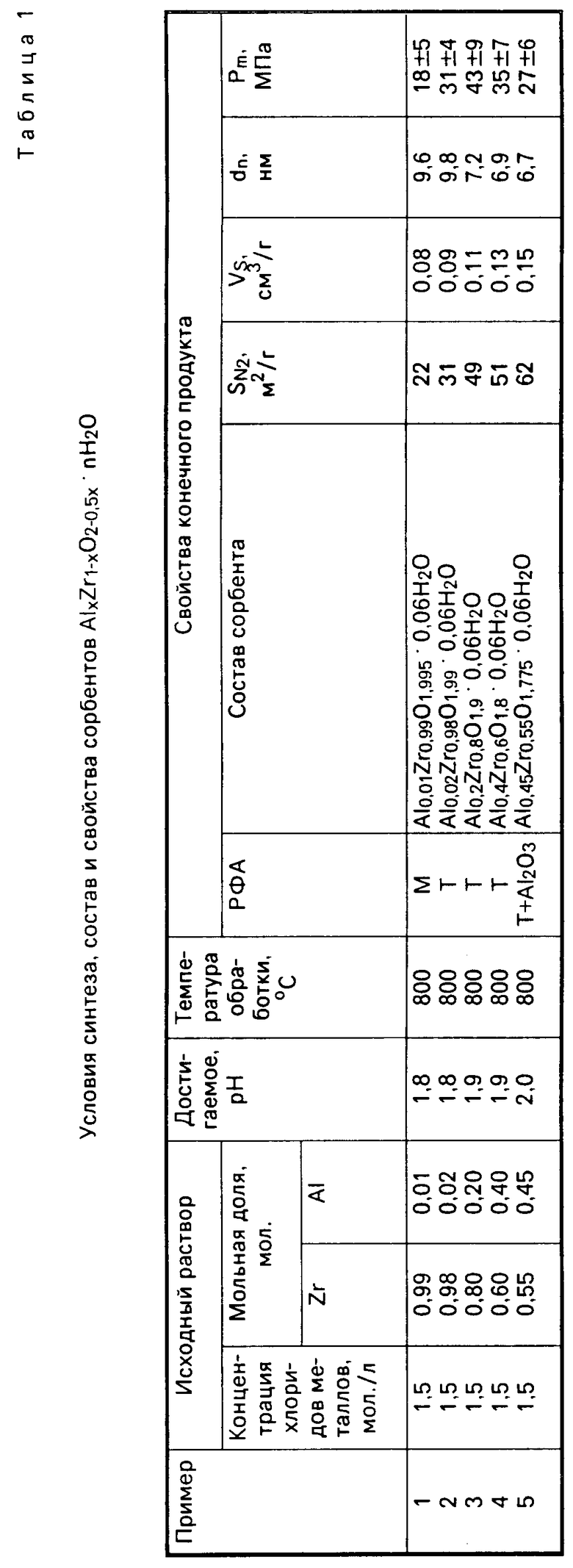
П р и м е р ы 6-14. Водный раствор хлоридов циркония и иттрия с суммарной концентрацией по металлам 1,4 мол/л, содержащий 0,01, 0,02, 0,08, 0,16, 0,40, 0,45 мол. по Y и 0,99, 0,98, 0,92, 0,84, 0,60, 0,55 мол. по Zr заливали в однокамерный электролизер и подвергали электролизу, как описано в примерах 1-5. В результате электролиза получали устойчивые золи с рН 1,7-2,0. Выход по току продукта в процессе электролиза составил 85-90% при температуре раствора 80оС и катодной плотности тока 550 А/м2.
Полученные золи диспергировали, гель-сферы отмывали, сушили, подвергали термообработке и продукт исследовали, как описано в примерах 1-5.
Экспериментальные данные для системы YxZr1-xO2-0,5x.nH2O приведены в табл. 2, из которой следует, что состав сорбента соответствует формуле YxZr1-xO2-0,5x.nH2O, где х 0,02-0,40;
n 0,01-0,8, представляет собой твердый раствор с тетрагональной или кубической решеткой ZrO2 и характеризуется средним диаметром пор 3-100 нм и сорбционным объемом пор 0,04-0,6 см3/г.
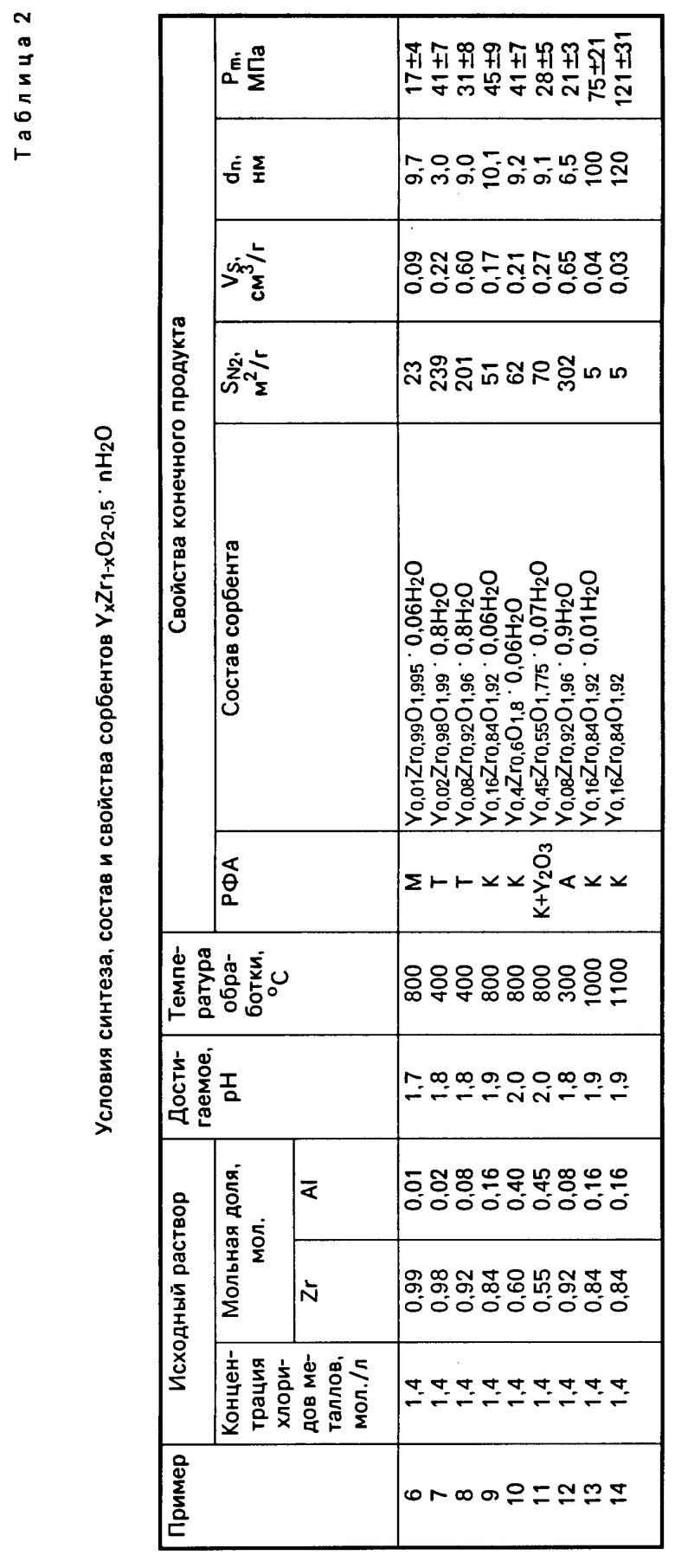
П р и м е р ы 15-19. Водный раствор хлоридов циркония и лантана с суммарной концентрацией по металлам 1,2 мол./л, содержащий 0,01, 0,02, 0,04, 0,40, 0,45 мол. по La и 0,99, 0,98, 0,96, 0,60, 0,55 мол. по Zr заливали в однокамерный электролизер и подвергали электролизу, как описано в примерах 1-14. В результате электролиза получали устойчивые во времени золи с рН 1,7-2,0. Выход по току продукта в процессе электролиза составил 85-90% при температуре раствора 80оС и катодной плотности тока 450 А/м2.
Полученные золи диспергировали, гель-сферы отмывали, сушили, подвергали термообработке и продукт исследовали, как описано в примерах 1-5.
Экспериментальные данные для системы LaxZr1-xO2-0,5x.nH2O приведены в табл. 3, из которой следует, что состав сорбента соответствует формуле LaxZr1-xO2-0,5x.nH2O, где х 0,02-0,40;
n 0,06-0,07 и представляет собой твердый раствор с тетрагональной или кубической решеткой ZrO2.
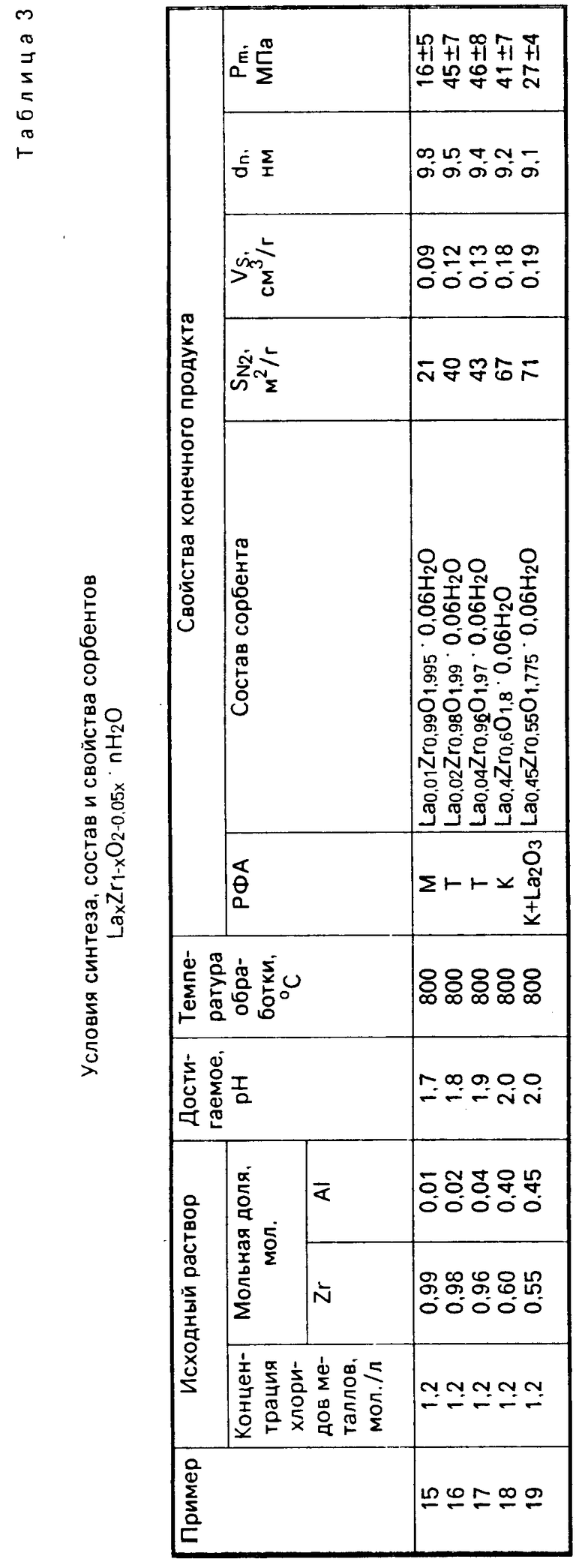
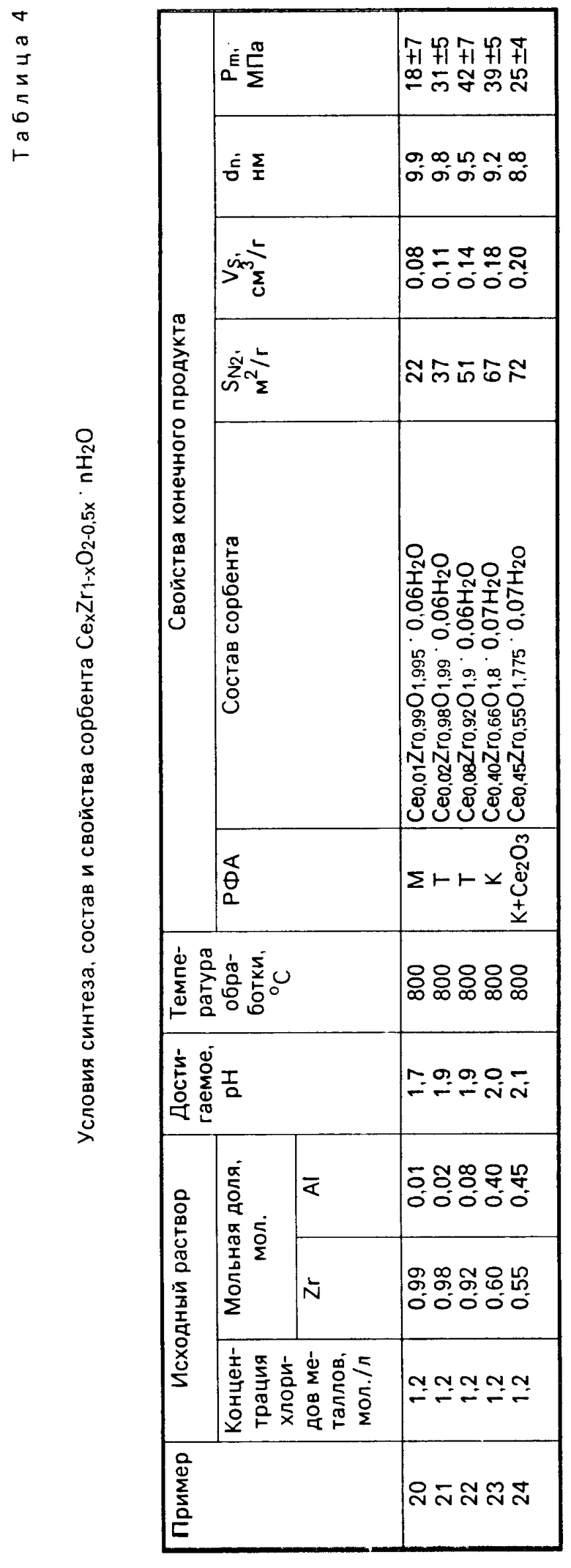
П р и м е р ы 20-24. Водный раствор хлоридов циркония и церия с суммарной концентрацией по металлам 1,2 мол./л, содержащий 0,01, 0,02, 0,04, 0,40, 0,45 мол. по Ce и 0,99, 0,98, 0,96, 0,60, 0,55 мол. по Zr заливали в однокамерный электролизер и также подвергали электролизу, как описано в примерах 1-14. В результате электролиза получали устойчивые во времени золи с рН 1,7-2,1.
Полученные золи диспергировали, гель-сферы отмывали, сушили, подвергали термообработке и продукт исследовали, как описано в примерах 1-5.
Экспериментальные данные для системы CexZr1-xO2-0,5x.nH2O приведены в табл. 4, из которой следует, что состав сорбента соответствует формуле CexZr1-xO2-0,5x.nH2O, где х 0,02-0,40;
n 0,06-0,07, и представляет собой твердый раствор с тетрагональной или кубической решеткой ZrО2.
Электролиз водных растворов хлоридов металлов можно вести в одно,-двух- или трехкамерном электролизере. В однокамерном аппарате упрощение процесса.
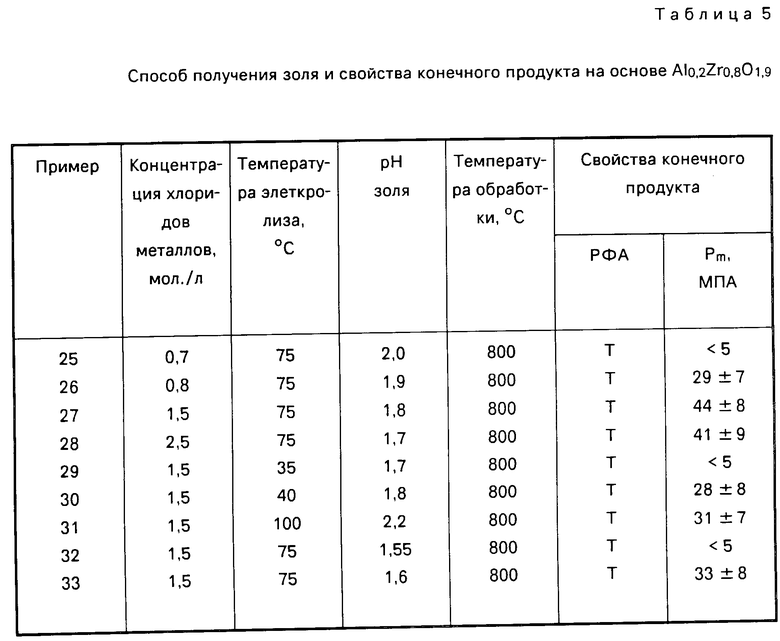
В табл. 5 приводятся экспериментальные данные (примеры 25-33) по влиянию температуры электролиза, концентрации металлов и величины рН золя на свойства конечного продукта на основе Al0,2Zr0,8O1,9.
П р и м е р ы 25-33. Водный раствор хлоридов циркония алюминия, содержащий 0,8 мол. по Zr и 0,2 мол. по Al с суммарной концентрацией по металлам 0,7, 0,8, 1,5, 2,5 мол/л заливали в электролизер и электролиз проводили при катодной плотности тока 450 А/м2, как описано в примерах 1-5. Температуру электролиза поддерживали 35, 40, 75 и 100оС. Полученные золи с различным значением рН диспергировали в водный раствор аммиака, гель-сферы отмывали, сушили, проводили термообработку и продукт исследовали, как описано в примерах 1-5.
Как следует из табл.5, конечный продукт с механической прочностью гранул более 30 МПа следует получать при следующих оптимальных условиях электролиза солянокислых растворов циркония с одним из металлов III группы: температуру электролиза водных солянокислых растворов названных металлов поддерживать от 40 до 100оС; общую концентрацию хлоридов металлов от 0,8 мол./л и более. Конечный золь доводят до рН 1,6-2,2.
Диспергирование золя гидроксида циркония с одним из металлов III группы Периодической системы Д.И.Менделеева, полученного электролизом, осуществляли путем распылительной сушки и вибрационного распыления.
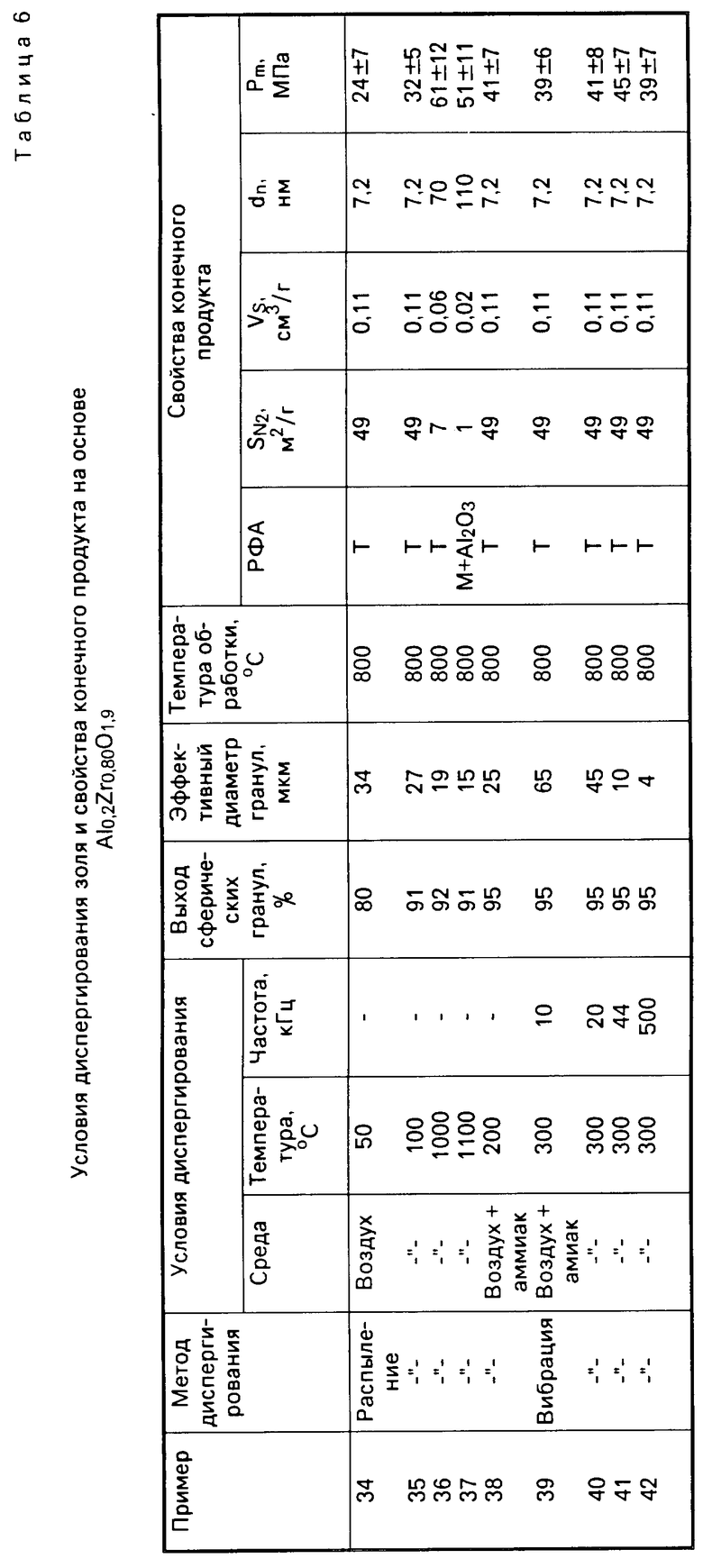
П р и м е р ы 34-42. Золь, содержащий 0,8 мол. по Zr и 0,2 мол. по Al, с общей концентрацией по металлам 1,5 мол./л и рН 1,8 диспергировали методом распылительной сушки через форсунку диаметром 0,8 мм в цилиндрический аппарат с воздушной средой при 50, 100, 1000, 1100оС. При температуре воздушной среды 100оС дополнительно в реакционную камеру вводили пары аммиака. Тот же золь диспергировали путем вибрационного распыления при частоте колебаний 10, 20, 44, 500 кГц в аппарат, содержащий пары аммиака при температуре реакционной среды 300оС. Полученный гранулированный продукт извлекали из аппарата, определяли на микроскопе количество гранул с формой, близкой к сферической, и размер гранул, затем материал отмывали водой, проводили термообработку и исследовали, как описано в примерах 1-5.
Экспериментальные данные по влиянию условий диспергирования золя, содержащего 0,2 мол. по Al и 0,8 мол. по Zr, приведены в табл.6.
Из табл. 6 следует, что при диспергировании золя распылением через форсунку или высокочастотной вибрацией в реакционную газообразную среду заметно уменьшается выход гранулированного продукта при температуре среды менее 100оС. При температуре среди более 1000оС уменьшаются сорбционные свойства конечного продукта в результате снижения сорбционных объемов пор и удельной поверхности. Введение паров аммиака в реакционную камеру при диспергировании золя приводит к увеличению выхода гранул со сферической формой.
Хроматографические испытания.
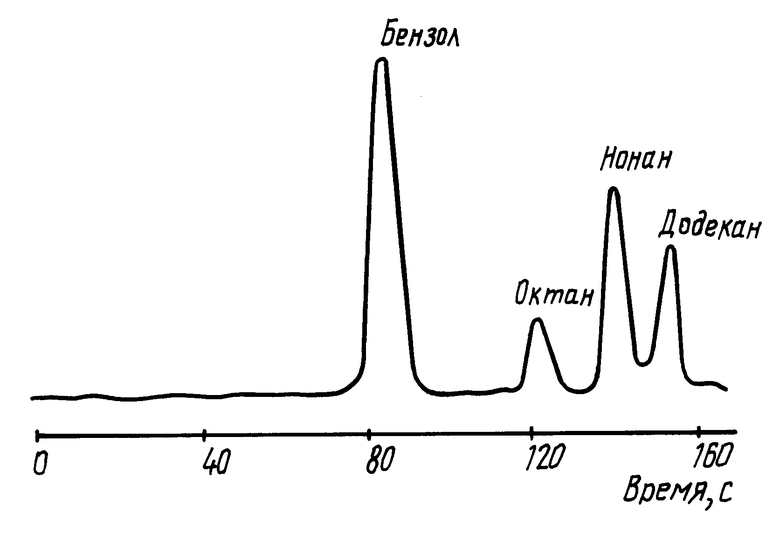
Для хроматографических испытаний был использован сорбент состава Y0,025Zr0,975O1,9875.0,06H2O, который имеет тетрагональную фазу ZrO2 и характеризуется диаметром пор 9,8 нм и сорбционным объемом пор 0,13 см3/г. Разделение органических веществ (бензола, октана, нонана и додекана) проводили на хроматографе АХМ-8MD(1) с использованием в качестве газа-носителя гелия. Сорбент использовали с зернением от 50 до 100 мкм. Основные условия разделения были следующими: диаметр колонки 1,2 мм; длина колонки 1 м; скорость пропускания 100 см3/ч; температура носителя 222оС; детектирование катарометром. На новом сорбенте была получена хроматограмма разделения органических веществ в выше приведенном порядке с четко разрешающими и симметричными пиками. Хроматограмма приведена на чертеже.
| название | год | авторы | номер документа |
|---|---|---|---|
| ГРАНУЛИРОВАННЫЙ НЕОРГАНИЧЕСКИЙ СОРБЕНТ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1992 |
|
RU2032460C1 |
| НЕОРГАНИЧЕСКИЙ СФЕРОГРАНУЛИРОВАННЫЙ ОБВОДНЕННЫЙ ИОНООБМЕННЫЙ МАТЕРИАЛ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1992 |
|
RU2034645C1 |
| НЕОРГАНИЧЕСКИЙ СФЕРОГРАНУЛИРОВАННЫЙ ПОРИСТЫЙ СОРБЕНТ НА ОСНОВЕ ГИДРОКСИДА ЦИРКОНИЯ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1994 |
|
RU2064825C1 |
| СПОСОБ ПОЛУЧЕНИЯ СФЕРОГРАНУЛИРОВАННЫХ МАТЕРИАЛОВ НА ОСНОВЕ ГИДРОКСИДА ИЛИ ОКСИДА ЦИРКОНИЯ | 2003 |
|
RU2235686C1 |
| Гранулированный неорганический сорбент и способ его получения | 1989 |
|
SU1776432A1 |
| НЕОРГАНИЧЕСКИЙ СФЕРОГРАНУЛИРОВАННЫЙ КОМПОЗИЦИОННЫЙ СОРБЕНТ НА ОСНОВЕ ГИДРОКСИДА ЦИРКОНИЯ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1996 |
|
RU2113024C1 |
| СПОСОБ ПОЛУЧЕНИЯ СФЕРОГРАНУЛИРОВАННЫХ СОРБЕНТОВ НА ОСНОВЕ ГИДРАТИРОВАННОГО ДИОКСИДА ЦИРКОНИЯ | 2005 |
|
RU2292949C2 |
| СПОСОБ СОРБЦИОННОЙ ОЧИСТКИ ВИНОМАТЕРИАЛА И УСТАНОВКА ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1993 |
|
RU2046630C1 |
| СПОСОБ ОЧИСТКИ ОТ РАДИОНУКЛИДОВ ВОДЫ ВЫСОКОГО УРОВНЯ АКТИВНОСТИ | 1995 |
|
RU2090944C1 |
| Способ получения неорганического сорбента для извлечения урана из растворов | 1981 |
|
SU1110004A1 |
Изобретение относится к сорбентам для хроматографии на основе диоксида циркония и может использоваться в различных видах хроматографии, в том числе в газовой и жидкостной. Предлагается сферогранулированный хроматографический материал состава: MexZr1-xO2-0,5x·n H2O, где Ме - металл III группы Периодической системы элементов; x=0,02 - 0,40; n=0,01 - 0,8, который представляет собой твердый раствор с тетрагональной или кубической решеткой и характеризуется средним диаметром пор 3 - 100 нм и сорбционным объемом пор 0,04-0,6 см3/г. Средний диаметр гранул материала составляет 3 - 600 мкм. Способ получения материала включает следующие стадии: электрохимический синтез золя до достижения pH 1,6 - 2,2, диспергирование золя в гелирующей среде (газовой либо водном растворе аммиака) путем вибрационного распыления, отделение образовавшихся гель-сфер, их отмывку и термообработку. 2 с. и 6 з. п. ф-лы, 1 ил., 6 табл.
MexZr1-xO2-0,5x· n H2O,
где x=0,02 0,40;
Me металл III группы;
n=0,01 0,8,
и характеризуется средним диаметром пор 3 100 нм и сорбционным объемом пор 0,04 0,6 см3/г.
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Шарыгин Л.М., Галкин В.М | |||
| и Штин А.П | |||
| Исследование пористой структуры гидратированной двуокиси циркония, полученной зольгель методом | |||
| Изв.АН СССР | |||
| Неорг.материалы, 1979, т.15, N 11, с.2051. | |||
Авторы
Даты
1995-04-10—Публикация
1992-03-25—Подача