Изобретение относится к медицинской промышленности, в частности к производству вирусных препаратов.
Прототипом изобретения является применяемый в настоящее время способ получения коммерческой культуральной антирабической вакцины (1). Метод основан на стационарном культивировании в матрасных колбах. Для культивирования клеток почек 3-4 недельных сирийских хомяков (ПСХ) и фиксированного вируса бешенства штамма Внуково 32, 32-38 пассажа используются матрасные колбы вместимостью 1-1,5 л.
Процесс культивирования включает в себя следующие стадии технологического процесса. ПСХ 3-4-недельных сирийских хомяков после дезагрегации раствором 0,25% трипсина и подсчета клеток заражают фиксированным вирусом бешенства штамма Внуково-32, 32-38 пассажа во взвесь путем адсорбции вируса на клетки, на магнитной мешалке, в течение 1-1,5 ч, доза заражения 0,01-0,001 ЛД50/кл. После адсорбции зараженные клетки засевают в матрасные колбы из расчета 50 ± 100 тыс/мл ростовой среды, имеющей в своем составе 0,5% ГЛА со средой 199 в соотношении 1:1 и 10% сыворотки крупного рогатого скота (КРС). На трипсинизацию (1 партия) уходит в среднем 60 голов сирийских хомяков (120 почек), которые засевают в 58-65 матрасных колб и помещают их в термальную камеру на +35 ± 1оС.
В процессе образования монослоя на 3-4 сутки производится смена среды, а на 7-8 сутки отмыв от КРС сформировавшегося монослоя раствором Эрла. После отмыва каждый матрас заливают поддерживающей средой, имеющей в своем составе 0,5% ГЛА с 5%-ным содержанием гидролизина или аминопептида и помещают в термальную камеру на + 32 ± 1оС. Сборы вируссодержащей культуральной жидкости производят через день. Количество сборов с каждого матраса 4-5. Весь технический процесс ведется с соблюдением правил асептики в стерильных боксовых помещениях.
Недостатком этого метода является низкий выход целевого продукта, большая трудоемкость процесса, отсутствие контроля роста клеток, риск контаминации посторонних микрофлорий. Доля ручного труда в технологическом цикле составляет 85%
За рубежом (Van Wezel, Нидерланды) применяется метод псевдосуспензионного культивирования клеток почек собак и вируса Pitman-Moore с целью получения антирабической вакцины (2). Культивирование проводится в стеклянных 40 л ферментерах на микроносителях ДЭАЭ-сефадекс А-50. Однако описание оптимальных параметров культивирования и данные о выходе продукта отсутствуют.
Цель изобретения повышение выхода целевого продукта за счет оптимизации процесса культивирования в биореакторе на микроносителях.
С этой целью культивирование клеток почек сирийских хомяков и фиксированного штамма вируса бешенства Внуково-32, 32-38 пассажа проводят в биореакторе на микроносителях Цитолар с дискретным режимом перемешивания: первые сутки 2-5 мин перемешивания, 120 мин остановка с последующим уменьшением времени остановки на 30 мин ежесуточно, с 4-го дня и далее остановка 30 мин, скорость вращения мешалки 15-20 об./мин.
Сравнительный анализ с прототипом показывает, что общим для них является получение вирусосодержащей взвеси на первично-трипсинизированной культуре клеток почек сирийского хомяка.
Отличительным признаком предлагаемого способа является проведение культивирования клеток и вируса в биореакторе на отечественных микроносителях Цитолар с дискретным режимом перемешивания.
Применение данного режима перемешивания обеспечивает благоприятные условия для прикрепления, роста и размножения клеток и вируса, равномерность условий роста клеток по всему объему аппарата, что позволяет повысить выход целевого продукта.
Проведение процесса в закрытой системе обеспечивает стерильность процесса в течение длительного времени, контроль роста и состояния клеток.
Применение микроносителей позволяет одновременно культивировать десятки, сотни миллиардов клеток в одном постоянном объеме, что обеспечивает повышение производительности труда.
В настоящее время у нас имеется единственный вид апробированных микроносителей (микроносители Цитолар 1,2) и показана возможность их применения для различных видов клеток.
Сравнительный анализ свидетельствует, что предлагаемое техническое решение соответствует критериям "новизна" и "cущественные отличия".
Способ осуществляют следующим образом.
После трипсинизации клетки ПСХ заражают во взвесь фиксированным вирусом бешенства штаммов Внуково-32, 32-38 пассажей путем адсорбции вируса на клетках на магнитной мешалке в течение 1-1,5 ч. Зараженные вирусом клетки (0,01-0,001 ЛД50/кл) в концентрации 500 ± 100 тыс. в 1 мл соединяют с ростовой средой, имеющей в своем составе 0,5%-ный гидролизат лактальбумина (ГЛА) в смеси со средой 199 в соотношении 1:1 с добавлением 10%-ной сыворотки крупного рогатого скота (КРС), загружают в стеклянный реактор вместимостью 50 л, в котором находятся микроносители Цитолар 1 или 2. Микроносители "Цитолар" выпускаются НПО "Биолар", г.Олайне, Латвия. Микроносители представляют собой частицы поперечно-сшитого денатурированного коллагена (желатина), синтезированного по оригинальной технологии. Все компоненты, из которых синтезированы микроносители Цитолар, применяются в медицинской практике, а получаемый продукт является биологически совместимым материалом. Микроносители гидрофильны, прозрачны, имеют гладкую поверхность, в изотоническом солевом растворе их удельная плотность не превышает 1,08 г/см3, диаметр частиц 110-280 мкм.
Концентрация микроносителей 10 г/л ростовой среды. Биореактор помещают на тележку с вмонтированной в нее магнитной мешалкой с блоком управления, перевозят в термальную камеру с температурой 35 ± 1оС и устанавливают определенный режим перемешивания:
Время работы Время остановки 1 сутки 2-5 мин 120 мин 2 сутки 2-5 мин 90 мин 3 сутки 2-5 мин 60 мин 4 сутки и далее 2-5 мин 30 мин
Скорость вращения мешалки 15-20 об/мин.
Отмыв и сборы. На 4-5 день по результатам визуального контроля качества монослоя проводят смену среды, которая имеет в своем составе 0,5%-ный ГЛА, среду 199 в соотношении 1:1 и 5% сыворотки крупного рогатого скота. По истечении 9-10 сут с момента загрузки биореактора и формирования монослоя на 75-85% разрешается производить отмыв культуры клеток от сыворотки КРС.
Отмыв проводится следующим образом. Ростовая питательная среда, находящаяся в реакторе, сливается в бутыль-приемник, а в реактор засасывается рабочий раствор Эрла, после оседания микроносителей раствор Эрла сливается и заливается новым раствором Эрла. Процедуру повторяют 3-4 раза. По окончании отмыва в реактор заливают поддерживающую среду, имеющую в своем составе 0,5% -ный ГЛА, среду 199 в соотношении 1:1 с 5%-ным аминопептидом или гидролизином. Реактор помещают в термальную комнату с температурой 31 ± 1оС, устанавливают на магнитную мешалку. Режим перемешивания: 2-5 мин работы мешалки, остановка 30 мин. Скорость вращения мешалки 15-20 об/мин. На 3-й день после отмыва проводится 1 сбор. После оседания микроносителей к выходу реактора подключают сифон для сбора вирусосодержащей жидкости (ВЖ) и с помощью отрицательного давления ВЖ отсасывается из реактора. Затем в реактор засасывается с помощью положительного давления новая порция поддерживающей среды и его помещают в термальную камеру на 32 ± 1оС до следующего сбора. Сборы делают через 1 день, максимальное количество сборов с одного биореактора 8.
Перед сбором контролируют качество монослоя на микроносителях. Все этапы производят с соблюдением правил асептики в стерильных помещениях. Контроль полуфабриката ведут по ТУ 42-14-86-76.
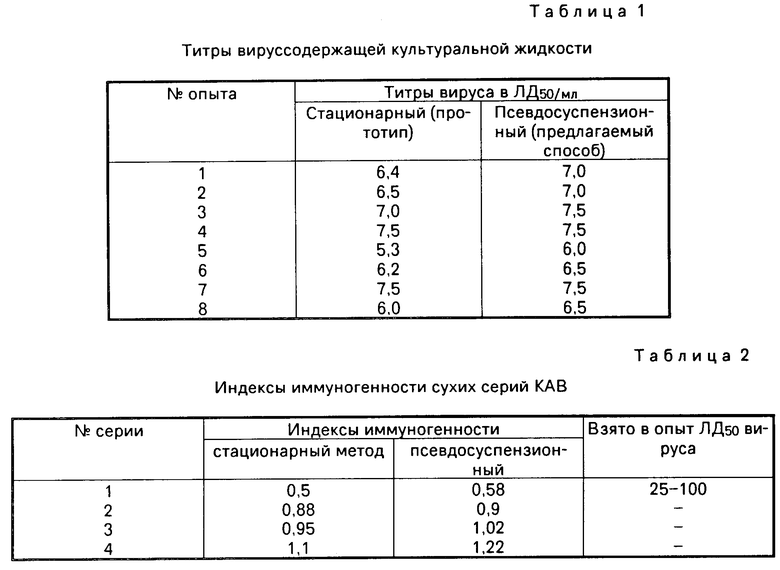
В табл.1 представлены титры вируссодержащей культуральной жидкости, полученной при различных способах культивирования.
Как видно из табл.1, титры вируссодержащей культуральной жидкости при псевдосуспензионном культивировании колеба- лись от 6,0 до 7,5 и были выше на 0,3-0,7, чем при стационарном режиме культивирования.
Из полученной вируссодержащей культуральной жидкости были изготовлены 4 серии культуральной антирабической вакцины (КАВ). Как видно из табл.2 индексы иммуногенности полученного препарата колебались от 0,58 до 1,22, против 25-100 ЛД50 фиксированного вируса бешенства штамма CVS и были не ниже, чем в контрольной группе (стационарный метод культивирования).
Как видно из табл.3 с одной партии хомяков при использовании псевдосуспензионного метода культивирования можно получить качественного полуфабриката в 2-2,5 раза больше, чем при стационарном методе, а также избавиться от 58-122 матрасных колб. Если учесть, что в неделю проводится 14-16 трипсинизаций, т. е. производится 14-16 партий по 60-65 хомяков, то необходимое расчетное количество матрасов составляют в среднем 60 мат. х 16960 матр. в неделю. Их с успехом заменят 10-14 биореакторов.
Таким образом, предлагаемый способ имеет более высокую производительность и более технологичен. Получаемый целевой продукт имеет высокую инфекционную и иммуногенную активность. Ожидаемый экономический эффект высок за счет сокращения численности производственного персонала и снижения расхода хомяков для получения препарата.
Обоснование параметров режима перемешивания, применяемого с 4-го дня культивирования, увеличение времени работы мешалки в биореакторе свыше 5 мин ведет к формированию монослоя на поверхности микроносителей на 60% (табл.4). При перемешивании в течение 1 мин не обеспечивается равномерное распределение микроносителей.
Увеличение времени остановки мешалки биореактора ведет к образованию конгломератов частиц микроносителей и клеток, что дает резкое уменьшение ростовой поверхности (табл. 5). При уменьшении времени остановки до 20 мин замедляется формирование монослоя.
Режим перемешивания клеток с микроносителями в первые 3 дня культивирования разработан с учетом характеристик клеточной культуры ПСХ и ее жизнеспособности (времени их закрепления и распластывания на поверхности микроносителей).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ВИРУССОДЕРЖАЩЕГО МАТЕРИАЛА ДЛЯ ИЗГОТОВЛЕНИЯ АНТИРАБИЧЕСКОЙ ВАКЦИНЫ | 1994 |
|
RU2083668C1 |
| СПОСОБ СТЕРИЛИЗУЮЩЕЙ ФИЛЬТРАЦИИ ВИРУССОДЕРЖАЩЕГО МАТЕРИАЛА ДЛЯ ПОЛУЧЕНИЯ КУЛЬТУРАЛЬНОЙ АНТИРАБИЧЕСКОЙ ВАКЦИНЫ | 1989 |
|
RU1755580C |
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКОСПЕЦИФИЧНОЙ ГЕТЕРОЛОГИЧНОЙ АНТИРАБИЧЕСКОЙ СЫВОРОТКИ | 2006 |
|
RU2322503C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВАКЦИНЫ ПРОТИВ БЕШЕНСТВА И ЧУМЫ ПЛОТОЯДНЫХ | 1994 |
|
RU2080125C1 |
| СПОСОБ СУСПЕНЗИОННОГО КУЛЬТИВИРОВАНИЯ ФИЛОВИРУСОВ В КЛЕТОЧНЫХ КУЛЬТУРАХ НА МИКРОНОСИТЕЛЯХ | 1993 |
|
RU2076905C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВАКЦИНЫ ПРОТИВ КЛЕЩЕВОГО ЭНЦЕФАЛИТА | 1993 |
|
RU2082432C1 |
| СПОСОБ ПОЛУЧЕНИЯ АНТИРАБИЧЕСКОЙ ВАКЦИНЫ | 2013 |
|
RU2538617C2 |
| СПОСОБ ПОЛУЧЕНИЯ АНТИРАБИЧЕСКОЙ ВАКЦИНЫ | 1986 |
|
SU1367487A1 |
| СПОСОБ ПОЛУЧЕНИЯ КУЛЬТУРАЛЬНОЙ ИНАКТИВИРОВАННОЙ ВАКЦИНЫ ПРОТИВ ВИРУСА БЕШЕНСТВА | 2023 |
|
RU2816765C1 |
| ВНК-21/13-13-ПЕРЕВИВАЕМАЯ МОНОСЛОЙНО-СУСПЕНЗИОННАЯ СУБЛИНИЯ КЛЕТОК ПОЧКИ НОВОРОЖДЕННОГО СИРИЙСКОГО ХОМЯЧКА, ПРЕДНАЗНАЧЕННАЯ ДЛЯ РЕПРОДУКЦИИ ВИРУСА ЯЩУРА И ВИРУСА БЕШЕНСТВА | 2014 |
|
RU2553552C1 |
Использование: вирусология, медицина. Сущность изобретения: после трипсинизации клетки почек сирийского хомяка заражают во взвесь фиксированным вирусом бешенства штамма Внуково-32, 32-38 пассажа. Зараженные клетки в концентарции 500 - 100 тыс. в 1 мл загружают в биореактор, в котором находятся микроносители Цитолар в концентрации 10 г/л ростовой среды. Культивирование проводят в дискретном режиме перемешивания: время перемешивания - 2 - 5 мин, время остановки в первые сутки - 120 мин, с последующим уменьшением времени остановки на 30 мин ежесуточно, с 4-го дня и далее остановка 30 мин. Скорость вращения мешалки - 15 - 20 об/мин.
СПОСОБ ПОЛУЧЕНИЯ КУЛЬТУРАЛЬНОЙ АНТИРАБИЧЕСКОЙ ВАКЦИНЫ, включающий заражение клеток почек сирийского хомяка фиксированным вирусом бешенства штамм Внуково 32 32 38 пассажа, его культивирование с последующим сбором вируссодержащей жидкости, отличающийся тем, что, с целью повышения выхода целевого продукта, культивирование проводят в биореакторе на микроносителях "Цитолар" с частотой вращения мешалки 15 20 мин-1 в дискретном режиме перемешивания: время перемешивания 2 5 мин, в первые сутки время остановки 120 мин, 2-е сутки 90 мин, 3-е сутки 60 мин, с 4-х суток и далее остановка 30 мин.
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Спускная труба при плотине | 0 |
|
SU77A1 |
Авторы
Даты
1995-04-10—Публикация
1991-02-15—Подача