Изобретение относится к области медицины, а именно к разработке и поиску новых противовирусных и бактериальных препаратов. Известно, что препарат алпизарин обладает противовирусной активностью (патент Японии N 1518445 на "Способ получения мангиферина", патент Англии N 2108383 на "Лекарственное средство алпизарин", патент США N 4436732 на "Лекарственное средство алпизарин", патент США N 4518592 на "Способ получения мангиферина", патент ФРГ N 31411970 на "Лекарственный препарат для лечения вирусных заболеваний", патент Франции N 8119820 на "Лекарственное средство алпизарин", патент Франции N 2486941 на "Способ получения мангиферина", авт. св. СССР N 1336301 на "Противовирусное средство алпизарин", заявка на патент РФ N 5014502 на "Способ получения мангиферина".
Алпизарин 2-C-β-D-глюкопиранозил-1,3,6,7-тетраоксиксантон получают из травы копеечника альпийского Hedysarum alpinum L. и копеечника желтеющего - Hedysarum flavescens Rgl. et Schmalh. семейства бобовых-Fabaceae (Leguminosae) и из листьев манго Mangifera indica L. семейства сумаховые - Anacardiaceae.
Известен противогерпетический препарат ВИРУ-МЕРЦ (мазь 1% по 5 г в тубах). Эффективен при простом герпесе кожи и слизистых оболочек в начальных стадиях заболевания. Недостатком препарата является:
узкий спектр действия;
не предупреждает развитие рецидивов;
не оказывает влияния на образование антител;
гиперергические реакции на коже (контактная аллергия), вызываемые применением препарата (проспект на препарат "ВИРУ-МЕРЦ" фирмы "Фармакос", Югославия).
Известен противогерпетический препарат ацикловир (зовиракс) (таблетки по 200 мг, крем 5% раствор для внутривенного вливания). Эффективен при кожных заболеваниях, вызываемых вирусом простого герпеса, включая первичные и рецидивирующие герпесы гениталий и герпес губ. Недостатком этого препарата является:
болезненность инъекций;
поражение почечных канальцев при длительном введении;
развитие устойчивости;
узкий спектр действия.
Известны методы и составы, использующие полинасыщенные жирные кислоты для лечения малярии и других заболеваний (WO 93/0008, кл. A 61 K 31/20, 1993).
Известны стабильные формы биологически активных протеинов для парантеральных инъекций, содержащие рекомбинантный интерлейкин-2 или интерферон-b, обладающие биологической активностью в отношении бактерий и вирусов (US 4816440, кл. A 61 K 37/02, 1989). Данное техническое решение принято за прототип [2]
Не все препараты, обладающие ингибирующим действием в отношении вируса герпеса, ингибируют развитие цитомегаловируса. Препараты оксолин (проспект "Оксолин", ЦБНТИмедпром), бонафтон (проспект "Бонафтон", ЦБНТИмедпром), арбидол (проспект "Арбидол", Всесоюзный научно-исследовательский химико-фармацевтический институт им. С. Орджоникидзе), виразол (проспект "Виразол", ICN Pharmaceuticals, Juc) обладают противогерпетической активностью, но тем не менее сведения об их активности в отношении цитомегаловируса отсутствуют.
Целью изобретения является расширение области применения алпизарина за счет выявления новых свойств препарата.
Указанная цель обеспечивается тем, что лечение вирусных и бактериальных инфекций, а также в качестве иммуностимулятора, иммуномодулятора и индуктора интерферона предлагается алпизарин 2-С- b-D-глюкопиранозил-1,3,6,7-тетраоксиксантон.
Экспериментально установлено, что алпизарин наряду с известным ранее действием на вирус герпеса обладает противовирусной активностью в отношении цитомегаловируса, вируса иммунодефицита и антимикробной активностью в отношении грамположительных и грамотрицательных бактерий (Mycobacterium tuberculosis, Entamoeba histolitica, Trichomonas vaginalis). Выявлены также его иммуностимулирующие, иммуномодулирующие и интерферониндуцирующие свойства.
Новизна и изобретательский уровень заключаются в выявлении новой совокупности признаков (спектра противовирусной активности), а также в выявлении антибактериальной активности в отношении грамположительных и грамотрицательных бактерий.
Способ получения алпизарина описан в заявке на патент N5014502 от 06.09.91 г. МКИ5 A 61 K 35/78 "Способ получения мангиферина".
Отличительной особенностью алпизарина является наличие наряду с противовирусной активностью антимикробной активности, а также иммуностимулирующих, иммуномодулирующих и интерферониндуцирующих свойств. Малотоксичен, полное отсутствие побочных эффектов.
По показателям токсичности при однократном внутрибрюшинном, внутрижелудочном способах введения лабораторным животным алпизарин является малотоксичным веществом. При внутрибрюшинном введении ЛД50 для самцов мышей, крыс и морских свинок равны соответственно: 1385±121; 780±84 и 650±39 мг/кг. При введении алпизарина в желудок мышам самцам и самкам ЛД50 увеличиваются в 10-12 раз, крысам самцам и самкам в 18-20 раз и составляют 13000-15900 мг/кг.
Алпизарин не обладает аллергизирующим, мутагенным и местнораздражающим действием.
Алпизарин разрешен к применению у взрослых и детей в качестве противовирусного средства при острых и рецидивирующих формах простого герпеса генитальной и экстрагенитальной локализации, экземе Капоши, при вирусных заболеваниях слизистой оболочки полости рта, опоясывающем лишае, ветряной оспе (решение Фармакологического комитета М3 РФ от 29 марта 1993 г.).
Пример 1. Изучение иммуномодулирующих свойств алпизарина.
Влияние алпизарина на гуморальное звено иммунитета.
В эксперименте использованы 200 мышей линии СВА (самцы, масса 20-22 г) и 60 беспородных крыс (самцы, масса 260-280 г). Основополагающей для изучения иммуномодулирующего действия алпизарина явилась модель иммунного ответа на гетерогенные эритроциты. Результаты оценивали по титру антител к эритроцитам барана (ЭБ) в микрореакции гемагглютинации и количеству антителообразующих клеток (АОК) селезенки. Число АОК в селезенке определяли методом локального гемолиза и модификации Cunningham (1965). Животных иммунизировали оптимальной дозой ЭБ. Алпизарин вводили в дозах 10 и 100 мг/кг в желудок мышам линии СВА в течение 5 дней, а крысам в течение 4 недель. В качестве растворителя был использован 40% диметилсульфоксид (ДМСО). В результате проведенных исследований обнаружено, что 5-кратное введение алпизарина в дозах 10 и 100 мг/кг в желудок мышам линии СВА существенно усиливало трансформацию В-лимфоцитов в плазматические клетки. Число АОК в селезенке в 2,5-4 раза увеличивалось. Кроме того, в 3-7 раз возросло количество антител к эритроцитам барана (табл. 1).
Полученные данные подтверждаются и в экспериментах на беспородных крысах, получавших препарат в дозах 10, 100, 500 мг/кг в желудок в течение 4 недель. Выявлен четкий дозозависимый эффект. Алпизарин в 1,5-2,5 раза увеличивал количество АОК в селезенке, стимулировал образование антител (табл. 2).
Таким образом, алпизарин в экспериментах на животных во всех испытанных дозах стимулировал образование антител к тимусзависимому антигену, повышал активность эффекторов гумморального иммунитета.
Изучение иммуностимулирующих свойств алпизарина.
Иммуностимулирующая активность алпизарина была изучена в модельной системе образования специфических цитолитических т-лимфоцитов (т-киллеров) в смешанной культуре лимфоцитов (Mixed Lympgocyte Culture, MLC) из селезенок аллогенных мышей.
Методика. С целью получения цитолитических лимфоцитов селезенки мышей BALB СЗН извлекали асептически, осторожно гомогенизировали в стеклянных гомогенизаторах Поттера в среде RPMI-1640, фильтровали через несколько слоев марли и подсчитывали с помощью зозонтрипанового синего количество живых клеток. Стимуляцию in vitro проводили по описанному ранее методу с некоторой модификацией. В качестве реагирующих клеток использовали лимфоциты мышей BALB/c (H-2d в концентрации 5•106 в 1 мл, в качестве стимулирующих клетки селезенки мышей СЗН (H-2k), облученных перед инкубацией дозой 1000 Р. Соотношение реагирующих и стимулирующих клеток в большинстве опытов составляло 5:1. Контролем служили монокультуры лимфоцитов BALS/c или облученные лимфоциты мышей СЗН. Культуральная среда содержала 100 мл среды дМЕМ, 20% инактивированной эмбриональной телячьей сыворотки (ТЭС), 2•103 м глутамина, 5•103 ХЕПЕС, 3•105 2-меркаптоэтанола, пенициллина и стрептомицина по 100 ЕД на 1 мл среды. Инкубацию проводили в 24 луночных плоскодонных платах 76-03 (Linbro) в термостате "Napco" при 5% CO2 в течение 5 сут. Препарат алпизарин растворяли в растворе Хенка, стерилизовали пропусканием через фильтр "Миллипор" и вносили в культуру в объеме 10 мкл на срок до 2 сут. Каждая серия опытов повторялась не менее 3 раз. Для определения активности образовавшихся в MLC специфических Т-киллеров лимфоциты инкубировали с клетками-мишенями в соотношении 0,2:1, 1:1, 5:1, 20:1 в 0,2 мл среды RPMI-1640 c 5% ТЭС в 96-луночных плоскодонных платах (FLOW LAB) в течение 18 ч при 37oC. В качестве мишеней использовали монослой лимфоцитов (H-2k, которые накануне опыта инкубировали со 100 мкКи Na251CrO4 в 1 мл среды RPMI-1640 с 5% ТЭС в течение 1 ч при 37oC. Затем клетки трижды отмывали средой 199 и разливали в лунки микроплат (FLOW LAB) в количестве 104 клеток на лунку. Каждое определение (одно соотношение лимфоцит: клетка-мишень) проводили в 6 параллельных пробах. Для определения спонтанного лизиса клетки-мишени инкубировали с той же средой без лимфоцитов. В наших опытах спонтанный лизис, как правило, равнялся 15-20% После окончания инкубирования на счет отбирали из каждой лунки по 0,1 мл надосаочной жидкости, которую переносили в пластиковые пробирки. Радиометрию образцов проводили на гамма-счетчике фирмы "Nuclеar Chicago". Процент специфического цитолиза определяли по формуле: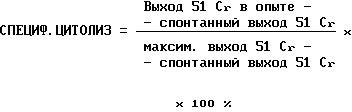
где максимальный выход 51 Cr выход изотопа в надосадочную жидкость после обработки клеток-мишеней 2% раствором додецилсульфата Na в 0,05 М растворе боратного буфера pH 9,9.
Результаты исследования отражены в табл.3 и 4.
Установлено, что алпизарин, добавленный в культуру in vitro на 0-2 день инкубации в концентрации 1 мкг/мл, усиливал образование Т-киллеров в 1,5-2,5 раза. Таким образом, можно говорить, что алпизарин обладает иммуностимулирующими свойствами в отношении клеточного иммунитета.
Пример 2. Изучение интерферониндуцирующих свойств алпизарина.
На интерферонпродуцирующую активность алпизарин испытывали у доноров и больных рецидивирующих герпесом.
В работе был использован метод определения способности клеток к выработке альфа- и гамма-интерферонов в цельной крови и в сравнении с общепринятыми индукторами гамма-интерферона стафилококковым эндотоксином типа А и альфа-интерферона вирусом болезни Нью-Каслс.
Выявлено, что препарат обладает способностью вызывать выработку интерферона, по количественным показателям сравнимую с выработкой гамма-интерферона под действием СЭА у исследуемых индивидуумов. Причем интерферониндуцирующая активность алпизарина проявлялась на клетках крови и не выявлена на диплоидных фиблобластах человека М-19, что доказывает действие препарата именно на клетках крови.
Кроме того, выявлена зависимость от дозы препарата на интерферонпродуцирующую активность клеток крови. У доноров одинаковой эффективностью обладали дозы препарата 10 и 100 мкг/мл, а у больных 50 мкг/мл. При типировании интерферонов доведением pH до 2 и проведением реакции нейтрализации с моноклональными антителами к альфа- и гамма-интерферонами человека обнаружено, что индуцируется кислотостабильный интерферон типа гамма.
Таким образом, алпизарин является перспективным препаратом для включения в курс противовирусной и иммунокоррегирующей терапии, так как он обладает, помимо известной противовирусной активности, способностью индуцировать продукцию гамма-интерферона в клетках крови.
Пример 3. Изучение эффективности алпизарина в отношении вируса иммунодефицита человека (СПИД).
Материалы и методы.
Вирусы. Использовали вирус иммунодефицита человека I типа, штамм HTLV-III, продуцируемый клеточной линией H9/IIIB.
Клетки. В работе использовали первично-трипсинизированную культуру фибробластов эмбрионов кур (ФЭК), перевиваемые культуры Т-лимфоцитов человека H9 и H9/IIIB, первичные культуры спленоцитов мышей линии C57BL/6.
Животные. Нелинейные белые мыши обоего пола.
Иммунные сыворотки. Используемые для контроля вирусных штаммов: сыворотки больных СПИД (B.F.Vestergaard, Государственный Институт сывороток, Копенгаген, Дания).
Заражение клеток H9 ВИЧ-I. Клетки H9 заражали ВИЧ-I, подсевая живые клетки культуры H9/IIIB. Препарат вносили в культуру H9 + H9/IIIB непосредственно после заражения. Опыты сопровождали контролем культуры без препарата и контролем токсичности доз алпизарина для клеток H9.
Уровень продукции ВИЧ-I зараженными культурами оценивали:
по количеству клеток (%), экспрессирующих вирусные антигены на мембранах, определяемому методом непрямой иммунофлуоресценции;
по активности обратной транскриптазы ВИЧ-I в супернатанте.
Влияние алпизарина на экспрессию СД4-рецептора оценивали после 24-часовой инкубации алпизарина с клетками H9 методом проточной флуоцитометрии на лазерном сортере с использованием моноклональных антител, меченных ФНТЦ-ОКТ4 (в качестве контроля ОКТ8).
Исследование эффективности алпизарина проводили в опытах in vitro в смешанной культуре клеток H9/IIIB и H9. Смесь (1:1) клеток готовили непосредственно перед опытом и разливали по 2 мл в каждую лунку в 24-луночных планшетах фирмы "Coster". Одновременно в лунки вносили алпизарин из расчета получить в лунках конечные концентрации 50, 25, 5 и 1 мкг/мл. Планшеты инкубировали при температуре 37oC и 5% CO2 в течение 7 сут. Жизнеспособность клеточных культур оценивали ежедневно с помощью инвертированного микроскопа. Результаты опыта учитывали на 7 сут методом непрямой иммунофлуоресценции с использованием сыворотки больного СПИД в разведении 1:40.
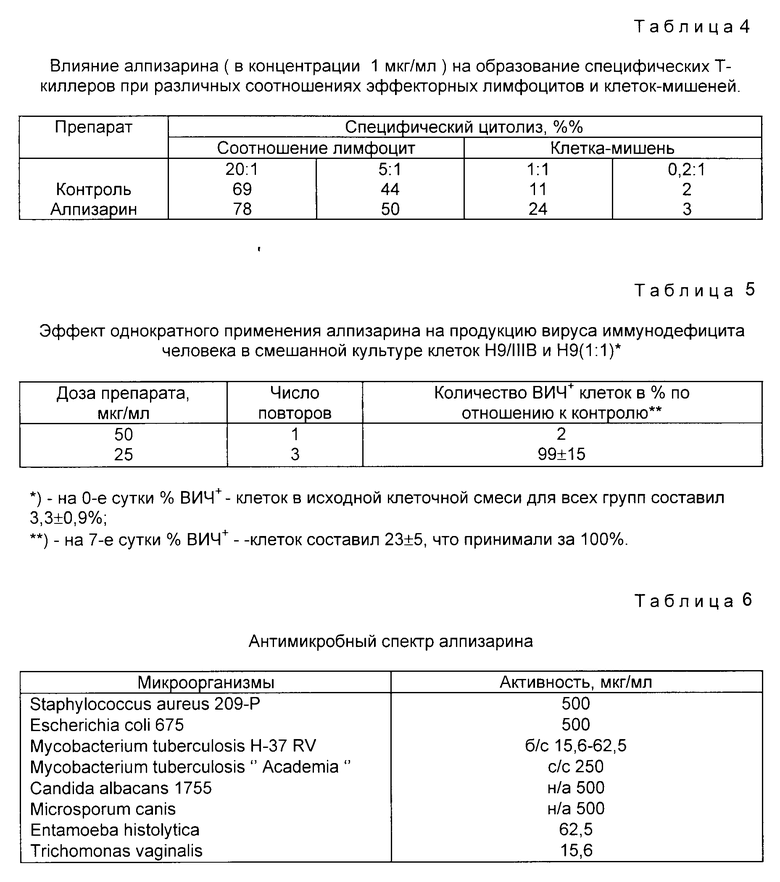
В результате исследования установлено (табл. 5), что алпизарин в концентрации 50 мкг/мл ингибирует почти полностью вирусную продукцию в изученной системе клеток H9/IIIB и H9. В более низких концентрациях (25, 5 и 1 мкг/мл) ингибирующий эффект алпизарина в данных условиях опыта не выявлен.
Полученные данные свидетельствуют о способности предохранения алпизарином неинфицированных вирусом клеток H9 от заражения их вирусом в условиях совместного культивирования с клетками H9/IIIB.
Пример 4. Действие алпизарина на цитомегаловирус в культуре клеток.
Целью исследования явилось изучение алпизарина на репродукцию цитомегаловируса (ЦМВ) в культуре клеток.
Материалы и методы.
Действие алпизарина на репродукцию цитомегаловируса изучали на диплоидных клетках человека М-19.
Диплоидные клетки получали из кожи и мышц 7-10-недельных эмбрионов человека.
Дезагрегацию тканей осуществляли 0,25% раствором трипсина. Аналогичный раствор фермента использовали для отделения клеток от стекла в процессе пассажей. В качестве среды роста применяли среду Игла МЕМ с 10% эмбриональной телячьей сывороткой. При морфологическом изучении линий отмечено, что культуры состоят из фибробластоподобных клеток. Кариологический анализ показал, что клетки относят к группе диплоидных линий.
В работе был использован эталонный штамм ЦМВ человека Ad-169. В культуре клеток вирус вызывал специфические цитопатические поражения на 7 сут с типичными внутриядерными включениями. Инфекционный титр составлял 105 ТЦД50/мл.
Препарат алпизарин применяли в концентрациях 250, 125, 50 и 25 мкг/мл.
Культивирование клеток проводили в пробирках на покровных стеклах с использованием среды Игла в 10% эмбриональной телячьей сыворотки. В пробирки с выросшими культурами добавляли 0,2 мл вируса с титром 105ТЦД50/мл. После адсорбции в течение 1 ч вирус удаляли и вводили поддерживающую среду роста: смесь среды Игла и среды 199 в равных объемах (50%) с 2% эмбриональной телячьей сыворотки.
Через 48 ч, а также в течение двух недель покровные стекла извлекали из пробирок, окрашивали гематоксилином и эозином и определяли количество очагов поражения клеточного пласта под световым микроскопом.
Результаты исследования.
В результате проведенных исследований установлено, что алпизарин в концентрациях 250, 125, 50 и 25 мкг/мл не оказывал токсического действия на незараженные клеточные культуры в течение всего периода наблюдения.
Алпизарин в концентрации 100 мкг/мл полностью подавлял репродукцию цитомегаловируса штамм Ad-169 на 5 lg ТЦД50/мл, что составляет 10 000 инфекционных доз вируса.
Пример 5. Изучение антимикробного спектра алпизарина.
Методика исследования.
При определении антимикробного спектра алпизарина использовали следующие тест-микроорганизмы: Staphylococcus aureus 209-P, Escherichia coli 675, Mycobacterium tuberculosis H-37 RV, Mycobacterium tuberculosis "Academia", Candida albicans 1755, Microsporum canis, Entamoeba histolytica, Trichomonas vaginalis.
При определении бактериостатической активности алпизарина использовали мясо-пептонный бульон (МПБ).
Фунгистатическое действие изучали в жидкой среде Сабуро.
Туберкулостатический эффект изучали в жидкой среде Сотона.
Навеску препарата не менее 10 мг вносили в стерильную пробирку и стерилизовали в течение 1 ч 95%-ным этиловым спиртом (этиловый спирт в концентрации 2% не оказывал антимикробного действия) из расчета 0,1 мл спирта на 5 мг препарата. Затем добавляли соответствующую каждому микроорганизму стерильную питательную среду в количестве, необходимом для создания исходной концентрации препарата 1000 мкг/мл. Из данной пробирки путем двухкратных серийных разведений готовили ряд убывающих концентраций. Последняя пробирка с чистой средой (без добавления препарата) служила контролем. После этого все пробирки (опытные и контрольные) засевали культурами микроорганизмов.
Взвеси грамположительных и грамотрицательных бактерий готовили в изотоническом растворе натрия хлорида по бактериальному стандарту мутности 10 ЕД (109 микробных тел/мл), затем в каждую пробирку вносили по 0,2 мл взвеси, содержащей 104 микробных тел/мл. Посевы инкубировали в термостате при температуре 37-38oC в течение 24 ч.
Взвесь грибов готовили в изотоническом растворе натрия хлорида по бактериальному стандарту мутности 10 ЕД, затем разводили изотоническим раствором в 20 раз. В опытные и контрольные пробирки засевали по 0,2 мл полученной взвеси. Посевы инкубировали при температуре 30oC: дрожжеподобные грибы в течение 48 ч, мицелиальные грибы 10-14 сут.
Взвеси микобактерий туберкулеза готовили в изотоническом растворе по стандарту БЦЖ, содержащему 5 мг бацилл в 1 мл. Полученную взвесь разводили средой Сотона 1:10 и вносили в каждую пробирку по 0,2 мл разведенной взвеси, содержащей 0,1 мг бацилл в 1 мл, и инкубировали в термостате при температуре 37oC в течение 7-10 сут.
Опыты проводили в трех повторностях.
Учет результатов.
Антибактериальный и антифунгальный эффект определяли по минимальной концентрации препарата (мкг/мл), при которой визуально не наблюдали роста микроорганизмов.
Результаты исследования.
В результате исследования установлено (табл. 6), что алпизарин ингибирует рост грамположительных и грамотрицательных бактерий в концентрации 500 мкг/мл; туберкулезных микобактерий в концентрации 15,6-62,5 мкг/мл, простейших в концентрации 15,6-62,5 мкг/мл. В отношении дрожжеподобных и мицелиальных грибов алпизарин не активен.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ВИРУСНЫХ ЗАБОЛЕВАНИЙ | 1994 |
|
RU2118163C1 |
| СПОСОБ ПОЛУЧЕНИЯ МАНГИФЕРИНА | 1991 |
|
RU2032413C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОТИВОВИРУСНОГО ПРЕПАРАТА "ГИПОРАМИН" | 1994 |
|
RU2098111C1 |
| ИММУНОМОДУЛИРУЮЩЕЕ СРЕДСТВО ПРИ ВТОРИЧНЫХ ИММУНОДЕФИЦИТНЫХ СОСТОЯНИЯХ | 2008 |
|
RU2375072C1 |
| ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКОЕ СРЕДСТВО "ПРОСТАНОРМ" ДЛЯ ЛЕЧЕНИЯ ПРОСТАТИТОВ, УРЕТРИТОВ И ДРУГИХ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ МОЧЕПОЛОВОЙ СФЕРЫ | 1996 |
|
RU2098119C1 |
| КОМПЛЕКС ПРИРОДНЫХ СОЕДИНЕНИЙ РАСТИТЕЛЬНОГО ПРОИСХОЖДЕНИЯ, АКТИВНЫЙ В ОТНОШЕНИИ ВИРУСНЫХ ИНФЕКЦИЙ, ПЕРЕДАВАЕМЫХ ПОЛОВЫМ ПУТЕМ | 2002 |
|
RU2200569C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ИНТЕРФЕРОНИНДУЦИРУЮЩЕЙ И ИММУНОМОДУЛИРУЮЩЕЙ (ИММУНОСТИМУЛИРУЮЩЕЙ) АКТИВНОСТЬЮ | 1987 |
|
RU2033157C1 |
| АРИЛ- И ГЕТЕРИЛАМИДЫ КАРБОАЛКОКСИСУЛЬФАНИЛОВЫХ КИСЛОТ | 1998 |
|
RU2199526C2 |
| 2,4-ДИОКСО-5-АРИЛИДЕНИМИНО-1,3-ПИРИМИДИНЫ | 1998 |
|
RU2198166C2 |
| N-ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ 5-ОКСИИМИНОБАРБИТУРОВОЙ КИСЛОТЫ | 1998 |
|
RU2188196C2 |

Использование: изобретение относится к медицине и касается биологически активного вещества пртивовирусного и антимикробного действия. Целью изобретения является выявление новой совокупности признаков (спектр пртивовирусный, антимикробной активности, иммуностимулирующих, иммуномодулирующих и интерферониндуцирующих свойств) у препарата алпизарина. Положительный эффект заключается в выявлении выраженной активности алпизарина в отношении цитомегаловируса, вируса иммунодефицита человека, туберкулезных микробактерий и простейших. 6 табл.
Применение алпизарина в качестве средства, обладающего действием против инфекционных агентов, таких, как вирус иммунодефицита человека, цитомегаловирус, туберкулезные микобактерии и простейшие.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Противовирусное средство "Алпиразин | 1974 |
|
SU1336301A1 |
| Устройство для сортировки каменного угля | 1921 |
|
SU61A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Патент США N 4816440, кл | |||
| Устройство для сортировки каменного угля | 1921 |
|
SU61A1 |
Авторы
Даты
1997-10-10—Публикация
1994-08-19—Подача