Изобретение относится к высокомолекулярным химическим соединениям, в частности к комплексным соединениям цисдиамминоплатины (II ).
Известно аналогичное по структуре соединение: сополимер Na-соли малеиновой кислоты с 1,4-диизопропоксибутеном-2 (ДИПБ) формулы (I):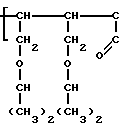 H
H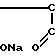 H
H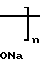 (I) n 8-10, М 2600-3300, но в отличие от заявленного соединения не содержащее комплексно-связанной платины. Установлено, что соединение формулы I проявляет противовирусную активность, но не оказывает противоопухолевого действия (см. табл.1).
(I) n 8-10, М 2600-3300, но в отличие от заявленного соединения не содержащее комплексно-связанной платины. Установлено, что соединение формулы I проявляет противовирусную активность, но не оказывает противоопухолевого действия (см. табл.1).
Ближайшим аналогом к заявленному соединению по противоопухолевой активности является цис-диамминодихлорплатины (II) (цисплатин), имеющая структурную формулу Pt
Pt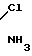
Цисплатин широко применяется в клинической практике в клинической практике лечения онкологических заболеваний. По механизму действия относится к цитостатикам, подавляющим синтез ДНК опухолевых клеток. Однако при проведении противоопухолевой терапии цисплатин, как и другие цитостатики, помимо действия на злокачественные новообразования оказывают значительное токсическое влияние на организм. Цисплатин в высокой степени токсическое вещество (ЛД50 12-14 мг/кг для мышей и крыс). Главным фактором, который лимитирует терапевтический курс и вынуждает прервать лечение повреждение в разной степени (в зависимости от дозы) извитых канальцев почек.
Целью изобретения является создание комплексного соединения цис-диамминоплатины (П) с сополимером Na-соли малеиновой кислоты и 1,4-диизопропоксибутена-2, обладающего противоопухолевой активностью с широким интервалом терапевтических доз при полном отсутствии нефротоксичности и иммунодепрессантного действия.
Соединения представляют собой аморфные порошки желтого цвета, хорошо растворимые в воде и физиологическом растворе, плохо растворимые в спиртах и нерастворимые в ацетоне, хлороформе, диэтиловом эфире и углеводородах. При нагревании комплексы разлагаются без плавления при температуре ≈ 190о С. Полимерные комплексы получают взаимодействием сополимера Na-соли малеиновой кислоты и 1,4-ДИПБ формулы I с цис-диамминодигидроксоплатиной (П) формулы (II), взятых в молярных соотношениях (8:1)-(2:1) (избыток полимерного компонента) в водном растворе.
Состав продуктов реакции (параметр х) регулируют путем изменения молярного соотношения Pt-содержащего и полимерного реагентов реакционной смеси (см. примеры).
Структуру полученных полимерных комплексов подтверждают методами элементного анализа, атомно-адсорбционной спектроскопии и ИК-спектроскопии.
Соединения формулы I характеризуются следующими колебательными частотами в ИК-спектрах (полученных на приборе Specord М80, см-1:
1390, 1610 валентные колебания СОО- -групп
2990-2940 валентные колебания С-Н-связей СН3-групп
1070-1100 валентные колебания простых эфирных связей С-О-С
530-470 валентные колебания связи Pt-N
Вышеприведенные спектральные данные, а также данные элементного анализа и атомно-адсорбционной спектроскопии (см.примеры) указывают на то, что полимерный комплекс имеет следующее строение: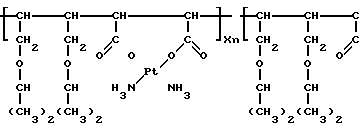 H
H H
H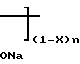
где х 0,11-0,44 (определяется по данным элементного анализа и атомно-адсорбционной спектроскопии); М определяют по молекулярной массе использованного для синтеза сополимера Na-соли малеиновой кислоты с 1,4-ДИПБ.
Получение комплексов иллюстрируется следующими примерами.
П р и м е р 1. В дистиллированной воде (100 мл) растворяют 0,18 г (0,0003 моль) Pt (NH3)2Cl2 и добавляют водный раствор 0,204 г (0,0012 моль AgNO3 (реакция I)
Pt(NH3)2Cl2+2AgNO3_→ [Pt(NH3)2(OH)2](NO3)2+AgCl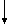
Выпавший осадок AgCl отфильтровывают, а фильтрат приливают при перемешивании к раствору сополимера Na-соли малеиновой кислоты и ДИПБ 0,39 г (0,0012 моль в расчете на мономерное звено), растворенному в 100 мл дистиллированной воды (реакция II)
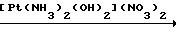 NaNO3+
NaNO3+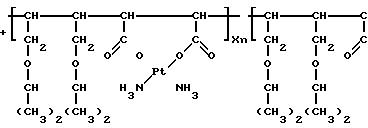 H
H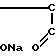 H
H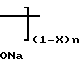
(II)
Для очистки от низкомолекулярных примесей (NaNO3, непрореагировавший платиновый комплекс) водный раствор комплексного соединения платины с сополимером подвергают ультрафильтрации, выделяют из раствора путем лиофильной сушки и досушивают в вакууме до постоянного веса.
Количества реагентов, взятых для реакции, соответствуют молярному соотношению 2:1 (избыток полимерного компонента). Выход 0,343 г (70% от теор. ).
Элементный состав полученного продукта.
Вычислено, С 39,6; Н 5,9; О 22,67; N 3,3; Na 5,3; Pt 23,0.
Найдено, 20,5; Н 6,4; N 2,9; Pt 20,1; Na 4,8.
Таким образом, получено комплексное соединение следующей формулы: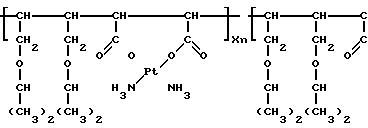 H
H H
H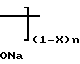
где х 0,44, М 4500, n 10.
П р и м е р 2. Условия получения комплексного соединения платины с сополимером аналогичны условиям, описанным в примере 1. Для реакции берут 0,39 г (0,0012 моль) сополимера Na-соли малеиновой кислоты с 1,4-ДИПБ, 0,09 г (0,0003 моль) Pt (NH3)2Cl2 и 0,117 г (0,0006 моль) AgNO3, что соответствует соотношению реагентов 4: 1 (избыток полимерного компонента). Выход 0,32 г (72% от теор.).
Элементный состав полученного продукта.
Вычислено, С 44,5; Na 9,1; Н 6,22; N 1,9; Pt 13.
Найдено, С 45,2; Н 6,8; N 1,7, Р 10; Na 8,3.
Таким образом, получено соединение
следующей формулы: H
H H
H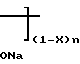
х 0,21, М 3000, n 8.
П р и м е р 3. Условия получения комплексного соединения платины с сополимером аналогичны условиям, описанным в примере 1. Для реакции берут 0,39 г (0,0012 моль) сополимера Na-соли малеиновой кислоты с 1,4-ДИПБ, 0,045 г (0,00015 моль) Pt(NH3)2Cl2 и 0,058 г (0,0003 моль) AgNO3, что соответствует соотношению реагентов 8:1 (избыток полимерного компонента). Получено 0,31 г (73,1% от теор.).
Элементный состав полученного продукта.
Вычислено, Na 11,3; С 47,3; Н 6,4; N 1; Pt 6,8.
Найдено, С 48,5; Н 7,6; Na 10,8; N следы; Р 6,0.
Выход 0,31 г (73,1% от теор.).
Таким образом, получено комплексное соединение следующей формулы: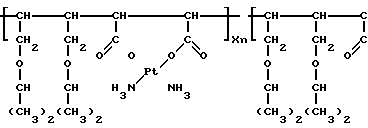 H
H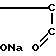 H
H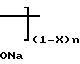
где х 0,11; n 10; М 3000.
Определение острой токсичности заявляемого соединения проводят по методу В.Б. Прозоровского.
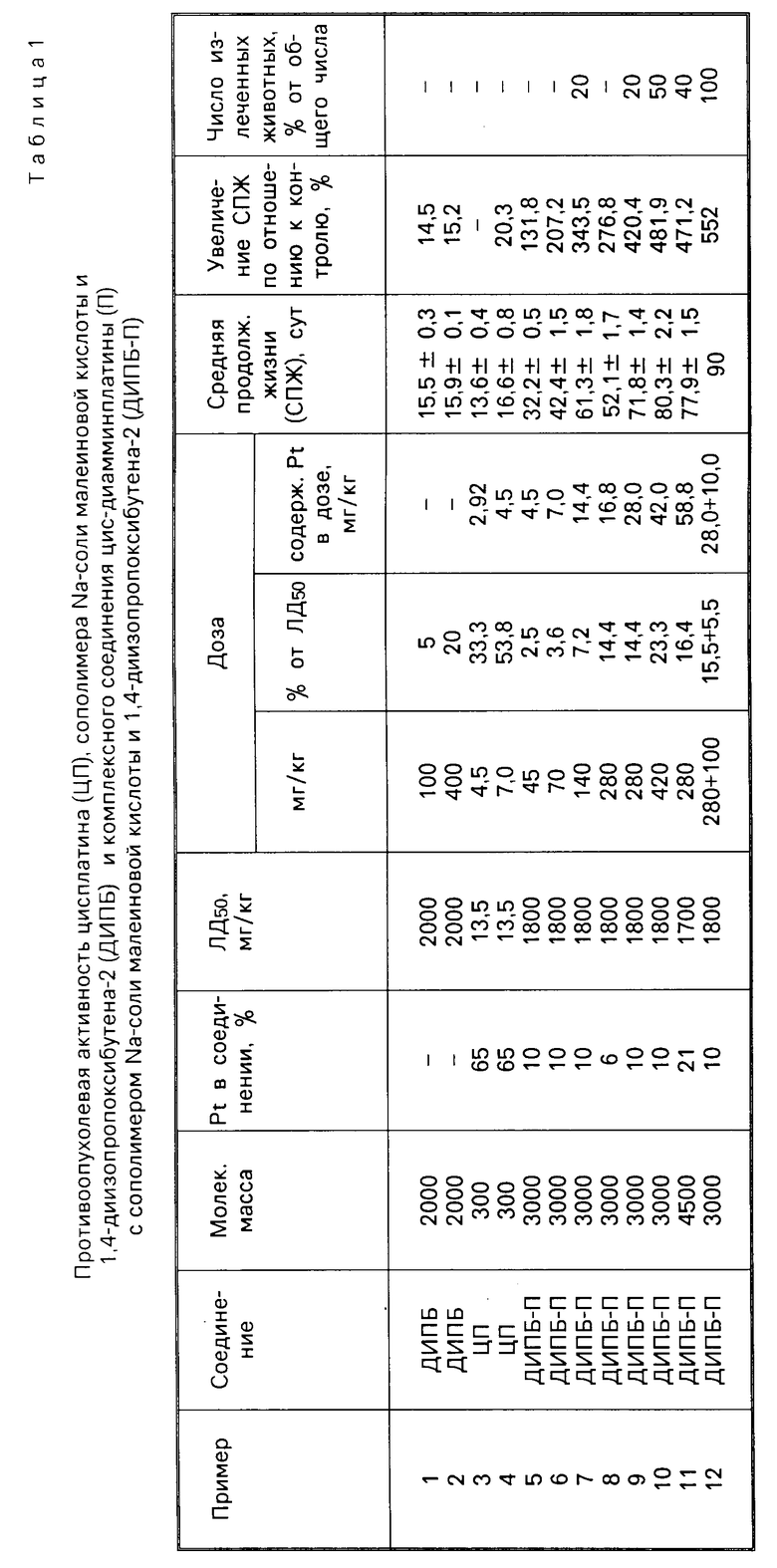
Изучение противоопухолевой активности полимерного комплекса платины проводят в эксперименте на беспородных мышах (самках массой 20-25 г) с привитой внутрибрюшинно аденокарциномой Эрлиха.
Асцитная карцинома Эрлиха опухоль, относительно резистентная к действию широко применяемого в настоящее время в клинике цисплатина формулы II и рекомендована Фармкомитетом СССР в качестве одной из моделей для испытания новых химиопрепаратов.
Перевивку опухоли осуществляется внутрибрюшинно введением 0,5 мл асцитической жидкости. Препараты растворяют в физиологическом растворе и вводят животным внутрибрюшинно однократно через сутки после перевивки опухоли. Эффективность проведенной терапии оценивают на основании изменения средней продолжительности жизни животных (СПЖ) в опыте по сравнению с контролем и по числу извлеченных животных. Результаты испытаний представлены в табл.1.
Изучена противоопухолевая активность комплекса на модели лимфолейкоза Р-388, также рекомендованного Фармкомитетом СССР для испытаний новых химиопрепаратов. При введении мышам с экспериментальным лимфолейкозом Р-288 ДИПБ-П в дозе 600 мг/кг наблюдалось увеличение СПЖ на 75% по сравнению с контролем, в то время как введение ЦП в максимально переносимой дозе 7 мг/кг приводит к увеличению СПЖ только на 30%
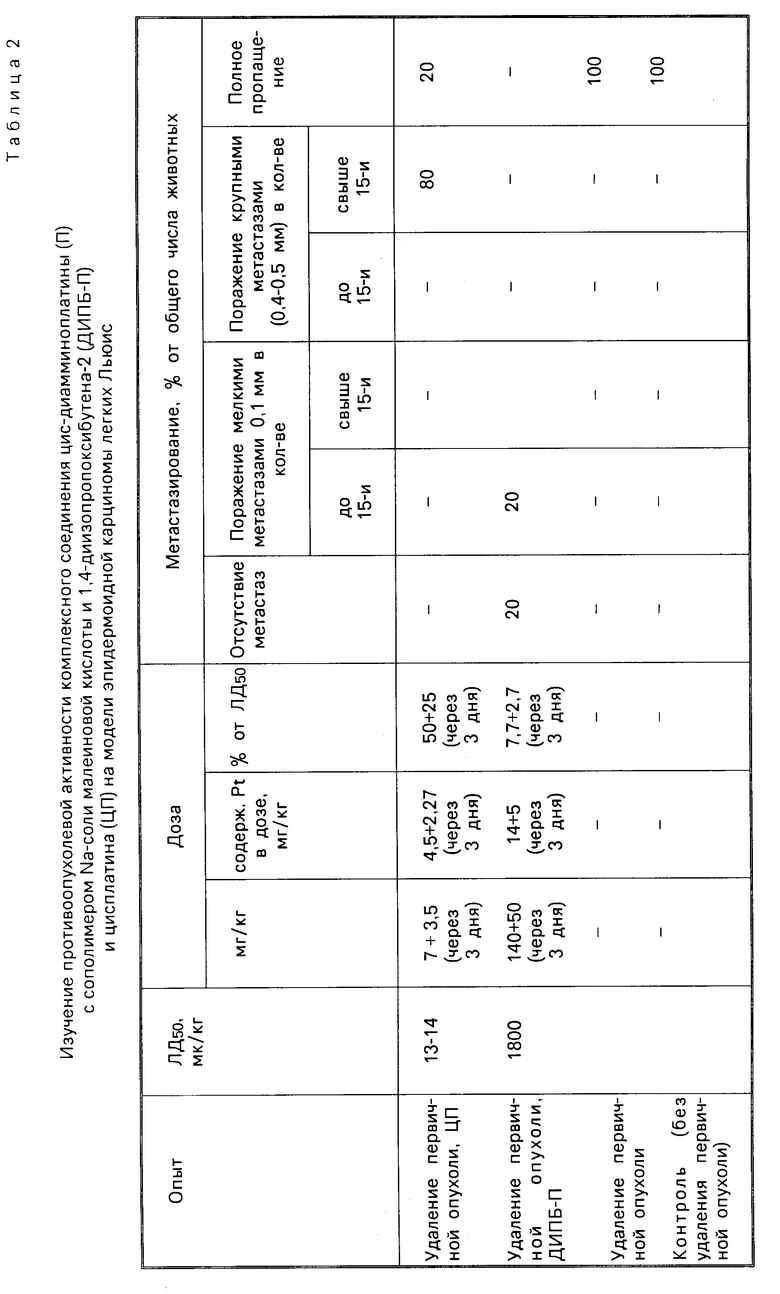
Следует остановиться на опытах с экспериментальной моделью метастазирования эпидермоидной карциномой легких Льюис (LLC). Из результатов, представленных в табл.2, видно, что метастазирование в легких при применении заявляемого полимерного комплекса снижается ≈ в 3 раза по сравнению с цисплатином.
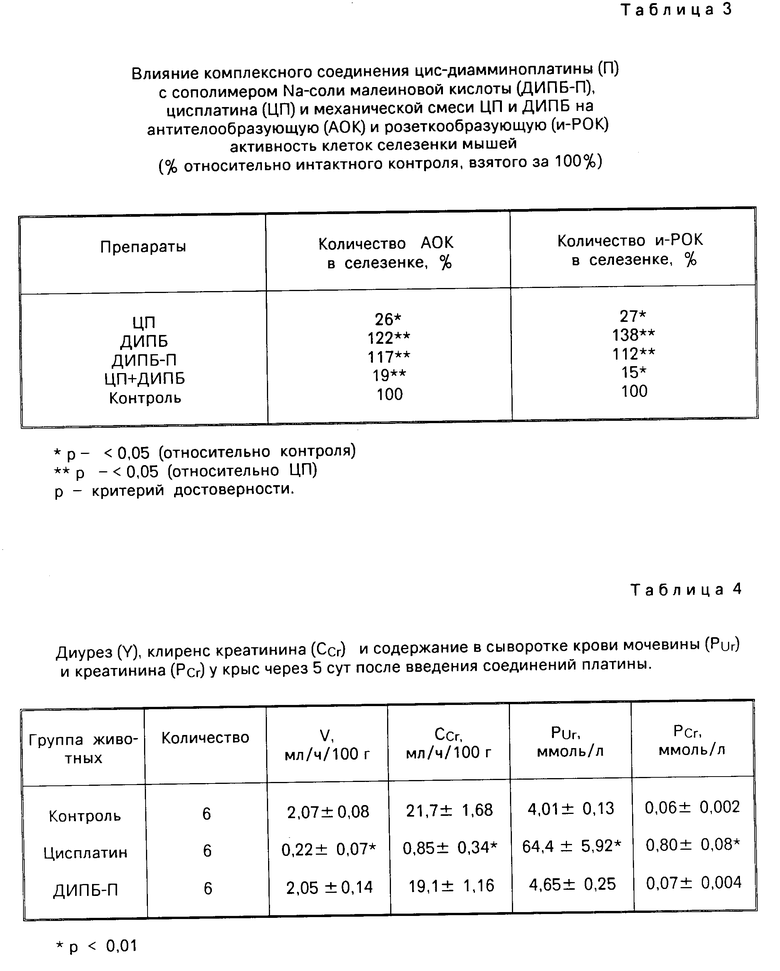
Проведено изучение влияния полимерного комплекса платины на некоторые показатели иммунного ответа. Исследования проводят на мышах-самцах линии СВА. В эксперименте используют пять групп животных, каждой из которых вводили, соответственно, цисплатин (аналог по биологической активности), сополимер Na-соли малеиновой кислоты и 1,4-диизопропоксибутена-2 (аналог по структуре), их механическую смесь, а также комплексное соединение платины. ЦП вводят в максимально переносимой дозе 7 мг/кг (содержащей 4,5 мг/кг платины), ДИПБ-П в дозе 45 мг/кг (содержащей 4,5 мг/кг платины). Механическую смесь составляют из расчета 40 мг/кг ДИПБ и 7 мг/кг ЦП (4,5 мг/кг платины). Препараты растворяют в физиологическом растворе и вводят животным внутрибрюшинно. Одновременно вводят антиген, в качестве которого используют эритроциты барана. В процессе исследований изучают следующие показатели: изменение антителообразующей способности клеток селезенки (АЛК) и розеткообразующую активность лимфоидных клеток селезенки (И-РОК). Полученные результаты представлены в табл.3.
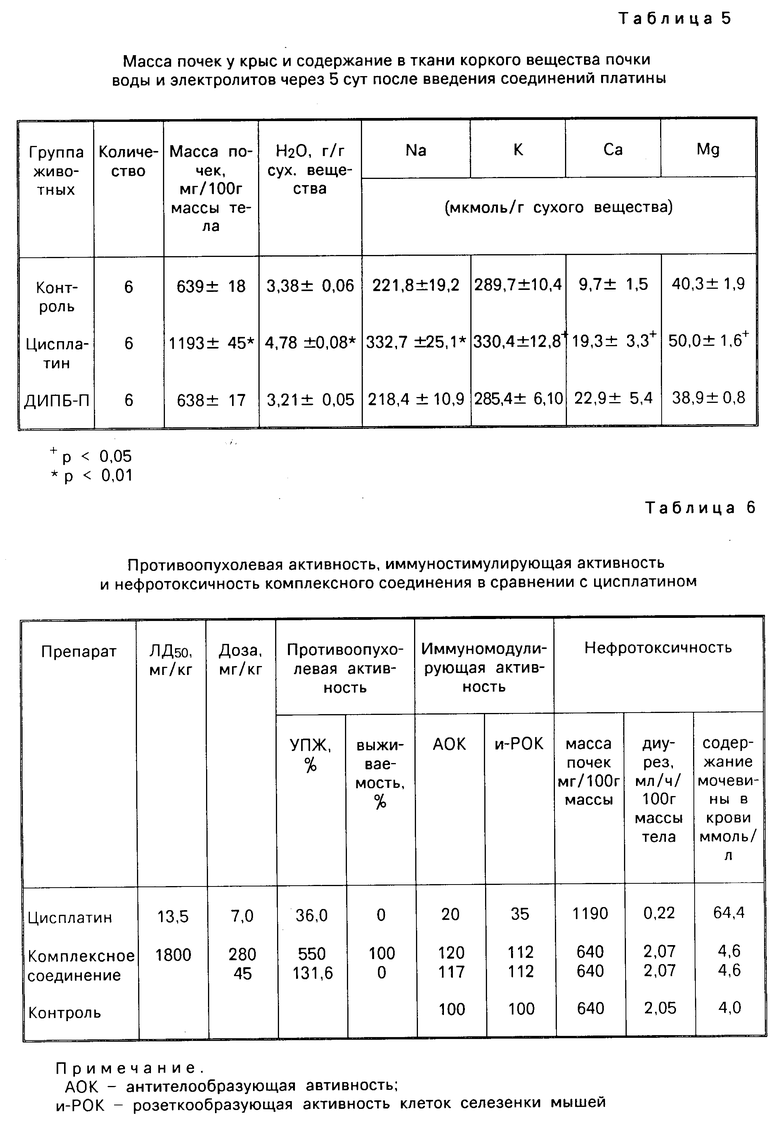
Изучено действие полимерного комплекса платины на почки. Опыты проводились на белых крысах-самках линии Вистар массой 180-200 г. Исследуемые соединения, растворенные в физиологическом растворе, вводят внутрибрюшинно. Влияние комплексного соединения на функцию почек сравнивают с действием на них цисплатина. Через 5 сут после введения цисплатина в дозе 5 мг/кг (3,5 кг/кг платины) у крыс выявляется типичная картина острой почечной недостаточности: отмечается выраженное нарушение экскреторной функции почки резко падает диурез, более чем в 20 раз снижается клубочковая фильтрация, определяемая по клиренсу эндогенного креатинина, концентрация мочевины в сыворотке крови увеличивается в 15 раз, равно как и содержание креатинина (см. табл. 4). Существенные изменения наблюдаются и в ткани почки вес органа увеличивается почти в 2 раза, развивается массивный отек почечной ткани, в ней повышается содержание Na, K, Ca, Mg (см. табл.5,6).
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПЛЕКСНОЕ СОЕДИНЕНИЕ ЦИС-ДИАМИНОПЛАТИНЫ (II) С СОПОЛИМЕРОМ NA-СОЛИ МАЛЕИНОВОЙ КИСЛОТЫ И ФУРАНА, ОБЛАДАЮЩЕЕ ИММУНОСТИМУЛИРУЮЩЕЙ И ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ, С ШИРОКИМ ИНТЕРВАЛОМ ТЕРАПЕВТИЧЕСКИХ ДОЗ ПРИ НИЗКОЙ НЕФРОТОКСИЧНОСТИ | 1990 |
|
RU2033998C1 |
| ЦИС-ХЛОРДИАММИН-1,3-ДИМЕТИЛКСАНТИНПЛАТИНЫ (II) ХЛОРИД ДИГИДРАТ, ПРОЯВЛЯЮЩИЙ ПРОТИВООПУХОЛЕВУЮ АКТИВНОСТЬ | 1990 |
|
SU1790190A1 |
| Соли сополимера малеиновой кислоты с циклооктен-4-карбоновой кислотой, обладающие противовирусными свойствами | 1989 |
|
SU1692988A1 |
| СРЕДСТВА, ПОДАВЛЯЮЩИЕ РОСТ РАКОВЫХ КЛЕТОК | 1993 |
|
RU2098096C1 |
| ПОЛИКОМПЛЕКСЫ 2-ХЛОРЭТИЛФОСФОНОВОЙ КИСЛОТЫ С N-СОДЕРЖАЩИМИ ПОЛИМЕРАМИ В КАЧЕСТВЕ ДЕФОЛИАНТОВ | 1994 |
|
RU2079512C1 |
| ПОЛИ-N-МЕТИЛ-N, N-ДИАЛЛИЛАМИНДИГИДРОФОСФАТ В КАЧЕСТВЕ КОМПОНЕНТА КАТАЛИЗАТОРА ГИДРОФОРМИЛИРОВАНИЯ ОЛЕФИНОВ | 1992 |
|
RU2049794C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТРИХЛОРОАММИНПЛАТИНАТА (II) КАЛИЯ ИЛИ АММОНИЯ ИЗ ТЕТРАХЛОРОПЛАТИНАТА (II) КАЛИЯ | 2006 |
|
RU2323886C2 |
| СПОСОБ ПОЛУЧЕНИЯ ИЗОМЕРОВ ДИХЛОРОДИАММИНПЛАТИНЫ (II) ИЗ СОЛИ МАГНУСА | 2006 |
|
RU2329952C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТРИХЛОРОАММИНПЛАТИНАТА(II) КАЛИЯ ИЛИ АММОНИЯ ИЗ ЦИСДИХЛОРОДИАММИНПЛАТИНА(II) | 2005 |
|
RU2303571C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЦИС-ДИХЛОРОАММИНИЗОПРОПИЛАМИНПЛАТИНЫ (II) | 2006 |
|
RU2309158C1 |
Изобретение относится к высокомолекулярным химическим соединениям. Использование: в медицине при лечении онкологических заболеваний. Комплексное соединение цис-диамминоплатины 2 с сополимером Na-соли малеиновой кислоты и 1,4-диизопропоксибутена-2 обладает противоопухолевой активностью с широким интервалом терапевтических доз при отсутствии нефротоксичности и иммунодепрессантного действия. 6 табл.
Комплексное соединение цис-диамминоплатины (II) с сополимером Na-соли малеиновой кислоты и 1,4-диизопропоксибутена-2 общей формулы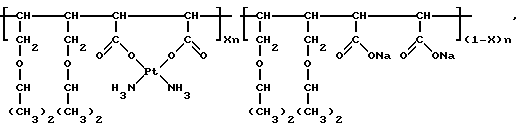
где
x 0,11 0,44;
n 8 10; 3000 4500,
3000 4500,
обладающее противоопухолевой активностью, с широким интервалом терапевтических доз при полном отсутствии нефротоксичности и иммунодепрессантного действия.
| М.А.Преснов, А.Л.Коновалова, В.П.Корольчук | |||
| Комплексные соединения платины в химиотерапии злокачественных опухолей | |||
| Вестник Академии медицинских наук СССР | |||
| Дверной замок, автоматически запирающийся на ригель, удерживаемый в крайних своих положениях помощью серии парных, симметрично расположенных цугальт | 1914 |
|
SU1979A1 |
Авторы
Даты
1995-05-10—Публикация
1990-01-29—Подача