Изобретение касается изыскания комплексных соединений платины (II), обладающих противоопухолевой активностью, а именно препарата цис-хлордиаммин-1,3-диметилксантинплатины (II) хлорид дигидрат формулы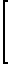
 Pt
Pt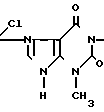 CH
CH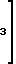 Cl•2H2O
Cl•2H2O
К известным противоопухолевым препаратам платины относятся цис-дихлордиаминплатина (II) (cisplatina, platictiam, platinol, neoplatin); цис-хлордиаминцитозинплатины (II) хлорид.
Препарат цис-дихлордиаминплатина (II) относится к классу неэлектролитных комплексов платины. Недостатком этого препарата является невысокая водная растворимость (0,1% ), что осложняет клиническое применение и технологию выделения препарата методом лиофилизации. Недостатком препарата цис-хлодиаминцитозинплатины (II) хлорид служит неустойчивость по отношению к кислороду воздуха в водном и физиологическом растворах, что приводит к образованию окрашенных примесей, содержащих трехвалентную платину, и вызывает необходимость применять препарат сразу после его растворения.
Цель изобретения синтез водорастворимого и устойчивого в водной среде, активного и малотоксичного катионного комплекса платины (II) триаминового типа цис-строения, содержащего молекулу гетероциклического азотсодержащего лиганда.
Отличие в строении и свойствах цисхлордиаммин-1,3-диметилксантинплатины (II) хлорида дигидрата от неэлектролитных комплексов платины (II) заключается в следующем: комплекс содержит однозарядный катион платины (II); наличие в комплексе молекулы липофильного лиганда 1,3-диметилксантина (теофиллина, Thp)-способствует липофильности комплекса и его мембранной проницаемости: наличие одного, а не двух, как в цис-дихлордиаминплатине (II), иона хлора делает комплекс способным к иному, чем у неэлектролитов, типу взаимодействия с ДНК, а именно к монофункциональному, а не бифункциональному, как у неэлектролитов, связыванию. Различие в механизме биохимического действия катионных и неэлектролитных комплексов перспективно в целях дифференциации и возможного расширения противоопухолевого действия препаратов платины.
К преимуществам изобретения в химическом отношении следует отнести (по сравнению с прототипом); хорошую водную растворимость (>10%); большую устойчивость по отношению к окислению и при хранении в водной среде; больший выход в процессе синтеза (70-80%) и отсутствие в конечном продукте примесей трехвалентной платины.
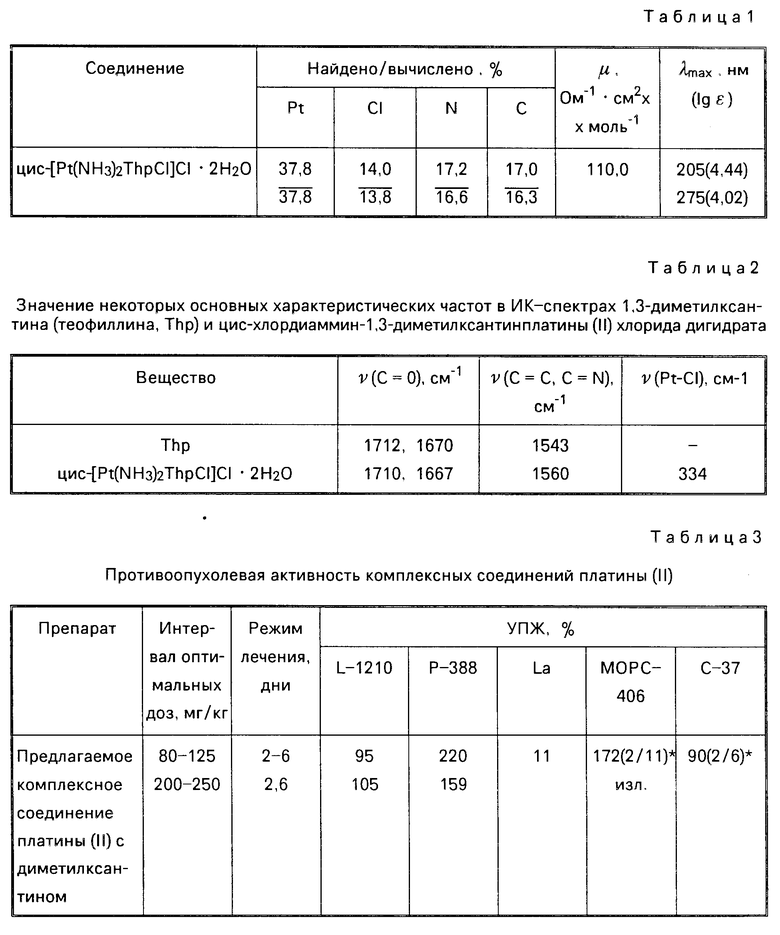
Цис-хлордиаммин-1,3-диметилксантинплатины (II) хлорид дигидрат получают взаимодействием цис-[Pt(NH3)2Cl2] и 1,3-диметилксантина. Реакцию проводят в солянокислой среде (pH 2) при нагревании на кипящей водяной бане взвеси в воде эквимолярных количеств реагирующих веществ. Целевой продукт выделяют ацетоном в виде белого порошка (пример 1). Состав и координационная формула установлены элементным анализом и измерением молярной электропроводности (см. табл. 1). Индивидуальность и чистота соединения доказана методом тонкослойной хроматографии на пластинках "Силуфол УФ-254" в двух системах растворителей: 1 этанол:ацетон:вода:уксусная кислота (конц.):аммиак (конц.)=50: 40: 10: 10: 10 (по объему); 2 пропанол:вода:уксусная кислота (конц.):аммиак (конц. )= 70:30:10:10 (по объему). Комплекс хроматографировался в обеих системах в виде одного пятна с Rf=0,62 (система 1) и 0,58 (система 2). Детекция пятен проводилась в парах иода и в УФ-излучении.
Растворимость комплекса в воде 10% При нагревании до 200оС комплекс разлагается до начала плавления. Для соединения характерно наличие в УФ-спектре полосы поглощения, характеристики которой приведены в табл. 1 λmax и lgε- длина волны в максимуме полосы поглощения и логарифм коэффициента молярного погашения при этой длине волны.
Ввиду невозможности проведения рентгеноструктурного анализа (из-за отсутствия монокристаллов) структура соединения определена методами МПР- и ИК-спектроскопии (табл. 2).
Излучение спектров протонного магнитного резонанса (ПМР) свободного теофиллина и предлагаемого соединения в дейтерированном диметилсульфоксиде (ДМСО-d6) показало, что в комплексе сигнал нелабильного протона H(8) теофиллина (δ=8,50 м. д.) сдвинут по сравнению со свободными лигандами (δ=8,00 м. д. ) в слабое поле на 0,50 м. д. В то же время в спектре ПМР комплекса наблюдается спин-спиновое взаимодействие протона Н(8) с магнитным ядром изотопа 195Pt с константой 3I195Pt-H(8)=80 Гц. Полученные данные свидетельствуют об участии к Н(8) атомов азота имидазольного цикла в координационной связи, что позволяет сделать однозначный вывод об образовании связи Pt-N.
Как видно из табл. 2, частоты полос поглощения карбонильной группы ν(C= O) практически не меняются при комплексообразовании, что свидетельствует об отсутствии связи Pt-O. В то же время увеличение частоты (C=C, C=N) на 17 см-1 указывает на образование связи платины с гетероциклическим азотом лиганда, что подтверждает выводы, сделанные при изучении спектров ПМР. Наличие полосы поглощения ν(Pt-Cl) 334 см-1 в ИК-спектре комплекса доказывает содержание в нем внутрисферного иона хлора.
П р и м е р. Навеску комплекса цис-[Pt(NH3)2Cl2] (0,6 г, 2 ммоль) и 1,3-диметилксантина (0,35 г, 2 ммоль) помещают в стакан с 50 мл дистиллированной воды, подкисленной до pH 2 соляной кислотой, закрывают часовым стеклом и нагревают в течение 2 ч на кипящей водяной бане, поддерживая уровень воды в стакане. Далее смесь охлаждают при комнатной температуре, отфильтровывают от остатка непрореагировавших исходных веществ, испаряют при комнатной температуре до объема 3 мл и выделяют конечный продукт добавлением 15-кратного избытка ацетона. Белый осадок конечного продукта отфильтровывают на воронке Гирша, отсасывая досуха, промывают ацетоном и высушивают на воздухе в течение 3 ч и далее до постоянной массы при температуре 70оС. Выход 0,85 г (75% от теоретического).
Изучение биологической активности проведено "ин витро" и "ин виво" на различных перевиваемых опухолях животных
Все исследования проведены в сравнении с близкими аналогами полученного соединения: хлор-цис-диамминцитозинпла- тины (II) хлоридом и цис-дихлордиамминплатиной (II), получавшей название "цисплатин" и широко применяемой в клинике для лечения онкологических заболеваний.
Исследование цитотоксической активности цис-хлордиаммин-1,3-диметилксантинплатины (II) хлорида проведено на клетках карциномы яичников человека (CaOV) радиометрическим методом по влиянию на включение 3H-тимидина в ДНК клеток CaOV. Использованы концентрации от 10-6 до 10-4 М.
CE50 т. н. доза, вызывающая 50% торможения включения меченого тимидина в клетки CaOV для данного соединения составляет 6·10-5 M, для препарата сравнения (цисплатина) 5·10-6М. Это свидетельствует о меньшей молярной токсичности полученного соединения.
Излучение противоопухолевой активности проведено на мышах линий C57Bl, BAlb/C, гибридах первых BDF, (C57Bl X ДВА) и беспородных животных.
Использованы следующие перевиваемые опухоли и лейкозы: лимфоидная лейкемия L-1210, гемоцитобластоз La, лейкоз P-388, плазмацитома МОРС-406, асцитная саркома 37, меланома B-16, аденокарцинома молочной железы Ca-755, фибросаркома MC-11 и лимфогенно метастазирующая эмбриокарцинома (ЛМЭК).
Вещества вводили в физиологическом растворе хлористого натрия внутрибрюшинно. Схемы терапии различны: однократная инъекция в максимально переносимой дозе (МПД), ежедневное введение в течение 5 дней и с интервалами в 96 ч. Терапевтический эффект оценивали по торможению роста солидных опухолей, увеличению продолжительности жизни леченых животных по сравнению с контролем (УПЖ) и излечению животных.
Установлено, что терапевтические дозы в зависимости от штамма и линии животных находятся в пределах 80-120 мг/кг при 5-дневном лечении, МПД при однократном введении 340 мг/кг.
Результаты исследования, полученные при оптимальных дозах и режиме применения препаратов, представлены в табл. 3.
Как видно из данных табл. 3, полученное соединение имеет широкий спектр противоопухолевого действия и проявляет высокую активность как при гемобластозах, так и на асцитных и плотных опухолях; на ряде штаммов по эффективности значительно превышает сравниваемые аналоги (на L-1210, P-388, МОРС-406, МС-11). На чувствительных к препарату опухолях (МОРС-406, C-37) помимо увеличения продолжительности жизни излечивает часть животных (33%). Цисплатин лишь увеличивает продолжительность жизни животных с плазмацитомой МОРС-406, без излечения. В то же время вещество полностью неактивно на лейкозе La, т. е. имеет определенные отличия по спектру противоопухолевого действия от сравниваемых препаратов.
Полученное соединение характеризуется большой длительностью сохранения противоопухолевого эффекта: на 17-е сутки после перевивки торможение роста Ca-755 составляет 91% меланомы B-16 81 MC 11 66% и значительной широтой терапевтического действия (диапазоны доз от минимально эффективной до максимально переносимой).
Исследование токсикологических свойств изобретения проведено на мышах линии Balb/C массой 20-22 г и на крысах линии Wistar массой 120-200 г.
Вещество растворяли в 0,9% -ном растворе хлорида натрия и вводили животным внутрибрюшинно в виде 2%-ного раствора.
Определены дозы, характеризующие токсичность препарата при однократном внутрибрюшинном применении. Они составляют соответственно для мышей МПД 340 мг/кг, ЛД50, 480 мг/кг; для крыс МПД 180 мг/кг, ЛД50 250 мг/кг.
Учитывая хорошую растворимость в воде, высокую противоопухолевую активность, проявленную при экспериментальном изучении, малую токсичность, соединение можно применять в медицине для лечения злокачественных заболеваний.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИЯ ДЛЯ ПРИГОТОВЛЕНИЯ ПРОТИВООПУХОЛЕВОГО СРЕДСТВА И СПОСОБ ПРИГОТОВЛЕНИЯ ПРОТИВООПУХОЛЕВОГО СРЕДСТВА НА ЕЕ ОСНОВЕ | 2016 |
|
RU2667128C2 |
| Способ получения комплексного соединения платины (II) с Н-ДНК, обладающего противоопухолевой активностью | 1988 |
|
SU1813089A3 |
| ЦИС-ХЛОРО-N, -(2' -ТЕТРАГИДРОФУРИЛ) -5-ФТОРУРАЦИЛАТОДИАММИНПЛАТИНА II, ПРОЯВЛЯЮЩАЯ ПРОТИВООПУХОЛЕВУЮ АКТИВНОСТЬ | 1992 |
|
RU2028301C1 |
| Способ получения комплексного соединения платины (II) с высокомолекулярной н-ДНК из селезенки крупного рогатого скота марки А, обладающего противоопухолевой активностью | 1988 |
|
SU1685944A1 |
| Способ получения комплексного соединения платины (II) с Н-ДНК, обладающего противоопухолевой активностью | 1988 |
|
SU1754722A1 |
| Цис-дихлороаквогуанозинплатина ( @ ),моноэтанол,проявляющая антиканцерогенную активность | 1980 |
|
SU886472A1 |
| ПЕНТАХЛОРОПЛАТИНАТ (IV)-4- МЕТИЛ-3-[(2- МЕТИЛ-4- ОКСИ-5-ПИРИМИДИНИЛ) МЕТИЛ-]-5-(2 -ОКСИЭТИЛ)ТИАЗОЛИЯ, ПРОЯВЛЯЮЩИЙ ПРОТИВООПУХОЛЕВУЮ АКТИВНОСТЬ | 1991 |
|
RU2050361C1 |
| НОВЫЕ КОМПЛЕКСЫ ПЛАТИНЫ IV С ПО СУЩЕСТВУ ПОВЫШЕННОЙ ПРОТИВООПУХОЛЕВОЙ ЭФФЕКТИВНОСТЬЮ | 2019 |
|
RU2802514C1 |
| БИСИМИДАЗОЛ-(1,10)-ФЕНАНТРОЛИНПЛАТИНА (III) ДИХЛОРИД, ПРОЯВЛЯЮЩИЙ ЦИТОСТАТИЧЕСКУЮ ПРОТИВООПУХОЛЕВУЮ АКТИВНОСТЬ | 1995 |
|
RU2089555C1 |
| ТРЕХЪЯДЕРНЫЕ КАТИОННЫЕ КОМПЛЕКСЫ ПЛАТИНЫ, ПРОЯВЛЯЮЩИЕ ПРОТИВООПУХОЛЕВУЮ АКТИВНОСТЬ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ЭТИ КОМПЛЕКСЫ | 1995 |
|
RU2130941C1 |
Использование: в качестве препарата, обладающего противоопухолевой активностью. Сущность изобретения: продукт-цис хлордиаммин-1,3-диметилксантинплатина (II), БФ C7H1 8Cl2N6O4Pt, выход 75%, т. пл. 200oС с разложением. Реагент 1: цис-дихлордиамминплатина. Реагент 2: 1,3-диметилксантин. Условия реакции: в воде при pH 2, при нагревании на кипящей бане. 3 табл.
Цис-хлордиаммин-1,3- диметилксантинплатины ii хлорид дигидрат формулы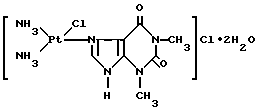
проявляющий противоопухолевую активность.
| "Cis-platin" | |||
| Current status New Developments | |||
| Ed | |||
| A | |||
| K | |||
| Prnstajko, S | |||
| T | |||
| Crooke, X | |||
| S | |||
| K | |||
| Carbon, p | |||
| Приспособление для обрезывания караваев теста | 1921 |
|
SU317A1 |
| Press, 1980 | |||
| Авторское свидетельство СССР N 1085209, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1996-04-27—Публикация
1990-08-08—Подача