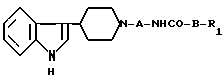
Изобретение относится к новым производным индолилпиперидина общей формулы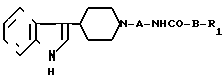 где R1 фенил, замещенный заместителями, выбранными из группы, содержащей низший алкил, гидроксил, защищенный гидроксил, галоген или низший алкокси,
где R1 фенил, замещенный заместителями, выбранными из группы, содержащей низший алкил, гидроксил, защищенный гидроксил, галоген или низший алкокси,
А низший алкилен,
В низший алкенилен, или их фармацевтически приемлемым солям, которые проявляют противоаллергическое действие.
Целью изобретения является создание новых соединений, обладающих более эффективным фармакологическим действием при низкой токсичности.
П р и м е р 1. К перемешанной смеси 3-[3-метокси-4-{(2-метоксиэтокси)метокси} фенил] -(Е)-акриловой кислоты (1,75 г) и тритиламин (1,81 мл) в сухом N,N-диметилформамиде (10 мл) медленно добавляется дифенилфосфинхлорид (1,47 г) при (-10)-(-15)оС при инертной атмосфере. После перемешивания в течение 30 мин, к реакционной смеси медленно добавляется раствор 1-(2-аминоэтил)-4-(3-индолил) пиперидин (1,5 г) в сухом N,N-диметилформамиде (10 мл) при -10оС. После перемешивания в течение 1 ч при комнатной температуре реакционная смесь вливается в ледяную воду (200 мл) и экстрагируется хлороформом (100 мл). Экстракт отмывается насыщенным раствором хлорида натрия и высушивается в присутствии сульфата магния. Раствор отгоняется и остаток подвергается колоночной хроматографии на силикагеле (47 г) и элюируется смесью хлороформа и метанола (10:1). Фракции, содержащие необходимое соединение, объединяются и концентрируются при пониженном давлении до получения сиропа 1-[2-[3-[3-метокси-4-{ (2-метоксиэтокси)метокси} фенил]-(Е)- пропеноиламино] -этил]-4-3-индолил)пиперидина (2,8 г).
ЯМР (СDCl3, δ): 1,6-3,3 (11H м), 3,37 (3Н, с), 3,55 (4Н, м), 3,85 (2Н, м), 3,89 (3Н, с), 5,32 (2Н, с), 6,35 (1Н, д, J 15,0 Гц),6,52 (IH,шир.c), 6,9-7,8 (8H,м), 7,57 (1H, д,J=15,0 Гц), 8,25 (1Н, шир.с).
П р и м е р 2. Нижеприведенные соединения были получены способом, аналогичным описанному в примере 1.
(1) 1-[2-[5-[3-метокси-4-{ (2-метоксиэтокси)метокси} -фенил]-(2Е, 4Е)-2,4-пентадиеноиламино] этил] -4-(3-индолил)пиперидинИК (Nujol): 3300, 1660, 1260, 1092, 990, 744 см-1
ЯМР (CDCl3, δ): 1,6-3,3 (11Н, м), 3,35 (3Н, с), 3,54 (4Н, м), 3,84 (2Н, м), 3,86 (3Н, с), 5,30 (2Н, с), 6,07 (1Н, д, 15,0 Гц), 6,70-7,80 (12Н, м), 9,30 (1Н, с).
Масс: 533 (М+), 213.
(2) 1-[3-[5-3-метокси-4-{ (2-метоксиэтокси)метокси} -фенил] -(2Е, 4Е)-2,4-пентадиеноиламино]пролин]-4-(3-индолил)пиперидин
ЯМР (CDCl3, δ): 1,5-3,6 (15Н, м), 3,36 (3Н, с), 3,6 (2Н, м), 3,87 (3Н, с), 3,87(3H, c) 3,90 (2Н, м), 5,35 (2Н, с), 6,02 (1Н, д, J 14,4 Гц), 6,6-7,9 (12Н, м), 8,55 (1Н, с).
Масс: 547 (М+)
(3) 1-[4-[5-[3-метокси-4-{ (2-метоксиэтокси)метокси} -фенил]-(2Е, 4Е)-2,4-пентадиеноиламино]бутил]-4-(3-индолил) пиперидин
ИК (Nujol): 3400, 3200 (шир.), 1650, 1377, 1260 см-1.
ЯМР (СDCl3, δ): 1,3-3,4 (17Н, м), 3,33 (3Н, с), 3,55 (2Н, м), 3,80 (5Н, шир. с), 5,27 (2Н, с), 6,11 (1Н, д, J 15,0 Гц), 6,5-8,0 (12Н, м) 9,23 (1Н, с).
Масс: 561 (М+)
(4) 1-[2-{5-(3,4-диметоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино}этил]-4-(3-индолил) пиперидин
т.пл. 196-198оС (рекристаллизирован из этанола)
ИК (Nujol): 3280, 1640, 1610, 1590, 1550, 1510 см-1,
ЯМР (DMSO-d6, δ): 1,4-3,5 (13Н, м), 3,78 (3Н, с), 3,81 (3Н, с), 6,15 (1Н, д, J 15,0 Гц), 6,8-7,6 (11Н, м), 7,99 (1Н, шир.т), 10,75 (1Н, шир.с).
Масс: 459 (М+), 213
Вычислено, C 73,18; H 7,24; N 9,14.
C28H33N3O3
Найдено, C 73,84; H 7,42; N 8,72.
(5) 1-[2-{5-(3,4,5-триметоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино}этил] -4-(3-индолил)пиперидин
т.пл. 86-100оС
ИК (Nujol): 3250, 1650, 1610, 1680 см-1.
ЯМР (DMSO-d6, δ): 1,4-3,6 (13Н, м), 3,70 (3Н, с), 3,83 (6Н, с), 6,19 (1Н, д, J 15,0 Гц), 6,7-7,7 (10Н, м), 8,02 (1Н, шир.т), 10,74 (1Н, шир.с).
Масс: 489 (М+) 289, 213.
Вычислено, C 69,23; H 7,31; N 8,35.
C29H35N3O4. 3/4H2O.
Найдено, C 69,38; H 7,08; N 8,40.
(6) 1-[2-{ 3-(4-гидрокси-3-метоксифенил)-(Е)-пропеноиламино} этил] -4- (3-индолил)пиперидин
т.пл. 115-135оС.
ИК (Nujol): 3300 (шир.), 1655, 1588, 1512 см-1.
(7) 1-[2-{5-(4-гидрокси-3-метоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино} этил]-4-(3-индолил) пиперидин
т.пл. 115-131оС.
ИК (Nujol): 3330 (шир.), 1660, 1377 см-1.
(8) 1-[3-{5-(4-гидрокси-3-метоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино} пропил]-4-(3-индолил)пиперидин
т.пл. 150-170оС.
ИК (Nujol): 3400, 3200 (шир.), 1638, 1580 см-1.
(9) 1-[4-{5-(4-гилрокси-3-метоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино} бутил]-4-(3-индолил) пиперидин, т.пл. 150-170оС.
ИК (Nujol): 3200 (шир.), 1640, 1580, 1270, 720 см-1.
(10) 1-[2-[5-[3,4-{Бис(2-метоксиэтокси)метокси}фенил]-(2Е, 4Е)-2,4-пентадиеноиламино] этил]-4-(3-индолил)-пиперидин. Это соединение использовалось в качестве исходного соединения примера 7-(4) без очистки.
(11) 1-[2-[5-[3,5-диметокси-4-{ (2-метоксиэтокси)метокси} -фенил] -(2Е, 4Е)-2,4-пентадиеноиламино]этил]-4-(3-индолил) пиперидин.
ИК (Nujol): 3300, 1650, 1580, 1125, 990, 960, 845, 745 см-1.
(12) 1-[3-[5-[3,5-диметокси-4-{ (2-метоксиэтокси)метокси} фенил] -(2Е, 4Е)-2,4-пентадиеноиламино]пропил-4]-(3-индолил) пиперидин.
ИК (чистый): 3300, 3000, 2990, 1650, 1615, 1580, 1130, 990, 960, 850 см-1.
(13) 1-[4-[5-[3,5-диметокси-4-{ (2-метоксиэтокси)метокси} -фенил] -(2Е, 4Е)-2,4-пентадиеноиламино]бутил]-4-(3-индолил) пиперидин.
ИК (чистый): 2900, 1650, 1580, 1550, 1120, 960, 860, 740 см-1.
(14) 1-[2-[5-[4-{(2-метоксиэтокси)метокси}-3,5-диметилфенил]-(2Е, 4Е)-2,4-пентадиеноиламино]этил]-4-(3-индолил) пиперидин.
Т пл. 163-164оС (рекристаллизован из этилацетата)
ИК (Nujol): 3450, 3300, 1645, 1615, 990, 970 см-1.
ЯМР (DMSO-d6, δ): 1,5-2,3 (6Н, м), 2,34 (6Н, с), 2,5-3,1 (7Н, м), 3,25 (3Н, с), 3,5, 3,8 (каждый 2Н, м), 5,05 (2Н, с), 6,15 (1Н, д, J15 Гц), 6,8-7,7 (10Н, м), 8,03 (1Н, м), 10,7 (1Н, м).
Масс (m/e): 531 (М+), 213 (основ.).
(15) 1-[2-[5-[3,5-Диизопропил-4-{ (2-метоксиэтокси)-метокси}фенил]-(2Е, 4Е)-2,4-пентадиеноиламино]-этил]-4-(3-индолил) пиперидин
ИК (чистый): 1660, 1650, 1615, 970 см-1.
(16) 1-[2-[5-[4-{(2-Метоксиэтокси)метокси}-3-метилфенил]-(2Е, 4Е)-2,4-пентадиеноиламино]этил]-4-(3-индолил) пиперидин.
Т.пл. 140-144оС.
ИК (Nujol): 3470, 3280, 1640, 1610, 1595, 1000, 980 см-1.
ЯМР (СDCl3, δ): 1,6-3,2 (13Н, м), 2,25 (3Н, с), 3,38 (3Н, с), 3,6, 3,8( каждый 2Н, м), 5,32 (2Н, с), 5,96 (1Н, д, J 15 Гц), 6,2-7,8 (11Н, м), 8,25 (1Н, м).
Масс (m/e): 517 (М+), 213 (основ.).
(17) 1-[2-[5-[3-Хлоро-4-{ (2-метоксиэтокси)метокси} -фенил] -(2Е, 4Е)-2,4-пентадиеноиламино]этил]-4-(3-индолил) пиперидин.
ИК (Nujol): 3450, 3300, 1645, 1610, 1050, 990 см-1.
ЯМР (DMSO-d6, δ ): 1,5-2,5 (6Н, м), 2,8-3,2 (7Н, м), 3,65 (3Н, с), 3,6, 3,8 (каждый 2Н, м), 5,39 (2Н, с), 6,10 (1Н, д, J 15 Гц), 6,8-7,9 (11Н, м), 8,05 (1Н, м), 10,75 (1Н, м).
Масс (m/e): 537, 213 (основ.).
(18) 1-[2-{5-(3,4-Дигидроксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино}этил] -4-(3-индолил) пиперидин.
ИК (Nujol): 3400, 3350, 1650, 1585, 1520 см-1.
Масс (m/e): 431 (М+), 213 (основ.).
(19) 1-[2-{ 5-(4-гидрокси-3,5-диметоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино}этил]-4-(3-индолил) пиперидин
ИК (Nujol): 3420, 1665, 1650, 1620, 1590, 1530, 1515, 1120 см-1.
Масс (m/e): 475 (М+), 213.
(20) 1-[4-{ 5-(4-гидрокси-3,5-диметоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино}бутил]-4-(3-индолил) пиперидин
ИК (Nujol): 3250, 1640,1600, 1540, 1510, 1130, 1110, 810 см-1.
(21) 1-[3-{ 5-(4-гидрокси-3,5-диметоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино}пропил]-4-(3-индолил) пиперидин
ИК (Nujol): 3420, 1658, 1610, 1575, 1550, 1510, 1120 см-1.
Масс (m/e): 489 (М+), 239, 233, 213 (основ.), 197.
(22) 1-[2-{5-(4-Ацетокси-3-метоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино} этил]-4-(3-индолил) пиперидин.
ИК (Nujol): 3440, 3250, 1760, 1655, 1620, 1560, 1505 см-1.
Масс (m/e): 487 (М+), 213 (основ.).
(23) 1-[2-{5-(3-Метокси-4-пропионилоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино}этил]-4-(3-индолил) пиперидин.
ИК (Nujol): 3430, 3250, 3060, 1750, 1655, 1620, 1560 см-1.
Масс (m/e): 501 (М+), 213 (основ.).
(24) 1-[2-{ 5-(4-этоксикарбонилокси-3,5-диметоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино}этил]-4-(3-индолил) пиперидин.
ИК (Nujol): 3360, 3300, 1750, 1640, 1590, 1130, 1000, 735 см-1.
Масс (m/e): 547 (М+), 228, 213 (основ.).
(25) 1-[4-{ 5-(4-Этоксикарбонилокси-3,5-диметоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино}бутил]-4-(3-индолил) пиперидин.
ИК (Nujol): 3380, 3250, 1750, 1655, 1620, 1595, 1555, 1130, 1050, 1000, 735 см-1.
Масс (m/e): 575 (М+), 531, 503, 285, 233, 213 (основ.).
(26) 1-[2-{ 5-(4-гидрокси-3,5-диметилфенил)-(2Е, 4Е)-2,4-пентадиеноиламино}этил]-4-(3-индолил) пиперидин.
ИК (Nujol): 3300, 1640, 1590, 1545, 990, 860 см-1.
Масс (m/e): 443 (М+), 213 (основ.).
(27) 1-[2-{5-(4-Гидрокси-3,5-диизопропилфенил)-(2Е, 4Е)-2,4-пентадиеноиламино}этил]-4-(3-индолил) пиперидин.
ИК (Nujol): 3400, 3300, 1650, 1630, 1585, 995, 870 см-1.
Масс (m/e): 499 (М+), 226, 213 (основ.).
(28) 1-[2-{ 5-(4-гидрокси-3-метилфенил)-(2Е, 4Е)-2,4-пентадиеноиламино} этил]-4-(3-индолил) пиперидин.
ИК (Nujol): 3200, 1640, 1575, 1550, 1000 см-1.
Масс (m/e): 429 (М+), 213 (основ.).
(29) 1-[2-{ 5-(3-хлоро-4-гидроксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино} этил]-4-(3-индолил) пиперидин
ИК (Nujol): 3420, 1650, 1590, 1000 см-1.
Масс (m/e): 449 (М+), 213 (основ.).
(30) 1-[2-{5-(4-ацетокси-3,5-диметоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино}этил]-4-(3-индолил) пиперидин
ИК (Nujol): 3380, 3320, 1755, 1650, 1620, 1595, 990, 745 см-1.
Масс (m/e): 517 (М+), 213 (основ.).
(31) 1-[2-[5-(3,5-дихлоро-4-{(2-метоксиэтокси)метокси}фенил]-(2Е, 4Е)-2,4-пентадиеноиламино]этил]-4-(3-индолил) пиперидин.
ИК (чистый): 1655, 1610, 995 см-1.
(32) 1-[2-[5-[3-метокси-2-{ (2-метоксиэтокси)метокси}-фенил]-(2Е, 4Е)-2,4-пентадиеноиламино]этил]-4-(3-индолил) пиперидин.
ИК (чистый): 1650, 1610, 1000, 960 см-1.
(33) 1-[2-[5-[4-Метокси-3-{ (2-метоксиэтокси)метокси}-фенил]-(2Е, 4Е)-2,4-пентадиеноиламино]этил]-4-(3-индолил) пиперидин.
Т.пл. 135-136оС (рекристаллизован из этилацетата).
ИК (Nujol): 3260, 1640, 1615, 1595, 1550, 1510 см-1.
ЯМР (DMSO-d6, δ): 3,75 (3Н, с), 5,23 (2Н, с), 6,11 (1Н, д, J 15 Гц), 6,7-7,6 (11Н, м), 7,96 (1Н, т), 10,7 (1Н, шир.).
Масс (m/e): 533, 445, 333, 213 (основ.).
(34) 1-[2-[5-[3,5-ди-трет-Бутил-2{(2-метоксиэтокси)-метокси}фенил]-(2Е, 4Е)-2,4-пентадиеноиламино] -этил] -4-(3-индолил) пиперидин, т.пл. 98-103оС (рекристаллизован из этанола).
ИК (Nujol): 3300, 1650, 1600, 970 см-1.
ЯМР (СDCl3, δ): 1,42 (18Н, с), 1,6-2,3 (6Н, м), 2,53 (2Н, т, J 7 Гц), 2,8 (3Н, м),(3H,c) 3,5 (2Н, м), 3,663,96 (каждый 2Н, м), 4,93 (2Н, с), 5,95 (1Н, д, J 15,5 Гц), 6,17 (1Н, т подобный), 6,6-7,7 (10H, м), 8,2 (1Н, с).
(35) 1-[2-{5-(3,5-ди-трет-Бутил-4-гидроксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино}этил]-4-(3-индолил) пиперидин.
ИК (Nujol): 3550, 3300, 3230, 1650, 1610, 1590, 1000 см-1.
Масс (m/e): 527 (М+), 226, 213.
(36) 1-[2-{ 5-(3,5-Дихлоро-4-гидроксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино}этил]-4-(3-индолил)-пиперидин.
Масс (m/e): 485 (М+2), 483 (М+), 213 (основ.).
(37) 1-[2-{5-(2-гидрокси-3-метоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино} этил]-4-(3-индолил) пиперидин
ИК (Nujol): 3400, 3240, 1650, 1605, 1600, 1530, 1090, 1005 см-1.
Масс (m/е): 445 (М+), 226, 213 (основ.).
(38) 1-[2-{5-(3-Гидрокси-4-метоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино} этил]-4-(3-индолил) пиперидин.
ИК (Nujol): 3350, 1650, 1615, 1590 см-1.
Масс (m/e): 445 (М+), 213 (основ.).
(39) 1-[2-[5-{3,4-бис(3-Этоксикарбонилокси)фенил}-(2Е, 4Е)-2,4-пентадиеноиламино]этил]-4-(3-индолил пиперидин
ИК (Nujol): 3500, 3350, 1775, 1650, 1620, 1000 см-1.
Масс (m/e): 529 (М+-46), 457, 285 (основ.) 213.
П р и м е р 3. К раствору 1-[2-[5-[3,5-ди-трет-Бутил-4-{(2-метоксиэтокси)метокси}фенил]-(2Е, 4Е)-2,4-пентадиеноиламино]этил]-4-(3-индолил) пиперидина (0,5 г) в метаноле (5 мл) добавляется по капле метансульфоновая кислота (0,26 мл) при 18-25оС. Через 2 ч реакционная смесь при помощи 2н-гидроокиси натрия доводится до рН 7,5, а затем выливается в насыщенный раствор бикарбоната натрия (50 мл). Полученный в результате преципитат собирается и отмывается водой. Затем преципитат подвергается колоночной хроматографии на силикагеле и элюируется смесью хлороформа и метанола (20:1 об.). Фракции, содержащие нужное соединение, объединяются и концентрируются при пониженном давлении. Остаток рекристаллизуется из 1,4-диоксана до получения белых кристаллов соединения 1-[2{5-(3,5-ди-трет-бутил-4-гидроксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино}-этил]-4-(3-индолил) пиперидина (0,28 г).
Т.пл. 108-115оС
ИК (Nujol): 3550, 3300, 3230, 1650, 1610, 1590, 1000 см-1.
ЯМР (CDCl3, δ): 1,43 (18Н, с), 1,6-2,3 (6Н, м), 2,53 (2Н, т, J 7 Гц), 2,7-3,2 (3Н, м), 3,45 (2Н, м), 5,33 (1Н, с), 5,93 (1Н, д, J 15,5 Гц), 6,15 (1Н, т, подоб.), 6,65-7,7 (10Н, м), 8,16 (1Н, с).
Масс (m/e): 527 (М+), 226, 213.
П р и м е р 4. К перемешанному раствору 1-[2-[5-[3,5-диметокси-4-{(2-метоксиэтокси)метокси}фенил]-(2Е, 4Е)-2,4-пентадиеноиламино]-этил]-4-(3-индолил) пиперидина (10,0 г) в метаноле (100 мл) медленно добавляется метансульфоновая кислота (2,3 мл) при комнатной температуре. После перемешивания в течение 2 ч, реакционная смесь при помощи 2н-водного раствора гидроокиси натрия доводится до рН 7,2 и выливается в раствор 4,5 бикарбоната натрия в 500 мл воды. После перемешивания в течение 30 мин, полученный в результате преципитат собирается путем фильтрации и отмывается 100 мл воды. Остаток подвергается колоночной хроматографии на силикагеле и элюируется смесью хлороформа и метанола. Фракции, содержащие нужное соединение, объединяются и концентрируются при пониженном давлении. Остаток рекристаллизуется из этанола для получения 1-[2-{5-(4-гидрокси-3,5-диметоксифенил)-(2Е, 4Е)-пентадиеноиламино}этил]-4-(3-индолил)пиперидина (6,69 г).
Т.пл. 199-202оС.
ИК (Nujol): 3420, 1665, 1650, 1620, 1590, 1530, 1515, 1120 см-1.
ЯМР (DMSO-d6, δ ): 1,5-2,4 (7Н, м), 2,7-3,5 (6Н, м), 3,81 (6Н, с), 6,15 (1Н, д, J 14 Гц), 6,8-7,8 (10Н, м) 8,0 (1Н, т), 8,68 (1Н, м), 10,75 (1Н, с).
Масс (m/e): 475 (М+), 213.
Вычислено, C 70,71; H 6,99; N 8,83.
C28H33N3O4.
Найдено, C 70,34; H 6,56; N 8,65.
П р и м е р 5. Смесь 1-[3-[5-[3,5-диметокси-4-{(2-метоксиэтокси)метокси} фенил] -(2Е, 4Е)-2,4-пентадиеноиламино] -пропил] -4-(3-индолил) пиперидина (1,67 г) и моногидрата р-толуолсульфокислоты (0,64 г) в метаноле (33 мл) подогревается в колбе с обратным холодильником в течение 30 мин в инертной атмосфере. После охлаждения до комнатной температуры, смесь добавляется по капле в водный раствор карбоната натрия. Полученное в результате порошковое вещество подвергается колоночной хроматографии на силикагеле и элюируется смесью хлороформа и метанола (10:1 об.). Фракции, содержащие нужное соединение, объединяются и концентрируются при пониженном давлении. Полученный остаток рекристаллизуется из смеси этанола и воды (7: 3об.) до получения 1-[3-{ 5-(4-гидрокси-3,5-диметоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино}пропил]-4-(3-индолил) пиперидин (0,51 г).
Т.пл. 176-179оС (рекристаллизован из смеси этанола и воды (8:2 об.).
ИК (Nujol): 3420, 1658, 1610, 1575, 1550, 1510, 1120 см-1.
ЯМР (DMSO-d6, δ): 1,4-2,5 (9Н, м), 2,6-3,5 (6Н, м), 3,79 (6Н, с), 6,10 (1Н, д, J 15 Гц), 6,7-7,7 (10Н, м), 8,05 (1Н, т подоб.), 8,7 (1Н, м), 10,72 (1Н, с).
Масс (m/e): 489 (М+), 239, 233, 213 (основ.) 197.
Вычислено, C 71,14; H 7,20; N 8,58.
C29H35N3O4
Найдено, C 70,79; H 7,12; N 8,57.
П р и м е р 6. Смесь 1-[2-[3-[3-метокси-4{(2-метоксиэтокси)метокси}-фенил] -(Е)-пропеноиламино] этил]-4-(3-индолил)-пиперидина (2 г) и моногидрата р-толуолсульфокислоты (1,05 г) в метаноле (40 мл) подогревается в колбе с обратным холодильником в течение 30 мин в инертной атмосфере. Затем раствор отгоняется при пониженном давлении, остаток отмывается водой (100 мл), при помощи раствора карбоната натрия значение рН доводится до 10 и полученный раствор экстрагируется этилацетатом. Экстракт отмывается насыщенным раствором хлорида натрия и высушивается в присутствии сульфата магния. После удаления раствора, остаток подвергается колоночной хроматографии на силикагеле (31 г) и элюируется смесью хлороформа и метанола (8:1 об.). Фракции, содержащие нужное соединение, объединяются и концентрируются при пониженном давлении для получения 1-[2-{3-(4-гидрокси-3-метоксифенил)-(Е)-пропеноиламино}этил]-4- (3-индолил) пиперидина (0,89 г).
Т.пл. 115-135оС
ИК (Nujol): 3300 (шир.), 1655, 1588, 1512 см-1.
ЯМР (DMSO-d6, δ): 1,5-3,6 (14Н, м), 3,83 (3Н, с), 6,50 (1Н, д, J 15,0 Гц), 6,7-7,7 (9Н, м), 7,83 (1Н, шир.т), 10,70 (1Н, с).
Масс: 419 (М+), 213.
Вычислено, C 70,00; H 7,06; N 9,80.
C15H29N3O3.1/2H2O
Найдено, C 70,18; H 6,92; N 9,85.
П р и м е р 7. Нижеприведенные соединения были получены способом, аналогичным описанному в примерах 3-6.
(1) 1-[2-{5-(4-Гидрокси-3-метоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино} этил]-4-(3-индолил) пиперидин.
Т.пл. 115-131оС.
ИК (Nujol): 3330 (шир.), 1660, 1377 см-1.
ЯМР (DMSO-d6, δ): 1,5-3,6 (13Н, м), 3,82 (3Н, с), 6,07 (1Н, д, J 15,0 Гц), 6,6-7,6 (8Н, м), 7,90 (1Н, шир.т), 9,20 (1Н, с), 10,68 (1Н, с).
Масс: 445 (М+), 213.
Вычислено, C 71,34; H 7,10; N 9,24.
C27H31N3O3.1/2H2O
Найдено, C 71,15; H 6,87; N 9,19.
(2) 1-[3-{5-(4-Гидрокси-3-метоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино} пропил]-4-(3-индолил)пиперидин.
Т.пл. 150-170оС.
ИК (Nujol): 3400, 3200 (шир.), 1638, 1580 см-1.
ЯМР (DMSO-d6, δ): 1,5-3,8 (15Н, м), 3,86 (3Н, с), 4,20 (1Н, шир.), 6,15 (1Н, д, J 14,0 Гц), 6,6-7,8 (11Н, м), 8,26 (1Н, шир.с), 10,82 (1Н, с).
Вычислено, C 65,85; H 6,97; N 7,55.
C28H33N3O3.1/2CHCl3.1/2C2H5OC2H5
Найдено, C 65,67; H 7,18; N 7,87.
(3) 1-[4-{5-(4-Гидрокси-3-метоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино} бутил]-4-(3-индолил) пиперидин
Т.пл. 150-170оС.
ИК(Nujol):3200 (шир.), 1640, 1580, 1270, 735 см-1.
ЯМР (DMSO-d6, δ): 1,2-3,7 (17Н, м), 3,80 (3Н, с), 6,07 (1Н, д. J 15,0 Гц), 6,6-7,8 (11Н, м), 8,10 (1Н, с), 9,25 (1Н, с), 10,82 (1Н, с).
Масс: 473 (М+), 213
Вычислено, C 66,33; H 7,16; N 7,37.
C29H35N3O3.1/2CHCl3.1/2C2H5OC2H5.
Найдено, C 66,02; H 7,47; N 7,33.
(4) 1-[2-{ 5-(3,4-Дигидроксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино}этил] -4-(3-индолил) пиперидин.
Т. пл. 138-158оС (разложение) (рекристаллизован из смеси этанола и воды (8:2 об.)).
ИК (Nujol): 3400, 3350, 1650, 1585, 1520 см-1.
ЯМР (DMSO-d6, δ): 1,5-3,6 (13Н, м), 7,93 (1Н, м), 10,73 (1Н, шир.).
Масс (m/e): 431 (М+), 213 (основ.).
Вычислено, C 70,07; H 7,49; N 8,63.
C26H29N3O3.6/5 этанол.
Найдено, C 69,77; H 7,39; N 8,67.
(5) 1-[4-{5-(4-Гидрокси-3,5-диметоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино}бутил]-4-(3-индолил) пиперидин
ИК (Nujol): 3250, 1640, 1600, 1540, 1510, 1130, 1110, 810 см-1.
(6) 1-[4-{ 5-(4-гидрокси-3,5-диметилфенил)-(2Е, 4Е)-2,4-пентадионоиламино}этил]-4-(3-индолил) пиперидин
Т.пл. 125-135оС (рекристаллизован из смеси этанол-вода (8:2 об.).
ИК (Nujol): 3300, 1640, 1590, 1545, 990, 840 см-1.
ЯМР (DMSO-d6, δ): 1,4-2,4 (6Н, м), 2,19 (6Н, с), 2,6-3,2 (7Н, м), 6,11 (1Н, д, J 15 Гц), 6,7-7,6 (10Н, м), 7,95 (1Н, м), 10,82 (1Н, м).
Масс (m/e): 443 (М+), 213 (основ.).
Вычислено, C 71,92; H 7,69; N 8,99.
C28H33N3O2.4/3H2O.
Найдено, C 72,00; H 7,69; N 8,88.
(7) 1-[2-{5-(4-гидрокси-3,5-диизопропилфенил)-(2Е, 4Е)-2,4-пентадиеноиламино}этил]-4-(3-индолил)пиперидин
Т.пл. 110-120оС (рекристаллизован из смеси этанол-вода (8:2 об.).
ИК (Nujol): 3400, 3300, 1650, 1630, 1585, 995, 870 см-1.
ЯМР (DMSO-d6, δ): 1,28 (12Н, д, J 9 Гц), 1,5-2,4 (6Н, м), 2,7-3,6 (9Н, м), 6,13 (1Н, д, J= 15 Гц), 6,8-7,6 (10Н, м), 7,95 (1Н, м), 8,4 (1Н, м), 10,73 (1Н, м).
Масс (m/e): 499 (М+), 226, 213 (основ.).
Вычислено, C 74,24; H 8,37; N 8,11.
C32H41N3O2.H2O.
Найдено, С 73,84; H 8,42; N 7,97;
(8) 1-[2-{ 5-(4-Гидрокси-3-метилфенил)-(2Е, 4Е)-2,4-пентадиеноиламино} этил]-4-(3-индолил) пиперидин
Т.пл. 138-141оС (рекристаллизован из смеси этанол-вода (8:2 об.).
ИК (Nujol): 3200, 1640, 1575, 1550, 1000 см-1.
ЯМР (DMSO-d6, δ): 1,5-3,6 (13Н, м), 2,20 (3Н, с), 6,10 (1Н, д, J 15 Гц), 6,7-7,7 (11 Гц, м), 7,93 (1Н, м), 9,65 (1Н, м), 10,73 (1Н, м).
Масс (m/e): 429 (М+), 213 (основ.).
Вычислено, C 71,73; H 7,47; N 9,29.
C27H31N3O2.5/4H2O.
Найдено, C 71,78; H 7,73; N 8,28.
(9) 1-[2-{5-(3-Хлоро-4-гидроксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино}-этил]-4-(3-индолил) пиперидин.
Т.пл. 139-155оС (рекристаллизован из смеси этанол-вода).
ИК (Nujol): 3420, 1650, 1590, 1000 см-1.
ЯМР (DMSO-d6, δ): 1,5-3,5 (13H, м), 6,12 (1Н, д, J 15Гц), 6,7-7,7 (11Н, м), 7,88 (1Н, м), 10,7 (1Н, м).
Масс (m/e): 449 (М+), 213 (основ.)
Вычислено, С 65,47; H 6,55; N 8,81.
C26H28Cl3N3O2.1,5H2O.
Найдено, C 65,88; H 6,44; N 8,78.
(10) 1-[2-{ 5-(3,5-Дихлоро-4-гидроксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино}этил]-4-(3-индолил) пиперидин.
Т.пл. 165-175оС (рекристаллизован из N,N-диметилформамида)
ЯМР (DMSO-d6, δ): 1,5-3,6 (13Н, м), 5,3 (1Н, м), 6,08 (1Н, д, J 15 Гц), 6,6-7,6 (10Н, м), 8,09 (1Н, м), 10,75 (1Н, с)
Масс (m/e): 485 (M+2), 483 (М+), 213 (основ.)
(11) 1-[2-{5-(2-гидрокси-3-метоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино} этил]-4-(3-индолил) пиперидин.
Т.пл. 184-186оС (рекристаллизован из этанола)
ИК (Nujol): 3400, 3240, 1650, 1605, 1600, 1530, 1090, 1005 см-1
ЯМР (DMSO-d6, δ): 1,4-3,6 (13Н, м), 3,78 (3Н, с), 6,11(1Н, д, J 15 Гц), 6,6-7,65 (11Н, м), 7,90 (1Н, т подоб.), 8,95 (1Н, шир.), 10,75 (1Н, с).
Масс (m/e): 445 (М+), 226, 213 (основ.).
(12) 1-[2-{5-(3-Гидрокси-4-метоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино} этил]-4-(3-индолил) пиперидин.
Т.пл. 135-140оС (рекристаллизован из этанола)
ИК (Nujol): 3350, 1650, 1615, 1590 см-1.
ЯМР (DMSO-d6, δ): 1,4-3,5 (13Н, м), 3,75 (3Н, с), 6,11 (1Н, д, J 12 Гц), 6,6-7,7 (11Н, м), 7,91 (1Н, т подоб.), 9,0 (1Н, шир.), 10,7 (1Н, с).
Масс (m/e): 445 (М+), 213 (основ.).
П р и м е р 8. К смеси 1-[2-{5-(4-гидрокси-3-метоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино} этил] -4-(3-индолил) пиперидина (0,89 г), сухого N-метилморфолина (1,0 г) и сухого N,N-диметилформамида (10 мл) медленно добавляется ацетилхлорид (0,26 г) при 5-10оС. После перемешивания в течение 1 ч, реакционная смесь выливается в воду (50 мл) и размешивается в течение 1 ч. Полученный в результате преципитат собирается, отмывается водой и затем рекристаллизуется из смеси этанола и воды (7:3 об.) для получения 1-[2-{5-(4-ацетокси-3-метоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино}этил]-4-(3-индолил) пиперидина (0,22 г).
Т.пл. 101-105оС (рекристаллизован из смеси этанола и воды (8:2 об.)
ИК (Nujol): 3440, 32500, 1760, 1655, 1620, 1560, 1505 см-1.
ЯМР (DMSO-d6, δ): 1,5-2,4 (6Н, м), 2,24 (3Н, с), 2,6-3,5 (7Н, м), 3,81 (3Н, с), 6,20 (1Н, д, J 15 Гц), 6,8-7,7 (11Н, м), 8,04 (1Н, м), 10,73 (1Н, с)
Масс (m/e): 487 (М+), 213 (основ.).
Вычислено, С 68,89; H 6,98; N 8,31.
C29H33N3O4.2H2O.
Найдено, 68,91; H 6,95; N 8,32.
П р и м е р 9. 1-[2-{5-(3-Метокси-4-пропионилоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино} этил] -4-(3-индолил) пиперидин был получен способом, аналогичным описанному в примере 8.
Т.пл. 157-158оС (рекристаллизован из этанола)
ИК (Nujol):3430, 3250, 3060, 1750, 1655, 1620, 1560 см-1.
ЯМP (DМSO-d6,δ ):1,15 (3Н, т, J 8 Гц), 1,5-2,4 (6Н, м), 2,62 (2Н, кв. J 8Гц), 2,4-3,2 (5Н, м), 3,33 (2Н, м), 3,82 (3Н, с), 6,22 (1Н, д, J 15 Гц), 6,9-7,7 (11Н, м), 8,05 (1Н, м), 10,75 (1Н, с)
Масс (m/e): 501 (М+), 213 (основ.).
Вычислено, C 69,34; H 7,18; N 8,09.
C30H35N3O4.H2O.
Найдено, C 69,19; H 7,09; N 8,06.
П р и м е р 10. К смеси 1-[2-{5-(4-гидрокси-3,5-диметоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино} этил] -4-(3-индолил) пиперидина (1 г) и пиридина (10 мл) медленно добавляется ацетилхлорид (0,48 мл) при 5-10оС. Через 1 ч реакционная смесь выливается в ледяную воду и экстрагируется этилацетатом. Экстракт отмывается насыщенным водным раствором хлорида натрия и высушивается в присутствии сульфата магния. Затем раствор отгоняется, а остаток подвергается колоночной хроматографии на силикагеле и элюируется смесью хлороформа с этанолом (10:1 об.). Фракции, содержащие нужное соединение, объединяются и концентрируются при пониженном давлении. Остаток обрабатывается смесью фумаровой кислоты (83 г) с метанолом (8 мл) и концентрируется при пониженном давлении до получения белых кристаллов. Эти кристаллы рекристаллизуются из этанола для получения 1-[2-{5-(4-ацетокси-3,5-диметоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино}этил]-4-(3-индолил) пиперидин 1/2 фумарат (0,25 г).
Т.пл. 202-209оС
ИК (Nujol): 3400, 1750, 1680, 1615, 1595, 1565 см-1.
ЯМР (DMSO-d6, δ): 1,6-2,15 (5Н, м), 2,32 (3Н, с), 2,2-3,6 (8Н, м), 4,82 (6Н, с), 6,22 (1Н, д, J 14 Гц), 6,64 (1Н, с), 6,7-7,7 (10Н, м), 8,29 (1Н, м), 10,75 (1Н, с)
Масс (m/e): 517 (М+), 213 (основ.).
Вычислено, C 63,77; H 6,68; N 6,97.
C30H35N3O5.1/2 фумарат. 3/2H2O.
Найдено, C 63,57; H 6,44; N 6,95.
П р и м е р 11. 1-[2-{5-(3,5-Диметокси-4-пропионилоксифенил)-(2Е, 4Е)-2,4-пентaдиеноиламино} этил]-4-(3-индолил) пиперидин 1/2 фурамат был получен способом, аналогичным описанному в примере 10.
Т.пл. 188-192оС (рекристаллизован из этанола)
ИК (Nujol): 3400, 1745, 1680, 1615, 1595, 1565 см-1.
ЯМР (DMSO-d6, δ): 1,13 (3Н, т, J 7 Гц), 1,6-2,2 (3Н, м), 2,2-3,7 (12Н, м), 3,81 (6Н, с), 6,21 (1Н, д, J 15 Гц), 6,62 (1Н, с), 6,8-7,6 (10Н, м), 8,3 (1Н, м), 10,78 (1Н, с)
Масс (m/e): 531 (М+), 213 (основ.)
Вычислено, C 64,27; H 6,86; N 6,81.
C31H37N3O5.1/2 фумарат.3/2H2O.
Найдено, C 64,17; H 6,78; N 6,78.
П р и м е р 12. К смеси 1-[2-{5-(4-гидрокси-3,5-диметоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино} этил]-4-(3-индолил)пиперидина (1,19 г), триэтиламина (1,74 мл) и сухого N,N-диметилформамида (12 мл) медленно добавляется смесь этилхлороформиата (0,33 г) и метиленхлорида (0,5 мл) при 0-5оС. В результате получается соединение 1-[2-{5-(4-этоксикарбонилокси-3,5-диметоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино}этил]-4-(3-индолил) пиперидин (0,74 г).
Т.пл. 90-98оС (рекристаллизован из смеси этанол-вода (8:2 об.).
ИК (Nujol): 3360, 3300, 1750, 1640, 1590, 1130, 1000, 735 см-1.
ЯМР (DMSO-d6,δ ): 1,28 (3Н, т, J 8 Гц), 1,5-3,6 (13Н, м), 3,81 (6Н, с), 4,23 (2Н, кв. J8 Гц), 6,21 (1Н, д, J 15 Гц), 6,8-7,7 (10Н, м), 8,05 (1Н, м), 10,71 (1Н, с).
Масс (m/e): 547 (М+), 228, 213 (основ.)
Вычислено, C 62,82; H 6,14; N 7,09.
C31H37N3O6.2,5H2O.
Найдено, C 62,74; H 6,93; N 7,05.
П р и м е р 13. Нижеприведенные соединения получены методом, аналогичным описанному в примере 13.
(1) 1-[4-{5-(4-Этоксикарбонилсилокси-3,5-диметоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино}бутил]-4-(3-индолил) пиперидин.
Т.пл. 90-98оС (рекристаллизован из смеси этанол-вода (8:2 об.))
ИК (Nujol): 3380, 3250, 1750, 1655, 1620, 1595, 1555, 1130, 1050, 1000, 735 см-1.
ЯМР (DMSO-d6, δ): 1,27 (3Н, т, J 8 Гц), 1,4-3,7 (17Н, м), 3,72 (6Н, м), 3,72 (6Н, с), 4,23 (2Н, кв. J 8 Гц), 6,20 (1Н, д, J 15 Гц), 6,8-7,75 (10Н, м), 8,10 (1Н, м), 10,76 (1Н, с).
Масс (m/e): 575 (М+), 531, 503, 285, 233, 213 (основ.).
Вычислено, C 67,01; H 7,81; N 6,52.
C33H41N3O6.3/2 этанол.
Найдено, C 66,39; H 7,74; N 6,52.
(2) 1-[4-{5-(3,5-Диметокси-4-пропионилоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино}бутил]-4-(3-индолил) пиперидингидрохлорид
Т.пл. 215-220оС (рекриcталлизован из ацетонитрила).
ИК (Nujol): 3250, 2650, 2500, 1760, 1650, 1595, 1130, 1010, 850, 750 см-1.
ЯМР (CDCl3, δ): 1,29 (3Н, т, J 8 Гц), 2,65 (2Н, кв. J 8 Гц), 1,5-3,7 (17Н, м), 3,80 (6Н, с), 6,35 (1Н, д, J 15 Гц), 6,6-7,7 (10Н, м), 7,9 (1Н, м), 9,05 (1Н, м), 11,3 (1Н, м).
Масс (m/e): 559 (М+), 503, 233, 213 (основ.)
(3) 1-[2-[5-{ 3,4-бис(этоксикарбонилокси)фенил} -(2Е, 4Е)-2,4-пентадиеноиламино]этил]-4-(3-индолил) пиперидин.
Т.пл. 135-137оС (рекристаллизован из смеси воды и этанола).
ИК (Nujol): 3500, 3350, 1775, 1650, 1620, 1000 см-1.
ЯМР (DMSO-d6, δ): 1,30 (6Н, т, J 8 Гц), 1,3-3,5 (13Н, м), 4,30 (4Н, кв. J 8 Гц), 6,25 (1Н, д, J 15 Гц), 6,6-7,7 (11Н, м), 8,08 (1Н, м), 10,73 (1Н, с).
Масс (m/e): 529 (М+-46), 457, 285 (основ.), 213.
П р и м е р 14. К смеси 1-[2-{5-(4-гидрокси-3,5-диметоксифенил)-(2Е, 4Е)-2,4-пентадиенсиламино} этил]-4-(3-индолил) пиперидина (2,0 г), триэтиламина (2,9 мл) и сухого N,N-диметилформамида (20 мл) медленно добавляется раствор ацетохлорида (0,5 г) и метиленхлорида (1,0 мл) при 5оС. Через 1 ч реакционная смесь выливается в воду (200 мл) и перемешивается в течение 1 ч. Полученный в результате преципитат собирается, отмывается водой и высушивается при комнатной температуре. Затем этот преципитат хроматографируется на силикагеле (60 г) и элюируется смесью хлороформа и метанола (20:1 об.). Фракции, содержащие нужное соединение, объединяются и концентрируются при пониженном давлении. Остаток рекристаллизуется из этилацетата, в результате чего получаются светло-желтые кристаллы 1-[2-{5-(4-ацетокси-3,5-диметоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино}этил]-4-(3-индолил) пиперидина (1,35 г).
Т.пл. 169-172оС
ИК (Nujol): 3380, 3320, 1755, 1650, 1620, 1595, 990, 745 см-1.
ЯМР (CDCl3, δ): 1,5-3,6 (13Н, м), 2,32 (3Н, с), 3,82 (6Н, с), 6,0 (1Н, д, J 15 Гц), 6,34 (1Н, м), 6,7-7,7 (10Н, м), 8,32 (1Н, м)
Масс (m/e): 517 (М+), 213 (основ.).
Вычислено, C 69,61; H 6,82; N 8,12.
C30H35N3O5.
Найдено, C 69,35; H 6,82; N 8,02.
П р и м е р 15. К перемешанной смеси 5 [3,5-диметокси-4-{(2-метоксиэтокси)метокси}фенил]-(2Е, 4Е)-2,4-пентадиеновой кислоты (1,35 г) и триэтиламина (1,17 мл) в сухом N,N-диметилформамиде (8 мл) медленно добавляется дифенилфосфинхлорид (0,97 г) при -10-(-15)оС в инертной атмосфере. После перемешивания в течение 1 ч, в реакционную смесь при той же температуре медленно добавляется раствор 1-(2-аминоэтил)-4-(3-индолил) пиперидина (0,97 г) в сухом N, N-диметилформамиде (8 мл). После перемешивания в течение 40 мин при той же температуре реакционная смесь выливается в ледяную воду (160 мл) и экстрагируется этилацетатом. Экстракт отмывается насыщенным раствором хлорида натрия и высушивается в присутствии сульфата магния. Раствор выпаривается, в результате чего получается сироп 1-[2-[5-[3,5-диметокси-4-{(2-метоксиэтокси)метокси} фенил]-(2Е, 4Е)-2,4-пентадиеноиламино]этил]-4-(3-индолил) пиперидин (1,97 г).
ИК (Nujol): 3300, 1650, 1610, 1580, 1125, 990, 960, 845, 745 см-1.
П р и м е р 16. К горячему раствору гидрата лимонной кислоты (2,65 г) в смеси воды и этанола (4:6 об./об, 50 мл) добавляли 1-2-{5-(4-гидрокси-3,5-диметоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино}этил]-4-(3-индолил) пиперидин (6,0 г), и затем добавляли смесь воды с этанолом (4:6, об./об. 50 мл). Полученную смесь перемешивали в течение 6 часов при температуре окружающего воздуха и полученный в результате осадок собирали фильтрацией. Остаток промывали смесью воды с этанолом и сушили с получением 1-[2-{5-(4-гидрокси-3,5-диметоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино} этил]-4-(3-индолил) пиперидинцитрата (7,2 г).
Т.пл. 140-142оС.
ИК (ньюол): 3600, 3370, 3300, 1745, 1645 см-1.
ЯМР (DMCO-d6, δ): 1,78-2,1 (4Н, мультиплет), 2,8-3,2 (5Н, мультиплет), 3,33-3,62 (4Н, мультиплет), 3,80 (6Н, синглет), 6,11 (1Н, дублет, J 14,8 Гц), 6,8-7,25 (8Н, мультиплет), 7,36 (1Н, дублет, J 7,9 Гц), 7,61 (1Н, дублет, J 7,5 Гц), 8,35 (1Н, широкая), 10,86 (1Н, широкий синглет).
П р и м е р 17. Смесь 1-[2-{5-(4-гидрокси-3,5-диметоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино} этил] -4-(3-индолил-пиперидина (7,0 г), фумаровой кислоты (1,708 г) и метанола (200 мл) нагревали с обратным холодильником. После полного растворения твердого вещества смесь отфильтровывали и фильтрат выстаивали при комнатной температуре. Полученный в результате осадок собирали фильтрацией, промывали метанолом (10 мл) и сушили с образованием 1-[2-{ 5-(4-гидрокси-3,5-диметоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино} этил]- 4-(3-индолил)пиперидин фумарата (7,58 г).
Т.пл. 138-140оС.
ИК (ньюол): 3400-3150, 1700, 1645 см-1.
ЯМР (ДМСО-d6, δ): 1,75-2,1 (4Н, мультиплет), 2,5-3,0 (5Н, мультиплет), 3,15-3,5 (4Н, мультиплет), 3,80 (6Н, синглет), 6,09 (1Н, дублет J 14,8 Гц), 6,60 (2Н, синглет), 6,77-7,15 (8Н, мультиплет), 7,33 (1Н, дублет, J 7,8 Гц), 7,59 (1Н, дублет, J 7,4 Гц), 8,38 (1Н, триплето-подобная), 10,82 (1Н, широкий синглет).
П р и м е р 18. Следующие соединения получали согласно методу аналогичному способу примера 17.
(1) 1-[2-{5-(4-Гидрокси-3,5-диметоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино} этил]-4-(3-индолил) пиперидин (-)-тартрат (51 омг получали из 1-[2-{5-(4-гидрокси-3,5-диметоксифенил)-(2Е, 4Е)-2,4-пентадиенcиламино}этил]-4-(3-индолил) пиперидин (0,5 г) и (-)-винной кисилоты (158 г).
Т.пл. 144-147оС (разл.)
ИК (ньюол): 3450-3150, 1710, 1645, 1600 см-1.
ЯМР (ДМСО-d6, δ): 1,75-2,10 (4Н, мультиплет), 2,5-3,0 (5Н, мультиплет), 3,2-3,5 (4Н, мультиплет), 3,80 (6Н, синглет), 4,14 (2Н, синглет), 6,10 (1Н, дублет, J 14,8 Гц), 6,8-7,26 (8Н, мультиплет), 7,34 (1Н, дублет, J7,8 Гц), 7,59 (1Н, дублет, J 7,4 Гц), 8,34 (1Н, триплето-подобная), 10,82 (1Н, широкий синглет).
(2) 2-[2-{5-(4-Гидрокси-3,5-диметоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино} этил] -4-(3-индолил) пиперидин сукцинат (0,25 г) получали из 1-[2-{5-(4-гидрокси-3,5-диметоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино}этил]-4-(3-индолил) пиперидина (0,5 г) и янтарной кислоты (124 мг).
Т.пл. 95-105оС (разл.)
ИК (ньюол): 3400-3100, 1720, 1650, 1590 см-1.
ЯМР (ДМСО-d6, δ): 1,61-2,12 (4Н, мультиплет), 2,17-2,22 (2Н, мультиплет), 2,40 (4Н, синглет), 2,5-2,6 (2Н, мультиплет), 2,7-2,9 (1Н, мультиплет), 3,0-3,17 (2Н, мультиплет), 3,23-3,42 (2Н, мультиплет), 3,80 (6Н, синглет), 6,10 (1Н, дублет, J 14,8 Гц), 6,78-7,25 (8Н, мультиплет), 7,33 (1Н, дублет, J7,8 Гц), 7,55 (1Н, дублет, J 7,4 Гц), 8,07 (1Н, триплето-подобная), 10,78 (1Н, широкий синглет).
П р и м е р 19. К горячему раствору (+)-винной кислоты (2,21 г) в смеси этанола и воды (9:1, об./об. 200 мл) добавляли 1-[2-{5-(4-гидрокси-3,5-диметоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино} этил] -4-(3-индолил) пиперидин (7,0 г) при барботировании системы газообразным азотом. После этого к системе добавляли смесь этанола и воды (9:1, об./об. 80 мл), смесь нагревали с обратным холодильником в течение 5 минут и затем перемешивали в течение 3 часов при температуре окружающего воздуха. Полученный в результате осадок собирали фильтрацией, промывали смесью этанола с водой (9:1, об./об./20 мл) и сушили в получением 1-[2-{5-(4-гидрокси-3,5-диметоксифенил)-(2Е, 4Е)-2,4-пентадиеноил-амино}этил]-4-(3-индолил) пиперидин (+)тартрата (8,18 г).
Т.пл. 142-146оС.
ИК (ньюол): 3450-3150, 1710, 1645, 1600 см-1.
ЯМР (ДМСО-d6, δ): 1,73-2,15 (4Н, мультиплет), 2,5-3,0 (5Н, мультиплет), 3,17-3,5 (4Н, мультиплет), 3,80 (6Н, синглет), 4,13 (2Н, синглет), 6,10 (1Н, дублет, J 14,8 Гц), 6,8-7,26 (8Н, мультиплет), 7,34 (1Н, дублет, J7,8 Гц), 7,58 (1Н, дублет, J 7,5 Гц), 8,30 (1Н, триплет-подобное), 10,82 (1Н, широкий синглет).
П р и м е р 20. 1-[2-{5-(4-Гидрокси-3,5-диметоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино} этил] -4-(3-индолил) пиперидин (4,5 г) растворяли в смеси метанола (90 мл), 1 н. хлористоводородной кислоты (18,9 мл) и воды (19,8 мл) и по каплям, при комнатной температуре добавляли воду. Полученный осадок собирали фильтрацией, промывали этанолом (9 мл) и сушили с получением 1-[2-{ 5-(4-гидрокси-3,5-диметоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино} этил]- 4-(3-индолил)пиперидин гидрохлорида (4,30 г).
Т.пл. 155оС.
ИК (ньюол): 3350, 2650, 1640, 1620 см-1.
ЯМР (ДМСО-d6, δ ): 2,0-2,3 (4Н, мультиплет), 3,0-3,3 (5Н, мультиплет), 3,5-3,75 (4Н, мультиплет), 3,80 (6Н, синглет), 6,13 (1Н, дублет, J 14,8 Гц), 6,8-7,4 (9Н, мультиплет), 7,69 (1Н, дублет, J 7,7 Гц), 8,67 (1Н, мультиплет), 8,72 (1Н, синглет), 10,60 (1Н, широкий синглет), 10,93 (1Н, синглет).
В качестве иллюстрации к использованию рассматриваемого соединения (1) ниже приводятся фармакологические данные тестов некоторых характерных представителей соединения (1).
Испытание 1.
Антагонистическoе действие на анафилактическую астму у морских свинок.
Методика.
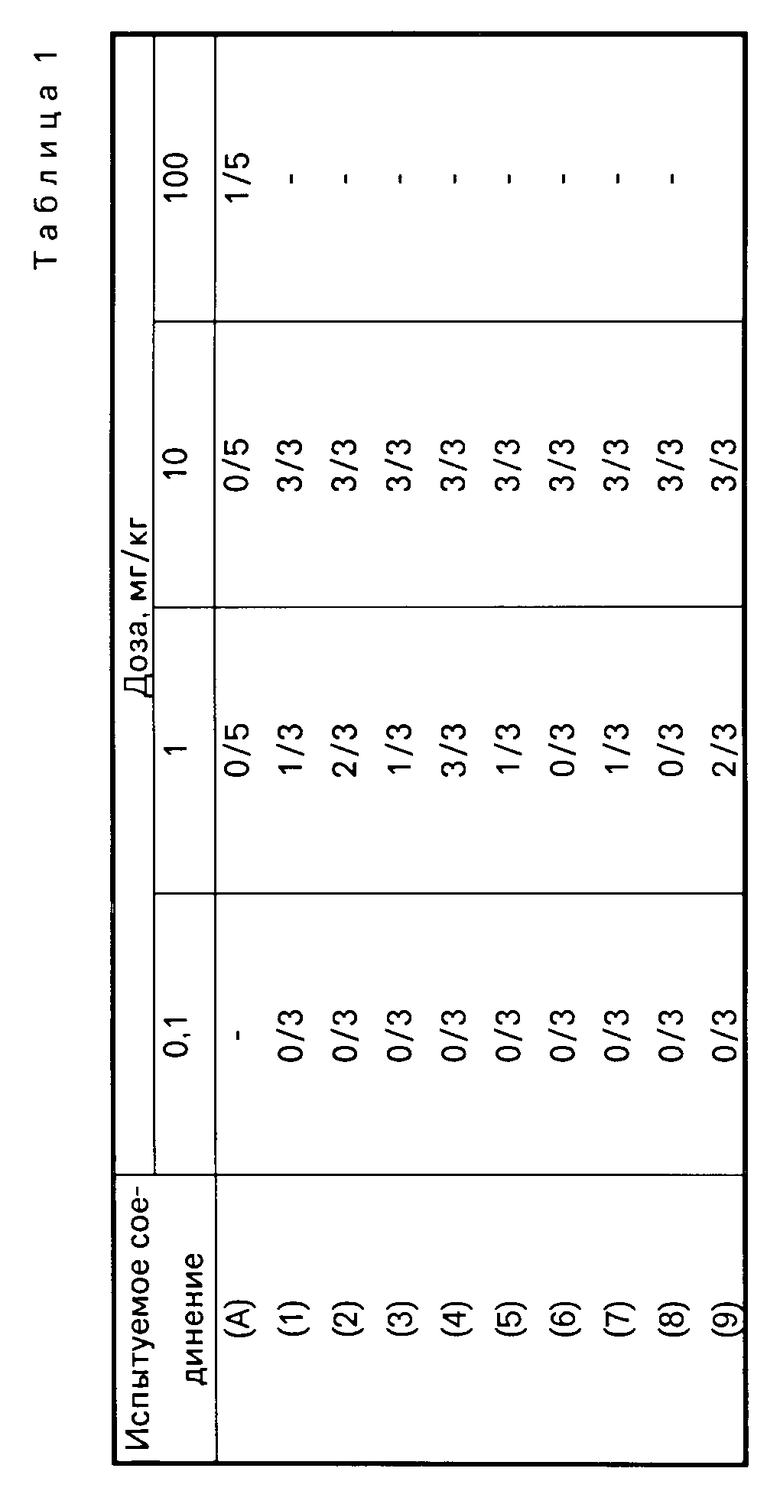
Были использованы самцы морских свинок вида Hartley весом 305-400 г. Эти животные были сенсибилизированы внутривенной инъекцией 0,5 мл/животное кроличьей антисывороткой к альбумину яичного белка/РСА титр антитела 4000). Через 24 ч животных помещали отдельно в пластичные камеры объемом 5,3 л. В каждую камеру вводили в виде аэрозоля с помощью стандартного пульверизатора 5% -ный раствор альбумина яичного белка со скоростью 0,16 мл/мин в течение 2 мин. За 30 мин до распыления растворa альбумина яичного белка было введено орально испытуемое соединение в различных концентрациях. Для оценки использовали количество морских свинок, оставшихся в живых в течение не менее 2 ч после распыления антигена при каждой введенной концентрации испытуемого соединения. Профилактическое действие к анафилаксису оценивали как отношение количества выживших морских свинок к количеству свинок используемой группы.
Испытуемое соединение 1-[2-[5-(4-Окси-3-метоксифенил)-(2Е,4Е)-2,4-пентадиеноил] аминоэтил] -4-бензги дроксипиперидин (здесь и далее указано как испытуемое соединение (А));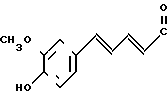


(А)
1-[2-[5-(4-Окси-3-метоксифенил)-(2Е, 4Е)-2,4-пентадиеноил]аминоэтил]-4-(3-индолил) пиперидин (здесь и далее указано как испытуемоe соединение (1));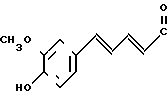
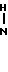

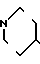
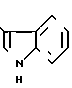
(1)
1-[2-[5-(4-окси-3,5-диметоксифенил)-(2Е, 4Е)-2,4-пентадиеноил]аминоэтил] -4-(3-индолил) пиперидин (здесь и далее указано как испытуемое соединение (2));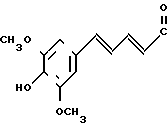
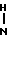


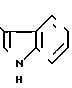
(2)
1-[2-[5-(4-ацетокси-3-метоксифенил)-(2Е, 4Е)-2,4-пентадиеноил]аминоэтил] -4-(3-индоил) пиперидин (здесь и далее указано как испытуемое соединение (3));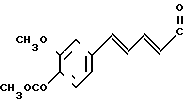
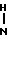

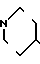
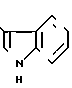
(3)
1-[2-[5-(4-этоксикарбонилокси-3,5-диметоксифенил-(2Е, 4Е)-2,4-пентадиеноил] аминоэтил] -4-(3-индолил) пиперидин (здесь и далее указано как испытуемое соединение (4));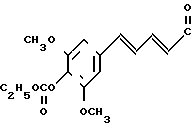

(4)
1-[2-[5-(4-окси-3,5-диметилфенил)-(2Е, 4Е)-2,4-пентадиеноил]аминоэтил] -4-(3-индолил) пиперидин (здесь и далее указано как испытуемое соединение (5));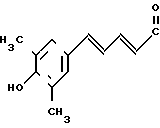

(5)
1-[2-[5-(4-окси-3,5-диизопропилфенил)-(2Е, 4Е)-2,4-пентадиеноил]аминоэтил] -4-(3-индолил) пиперидин (здесь и далее указано как испытуемое соединение (6));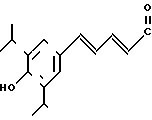
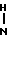

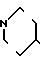
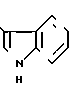
(6)
1-[2-[5-(3-хлор-4-оксифенил)-(2Е, 4Е)- 2,4- пентадиеноил]аминоэтил]-4-(3-индолил) пиперидин (здесь и далее указано как испытуемое соединение (7));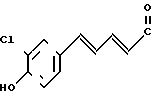

(7) 1-[2-[3-(4-окси-3-метоксифенил)-(Е)-пропеноил] аминоэтил]-4-(3-индолил) пиперидин (здесь и далее указано как испытуемое соединение (8));
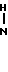

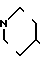
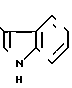
(8)
1-[4-[5-(4-окси-3-метоксифенил)-(2Е, 4Е)-2,4-пентадиеноил]аминобутил]-4-(3-индолил) пиперидин (здесь и далее указано как испытуемое соединение (9));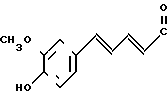


(9)
1-[2-{ 5-(4-ацетокси-3,5-диметоксифенил)-(2Е, 4Е)-2,4-пентадиеноиламино} этил]-4-(3-индолил)-пиперидин (соединение 10)
1-[2-{5-(3,5-дихлор-4-гидроксифенил-(2Е, 4Е)-2,4-пентадиеноиламино}этил] -4-(3-индолил) пиперидин (соединение 11).
Результаты испытания приведены в табл. 1.
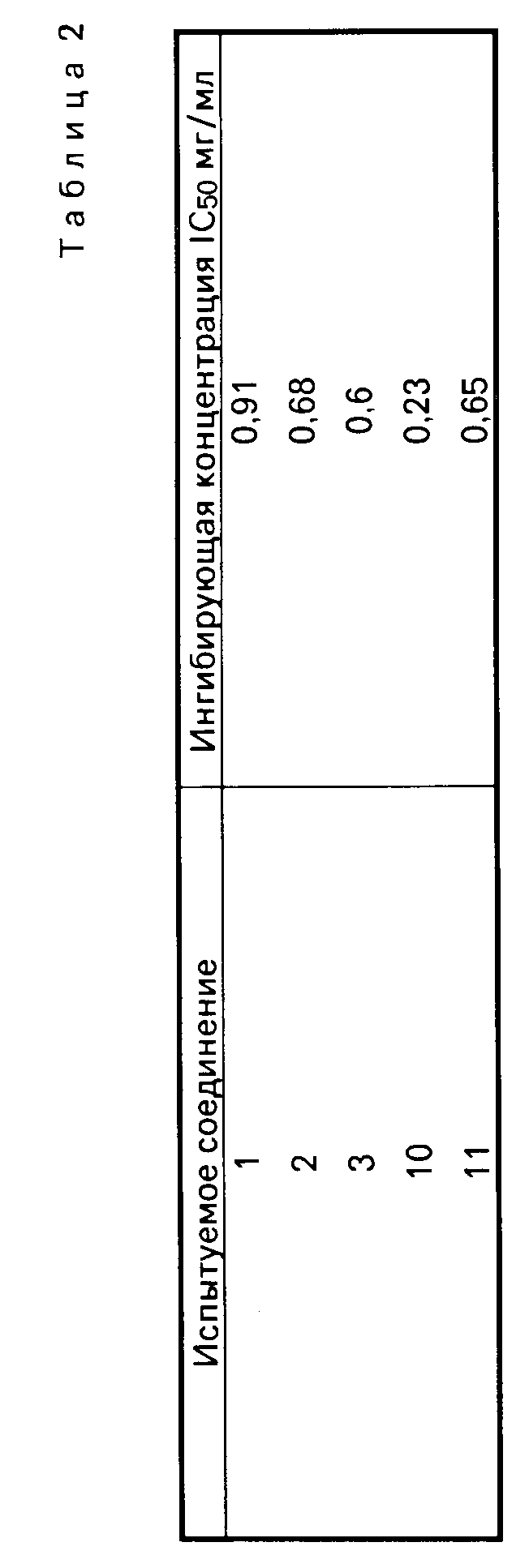
Тест 2.
Противодействие медленно-реагирующему веществу "А" (SRS-А).
От крыс, которым был введен гликоген, были собраны клетки перитонеального экссудата, приведенного затем в концентрации 1 х 107 кмл/мл с помощью раствора Tyrode. Один миллилитр клеточной суспензии инкубировался в присутствии индометацина (10 мг/мл) и исследуемого соединения в каждой концентрации в течение 10 мин, а затем в течение 10 мин в присутствии Са++ ионофора (А23187, 1 мг/мл). Супернатант собирался путем центрифугирования и SRS А-активность определялась исходя из сократительной способности подвздошной кишки изолированных морских свинок в присутствии мепирамина, атропина и метизергина.
Ниже представлены результаты испытания, выраженные в виде 50% ингибирующей концентрации к синтезу SRS-А или секреции клеток перитонеального экссудата.
Результаты испытаний приведены в табл. 2.
Для более детальной иллюстрации изобретения ниже приводятся композиции и примеры их изготовления.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных индолилпиперидина или их солей | 1989 |
|
SU1814645A3 |
| Способ получения производных индолилпиперидина или их солей | 1989 |
|
SU1804460A3 |
| ПРОИЗВОДНЫЕ ПЕПТИДОВ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ПРЕДУПРЕЖДЕНИЯ И УСТРАНЕНИЯ ТРОМБОЗОВ | 1992 |
|
RU2103276C1 |
| СПОСОБ ПОЛУЧЕНИЯ СОЕДИНЕНИЙ ЦЕФЕМА ИЛИ ИХ КИСЛОТНО-АДДИТИВНЫХ СОЛЕЙ | 1988 |
|
RU2017744C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ТИАЗОЛА ИЛИ ИХ СОЛЕЙ С ГАЛОИДВОДОРОДНОЙ КИСЛОТОЙ | 1990 |
|
RU2010026C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПИРАЗОЛПИРИДИНОВОГО ПРОИЗВОДНОГО ИЛИ ЕГО СОЛИ | 1990 |
|
RU2007403C1 |
| ПРОИЗВОДНЫЕ ТИАЗОЛА | 1991 |
|
RU2048468C1 |
| ПРОИЗВОДНЫЕ ПИРАЗОЛО [1,5-А] ПИРИДИНА, ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1992 |
|
RU2069662C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ПИРАЗОЛА ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫХ СОЛЕЙ | 1990 |
|
RU2021990C1 |
| ТРИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ | 1989 |
|
RU2007406C1 |
Использование: в качестве веществ, обладающих противоаллергическим действием. Сущность изобретения: продукт производные индолилпиперидина общей формулы I, где R1 -фенил, замещенный заместителями, выбранными из группы, содержащей низший алкил, гидроксил, защищенный гидроксил, галоген или низший алкокси; А низший алкилен, В низший алкенилен, или их фармацевтически приемлемые соли. Структура ф-лы I: 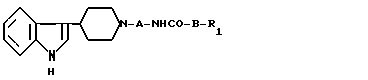 6 з.п. ф-лы, 2 табл.
6 з.п. ф-лы, 2 табл.
где R1 фенил, замещенный заместителями, выбранными из группы, содержащей низший алкил, гидроксил, защищенный гидроксил, галоген, или низший алкокси;
А низший алкилен;
В низший алкенилен;
или их фармацевтически приемлемые соли.
| 0 |
|
SU157420A1 | |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1995-07-09—Публикация
1991-11-28—Подача