Изобретение относится к новому пептидному соединению и к его соли. Более конкретно, оно относится к новому пептидному соединению и его соли, которое представляет собой антагонист IIb/IIa гликоперотеина и ингибитор агрегирования тромбоцитов и использовано как
лекарство для профилактики или лечения заболеваний, вызываемых образованием тромбов, таких как артериальный тромбоз; атеросклероз; ишемические болезни сердца (например, стенокардия (например, устойчивая стенокардия, неустойчивая стенокардия, включая угрозу инфаркта, и т.д.), инфаркт миокарда (например, острый инфаркт миокарда и др.), коронарный тромбоз и т.д.); ишемические болезни головного мозга (например, церебральный инфаркт {например, церебральный тромбоз (например, острый церебральный тромбоз и др.), эмболия головного мозга и др.}, преходящая церебральная ишемия, цереброваскулярный спазм после арахноидальное кровотечение и др.) и т.п.; легочно-сосудистые заболевания (например, легочный тромбоз, легочная эмболия и др.); расстройства периферического кровообращения (например, облитерирующий артериосклероз, облитерирующий тромбоангиит (т.е. болезнь Бюргера), болезнь Рейно, осложнения сахарного диабета (например, диабетическая ангиопатия и др.), флеботромбоз (например, тромбоз глубоких вен и др.) и т.п.;
лекарство для профилактики или лечения рестеноза и/или реокклюзии, как, например, рестеноз и/или реокклюзия после подкожной транслюминальной коронарной ангиопластики (РТСА), рестеноз и/или реокклюзия после введения тканевого плазминогенного активатора (ТРА) и т.п.;
лекарство для вспомогательной терапии при лечении тромболитическими средствами (например, ТРА и др.) или антикоагулянтом (например, гепарин и др.);
лекарство для профилактики и/или лечения рассеянной внутрисосудистой коагуляции (DIC), тромботической тромбоцитопении, основного тромбоза, воспалительных заболеваний (например, нефрит и др.), иммунной системы заболеваний и т.п.;
лекарство для профилактики и/или лечения образования тромбов в случае сосудистой хирургии, замены клапанов, экстракорпоральное кровообращение (например, гемодиализ и др.), трансплантации и т.п.;
лекарство для подавления развития метастазов; и т.п.
Ожидают, что пептидное соединение по данному изобретению окажется полезным в качестве ингибитора клеточной адгезии и, следовательно, лекарства для профилактики и/или печения рассеянной внутрисосудистой коагуляции крови (DIC), тромботической тромбопении, основного тромбоза, воспалений (например, нефрит и др.), заболеваний иммунной системы и т.п.; лекарства для подавления метастазов и т.п.
В соответствии с этим, одной из целей изобретения является создание нового пептидного соединения или его соли, которое может использоваться как указывалось выше.
Еще одной целью изобретения является обеспечение способов получения указанного нового пептидного соединения или его соли.
Целью изобретения является далее обеспечение фармацевтической композиции, включающей, в качестве активного ингредиента, указанное пептидное соединение иди его соль.
Далее, целью изобретения является также разработка методов использования указанного пептидного соединения или его соли для профилактики и/или лечения вышеперечисленных заболеваний человеческого существа или животного.
Целевое пептидное соединение по данному изобретению можно представить следующей формулой (I):
где R1 это арил, который может нести один или более подходящих заместителей;
R2 это карбокси/низший/алкил или защищенный карбокси/низший/алкил,
R3 это карбоксил или защищенный карбоксил,
A1 это алкилен, который может иметь один или более подходящих заместителей,
A2 это группа формулы: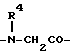
где R4 это низший алкил или группа формулы:
-NHCH2CH2CO-,
A3 это низший алкилен, который может иметь один или более подходящих заместителей,
l, m и n каждый, одинаковый или различный, представляет собой целое от 0 до 1,
при условии, что A2 не представляет собой группу формулы:
-NHCH2CH2CO-,
когда l это целое, равное 0.
Целевое соединение (I) или его соль можно получить следующими способами.
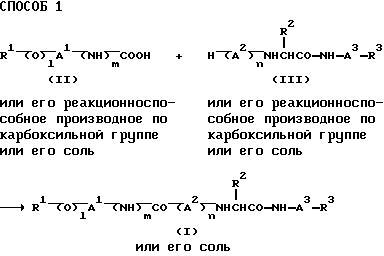



где R1, R2, R3, A1, A3, l, m и n каждая как определено выше,
R
R
R
R
R
R
R
A
A
Среди исходных соединений (II), (III), (IV), (V) и (VI) имеются новые соединения. Их можно получить из известных соединений традиционными для данной области способами или способами, аналогичными описанным в разделах Препараты и/или Примеры данного описания.
Подходящие фармацевтически приемлемые соли целевого соединения (I) представляют собой обычные нетоксичные соли, включая соли металлов, такие как соли щелочного металла (например, соль натрия, калия и так далее) и соли щелочноземельного металла (например, соль кальция, соль магния и тому подобные), соль аммония, соль органического основания (например, соль триметиламина, соль триэтиламина, соль пиридина, соль пиколина, соль дициклогексиламина, соль N,N-дибензилэтилендиамина и т.п.), соль присоединения органической кислоты (например, формиат, ацетат, трифторацетат, малеат, тартрат, метансульфонат, бензилсульфонат, толуолсульфонат и т.п.), соль присоединения неорганической кислоты (например, гидрохлорид, гидробромид, гидроиодид, сульфат, фосфат и т.п.), соль аминокислоты (например, соль аргинина, соль аспарагиновой кислоты, соль глутаминовой кислоты и т.п.) и др.
При описании изобретения примеры различных определений подробно понимать следующим образом.
Термин "низший" используется для обозначения от 1 до 6 атомов углерода, если не указано по-другому.
Подходящий "арил" может включать фенил, нафтил (например, 1-нафтил, 2-нафтил), антрил (например, 1-антрил, 2-антрил, 9-антрил и др.) и т.п., причем предпочтительным арилом является фенил.
Этот "арил" может иметь один или более (предпочтительно, 1 - 3) подходящих заместителей, таких как амидино-, защищенная амидино-группа и т.п.
Подходящая защитная группа в "защищенной амидино-группе" может включать ар(низший)алкил, такой как моно-, или ди-, или трифенил(низший)алкил (например, бензил, фенетил, 1-фенилэтил, бензгидрил, тритил и т.п.), ацил, как будет показано ниже, и др.
Подходящий ацил может представлять собой алифатический ацил, ароматический ацил, арилалифатический ацил и гетеро-цикло-алифатический ацил, которые являются производными карбоновой кислоты, угольной кислоты, карбаминовой кислоты, сульфоновой кислоты и т.п.
В качестве примера ацильной группы в соответствии с данным объяснением можно привести низший алканоил (например, формил, ацетил, пропионил, гексаноил, пивалоил и др. ), моно (или ди, или три)-галоген(низший)алканоил (например, хлорацетил, трифторацетил и др. ), низший алкоксикарбонил (например, метоксикарбонил, этоксикарбонил, трет-бутоксикарбонил, трет-пентиоксикарбонил, гексилоксикарбонил и др.), моно (или ди, или три)-галоген(низший) алкоксикарбонил (например, хлорметоксикарбонил, дихлорэтоксикарбонил, трихлорэтоксикарбонил и др.), ароил (например, бензоил, толуоил, ксилоил, нафтоил и др.), ар(низший)алканоил, такой как фенил(низший)алканоил (например, фенилацетил, фенилпропионил и др.), арилоксикарбонил (например, фенилоксикарбонил, нафтилоксикарбонил и др.), арилокси(низший)алканоил, такой как фенокси(низший)алканоил (например, феноксиацетил, феноксипропионил и др. ), арилглиоксилоил (например, фенилглиоксилоил, нафтилглиоксилоил, и др. ), арил(низший)алкоксикарбонил, который может иметь подходящие заместители, такие как фенил(низший)алкоксикарбонил, который, возможно, включает нитро- или низшую алкокси-группу (например, бензилоксикарбонил, фенилоксикарбонил, р-нитробензилоксикарбонил, р-метоксибензилоксикарбонил и др.), тиенилацетил, имидазолилацетил, фурилацетил, тетразолилацетил, триазолилацетил, тиадиазолилацетил, тиенилпропионил, тиадиазолилпропионил, низший алкилсульфонил (например, метилсульфонил, этилсульфонил, пропилсульфонил, изопропиосульфонил, пентилсульфонил, бутилсульфонил и др. ), арилсульфонил (например, фенилсульфонил, толил сульфонил, ксилилсульфонил, нафтилсульфонил и др.), арил/низший/алкилсульфонил, такой как фенил/низший/алкилсульфонил (например, бензилсульфонил, фенетилсульфонил, бензгидрилсульфонил и др.) и т.п.
Предпочтительным примером "защищенной амидино-группы" может служить N-арил/низший/алкоксикарбониламидино, более предпочтительным может быть N-фенил/низший/алкоксикарбонил-амидино-, намного более предпочтительным примером может служить N-фенил/C1-C4/алкоксикарбониламидино-группа, и наиболее предпочтительным примером является N-бензилоксикарбониламидино-группа.
Подходящими "низшими алкилами" могут быть алкилы с прямой или разветвленной цепью, такие как метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил, трет-бутил, пентил, гексил и т.п., предпочтительным среди которых может быть /C1-C4/алкил, и подходящий остаток "низшего алкила" в "карбокси(низший)алкиле" может относиться к указанному "низшему алкилу".
Подходящие примеры "карбокси(низший)алкила" могут включать карбоксиметил, 1-карбоксиэтил, 2-карбоксиэтил, 2-карбоксипропил, 3-карбоксибутил, 2-карбокси-1,1-диметилэтил, 5-карбоксипентил, 6-карбоксигексил и т.п., предпочтительным среди которых может быть карбокси/C1-C4/алкил и более предпочтительным - карбоксиметил или 2-карбоксиэтил.
Подходящий остаток "защищенной карбокси-группы" в "защищенном карбокси(низший)алкиле" может представлять собой этерифицированную до сложного эфира карбокси-группу и т.п., и конкретными примерами остатка сложного эфира в указанной этерифицированной карбокси-группе могут служить такие, как сложный эфир низшего алкила (например, метиловый эфир, этиловый эфир, пропиловый эфир, изопропиловый эфир, бутиловый эфир, изобутиловый эфир, трет-бутиловый эфир, пентиловый эфир, гексиловый эфир, 1-циклопропилэтиловый эфир и др. ), который может содержать подходящие заместители, например, низший алканоилокси/низший/алкиловый эфир /например, ацетоксиметиловый эфир, пропионилоксиметиловый эфир, бутирилоксиметиловый эфир, валерилоксиметиловый эфир, пивалоилоксиметиловый эфир, 1-ацетилоксиэтиловый эфир, 1-пропионилоксиэтиловый эфир, пивалоилоксиметиловый эфир, 2-пропионилоксиэтиловый эфир, гексаноилоксиметиловый эфир и др./, низший алкансульфонил/низший/алкиловый эфир /например, 2-мезилэтиловый эфир и др./, или моно/или ди, или три/галоген/низший/алкиловый эфир /например, 2-иодоэтиловый эфир, 2,2,2-трихлорэтиловый эфир, и др./; низший алкениловый эфир /например, виниловый эфир, аллиловый эфир, и др./; низший алкиниловый эфир (например, этиниловый эфир, пропиниловый эфир и др.); арил/низший/алкиловый эфир, который может содержать подходящие заместители (например, бензиловый эфир, 4-метоксибензиловый эфир, 4-нитробензиловый эфир, фенетиловый эфир, тритиловый эфир, бензгидриловый эфир, бис(метоксифенил)метиловый эфир, 3,4-диметоксибензиловый эфир, 4-гидрокси-3,5-ди-трет-бутил-бензиловый эфир и др.); ариловый эфир, который может содержать подходящие заместители (например, фениловый эфир, 4-хлорфениловый эфир, толиловый эфир, 4-трет-бутилфениловый эфир, ксилиловый эфир, мезитиловый эфир, кумениловый эфир и др.); или т.п., предпочтительным среди которых может быть моно-, или ди-, или трифенил/C1-C4/алкиловый эфир, и наиболее предпочтительным может быть бензиловый эфир.
Подходящий остаток "низшего алкила" в "защищенном карбокси/низший/алкила" может относиться к вышеуказанному "низшему алкилу".
В качестве подходящего примера указанного "защищенного карбокси/низший/алкила" можно упомянуть фенил/низший/алкоксикарбонил/низший/алкилы, среди которых предпочтительными могут являться /C1-C4/алкоксикарбонил/C1-C4алкил, а более предпочтительным - бензилоксикарбонилметил или 2-бензилоксикарбонилэтил.
К подходящим "защищенным карбокси" можно отнести группы, приведенные в качестве примеров "защищенных карбокси" остатков "защищенного карбокси/низший/алкила".
Подходящими примерами "защищенной карбокси" могут служить фенил/низший/алкоксикарбонил, предпочтительным может являться фенил/C1-C4/алкоксикарбонил, и более предпочтительным - бензилоксикарбонил; или низший алкоксикарбонил, предпочтительным из которых может быть /C1-C4/алкоксикарбонил и более предпочтительным - метоксикарбонил или этоксикарбонил.
Подходящими "алкиленами" могут быть алкилены, содержащие от 1 до 12 атомов углерода, такие как метилен, этилен, триметилен, тетраметилен, пентаметилен, гексаметилен, гептаметилен, октаметилен, нонаметилен, декаметилен, ундекаметилен, додекаметилен и т. п. , предпочтительными могут быть /C1-C10/-алкилен и более предпочтительными - метилен, этилен, триметилен, тетраметилен, пентаметилен или гептаметилен.
Такой "алкилен" может содержать один или более (предпочтительно от 1 до 3) подходящих заместителей, таких как амино, защищенный амино и т.п.
К подходящим защитным группам в указанном "защищенном амино" можно отнести группы, приведенные в качестве примеров "защищенной амидино-группы".
Предпочтительным примером "защищенной амино" может служить низший алкиламино или низший алкоксикарбониламино, где более предпочтительным может быть /C1-C4/алканоиламино или /C1-C4/алкоксикарбониламино и наиболее предпочтительным - ацетиламино или трет-бутоксикарбониламино.
Подходящие "низшие алкилены" могут включать метилен, этилен, триметилен, тетраметилен, пентаметилен, гексаметилен и т.п., где предпочтительным может быть /C1-C4/алкилен, и более предпочтительным - метилен или триметилен.
Такой "низший алкилен" может содержать один или более (предпочтительно от 1 до 3) подходящих заместителей, таких как вышеупомянутый низший алкил; арил/низший/алкил, который может содержать один или более подходящих заместителей, значения которых будут объяснены ниже; гидрокси/низший/алкил /например, гидроксиметил, 1-гидроксиэтил, 2-гидроксиэтил, 3-гидроксипропил, 2-гидроксибутил, 1,1-диметил-2-гидроксиэтил, 5-гидроксипентил, 6-гидроксигексил и др./; защищенный гидрокси/низший/алкил, значение которого будет объяснено позже; /цикло/низший/алкил/-/низший/алкил (например, циклопропилметил, циклобутилметил, циклогексилметил, 2-циклопентилэтил, 1-циклогексилэтил, 3-циклопентилпропил, 2-циклогексилбутил, 1,1-диметил-2-циклопропилэтил, 5-циклобутилпентил, 6-циклогексилэтил и др.); гетероцикло/низший/алкил, значение которого будет дано позже и т.п.
Подходящий "арил/низший/алкил" или "низший алкилен", описанные выше, может включать моно/или ди, или три/-фенил/низший/алкил, такой как бензил, фенетил, 2-фенилпропил, 4-фенилбутил, 1,1-диметил-2-фенилэтил, 5-фенилпентил, 6-фенилгексил, дифенилметил, 1,2-дифенилэтил, тритил, 1,2,3-трифенилпропил и т. п., где предпочтительным может быть фенил-/C1-C4/алкил, а более предпочтительным - бензил.
Такой "арил/низший/алкил" может содержать один или более (предпочтительно от 1 до 3) подходящих заместителей, таких как гидрокси; защищенная гидрокси (например, арил/низший/-алкилокси, где "остаток арил/низший/алкил" может относиться к приведенным выше в качестве примеров; ацилокси, где остаток "ацил" может относиться к вышеопределенным и др.); низшая алкокси-группа (например, метокси, этокси, пропокси, бутокси, трет-бутокси, пентилокси, гексилокси и др.); и т.п., где предпочтительной группой может быть гидрокси, фенил/C1-C4/-алкилокси или /C1-C4/алкокси, и более предпочтительной - гидрокси, бензилокси, метокси или этокси.
Подходящие "защищенные гидрокси/низший/алкилы" могут включать арил/низший/алкилокси/низший/алкил, ацилокси/низший/алкил и т.п., где остаток "арил/низший/алкил", остаток "ацил" и остаток "/низший/алкил" могут относиться к вышеуказанным.
Предпочтительный "защищенный гидрокси/низший/алкил" может представлять собой фенил/C1-C4/алкилокси/C1-C4/алкил, и более предпочтительный - это бензилоксиметил или 1-бензилоксиэтил.
Подходящий "гетероциклический" остаток в "гетероцикло-/низший/алкиле" обозначает насыщенную или ненасыщенную, моноциклическую или полициклическую гетероциклическую группу, содержащую по крайней мере один гетероатом, такой как кислород, сера, азот и т.п. И особенно предпочтительной гетероциклической группой может быть такая, как ненасыщенная 3-8-членная гетероциклическая группа, содержащая от 1 до 4 атомов азота, например, пирролил, пирролинил, имидазолил, пиразолил, пиридил и его N-окись, пиримидил, пиразинил, пиридазинил, триазолил (например, 4Н-1,2,4-триазолил, 1Н-1,2,3-триазолил, 2Н-1,2,3-триазолил и др.), тетразолил (например, 1Н-тетразолил, 2Н-тетразолил и др. ), дигидротриазинил (например, 4,5-дигидро-1,2,4-триазинил, 2,5-дигидро-1,2,4-триазинил, и др.) и т.п.;
насыщенная 3-8-членная гетеромоноциклическая группа, содержащая от 1 до 4 атомов азота, например, пирролидинил, имидазолидинил, пиперидил (например, пиперадино, и др.), пиперазинил и др.;
ненасыщенная конденсированная гетероциклическая группа, содержащая от 1 до 5 атомов азота, например, индолил, изоиндолил, индолизинил, бензилимидазолил, хинолил, изохинолил, индазолил, бензотриазолил, тетразолопиридил, тетразолопиридазинил (например, тетразоло/1,5- /пиридазинил, и др.);
ненасыщенная 3-8-членная гетеромоноциклическая группа, содержащая от 1 до 2 атомов кислорода и от 1 до 3 атомов азота, например, оксазолил, изоксазолил, оксадиазолил, (например, 1,2,4-оксадиазолил, 1,3,4-оксадиазолил, 1,2,5-оксадиазолил и др.) и т.п.;
насыщенная 3-8-членная гетеромоноциклическая группа, содержащая от 1 до 2 атомов кислорода и от 1 до 3 атомов азота, например, морфолинил, оксазолидинил (например, 1,3-оксазолидинил и др.) и т.д.;
ненасыщенная конденсированная гетероциклическая группа, содержащая от 1 до 2 атомов кислорода и от 1 до 3 атомов азота, например, бензоксазолил, бензоксадиазолил и др.;
ненасыщенная 3-8-членная гетеромоноциклическая группа, содержащая от 1 до 2 атомов серы и от 1 до 3 атомов азота, например, 1,3-тиазолил, 1,2-тиазолил, тиазолинил, тиадиазолил (например, 1,2,4-тиадиазолил, 1,3,4-тиадиазолил, 1,2,5-тиадиазолил, 1,2,3-тиадиазолил) и т.п.;
насыщенная 3-8-членная гетеромоноциклическая группа, содержащая от 1 до 2 атомов серы и от 1 до 3 атомов азота, например, тиазолидинил и др.;
ненасыщенная 3-8-членная гетеромоноциклическая группа, содержащая от 1 до 2 атомов серы и от 1 до 3 атомов азота, например, бензотиазолил, бензотиадиазолил и др.;
ненасыщенная 3-8-членная гетеромоноциклическая группа, содержащая от 1 до 2 атомов кислорода, например, фурил, пиранил, диоксолил и др.;
насыщенная 3-8-членная гетеромоноциклическая группа, содержащая от 1 до 2 атомов кислорода, например, оксоланил, тетрагидропиранил (например, тетрагидро-2Н-пиран-2-ил и др.), диоксоланил и т.п.;
ненасыщенная конденсированная гетероциклическая группа, содержащая от 1 до 2 атомов кислорода, например, изобензофуранил, хроменил (например, 2Н-хромен-3-ил и др.), дигидрохроменил (например, 3,4-дигидро-2Н-хромен-4-ил и др.) и др.; и т.п.
Предпочтительный "гетероциклический" остаток может быть 3-8-членной гетеромоноциклической группой, содержащей от 1 до 4 атомов азота, в более предпочтительном варианте это может быть пиридил.
Среди подходящих заместителей "низшего алкилена" предпочтительным может быть /C1-C4/алкил; фенил/C1-C4/алкил, который может включать от 1 до 3 гидрокси, фенил/C1-C4/алкилокси или /C1-C4/алкокси-групп; гидрокси/C1-C4/алкил; фенил-/C1-C4/алкилокси/C1-C4/алкил; цикло/C5-C6/алкил/C1-C4/алкил; или пиридил/C1-C4/алкил, и более предпочтительным может быть метил, этил, пропил, изопропил, бутил, 1-метилпропил, 2-метилпропил, трет-бутил, бензил, /4-гидроксифенил/метил, /4-бензилоксифенил/метил, /4-метоксифенил/метил, /4-этоксифенил/-метил, гидроксиметил, 1-гидроксиэтил, бензилоксиметил, 1-бензилоксиэтил, циклогексилметил или 2-пиридилметил.
Термин "/гидрокси/-арил/низший/алкил" обозначает арил/низший/алкил, содержащий гидрокси-группу.
Термин "/защищенный гидрокси/-арил/низший/алкил" обозначает арил/низший/алкил, содержащий защищенную гидрокси-группу.
Далее дается подробное объяснение способов получения целевых соединений данного изобретения.
Способ 1
Целевое соединение (I) или его соль можно получить по реакции взаимодействия соединения (II), или его реакционноспособного производного по карбокси-группе, или его соли с соединением (III), или с его реакционноспособным производным по амино-группе, или с его солью.
Подходящие реакционноспособные производные по карбокси-группе соединения (II) могут включать галогенгидрид, ангидрид кислоты, активированный амид, активированный эфир и т.п.
Подходящими примерами реакционноспособных производных могут служить хлор-ангидрид; азид кислоты; смешанный ангидрид с кислотой, такой как замещенная фосфорная кислота (например, диалкилфосфорная кислота, фенилфосфорная кислота, дифенилфосфорная кислота, дибензилфосфорная кислота, галогенированная фосфорная кислота и др.), диалкилфосфористая кислота, сернистая кислота, тиосерная кислота, серная кислота, сульфоновая кислота, (например, метансульфоновая кислота и др.), алифатическая карбоновая кислота (например, уксусная кислота, пропионовая кислота, масляная кислота, изомасляная кислота, триметилуксусная кислота, валериановая кислота, изовалериановая кислота, 2-этилмасляная кислота, трихлоруксусная кислота, и др.) или ароматическая карбоновая кислота (например, бензойная кислота и др.); ангидрид асимметрической кислоты; активированный амид с имидазолом, 4-замещенным имидазолом, диметилпиразолом, триазолом, тетразолом или 1-гидрокси-1Н-бензотриазолом; или активированный сложный эфир, (например, цианометиловый эфир, метоксиметиловый эфир, диметилиминометиловый эфир, метоксиметиловый эфир, диметилиминометиловый эфир /(CH3)2N+=CH-/, виниловый эфир, пропаргиловый эфир, р-нитрофениловый эфир, 2,4-динитрофениловый эфир, трихлорфениловый эфир, пентахлорфениловый эфир, мезилфениловый эфир, фенилазофениловый эфир, фениловый тиоэфир, р-нитрофениловый тиоэфир, р-крезиловый тиоэфир, карбоксиметиловый тиоэфир, пираниловый эфир, пиридиловый эфир, пиперидиловый эфир, 8-хинолиловый эфир и др.) или сложный эфир с N-гидрокси-соединением (например, N,N-диметилгидроксиламином, 1-гидрокси-2-(1Н)-пиридоном, N-гидроксисукцинимидом, N-гидроксифталимидом, 1-гидрокси-1Н-бензотриазолом и др.) и т.п. Эти реакционноспособные производные можно произвольно выбирать из вышеперечисленных, в соответствии с типом соединения (II).
Подходящими солями соединения (II) и его реакционноспособным производным можно считать те, примеры которых приведены для соединения (I).
Подходящие реакционноспособные производные по аминогруппе соединения (III) могут включать амин типа Шиффова основания или его изомер типа таутомерного енамина, получаемый по реакции соединения (III) с карбонильным соединением, таким как альдегид, кетон или т.п.; производное силила, получаемое по реакции соединения (III) с силильным соединением, таким как бис/триметилсилил/ацетамид, моно/триметилсилил/-ацетамид, бис/триметилсилил/мочевина и т.п.; производное, получаемое по реакции соединения (II) с трихлоридом фосфора или с фосгеном и т.п.
Подходящие соли соединения (III) и его реакционноспособные производные можно отнести к примерам соединения (I).
Реакцию обычно проводят в обычном растворителе, таком как вода, спирт (например, метанол, этанол и др.), ацетон, диоксан, ацетонитрил, хлороформ, метиленхлорид, этиленхлорид, тетрагидрофуран, этилацетат, N,N-диметилформамид, пиридин или любой другой органический растворитель, не влияющий неблагоприятно на протекание реакции. Эти традиционные растворители можно использовать также в смеси с водой.
В случае, когда соединение (II) используется в виде свободной кислоты или в виде ее соли, реакцию целесообразно проводить в присутствии традиционного конденсирующего агента, такого как N,N'-дициклогексилкарбодиимид; N-циклогексил-N'-морфолиноэтилкарбодиимид; N-циклогексил-N'-/4-диэтиламино-циклогексил/карбодиимид; N,N'-диэтилкарбодиимид, N,N'-диизопропилкарбодиимид; N-этил-N'-/3-диметиламинопропил/карбодиимид; N,N'-карбонил-бис-/2-метилимидазол/; пентаметиленкетон-N-циклогексилимин; дифенилкетон-N-циклогексилимин; этоксиацетилен; 1-алкокси-1-хлорэтилен, триалкилфосфит; этилполифосфат; изопропилполифосфат; оксихлорид трехвалентного фосфора (хлорид фосфорила); трихлорид фосфора; тионилхлорид; оксалилхлорид; галогенформиат низшего алкила (например, этилхлорформиат, изопропилхлорформиат и др.); трифенилфосфин; 2-этил-7-гидроксибензилоксазолиния соль; внутримолекулярная соль 2-этил-5-/м-сульфофенил/изоксазолиния гидроксида; 1-/р-хлорбензолсульфонилокси/-6-хлор-1Н-бензотриазол; так называемый реактив Вилсмейера, получаемый по реакции N,N-диметилформамида с тионилхлоридом, фосгеном, трихлорметилформиатом, оксихлоридом фосфора, метансульфонилхлоридом и др.; и т.п.
Реакцию можно также проводить в присутствии неорганического или органического основания, такого как карбонат щелочного металла, бикарбонат щелочного металла, три/низший/алкил-амин, пиридин, N-/низший/алкилморфолин, N,N-ди/низший/-алкилбензиламин и т.п.
Температура реакции не является критическим фактором, и обычно реакцию проводят в различных условиях - от "на холоду" до "при нагревании".
Способ 2
Целевое соединение (Ia) или его соль можно получить по реакции взаимодействия соединения (IV), или его реакционноспособного производного по карбокси-группе, или его соли с соединением (V), или с его реакционноспособным производным по амино-группе, или с его солью.
Эту реакцию можно проводить аналогично вышеупомянутому Способу 1, и, следовательно, тип и условия проведения реакции (например, реакционноспособные производные, растворитель, температура реакции и др.) соответствуют описанным в Способе 1.
Способ 3
Целевое соединение (Ic) или его соль можно получить, вводя соединение (Ib) или его соль в реакцию удаления амидинозащитной группы.
Эту реакцию проводят в соответствии с традиционными методами, такими как гидролиз, восстановление и т.п.
Гидролиз обычно проводят в присутствии основания или кислоты, включая Льюисову кислоту. Подходящие основания могут включать неорганические основания и органические основания, такое как щелочной металл (например, натрий, калий и др.), щелочноземельный металл (например, магний, кальций и др.), их гидроксид, или карбонат, или бикарбонат, триалкиламин (например, триметиламин, триэтиламин и др.), пиколин, 1,5-диазабицикло/4.3.0/нон-5-ен, 1,4-диазабицикло/2.2.2/октан, 1,8-диазабицикло/5.4.0/ундек-7-ен и т.п.
Подходящие кислоты могут включать органическую кислоту (например, муравьиную кислоту, уксусную кислоту, пропионовую кислоту, трихлоруксусную кислоту, трифторуксусную кислоту и др.) и минеральную кислоту (например, хлористоводородную кислоту, бромистоводородную кислоту, серную кислоту, хлористый водород, бромистый водород и др.).
Реакцию удаления с использованием Льюсовой кислоты, такой как тригалогенуксусная кислота (например, трихлоруксусная кислота, трифторуксусная кислота и др. ), предпочтительно проводят в присутствии катионных связывающих агентов (например, анизол, фенол и др.).
Реакцию обычно проводят в растворителе, таком как вода, спирт (например, метанол, этанол и др. ), хлористый метилен, тетрагидрофуран, их смесь или любой другой растворитель, не влияющий неблагоприятно на протекание реакции. В качестве растворителя можно также использовать жидкое основание или кислоту. Температура реакции не является критическим фактором, и реакцию обычно проводят в условиях от "на холоду" до "при нагревании".
Метод восстановления, применимый для проведения реакции удаления, может включать химическое восстановление или каталитическое восстановление.
Подходящими для использования в данной реакции восстановителями является сочетание металла (например, олова, цинка, железа и др.) или соединение металла (например, хлорид хрома, ацетат хрома и др.) и органической или минеральной кислоты (например, муравьиная кислота, уксусная кислота, пропионовая кислота, трифторуксусная кислота, р-толуолсульфоновая кислота, хлористоводородная кислота, бромистоводородная кислота и др.).
Катализаторы, подходящие для использования при каталитическом восстановлении, представляют собой традиционные катализаторы, такие как платиновые (например, платиновая пластина, платиновая губка, платиновая чернь, коллоидная платина, оксид платины, платиновая проволока и др.), палладиевые катализаторы (например, палладиевая губка, палладиевая чернь, оксид палладия, палладий-на-угле, коллоидный палладий, палладий-на-сульфате бария, палладий-на-карбонате бария и др.), никелевые катализаторы (например, восстановленный никель, оксид никеля, никель Ренея и др.), кобальтовые катализаторы (например, восстановленный кобальт, кобальт Ренея и др.), железные катализаторы (например, восстановленное железо, железо Рэнея и др.), медные катализаторы (например, восстановленная медь, медь Рэнея, медь Ульмана и др.) и т.п.
Восстановление обычно проводят в среде традиционного растворителя, который не влияет неблагоприятно на протекание реакции, такого как вода, метанол, этанол, пропанол, N,N-диметилформамид или их смесь. Кроме того, в случае, когда вышеупомянутые кислоты, используемые для химического восстановления, представляют собой жидкости, их также можно использовать как растворители. Далее, подходящим для каталитического восстановления растворителем может быть вышеупомянутый растворитель, а также другие традиционные растворители, такие как диэтиловый эфир, диоксан, тетрагидрофуран и др. или их смеси.
Температура реакции подобного восстановления не является критическим параметром, и реакцию обычно проводят в условиях от "на холоду" до "при нагревании".
В объем данного изобретения входит случай, когда защищенный карбокси/низший/алкил в R2 трансформируется в карбокси/низший/алкил, случай, когда защищенная карбокси-группа в R3 превращается в карбокси-группу, а также случай, когда низший алкилен, содержащий защищенный гидрокси/низший/алкил, или низший алкилен, содержащий /защищенная гидрокси/-арил-/низший/алкил в A3 преобразуется в низший алкилен, содержащий гидрокси/низший/алкил, или в низший алкилен, содержащий /гидрокси/-арил/низший/алкил.
Способ 4
Целевое соединение (Ie) или его соль можно получить, подвергая соединение (Id) или его соль реакции удаления карбокси-защитной группы.
Эту реакцию можно проводить аналогично реакции Способа 3, рассмотренного выше, так что режим и условия проведения реакции (например, основание, кислота, катализатор, растворитель, температура реакции и др.) соответствуют указанным в Способе 3.
Данное изобретение включает случай, когда арил, содержащий защищенную амидино-группу в R1, превращается в арил, содержащий амидино-группу, случай, когда защищенная карбокси-защищенная группа в R3 превращается в карбокси-группу, а также случай, когда низший алкилен, содержащий защищенный гидрокси/низший/алкил, или низший алкилен, содержащий /защищенная гидрокси/-арил/низший/алкил в A3, превращается в низший алкилен, содержащий гидрокси/низший/алкил, или низший алкилен, содержащий /гидрокси/-арил/низший/алкил.
Способ 5
Целевое соединение (Ig) или его соль можно получить, подвергая соединение (If) или его соль реакции удаления гидрокси-защитной группы.
Эту реакцию можно проводить аналогично реакции вышеупомянутого Способа 3, так что режим и условия проведения реакции (например, основание, кислота, катализатор, растворитель, температура реакции и др.) соответствуют рассмотренным в Способе 3.
Данное изобретение включает случай, когда арил, имеющий защищенную амидино-группу в R1, превращается в арил, имеющий амидино-группу, случай, когда защищенный карбокси/низший/алкил в R2, преобразуется в карбокси/низший/алкил, и случай, когда защищенная карбокси-группа в R3 преобразуется в карбокси-группу.
Способ 6
Целевое соединение (Ii) или его соль можно получить, подвергая соединение (Ih) или его соль реакции удаления карбокси-защитной группы.
Эту реакцию можно проводить аналогично реакции, вышеупомянутого Способа 3, и, следовательно, режим и условия проведения реакции (например, основание, кислота, катализатор, растворитель, температура реакции и др.) соответствуют рассмотренным при описании Способа 3.
В объем данного изобретения входит случай, когда арил, имеющий защищенную амидино-группу в R1, превращается в арил, содержащий амидино-группу, случай, когда защищенный карбокси/низший/алкил в R2 превращается в карбокси/низший/алкил, и случай, когда низший алкилен, содержащий защищенный гидрокси/низший/алкил, или низший алкилен, содержащий /защищенная гидрокси/-арил/низший/алкил в A3, превращается в низший алкилен, имеющий гидрокси/низший/алкил, или в низший алкилен, имеющий /гидрокси/-арил/низший/алкил.
Способ 7
Целевое соединение (Ij) или его соль можно получить по реакции превращения группы тиокарбамоила соединения (VI) или его соли в амидино-группу.
Подходящие соли соединений (Ij) и (VI) можно рассматривать как примеры, приведенные при описании соединения (I).
Эту реакцию можно проводить как реакцию взаимодействия соединения (VI) или его соли с алкилирующим агентом, таким как алкилгалогенид (например, метилиодид, этилбромид и др. ) и т.п., в подходящем растворителе, таком как ацетон диоксан, тетрагидрофуран и т.п., при комнатной температуре, в тепле или при нагревании, а затем как взаимодействие полученного промежуточного продукта, с выделением или без, с аммиаком или его производным, таким как ацетат аммония, галогенид аммония (например, хлорид аммония и др.), в подходящем растворителе, таком как спирт (например, метанол, этанол и др.), N, N-диметилформамид и т.п., в тепле или при нагревании.
В тех случаях, когда соединение (I), получаемое по вышеупомянутым способам, находится в свободном виде, его можно превратить в соль традиционными методами. С другой стороны, когда получаемое таким образом целевое соединение (I) представляет собой соль, его можно перевести в свободное состояние или в другую солевую форму также известными методами.
Следует отметить, что целевое соединение (I) может включать стереоизомеры вследствие присутствия асимметричного атома (атомов) углерода.
Далее, с целью продемонстрировать полезность целевого соединения (I), будут приведены некоторые данные фармакологических испытаний представителей соединения (I) по данному изобретению.
Тест 1: Эффект на склеивание тромбоцитов, вызываемое аленозин дифосфатом (АДР) Испытуемое соединение: (I) целевое соединение (7) Примера 7
Методика теста
Из крови человека приготовили богатую тромбоцитами плазму (PRP), в которой содержится 3 • 108 тромбоцитов/мл. К 225 мкл PRP добавили 25 мкл раствора лекарства, а затем перемешивали в течение 2 мин при 37oC. К раствору добавили 5 мкл АДР (окончательно 2,5 мкМ) в качестве инициатора агглютинации. Степень агглютинации определяли с помощью прибора для измерения агглютинации (NKK HEMA-TPACEP I). Активность ингибитора (испытуемое соединение) выражалась в виде величины IC50, т.е. дозы, требуемой для подавления склеивания тромбоцитов на 50%.
Раствор лекарства х - испытуемое соединение растворяли в диметилсульфоксиде.
Результаты теста
Испытуемое соединение IC50 /М/
(I) 1,0•10-7
Тест 2: Связывание фибриногена с тромбоцитами
Испытуемое соединение
то же соединение (I), что и в Тесте 1
Методика проведения теста
Промытые тромбоциты человека получили из обогащенной тромбоцитами плазмы путем гель-фильтрации. Промытые тромбоциты активировали действием 20 мкМ АДР в течение 10 мин, а затем фиксировали в течение 30 мин 0,8% параформальдегидом. Затем тромбоциты отмыли центрифугированием и приготовили суспензию в буфере HEPES-Tyrodes, содержащем 2 мМ CaCl2 и 1 мМ MgCl2.
350 мкл Тромбоцитов термостатировали при конечной концентрации 2 • 108/мл с 100 мкг/мл 1251-фиброногена и испытываемого соединения. Реакция продолжалась в течение 30 мин при комнатной температуре. Затем на 20% сахарозу нанесли слой из трех порций по 100 мкл и получили лепешку тромбоцитов в результате центрифугирования при 10 000 об/мин в течение 5 мин. Лепешку отделили, отрезав кончик пробирки с помощью лезвия и сосчитали на счетчике гамма-излучения.
Удельное связывание вычисляли, вычитая связывание в присутствии 50-кратного избытка немеченного фибриногена. Результаты выражались в виде величины IC50, т.е. в виде дозы, необходимой для подавления связывания на 50%.
Результаты теста
Испытуемое соединение IC50
(I) 2.9 • 10-8
Тест 3: Тест на повышение тромболитической активности ТРА при моделировании тромбоза у морских свинок
Испытуемое соединение
(I) целевое соединение (13) Примера 13
Методика проведения испытаний
Самцам морских свинок Хартли (500-800 г) сделали анестезию уретаном (1,25 г/кг внутрибрюшинно). Сонную артерию и шейную вену тщательно исследовали после того, как посередине шеи был сделан разрез. В вену ввели канюлю полиэтиленового катетера (РЕ50; Becton Dikinson, США) для впрыскивания и вливания лекарства. Вокруг сонной артерии поместили pulse Dopplar flow probe для регистрации скорости тока крови с целью наблюдения образования тромбов и тромболиза. Тромбоз сонной артерии вызывали методом FeCl3 по следующей методике:
квадратную (1 мм х 1 мм) фильтровальную бумагу типа ADVANTEC N 2, пропитанную 20% FeCl3, поместили на сонную артерию, которая закупоривается тромбом.
Когда скорость тока крови упала до нуля, фильтровальную бумагу убрали с сосуда, и промыли сонную артерию больше 4 раз физиологическим раствором. Через 3 мин после промывания ввели испытуемое соединение или физиологический раствор, и через 3 мин г-ТРА (торговая марка Actilyse, Bochringer Ingelheim Ltd.) вливали в течение 60 мин.
Животных разделили на следующие группы.
Группа 1 (5 животных): Физиологический раствор и т-ТРА при 0,30 мг/кг шарик внутривенно + 1,0 мг/кг/ч внутривенное вливание.
Группа 2 (5 животных): Испытуемое соединение при 0,32 мг/кг внутривенно шарик и т-ТРА при 0,30 мг/кг внутривенно шарик + 1,0 мг/кг/час внутривенное вливание.
Ре-перфузию определяли как 50% восстановление скорости тока крови в сонной артерии по сравнению с первоначальным значением. Ток крови восстанавливался за 90 мин.
Результаты теста
Количество животных, у которых наблюдалась реперфузия, в каждой группе оказалось следующим.
Группа - Число животных, у которых наблюдалась реперфузия
1 - 1
2 - 5
Фармацевтическую композицию по данному изобретению можно использовать в виде фармацевтического препарата, например, в виде твердой, полутвердой или жидкой готовой формы, которая содержит целевое соединение (I) или его фармацевтически приемлемую соль в качестве активного ингредиента, смешанного с органическим или неорганическим носителем или эксципиентом, подходящим для введения или вдувания ректально, в легкие (носовые или буккальные ингаляции), в нос, в глаза, наружно (местно), перорально или парентерально (включая подкожно, внутривенно и внутримышечно).
Активный ингредиент может быть смешан, например, с обычными нетоксичными, фармацевтически приемлемыми носителями для таблеток, пилюль, пастилок, капсул, суппозиториев, кремов, мазей, аэрозолей, порошков для вдувания, растворов, эмульсий, суспензий, а также для любой другой пригодной для использования готовой формы. И, при необходимости, могут быть использованы, кроме того, стабилизирующие, вспомогательные добавки, загустители и красители, а также одушки.
Целевое соединение (I) или его фармацевтически приемлемая соль входит/входят в фармацевтическую композицию в количестве, достаточном для создания желательного эффекта на развитие или состояние заболевания.
Фармацевтическую композицию по данному изобретению можно изготовить традиционными для данной области способами. При необходимости к фармацевтической композиции по данному изобретению можно применить методику, обычно используемую для повышения биологической доступности лекарства.
Для введения композиции человеческому существу или животному предпочтительно использовать внутривенный путь (включая внутривенное вливание), внутримышечное, легочное или пероральное введение или вдувание, включая аэрозоли, с помощью ингалятора, дающего отмеренные дозы, распылителя или ингалятора сухого порошка.
Хотя дозировка терапевтически эффективного количества целевого соединения (I) меняется и зависит от возраста и состояния каждого отдельного пациента, для профилактики и/или лечения вышеуказанных заболеваний человека и животных дается, как правило, в случае внутривенного введения: дневная доза 0,001-100 мг целевого соединения (I) на кг веса тела человека или животного, в случае введения внутримышечно, дневная доза 0,001-100 мг целевого соединения (I) на кг веса тела человека или животного, в случае введения внутримышечно, дневная доза 0,001-100 мг целевого соединения (I) на кг веса тела человека или животного, в случае введения перорально, дневная доза 0,001-200 мг целевого соединения (I) на кг веса тела человека или животного.
Примеры фармацевтических композиций.
Сухие капсулы, содержащие 100 мг соединений примера 7.
Ингредиент - Количество мг на капсулу.
Соединение примера 7 - 100
Лактоза - 45,8
Стеарат магния - 4,2
- 150
Ингредиенты измельчают в порошок до заданного размера частиц, перемешивают около 10 минут и помещают в сухие желатиновые капсулы.
Таблетки
Ингредиент - Количество мг на таблетку
Соединение примера 13 - 100
Прожелатинизированный кукурузный крахмал - 72
Микрокристаллическая целлюлоза - 77
Стеарат магния - 1
- 250
Соединение тонко измельчают и смешивают с измельченными инертными ингредиентами согласно рецептуре, а затем прессуют в таблетки по стандартной методике на установке для прессования таблеток.
Метод получения 1.
Смесь 4-цианофенола (5,95 г), этил-5-бромвалерата (11,5 г), карбоната калия (7,6 г) в N,N-диметилформамиде (60 мл) перемешивали при комнатной температуре в течение 14 ч.
Реакционную смесь вылили в воду и экстрагировали полученную смесь этилацетатом. Экстракт промыли насыщенным водным раствором бикарбоната натрия, водой и водным раствором хлорида натрия, после чего высушили над сульфатом магния. После фильтрации высушили под вакуумом фильтрат, а полученный осадок промыли диэтиловым эфиром, получив этил-5-(4-цианофенокси)валерат (11,21 г.)
т.пл.: 55-57oC
ИК (нуджол): 2200, 1725, 1600, 15 см-1
ЯМР (ДМСО-d6, δ): 1,18 (3Н, триплет, J=7 Гц), 1,4-1,88 (4Н, мультиплет, 2,37 (2Н, триплет, J=7 Гц), 3,8-4,13 (4Н, мультиплет), 7,1 (2Н, дублет, J= 8,9 Гц), 7,76 (2Н, дублет, J=8,9 Гц)
МС (M/Z)): 247 (М+)
Следующие соединения (Методы получения 2 и 3) были получены аналогично Методу получения 1.
Метод получения 2
Этил-4-(4-цианофенокси)бутират
т.пл.: 56-57oC
ИК (нуджол): 2220, 1735, 1610, 1510 см-1
ЯМР (ДМСО-d6, δ): 1,18 (3Н, триплет, J=4,7 Гц), 2,00 (2Н, мультиплет), 2,47 (2Н, триплет, J=4,8 Гц), 4,07 (4Н, мультиплет), 7,09 (2Н, дублет, J=4,6 Гц), 7,76 (2Н, дублет, J=4,6 Гц)
МС (M/Z): 233 (М+)
Метод получения 3
Этил-6-(4-цианофенокси)гексаноат
т.пл.: 45-46oC
ИК нуджол): 2220, 1720, 1590, 1565 см-1
ЯМР (ДМСО-d6, δ): 1,18 (3Н, триплет, J=7,1 Гц), 1,3-1,83 (6Н, мультиплет), 2,31 (2Н, триплет, J= 7,1 Гц), 3,9-4,2 (4Н, мультиплет), 7,09 (2Н, дублет, J=8,9 Гц), 7,75 (2Н, дублет, J=8,9 Гц)
МС (M/Z): 261 (М+)
Метод получения 4
Через раствор этил-5-(4-цианофенокси)валерата (2,47 г) в этаноле (250 мл) барботировали хлористый водород при охлаждении ледяной водой в течение 4 ч. После того, как окончание реакции было определено с помощью тонкослойной хроматографии, при комнатной температуре барботировали азот, выпарили полученную смесь в вакууме и промыли полученный осадок диэтиловым эфиром, что дало этил-5-/4-(1-(этокси)иминометил)фенокси/валерата гидрохлорид (28,26 г).
т.пл.: 110oC (разл.)
ИК (нуджол): 1720, 1635, 1600 см-1
ЯМР (ДМСО-d6, δ): 1,18 (3Н, триплет, J=7,1 Гц), 1,47 (3Н, триплет, J=7 Гц), 1,5-1,9 (4Н, мультиплет), 2,38 (2Н, триплет, J=7 Гц), 4,05 (2Н, квартет, J= 7,1 Гц), 4,12 (2Н, триплет, J=5,8 Гц), 4,61 (2Н, квартет, J=7 Гц), 7,16 (2Н, дублет, J=9 Гц), 8,14 (2Н, дублет, J=9 Гц), 11,54 (1Н, широкий синглет)
МС (M/Z): 293 (М+ свободный)
Следующие соединения (методы получения 5 и 6) получены аналогично Методу получения 4.
Метод получения 5
Этил-4-/4-(1-(этокси)иминометил)фенокси/бутирата гидрохлорид.
т.пл. 102-104oC
ИК (нуджол): 3420, 1735, 1610 см-1
ЯМР (ДМСО-d6, δ): 1,18 (3Н, триплет, J=4,7 Гц), 1,47 (3Н, триплет, J=4,6 Гц), 2,01 (2Н, мультиплет), 2,48 (2Н, триплет, J=4,8 Гц), 4,09 (4Н, мультиплет), 4,60 (2Н, J=4,6 Гц), 7,16 (2Н, дублет, J=4,6 Гц), 8,15 (2Н, дублет, J= 4,6 Гц)
Метод получения 6
Этил-6-/4-(1-(этокси)иминометил)фенокси)гексаноата гидрохлорид
т.пл.: 107oC (разл.)
ИК (нуджол): 1720, 1600, 1580, 1510 см-1
ЯМР (ДМСО-d6, δ): 1,17 (3Н, триплет, J=7 Гц), 1,3-1,84 (6Н, мультиплет), 1,47 (3Н, триплет, J= 7 Гц), 2,31 (2Н, триплет, J=7,1 Гц), 3,92-4,2 (4Н, мультиплет), 4,61 (2Н, квартет, J=7 Гц), 7,16 (2Н, дублет, J=9 Гц), 8,14 (2Н, дублет, J=9 Гц), 11,54 (1Н, широкий синглет)
МС( M/Z): 307 (М+ свободный)
Метод получения 7
Смесь этил-5-/4-(1-(этокси)иминометил)фенокси/валерата гидрохлорида (28,2 г), хлорида аммония (4,8 г), этанольного раствора аммиака (42 мл) в этаноле (300 мл) перемешивали и нагревали с обратным холодильником в течение 15 ч. После охлаждения до комнатной температуры смесь отфильтровали, фильтрат выпарили в вакууме и полученный осадок промыли диэтиловым эфиром, получив в результате этил-5-(4-амидинофенокси)валерата гидрохлорид (27,28 г).
т.пл.: 150-155oC (разлаг.)
ИК (нуджол): 3350, 1710, 1660, 1490 см-1
ЯМР (ДМСО-d6, δ): 1,18 (3Н, триплет, J=7,1 Гц), 1,5-1,85 (4Н, мультиплет), 2,38 (2Н, триплет, J=7,1 Гц), 4,05 (2Н, квартет, J=7,1 Гц), 4,1 (2Н, триплет, J= 5,8 Гц), 7,15 (2Н, дублет, J=8,9 Гц), 7,85 (2Н, дублет, J=8,9 Гц), 8,65 (4Н, уширено)
МС (M/Z): 264 (М+ - свободный)
Следующие соединения (Методы получения 8 и 9) получены аналогично Методу получения 7.
Метод получения 8
Этил-4-(4-амидинофенокси)бутирата гидрохлорид
т.пл.: 81-84oC (разлаг.)
ИК (нуджол): 3420, 3250, 3100, 1720, 1670, 1600 см-1
ЯМР (ДМСО-d6, δ): 1,18 (3Н, триплет, J=7,1 Гц), 1,9-2,1 (2Н, мультиплет), 2,47 (2Н, триплет, J=7,3 Гц), 3,95-4,23 (4Н, мультиплет), 7,14 (2Н, дублет, J=8,9 Гц), 7,88 (2Н, дублет, J=8,9 Гц), 8,93 (4Н, широкий синглет)
МС (M/Z): 250 (М+ свободный)
Метод получения 9
Этил-6-(4-амидинофенокси)гексаноата гидрохлорид
т.пл.: ≈ 135oC (разлаг.)
ИК (нуджол): 3420, 3260, 3100, 1720, 1660, 1600 см-1
ЯМР (ДМСО-d6, δ): 1,17 (3Н, триплет, J=7,1 Гц), 1,31-1,85 (6Н, мультиплет), 2,32 (2Н, триплет, J=7,1 Гц), 3,95-4,2 (4Н, мультиплет), 7,14 (2Н, дублет, J=8,9 Гц), 7,89 (2Н, дублет, J=8,9 Гц), 8,69 (4Н, уширенный)
МС (M/Z-; 278 (М+ свободный)
Метод получения 10
К смеси этил-5-(4-амидинофенокси)валерата гидрохлорида (14,6 г) в смеси тетрагидрофурана (150 мл) и 1 н. раствора гидроксида натрия добавили бензилоксикарбонилхлорид (10,4 мл) при охлаждении ледяной водой в течение 1 ч. Смесь перемешивали в течение 2 ч при 10oC, поддерживая pH = 10 с помощью 1 н. раствора гидроксида натрия. Реакционную смесь вылили в этилацетат (300 мл), и отделенный органический слой промыли водным раствором хлорида натрия и высушили над сульфатом магния. Полученный после фильтрации фильтрат выпарили в вакууме и промыли полученный осадок диэтиловым эфиром, получив этил-5-/4-(N-бензилоксикарбониламидино)фенокси/валерат (17,48 г).
т.пл.: 88-90oC
ИК (нуджол): 3420, 3280, 1715, 1660, 1590, 1560 см-1
ЯМР (ДМСО-d6, δ): 1,17 (3Н, триплет, J=7,1 Гц), 1,55-1,85 (4Н, мультиплет), 2,37 (2Н, триплет, J= 7 Гц), 4,04 (2Н, квартет, J=7 Гц), 4,05 (2Н, триплет, J=5,8 Гц), 5,1 (2Н, синглет), 7,0 (2Н, дублет, J=8,9 Гц), 7,24-7,46 (5Н, мультиплет), 7,98 (2Н, дублет, J=8,9 Гц), 9,11 (2Н, широкий синглет)
МС (M/Z): 398 (М+)
Следующие соединения (методы получения 11 и 12) были получены аналогично Методу получения 10.
Метод получения 11
Этил-4-/4-(N-бензилоксикарбониламидино)фенокси/бутират
т.пл.: 110-112oC
ИК (нуджол): 3430, 3290, 1720, 1655, 1595, 1565 см-1
ЯМР (ДМСО-d6, δ): 1,18 (3Н, триплет, J=7,1 Гц), 1,84-2,1 (2Н, мультиплет), 2,46 (2Н, триплет, J=7,1 Гц), 3,9-4,19 (4Н, мультиплет), 5,12 (2Н, синглет), 7,01 (2Н, дублет, J=8,9 Гц), 7,23-7,5 (5Н, мультиплет), 7,97 (2Н, дублет, J=8,9 Гц), 9,31 (2Н, широкий синглет)
МС (M/Z): 384 (М+)
метод получения 12
Этил-6-/4-(N-бензилоксикарбониламидино)фенокси/гексаноат
т.пл.: 96-99oC
ИК (нуджол): 3430, 3300, 1725, 1660, 1600, 1570, 1490 см-1
ЯМР (ДМСО-d6, δ): 1,17 (3Н, триплет, J=7,1 Гц), 1,3-1,84 (6Н, мультиплет), 2,31 (2Н, триплет, J=7,1 Гц), 3,92-4,16 (4Н, мультиплет), 5,1 (2Н, синглет), 7,0 (2Н, дублет, J=8,9 Гц), 7,25-7,5 (5Н, мультиплет), 7,99 (2Н, дублет, J=8,9 Гц), 9,12 (2Н, широкий синглет)
МС (M/Z): 412 (М+)
Метод получения 13
Смесь этил-5-/4-(N-бензилкарбониламидино)фенокси/-валерата (17,4 г) в 10% хлористоводородной кислоте (150 мл) и уксусной кислоте (100 мл) перемешивали при 50oC в течение 1,5 ч. После охлаждения до комнатной температуры реакционную смесь довели до pH 4,0 с помощью 4 н. раствора гидроксида натрия. Собрали образовавшийся осадок и получили 5-/4-(N-бензилоксикарбониламидино)-фенокси/валериановую кислоту (14,87 г).
т.пл.: ≈ 103oC (разлаг.)
ИК (нуджол): 3300, 1735, 1640, 1600, 1560, 1510 см-1
ЯМР (ДМСО-d6, δ): 1,53-1,85 (4Н, мультиплет), 2,29 (2Н, триплет, J=7,2 Гц), 4,06 (2Н, триплет, J=5,8 Гц), 5,16 (2Н, синглет), 7,04 (2Н, дублет, J= 8,9 Гц), 7,3-7,5 (5Н, мультиплет), 7,95 (2Н, дублет, J=8,9 Гц), 9,54 (1Н, уширенный), 12,07 (1Н, уширенный)
МС (M/Z): 370 (М+)
Следующие соединения (Методы получения 14 и 15) были получены аналогично методике Метода получения 13.
Метод получения 14
4-/4-(N-Бензилоксикарбониламидино)фенокси/масляная кислота
т.пл.: ≈ 143oC (разлаг.)
ИК (нуджол): 1730, 1600, 1560 см-1
ЯМР (ДМСО-d6, δ): 1,3-1,8 (6Н, мультиплет), 2,24 (2Н, триплет, J=7 Гц), 4,03 (2Н, триплет, J= 6,4 Гц), 5,11 (2Н, синглет), 7,0 (2Н, дублет, J=8,9 Гц), 7,2-7,55 (5Н, мультиплет), 7,98 (2Н, дублет, J=8,9 Гц), 9,22 (1Н, уширенный), 12,02 (1Н, уширенный)
Формулы исходных соединений, а также целевых соединений, представленных в нижеследующих Примерах, приведены в табл.1
В приведенных в табл.1 формулах Am(Z) обозначает N-бензилоксикарбониламидино, Am означает амидино, Asp означает Z-аспарагиновую кислоту, VaI означает Z-валин, Sar означает саркаозин, Leu означает L-лейцин, BZI означает бензил и tBu означает трет-бутил.
Пример 1
К смеси 5-/4-(N-бензилоксикарбониламидино)фенокси/валериановой кислоты (0,5 г), исходного соединения (I) (0,61 г) и 1-гидрокси-1Н-бензотриазола (0,21 г) в N,N-диметилформамиде (5 мл) добавили 1-(3-диметиламинопропил)-3-этилкарбодиимид (0,25 мл) и перемешивали смесь при комнатной температуре в течение 2 ч.
Реакционную смесь вылили в смесь воды (50 мл) и этилацетата (30 мл) и довели pH до 9,5 действием 4 н. раствора гидроксида натрия. Отделенный органический слой промыли насыщенным раствором гидрокарбоната натрия, водой и водным раствором хлорида натрия и высушили над сульфатом магния. Фильтрат, полученный после фильтрации, выпарили в вакууме, что дало целевое соединение (I) (1.08 г) в виде масла.
ЯМР (ДМСО-d6, δ): 0,83 (6Н, дублет, J=6,7 Гц), 1,53-1,8 (4Н, мультиплет), 2,16 (2Н, мультиплет), 2,5-2,85 (2Н, мультиплет), 4,01 (2Н, типа триплета), 4,15-4,28 (1Н, мультиплет), 5,0-5,23 (7Н, мультиплет), 6,99 (2Н, дублет, J= 8,9 Гц), 7,2-7,5 (15Н, мультиплет), 7,98 (2Н, дублет, J=8,9 Гц), 8,15 (1H, дублет, J=8,2 Гц), 8,25 (1Н, дублет, J=8,1 Гц), 9,1 (1Н, уширенный)
Пример 2
Целевое соединение (2) получили из исходного соединения (2А) и исходного соединения (28) по методике, аналогичной описанной в Примере 1.
ЯМР (ДМСО-d6, δ): 0,84 (6Н, дублет, J=6,7 Гц), 1,8-2,2 (3Н, мультиплет), 2,25 (2Н, типа триплета), 2,5-2,9 (2Н, мультиплет), 4,01 (2Н, типа триплета), 4,20 (1Н, мультиплет), 4,76 (1Н, мультиплет), 5,0-5,2 (1Н, мультиплет), 5,07 (2Н, синглет), 5,10 (2Н, синглет), 5,11 (2Н, синглет), 6,99 (2Н, дублет, J=8,9 Гц), 7,24-7,53 (15Н, мультиплет), 7,98 (2Н, дублет, J=9 Гц), 8,16 (1Н, дублет, J=8 Гц), 8,30 (1Н, дублет, J=7,9) 9,11 (1Н, уширенный)
Пример 3
Целевое соединение (3) получили из исходного соединения (3А) и исходного соединения (3В) в соответствии с методикой, аналогичной описанной в Примере 1.
ИК (нуджол): 3300, 1730, 1650, 1600 см-1
ЯМР (ДМСО-d6, δ): 0,83 (6Н, дублет, J=6,7 Гц), 1,3-1,8 (6Н, мультиплет), 1,9-2,2 (3Н, мультиплет), 2,5-2,9 (2Н, мультиплет), 4,01 (2Н, типа триплета), 4,13-4,25 (1Н, мультиплет), 4,66-4,83 (1Н, мультиплет), 5,0-5,15 (2Н, мультиплет), 6,98 (2Н, дублет, J=8,9 Гц), 7,2-7,52 (15Н, мультиплет), 7,98 (2Н, дублет, J=8,9 Гц), 8,05-8,3 (2Н, мультиплет), 9,1 (1Н, уширенный)
Пример 4
Целевое соединение (4) было получено из исходного соединения (4А) и исходного соединения (4В) по методике, аналогичной методике Примера 1.
т.пл.: 45-50oC
ИК (нуджол): 3200 (br), 1640, 1600 см-1
ЯМР (ДМСО-d6, δ): 1,84 (6Н, дублет, J=6,7 Гц), 2,05 (1Н, мультиплет), 2,6-2,9 (4N, мультиплет), 2,78 и 2,97 (3Н, каждый синглет), 3,96 и 4,03 (2Н, каждый - синглет), 4,18 (1Н, мультиплет), 4,84 (1Н, широкий синглет), 5,0-5,1 (8Н, мультиплет), 6,99 (2Н, дублет, J=8,9 Гц), 7,2-7,5 (15Н, мультиплет), 7,96 (2Н, дублет, J=9,8 Гц), 8,13 и 8,60 (1Н, каждый - дублет, J=8,0 Гц, 7,9 Гц), 8,34 (1Н, мультиплет), 9,11 (2Н, широкий синглет)
Пример 5
Смесь исходного соединения (5) (1 г) и 10% Pd-C (0,6 г) в смеси 1 н. хлористоводородной кислоты (5 мл) и тетрагидрофурана (10 мл) перемешивали в атмосфере газообразного H2 при комнатной температуре в течение 6 ч.
Полученный после фильтрования фильтрат выпарили в вакууме. Полученное вещество подвергли препаративной ВЭЖХ и получили целевое соединение (5) (0,374 г).
Условия проведения ВЭЖХ
колонка : УМС-РАСК R-ODS-15S-15 S-15 120A ODS 50 ϕ х 250 мм
элюирование : CH3CN: 0,1% водный раствор трифторуксусной кислоты = 1:4
поток : 118 мл/мин
время удерживания : 8 мин
т.пл.: ≈ 147oC
ИК (нуджол): 3300, 3080, 1660, 1600, 1530 см-1
ЯМР (ДМСО-d6, δ): 0,84 (6Н, дублет, J=6,7 Гц), 1,54-1,84 (4Н, мультиплет), 2,03 (1Н, мультиплет), 2,19 (2Н, типа триплета), 2,36-2,78 (2Н, мультиплет), 3,97-4,2 (3Н, мультиплет), 4,65 (1Н, мультиплет), 7,15 (2Н, дублет, J= 8,9 Гц), 7,76 (1Н, дублет, J=7,8 Гц), 7,81 (2Н, дублет, J=8,9 Гц), 8,25 (1Н, дублет, J=7,8 Гц), 9,05 (2Н, синглет), 9,14 (2Н, синглет)
МС (M/Z) : 451 (М + 1 свободный)
Пример 6
Целевое соединение (6) было получено из исходного соединения (6) по методике, аналогичной Примеру 5.
Условия проведения ВЭЖХ
колонка : УМС-РАСК R-ODS-15 S-15 120A ODS 50 ϕ х 250 мм
элюирование : CH3CN : 0,1% водный раствор трифторуксусной кислоты = 17: 83
поток : 118 мл/мин
время удерживания : 7,355 мин
т.пл.: ≈ 195oC (разлаг.)
ИК (нуджол): 3320, 3100, 1655, 1610, 1540, 1490 см-1
ЯМР (ДМСО-d6, δ): 0,84 (6Н, дублет, J=6,7 Гц), 1,8-2,16 (3Н, мультиплет), 2,3 (2Н, триплет, J=7,3 Гц), 2,3-2,8 (2Н, мультиплет), 3,98-4,2 (3Н, мультиплет), 4,65 (1Н, мультиплет), 7,14 (2Н, дублет, J=8,9 Гц), 7,79 (1Н, дублет, J=8,5 Гц), 7,82 (2Н, дублет, J=8,9 Гц), 8,30 (1Н, дублет, J=7,7 Гц), 9,03 (2Н, синглет), 9,14 (2Н, синглет)
Пример 7
Целевое соединение (7) было получено из исходного соединения (7) по методике, аналогичной Примеру 5.
Условия проведения ВЭЖХ
колонка: УМС-РАСК R-ODS-15 S-15 120A ODS : 50 ϕ х 250 мм
элюирование : CH3CN: 0,1% водный раствор трифторуксусной кислоты = 1,1: 4,4
поток: 118 мл/мин
время удерживания : 9,784 мин
т.пл.: ≈ 190oC (разлаг.)
ИК (нуджол): 3320, 3100, 1670, 1610, 1540, 1490 см-1
ЯМР (ДМСО-d6, δ): 0,84 (6Н, дублет, J=5,7 Гц), 1,3-1,85 (6Н, мультиплет), 1,93-2,25 (3Н, мультиплет), 2,36-2,79 (2Н, мультиплет), 3,97-4,21 (3Н, мультиплет), 4,5-4,76 (1Н, мультиплет), 7,14 (2Н, дублет, J=8,9 Гц), 7,72 (1Н, дублет, J=8,6 Гц), 7,81 (2Н, дублет, J=8,9 Гц), 8,23 (1Н, дублет, J=7,8 Гц), 9,0 (2Н, синглет), 9,14 (2Н, синглет)
МС (M/Z): 465 (М+1 свободный)
Пример 8
Целевое соединение (8) получили из исходного соединения (8) по методике, аналогичной Примеру 5.
Условия проведения ВЭЖХ
элюирование : CH3CH : 0,1% водный раствор трифторуксусной кислоты = 15: 85
время удерживания : 8,0 минут
(колонка и поток такие же, как и в Примере 5)
т.пл.: 62-68oC
ИК (нуджол): 3200 (br), 1640 см-1
ЯМР (ДМСО-d6, δ) : 0,86 (6Н, дублет, J=6,8 Гц), 2,04 (1Н, мультиплет), 2,4-2,8 (2Н, мультиплет), 2,80 и 3,00 (3Н, каждый синглет), 3,8-4,2 (3Н, мультиплет), 4,68 (1Н, мультиплет), 4,94 и 5,05 (2Н, каждый синглет), 7,13 (2Н, дублет, J=8,9 Гц), 7,98 (2Н, дублет, J=8,9 Гц), 7,9 и 8,00 (1Н, каждый дублет, J=7,0, 8,5 Гц), 8,30 и 8,59 (1Н, каждый дублет, J=8,0, 7,9 Гц), 9,03 (2Н, синглет), 9,13 (2Н, синглет)
Пример 9
(1) Исходное соединение (9В) получили из 2-/4-(N-бензилоксикарбониламидино)фенокси/уксусной кислоты и из исходного соединения (9А) по методике, аналогичной Примеру 1.
Смесь полученного таким образом исходного соединения (9В), анизола (20 мл) и трифторуксусной кислоты (80 мл) перемешивали в течение 2 ч 45 мин.
Удалили трифторуксусную кислоту при пониженном давлении, а остаток растерли с диэтиловым эфиром, что дало исходное соединение (9С) (19,49 г).
т.пл.: 152-156oC
ИК (нуджол): 1630, 1600, 1560, 1500 см-1
ЯМР (ДМСО-d6, δ): 2,84 и 3,06 (3Н, каждый синглет), 4,01 и 4,19 (2Н, каждый синглет), 4,91 и 5,09 (2Н, каждый синглет), 5,34 (2Н, синглет), 7,06 и 7,08 (2Н, каждый дублет, J=8,8 Гц), 7,3-7,6 (5Н, мультиплет), 7,78 (2Н, дублет, J=8,8 Гц)
(2) Целевое соединение (9А) получили из полученного таким образом исходного соединения (9С) и из исходного соединения (9Д) по методике, аналогичной описанной в Примере 1.
Защитные группы целевого соединения (9А) удалили аналогично Примеру 5 и получили целевое соединение (9В).
т.пл.: 41-45oC
ИК (нуджол): 3250, 1630, 1610 см-1
ЯМР (ДМСО-d6, δ): 0,7-1,0 (6Н, мультиплет), 1,3-1,7 (3Н, мультиплет), 2,3-2,8 (2Н, мультиплет), 2,80 и 3,00 (3Н, каждый синглет), 3,97 и 4,04 (2Н, каждый синглет), 4,18 (1Н, мультиплет), 4,67 (1Н, мультиплет), 5,93 и 5,05 (2Н, каждый синглет), 7,13 (2Н, дублет, J=8,7 Гц), 7,77 (2Н, дублет, J=8,7 Гц), 7,98 и 8,17 (1Н, каждый дублет, J=7,9 Гц), 8,24 и 8,55 (1Н, каждый дублет, J=7,9 Гц), 8,55 и 9,13 (4Н, каждый синглет)
МС (M/Z): 494 (М+1)
Условия проведения ВЭЖХ
элюирование: CH3CN: 0,1% водный раствор трифторуксусной кислоты = 17:83
время удерживания: 11,0 минут
(колонка и поток такие же, как и в Примере 5)
Следующие соединения (Примеры с 10 по 12) получены из соответствующих солей трифторуксусной кислоты традиционным способом.
Пример 10
Целевое соединение (10)
ИК (нуджол): 3420, 3270, 1690, 1635, 1600, 1540, 1480 см-1
ЯМР (ДМСО-d6, δ): 0,84 (6Н, дублет, J=6,3 Гц), 1,8-2,2 (3Н, мультиплет), 2,3 (2Н, триплет J=7,3 Гц), 2,3-2,8 (2Н, мультиплет), 3,96-4,2 (3Н, мультиплет), 4,65 (1Н, мультиплет), 7,14 (2Н, дублет, J=8,9 Гц), 7,8 (1Н, дублет, J= 8,5 Гц), 7,85 (2Н, дублет, J=8,9 Гц), 8,35 (1Н, дублет, J=7,7 Гц), 9,04 (2Н, синглет, 9,24 (2Н, синглет), 12,51 (1Н, широкий синглет)
Элементный анализ
C20H28N4O7•HCl•H2O
Вычислено: C 48,93; H 6,36; N 11,41; Cl 7,22
Найдено: C 48,77; H 6,52; N 11,22; Cl 6,98
т.пл.: 198oC (разлаг.)
Пример 11
Целевое соединение (11)
т.пл.: 163oC (разлаг.)
ИК (нуджол): 3270, 1700, 1665, 1630, 1605, 1535, 1480 см-1
ЯМР (ДМСО-d6, δ): 0,84 (6Н, дублет, J=6,1 Гц), 1,29-1,85 (6Н, мультиплет), 1,91-2,23 (3Н, мультиплет), 2,35-2,78 (2Н, мультиплет), 3,98-4,2 (3Н, мультиплет), 4,55-4,73 (1Н, мультиплет), 7,14 (2Н, дублет, J=8,9 Гц), 7,72 (1Н, дублет, J=8,7 Гц), 7,83 (2Н, дублет, J=8,9 Гц), 8,25 (1Н, дублет, J=7,7 Гц), 8,94 (2Н, синглет), 9,20 (2Н, синглет)
Пример 12
Целевое соединение (12)
т.пл.: 133 140oC
ИК (нуджол): 3000-3300 (широкий синглет), 1710 (плечо), 1630 (широкий brs синглет) см-1
ЯМР (ДМСО-d6, δ): 0,86 (6Н, дублет, J=6,8 Гц), 2,05 (1Н, мультиплет), 2,80 и 3,01 (3Н, каждый синглет), 2,4-2,8 (2Н, мультиплет), 3,8-4,2 (3Н, мультиплет), 4,68 (1Н, мультиплет), 4,94 и 5,06 (2Н, каждый синглет), 7,13 (2Н, дублет, J=8,8 Гц), 7,80 (2Н, дублет, J=8,8 Гц), 7,8 и 8,0 (1Н, каждый дублет, J= 7,0 и 8,5 Гц), 8,37 и 8,68 (1Н, каждый дублет, J=8,0 и 7,9 Гц), 9,05 (2Н, синглет), 9,24 (2Н, синглет)
МС (M/Z): 480 (М+ + 1)
Условия проведения ВЭЖХ
колонка: УМС-РАСК R-ODS-15 S-15 120A ODS 50 ϕ х 250 мм
элюирование: CH3CN: 0,1% водный раствор трифторуксусной кислоты = 15:85
поток: 1 мл/мин
время удерживания: 8,1 мин
Формулы исходного и целевого соединений в следующем Примере 13 можно представить следующим образом.

(Am, Asr и VaI каждое как определено выше)
Пример 13
Раствор исходного соединения (13) (79 г) в 0,02 М буфере пиридин-уксусная кислота (pH 5) (1 л) подвергли колоночной хроматографии на ионообменной смоле (2 л), элюируя 0,5 М буфером пиридин-уксусная кислота.
Фракции, содержащие целевое соединение, соединили и сконцентрировали при пониженном давлении, получив целевое соединение (13) (62,54 г).
т.пл.: 171oC (разлаг.)
ИК (нуджол): 3310, 1650, 1600, 1520 см-1
ЯМР (ДМСО-d6, δ): 0,80 (6Н, дублет, J=6,8 Гц), 1,8-2,73 (7Н, мультиплет), 3,8-4,25 (3Н, мультиплет), 4,56 (1Н, мультиплет), 7,10 (2Н, дублет, J= 8,8 Гц), 7,44 (1Н, дублет, J=8,1 Гц), 7,74 (2Н, дублет, J=8,7 Гц), 8,39 (1Н, дублет, J=7,6 Гц), 8,75 (1,5H, синглет), 11,25 (1,5H, синглет)
МС (M/Z): 437 (М++1)
Элементный анализ
C20H28N4O7•1,2H2O
Метод получения 16
Смесь DL-4-циано-N-ацетилфенилаланина (114,0 г), хлорида кобальта (11) (0,63 г) и ацилазы Amano 15000 (торговая марка) (6,27 г) в 1 н. водном растворе гидроксида натрия (492 мл) довели до pH 7,5, добавляя 0,1 н. хлористоводородную кислоту и 0,1 н. водный раствор хлорида натрия, а затем перемешивали при 33-36oC в течение 20 ч. Реакционную смесь довели до pH 1 с помощью 10% хлористоводородной кислоты, а затем промыли этилацетатом и собрали фильтрацией образовавшийся осадок. Осадок промыли 10% хлористоводородной кислотой и водой, получив 4-циано-N-ацетил-D-фенилаланин (32,00 г).
т.пл.: 173-175oC
(α)D (C=1, MeOH) = - 12,9°
ИК (нуджол): 2210, 1715, 1600, 1520 см-1
ЯМР (ДМСО-d6, δ): 1,78 (3Н, синглет), 2,92 (1Н, двойной дублет, J=13,8, 9,8 Гц), 3,15 (1Н, двойной дублет, J=13,8 Гц, 4,9 Гц), 4,48 (1Н, мультиплет), 7,44 (2Н, дублет, J=8,2 Гц), 7,76 (2Н, дублет, J=8,2 Гц), 8,25 (1Н, дублет, J=8,2 Гц)
Кислотный водный слой довели до pH 7,5, добавляя водный раствор гидроксида натрия, добавили триэтиламин (32,2 мл) и ди-трет-бутилдикарбонат (83,59 г) и перемешивали при комнатной температуре в течение 5 дн. Реакционную смесь довели до pH 6,0 с помощью 10% хлористоводородной кислоты и экстрагировали этилацетатом. Отделенный органический слой промыли водой и раствором соли и высушили над сульфатом магния. После выпаривания в вакууме осадок промыли н-гексаном, получив 4-циано-N-трет-бутоксикарбонил-L-фенилаланин (43,50 г)
т.пл.: 149-150oC
(α)D (C=1, MeOH) = + 6,1°
ИК (нуджол): 3350, 3180, 2240, 1730, 1680, 1600, 1505 см-1
ЯМР (ДМСО-d6, δ): 1,31 (9Н, синглет), 2,91 (1Н, двойной дублет, J=13,7 Гц, 10,9 Гц), 3,14 (1Н, двойной дублет, J=13,7 Гц, J=10,9 Гц), 4,18 (1Н, мультиплет), 7,20 (1Н, дублет, J=8,6 Гц), 7,46 (2Н, дублет, J=8,1 Гц), 7,76 (2Н, дублет, J=8,1 Гц)
Элементный анализ
Вычислено: C 62,05; H 6,24; N 9,24
Найдено: C 62,38; H 6,32; N 9,55
Метод получения 17
Через раствор 4-циано-N-трет-бутоксикарбонил-L-фенилаланина (31,50 г) в пиридине (400 мл) и триэтиламине (190 мл) барботировали сернистый водород при комнатной температуре в течение 2 ч, и оставили смесь при комнатной температуре на ночь. Реакционную смесь разбавили водой и этилацетатом и довели до pH 4,5, добавляя концентрированную хлористоводородную кислоту, и экстрагировали этилацетатом. Отделенный органический слой промыли разбавленной хлористоводородной кислотой и водой и высушили над сульфатом магния. После выпаривания в вакууме осадок собрали фильтрацией и промыли н-гексаном, получив 4-тиокарбамоил-N-трет-бутоксикарбонил-L-фенилаланин (30,31 г).
т.пл.: 254-256oC (разлаг.)
(α)D (MeOH, C=1) = +29,40°
ИК (нуджол): 3280, 3110, 1670, 1605, 1510 см-1
ЯМР (ДМСО-d6, δ): 1,32 (9Н, синглет), 2,87 (1Н, двойной дублет, J=13,7 Гц, J= 10,3 Гц), 3,05 (1Н, двойной дублет, J=13,7 Гц, J=4,5 Гц), 4,12 (1Н, мультиплет), 7,15 (1Н, дублет, J=8,4 Гц), 7,28 (2Н, дублет, J=8,2 Гц), 7,83 (2Н, дублет, J= 8,2 Гц), 9,43 (1Н, широкий синглет), 9,80 (1Н, широкий синглет)
Элементный анализ
Найдено: C 55,19, H 6,32, S 9,99 N 8,38
Вычислено: C 55,53, H 6,21, S 9,88 N 8,63
Метод получения 18
Раствор 4-тиокарбамоил-N-трет-бутоксикарбонил-L-фенилаланина (30,06 г) и метилиодида (63,5 мл) в ацетоне (300 мл) перемешивали и нагревали с обратным холодильником в течение 40 минут, после чего удалили растворитель под вакуумом. Полученное вещество растворили в метаноле (300 мл), добавили ацетат аммония (10,71 г), а затем смесь нагревали с обратным холодильником при перемешивании в течение 4 ч 30 мин. Реакционную смесь охладили и отфильтровали образовавшийся осадок. Фильтрат выпарили под вакуумом, полученное вещество растерли с этанолом и диэтиловым эфиром и промыли диэтиловым эфиром, получив 4-амидино-N-третбутоксикарбонил-L-фенилаланина гидроиодид (13,83 г).
т.пл.: 184-188oC (разлаг.)
ИК (нуджол): 1670, 1600, 1560 см-1
ЯМР (ДМСО-d6, δ): 1,33 (9Н, синглет), 2,7-3,2 (2Н, мультиплет), 3,97 (1Н, мультиплет), 7,23 (2Н, дублет, J=8,0 Гц), 7,4-8,0 (6Н, мультиплет)
МС (m/z): 308 (М++1)
Метод получения 19
К смеси 4-амидино-N-трет-бутоксикарбонил-L-фенилаланина гидроиодида (1,00 г), в 4 н. водного раствора гидроксида натрия (1,15 мл), тетрагидрофурана (2 мл) и воды (10 мл) добавили раствор бензилоксикарбонилхлорида в тетрагидрофуране (2 мл), pH которого доведен до 12≈12,5 с помощью 4 н. водного раствора гидроксида натрия. Реакционную смесь разбавили водой и диэтиловым эфиром, отделенный водный слой нейтрализовали 10% хлористоводородной кислотой, экстрагировали этилацетатом, промыли водой и раствором соли и высушили над сульфатом магния. Осадок, полученный после выпаривания в вакууме, собрали фильтрацией и промыли диэтиловым эфиром, что дало 4-(N-бензилоксикарбониламидино)-N-трет-бутоксикарбонил-L-фенилаланин (0,53 г).
т.пл.: 112-115oC
ИК (нуджол): 3300, 1680, 1620, 1560, 1500 см-1
ЯМР (ДМСО-d6, δ): 1,31 (9Н, синглет), 2,8-3,2 (2Н, мультиплет), 4,12 (1Н, мультиплет), 5,11 (1Н, синглет), 7,12 (1Н, дублет, J=8,3 Гц), 7,3-7,5 (7Н, мультиплет), 7,91 (2Н, дублет, J=8,3 Гц), 9,14 (широкий синглет)
Метод получения 20
4-(N-Бензилоксикарбониламидино)-N-ацетил-D-фенилаланин получили из 4-циано-N-ацетил-D-фенилаланина по методике, аналогичной методике Методов получения 17, 18 и 19.
т.пл.: 140-145oC (разлаг).
ИК (нуджол): 3250 (широкий синглет), 1740, 1605 см-1
ЯМР (ДМСО-d6, δ): 1,77 (3Н, синглет), 2,90 (1Н, двойной дублет, J=13,8, 10,0 Гц), 3,16 (1Н, двойной дублет, J=13,8, 4,5 Гц), 4,46 (1Н, мультиплет), 5,27 (2Н, синглет), 7,2-7,5 (7Н, мультиплет), 7,80 (2Н, дублет, J=8,2 Гц), 8,32 (1Н, дублет, J=8,2 Гц)
Метод получения 21
Смесь этил-5-(4-амидинофенил)-2,4-пентадиеноата гидрохлорида (20,00 г) и 10% Pd-C (5,00 г) в этаноле (500 мл) перемешивали в атмосфере газообразного H2 при комнатной температуре в течение 3 ч. После фильтрации фильтрат выпарили в вакууме. Полученный осадок промыли диэтиловым эфиром и получили 5-/4-амидинофенил/пентаноата гидрохлорид /19,32 г/.
ИК /нуджол/: 3400, 3100, 1730, 1660 см-1
ЯМР (ДМСО-d6, δ): 1,16 /3Н, триплет, J=7,1 Гц/, 1,52-1,61 /4Н, мультиплет/, 2,32 (2Н, триплет, J=6,9 Гц/, 2,66 /2Н, триплет, J=7,0 Гц/, 4,04 /2Н, квартет, J= 7,1 Гц/, 7,45 /2Н, дублет, J=8,8 Гц/, 7,78 /2Н, дублет, J=8,3 Гц/, 9,21 /2Н, синглет/, 9,26 /2Н, синглет/
МС /m/z/: 248 /М+/
Метод получения 22
Этил-3-/4-амидинофенил/пропионата гидрохлорид получили по методике, аналогичной Примеру 21.
ИК /нуджол/: 3350, 3150, 1720, 1670, 1210 см-1
ЯМР (ДМСО-d6, δ): 1,16 /3Н, триплет, J=7,1/, 2,69 /2Н, триплет, J=7,4 Гц/, 2,95 /2Н, дублет, J=8,3 Гц/, 4,09 /2Н, квартет, J=7,1 Гц/, 7,48 /2Н, дублет, J=8,3 Гц/, 7,82 /2Н, дублет, J=8,3 Гц/, 8,94 /4Н, широкий синглет/
МС /m/z/: 220 /М+/
Следующие соединения (Методы получения с 23 по 25) были получены аналогично методике Метода получения 10.
Метод получения 23
Этил-3-/4-(N-бензилоксикарбониламидино)фенил/пропионат
ЯМР (ДМСО-d6, δ): 1,15 /3Н, триплет, J=7,1 Гц/, 2,65 /2Н, триплет, J=7,4 Гц/, 2,91 /2Н, триплет, J=7,4 Гц/, 4,03 /2Н, квартет, J=7,1 Гц/, 5,10 /2Н, синглет/, 7,31-7,41 /7Н, мультиплет/, 7,90 /2Н, дублет, J=8,3 Гц/, 9,13 /2Н, широкий синглет/
МС (m/z): 354 /М+/
Метод получения 24
Этил-5-/4-(N-бензилоксикарбониламидино)фенил/пентаноат
ИК (нуджол/: 3450, 3300, 1730, 1600, 1250 см-1
ЯМР (ДМСО-d6, δ): 1,16 /3Н, триплет, J=7,1 Гц/, 1,56-1,58 /4Н, мультиплет/, 2,31 /2Н, триплет, J=6,9 Гц/, 2,64 /2Н, триплет, J=7,0 Гц/, 4,03 /2Н, квартет, J= 7,1 Гц/, 5,11 /2Н, синглет/, 7,23-7,40 /7Н, мультиплет/, 7,90 /2Н, дублет, J=8,3 Гц/, 9,23 /2Н, широкий синглет/
Метод получения 25
Этил-8-/4-(N-бензилоксикарбониламидино)фенокси/октаноат
т.пл.: 93-95oC
ИК /нуджол/: 3420, 3290, 1720, 1650, 1590, 1560, 480 см-1
ЯМР (ДМСО-d6, δ): 1,17 /3Н, триплет, J=7,1/, 1,15-1,83 /10Н, мультиплет/, 2,27 /2Н, триплет, J=7,2/, 4,01 /2Н, типа триплета/, 4,04 /2Н, квартет, J= 7,1 Гц/, 5,10 /2Н, синглет/, 7,0 /2Н, дублет, J=8,9 Гц/, 7,36 /5Н, мультиплет/, 7,98 /2Н, дублет, J=8,9 Гц/, 9,09 /2Н, широкий синглет/
Метод получения 26
Этил-5-/4-(N-бензилоксикарбониламидинофенил)/пентаноат (22,00 г) в концентрированной хлористоводородной кислоте (220 мл) перемешивали при комнатной температуре в течение 3 нед. Реакционную смесь отфильтровали и растворили отфильтрованный осадок в смеси воды и этилацетата, довели pH до 10,50, добавляя водный раствор гидроксида натрия, pH отделенного водного слоя довели до 4,5, добавляя 10% хлористоводородную кислоту, и экстрагировали этилацетатом, а отделенный органический слой промыли раствором соли и высушили над сульфатом магния, фильтрат, полученный после фильтрации, выпарили в вакууме, а образовавшийся осадок растерли с диизопропиловым эфиром и получили 5-[4-(N-бензилоксикарбониламидинофенил)]-пентановую кислоту (12,0 г).
ИК (нуджол): 3350, 3200, 1700, 1660, 1620, 1250 см-1
ЯМР (ДМСО-d6, δ): 1,50-1,60 (4Н, мультиплет), 2,23 (2Н, триплет, J=6,9 Гц), 2,64 (2Н, триплет, J= 7,0 Гц), 5,10 (2Н, синглет), 7,27-7,42 (7Н, мультиплет), 7,90 (2Н, дублет, J=8,3 Гц), 9,11 (2Н, широкий синглет), 12.01 (1Н, широкий синглет)
МС (m/z): 355 (М+ +1)
Метод получения 27
3-/4(N-Бензилоксикарбониламидино)фенил/пропионовую кислоту получили по методике, аналогичной описанной в Методе получения 26.
ЯМР (ДМСО-d6, δ): 2,56 (2Н, триплет, J=7,4 Гц), 2,88 (2Н, триплет, J=7,4 Гц), 5,10 (2Н, синглет), 7,32-7,38 (8Н, мультиплет), 7,90 (2Н, дублет, J=8,3 Гц), 9,08 (1Н, широкий синглет)
Метод получения 28
8-/4(N-Бензилоксикарбониламидино)фенокси/октановую кислоту получили аналогично Методу получения 13.
т.пл.: 130oC (разлаг.)
ИК (нуджол): 1760, 1700, 1600 см-1
ЯМР (ДМСО-d6, δ): 1,15-1,8 (10Н, мультиплет), 2,20 (2Н, триплет, J=7,2 Гц), 4,07 (2Н, триплет, J=6,4 Гц), 5,27 (2Н, синглет), 7,09 (2Н, дублет, J= 8,9 Гц), 10,0 (1Н, уширенный), 12,0 (1Н, уширенный)
Метод получения 29
Смесь этил-4-(4-цианофенокси)бутирата (4,7 г) в тетрагидрофуране (23,5 мл) и 1 н. раствора гидроксида натрия (40,2 мл) нагревали с обратным холодильником в течение 2 ч при перемешивании. Реакционную смесь довели до pH 2,0, добавляя 10% хлористоводородную кислоту, и собрали образовавшийся осадок фильтрованием, получив 4-(4-цианофенокси)масляную кислоту (4,06 г).
т.пл.: 210oC
ИК (нуджол): 3175, 2220, 1730, 1600, 1510 см-1
ЯМР (ДМСО-d6, δ): 1,96 (2Н, мультиплет), 2,39 (2Н, мультиплет), 4,08 (2Н, мультиплет), 7,08 (2Н, дублет, J=8,9 Гц), 7,76 (2Н, дублет, J=8,9 Гц), 12,18 (1Н, синглет)
Метод получения 30
5-(4-Цианофенокси)пентановую кислоту получили по методике, аналогичной описанной в Методе получения 29.
т.пл.: 160oC
ИК (нуджол): 3200, 2225, 1720, 1600, 1560, 1505 см-1
ЯМР (ДМСО-d6, δ): 1,5-1,85 (4Н, мультиплет), 2,29 (2Н, триплетоподобный), 4,05 (2Н, мультиплет), 7,09 (2Н, дублет, J=6,9 Гц), 7,76 (2Н, дублет, J=6,9 Гц)
Метод получения 31
Смесь 4-(4-цианофенокси)масляной кислоты (1 г), триэтиламина (0,75 мл) и дифенилфосфорилазида (1,16 мл) в тетрагидрофуране (10 мл) нагревали с обратным холодильником в течение 6 ч при перемешивании. К полученной смеси добавили исходное соединение (Р-31) (2,4 г) при комнатной температуре, и смесь перемешивали в тех же условиях в течение 15 ч. Реакционную смесь вылили в смесь этилацетата (30 мл) и воды (100 мл) и довели до pH 10, добавляя 4 н. раствор гидроксида натрия. Отделенный органический слой промыли разбавленной хлористоводородной кислотой, насыщенным водным раствором бикарбоната натрия, водой и раствором соли, высушили над сульфатом магния и выпарили в вакууме, получив целевое соединение (Р-31) (1,7 г).
т.пл.: 106-109oC
ИК (нуджол): 3360, 3300, 3270, 2225, 1725, 1630, 1600 см-1
ЯМР (ДМСО-d6, δ): 0,82 (6Н, дублет, J=5,6 Гц), 1,83 (2Н, триплет, J=6,3 Гц), 2,05 (1Н, мультиплет), 2,4-2,8 (2Н, мультиплет), 3,15 (2Н, мультиплет), 4,05 (2Н, триплет, J=6,2 Гц), 4,23 (1Н, мультиплет), 4,61 (1Н, мультиплет), 5,05 (2Н, синглет), 5,10 (2Н, синглет), 6,22-6,4 (2Н, мультиплет), 7,08 (2Н, дублет, J=8,9 Гц), 7,35 (10H, мультиплет), 7,75 (2Н, дублет, J=8,9 Гц), 8,15 (1Н, дублет, J=8,3 Гц)
FAB-MASS: 615 (М+ +1)
Метод получения 32
Целевое соединение (Р-32) получили по методике, аналогичной Методу получения 31.
т.пл.: 115-122oC
ИК (нуджол): 3300, 2220, 1730, 1625, 1600, 1540 см-1
ЯМР (ДМСО-d6, δ): 0,83 (6Н, дублет, J=6,7 Гц), 1,52 (2Н, мультиплет), 1,69 (2Н, мультиплет), 2,06 (1Н, мультиплет), 2,5-2,8 (2Н, мультиплет), 3,05 (2Н, мультиплет), 4,05 (2Н, триплет, J=6,2 Гц), 4,23 (1Н, мультиплет), 4,63 (1Н, мультиплет), 5,06 (2Н, синглет), 5,11 (2Н, синглет), 6,2-6,4 (2Н, мультиплет), 7,08 (2Н, дублет, J= 8,9 Гц), 7,35 (10Н, мультиплет), 7,74 (2Н, дублет, J=8,9 Гц), 8,16 (1Н, дублет, J=8,3 Гц)
Следующие соединения (методы получения 33 и 34) были получены по методике, аналогичной Методу получения 17.
Метод получения 33
Целевое соединение (Р-33)
т.пл.: 139oC
ИК (нуджол): 3430, 3320, 3200, 1730, 1715, 1630, 1540 см-1
ЯМР (ДМСО-d6, δ): 0,83 (6Н, дублет, J=6,5 Гц), 1,93 (2Н, триплетоподобный), 2,05 (1Н, мультиплет), 2,4-2,8 (2Н, мультиплет), 3,15 (2Н, мультиплет), 4,03 (2Н, триплетоподобный), 4,23 (1Н, мультиплет), 4,62 (1Н, мультиплет), 5,06 (2Н, синглет), 5,11 (2Н, синглет), 6,2-6,42 (2Н, мультиплет), 6,93 (2Н, дублет, J=8,8 Гц), 7,34 (10Н, мультиплет), 7,95 (2Н, дублет, J=8,8 Гц), 8,15 (1Н, дублет, J=8,2 Гц), 9,32 (1Н, синглет), 9,64 (1Н, синглет)
Метод получения 34
Целевое соединение (Р-34)
т.пл.: 130oC
ЯМР (ДМСО-d6, δ): 0,83 (6Н, дублет, J=5,8 Гц), 1,52 (2Н, мультиплет), 1,69 (2Н, мультиплет), 2,06 (2Н, мультиплет), 2,4-2,8 (2Н, мультиплет), 3,05 (2Н, мультиплет), 4,01 (2Н, триплет, J=6,0 Гц), 4,23 (1Н, мультиплет), 4,62 (1Н, мультиплет), 5,06 (2Н, синглет), 5,11 (2Н, синглет), 6,2-6,4 (2Н, мультиплет), 6,93 (2Н, дублет, J= 8,9 Гц), 7,35 (10Н, мультиплет), 7,95 (2Н, дублет, J= 8,9 Гц), 8,15 (1Н, дублет, J=8,3 Гц), 9,32 (1Н, синглет), 9,64 (1Н, синглет)
В приведенных выше Методах получения 31-34 формулы исходных и целевых соединений имеют следующий вид, приведенный в табл.2 (в формулах Asp, VaI и BZI каждое как объяснено в табл. 2).
Метод получения 35
Смесь 60% гидрида натрия (7,92 г) в тетрагидрофуране (100 мл) перемешивали при -10oC в атмосфере газообразного азота. В реакционную смесь налили этил-5-диэтоксифосфорил-3-пентеноат (49,61 г) и перемешивали в течение 1 ч при -10oC. В реакционную смесь налили р-цианобензальдегид (20,00 г) в тетрагидрофуране (50 мл) и перемешивали в течение 3 ч при 0oC. Реакционную смесь вылили в смесь соляного раствора и этилацетата. Отделенный органический слой высушили над сульфатом магния и обработали активированным углем. После фильтрации фильтрат выпарили в вакууме. Остаток подвергли колоночной хроматографии на силикагеле и элюировали смесью этилацетат/н-гексан = 1:4. Фракции, содержащие целевое соединение, соединили и выпарили в вакууме, получив 5-(4-цианофенил)-2,4-пентадиеноат (10,04 г).
ИК (нуджол): 2250, 1720, 1630, 1250 см-1
ЯМР (ДМСО-d6, δ): 1,24 (3Н, триплет, J=7,1 Гц), 4,16 (2Н, квартет, J=7,1 Гц), 6,18 (1Н, дублет, J=12,5 Гц), 7,13-7,49 (3Н, мультиплет), 7,74 (2Н, дублет, J=8,5 Гц), 7,85 (2Н, дублет, J=8,5 Гц)
МС (m/z): 227 (М+)
Следующие соединения (методы получения 36 и 37) были получены по методике, аналогичной Методу получения 4.
Метод получения 36
Этил-3-/4-(1-(этокси)иминометил)фенил/акрилата гидрохлорид
ИК (нуджол): 1720, 1640, 1320, 1180 см-1
ЯМР (ДМСО-d6, δ): 1,28 (3Н, триплет, J=7,1 Гц), 1,49 (3Н, триплет, J=7,0 Гц), 4,21 (2Н, квартет, J=7,1 Гц), 4,66 (2Н, квартет, J=7,0 Гц), 6,86 (1Н, дублет, J= 16,0 Гц), 7,59 (1Н, дублет, J=16,0 Гц), 7,79 (2Н, дублет, J=8,7 Гц), 8,18 (2Н, дублет, J=8,7 Гц)
МС (m/z): 247 (М+)
Метод получения 37
Этил-5-/4-(1-(этокси)иминометил)фенил/-2,4-пентадиеноата гидрохлорид
ИК (нуджол): 3400, 1720, 1620, 1250 см-1
ЯМР (ДМСО-d6, δ): 1,25 (3Н, триплет, J=7,1 Гц), 1,49 (3Н, триплет, J=7,0 Гц), 4,16 (2Н, квартет, J=7,1 Гц), 4,63 (2Н, квартет, J=7,0 Гц), 6,20 (1Н, дублет, J=14,2 Гц), 7,17-7,46 (3Н, мультиплет), 7,84 (2Н, дублет, J=8,5 Гц), 8,15 (2Н, дублет, J=8,5 Гц)
МС (m/z): 273 (М+)
Метод получения 38
В смесь этил-5-/4-((1-этокси)иминометил)фенил/-2,4-пентадиеноата гидрохлорида (22,00 г) в этаноле (220 мл) налили 9 н. раствор аммиака в этаноле (19,7 мл) и нагревали с обратным холодильником в течение 15 ч. После охлаждения до комнатной температуры реакционную смесь выпарили в вакууме, осадок промыли диизопропиловым эфиром и получили этил-5-(4-амидинофенил)-2,4-пентадиеноата гидрохлорид (20,15 г).
ИК (нуджол): 3400, 1720, 1630, 1250 см-1
ЯМР (ДМСО-d6, δ): 1,25 (3Н, триплет, J=7,1 Гц), 4,17 (2Н, квартет, J=7,1 Гц), 6,18 (1Н, дублет, J=14,4 Гц), 7,15-7,51 (3Н, мультиплет), 7,78 (2Н, дублет, J=8,5 Гц), 7,89 (2Н, дублет, J=8,5 Гц), 9,30 (2Н, синглет), 9,48 (2Н, синглет)
МС (m/z): 244 (М+)
Метод получения 39
Этил-3-(4-амидинофенил)акрилата гидрохлорид получили аналогично Методу получения 7.
ИК (нуджол): 3400, 1720, 1320, 1200 см-1
ЯМР (ДМСО-d6, δ): 1,28 (3Н, триплет, J=7,1 Гц), 4,22 (2Н, квартет, J=7,1 Гц), 6,86 (1Н, дублет, J=16,1 Гц), 7,73 (1Н, дублет, J=16,1 Гц), 7,91 (2Н, дублет, J=8,5 Гц), 7,98 (2Н, дублет, J=8,5 Гц), 8,76 (4Н широкий синглет)
МС (m/z): 218 (М+)
Метод получения 40
3-/4-(N-Бензилоксикарбониламино)фенил/пропионовую кислоту получили по методике, аналогичной Методу получения 26.
ЯМР (ДМСО-d6, δ): 2,56 (2Н, триплет, J=7,4 Гц), 2,88 (2Н, триплет, J=7,4 Гц), 5,10 (2Н, синглет), 7,32-7,38 (8Н, мультиплет), 7,90 (2Н, дублет, J=8,3 Гц), 9,08 (1Н, широкий синглет)
Формулы исходных и целевых соединений в следующих Примерах показаны в табл.3.
В формулах, приведеных в табл. 3 Am/Z/, Am, Bzl, Asp, Val, Sar и Leu каждое соответствует определениям, указанным выше, Tyr означает 1-тирозин, Ser означает L-серин, Gly означает глицин, Ala означает L-аланин, β Ala означает β -аланин, Phe означает L-фенилаланин, D-VaI означает D-валин, Thr означает L-треонин, Ile означает L-изолейцин, Nle означает L-норлейцин, Glu означает L-глутаминовую кислоту, Me означает метил, Et означает этил, Ac означает ацетил и Boc означает трет-бутоксикарбонил.
Следующие соединения (примеры с 14 по 20) были получены по методике, аналогичной методике Примера 1.
Пример 14
Целевое соединение (14)
т.пл.: 95-100oC
ИК (нуджол): 3300, 1730, 1710, 1650, 1625, 1530 см-1
ЯМР (ДМСО-d6, δ): 0,82 (6Н, дублет, J=6,6 Гц), 1,34-1,68 (4Н, мультиплет), 1,92-2,22 (3Н, мультиплет), 2,4-2,85 (4Н, мультиплет), 4,1-4,29 (1Н, мультиплет), 4,65-5,84 (1Н, мультиплет), 4,1-4,29 (1Н, мультиплет), 4,65-4,84 (1Н, мультиплет), 5,05 (2Н, синглет), 5,1 (4Н, синглет), 7,1-7,52 (17Н, мультиплет), 7,9 (2Н, дублет, J=8,1 Гц), 8,11 (1Н, дублет, J=8,2 Гц), 8,22 (1Н, дублет, J=7,9 Гц), 9,12 (2Н, широкий синглет)
Пример 15
Целевое соединение (15)
т.пл.: ≈125oC /разл./
ИК (нуджол): 3300, 1725, 1650, 1605, 1490 см-1
ЯМР (ДМСО-d6, δ): 1,5-1,85 (4Н, мультиплет), 2,14 (2Н, типа триплета), 2,5-3,01 (4Н, мультиплет), 3,56 (3Н, синглет), 4,01 (2Н, мультиплет), 4,36 (1Н, мультиплет), 4,73 (1Н, мультиплет), 5,07 (2Н, синглет), 5,1 (2Н, синглет), 6,65 (2Н, дублет, J=8,4 Гц), 6,9-7,1 (4Н, мультиплет), 7,24-7,5 (12Н, мультиплет), 7,98 (2Н, дублет, J=8,9 Гц), 8,17 (2Н, дублет, J=6,7 Гц), 8,95-9,37 (2Н, широкий)
Пример 16
Целевое соединение (16)
т.пл.: ≈128oC /разл./
ИК (нуджол): 3300, 1730, 1640, 1600, 1530 см-1
ЯМР (ДМСО-d6, δ): 1,5-1,83 (4Н, мультиплет), 2,14 (2Н, типа триплета), 2,5-3,05 (4Н, мультиплет), 3,58 (3Н, синглет), 3,69 (3Н, синглет), 4,01 (2Н, типа триплета), 4,40 (1Н, мультиплет), 4,72 (1Н, мультиплет), 5,07 (2Н, синглет), 5,10 (2Н, синглет), 6,82 (2Н, дублет, J=8,6 Гц), 6,99 (2Н, дублет, J= 8,9 Гц), 7,10 (2Н, дублет, J=8,6 Гц), 7,22-7,50 (12Н, мультиплет), 7,99 (2Н, дублет, J=8,8 Гц), 8,1-8,29 (2Н, мультиплет), 9,14 (1Н, широкий синглет)
Пример 17
Целевое соединение (17)
т.пл.: 120oC /разл./
ИК (нуджол): 3300, 1730, 1640, 1605, 1500 см-1
ЯМР (ДМСО-d6, δ): 1,48-1,8 (4Н, мультиплет), 2,13 (2Н, типа триплета), 2,4-3,06 (4Н, мультиплет), 3,69 (3Н, синглет), 4,00 (2Н, типа триплета), 4,46 (1Н, мультиплет), 4,73 (1Н, мультиплет), 5,05 (4Н, синглет), 5,10 (2Н, синглет), 6,79 (2Н, дублет, J=8,6 Гц), 6,98 (2Н, дублет, J=8,9 Гц), 7,08 (2Н, дублет, J=8,6 Гц), 7,17-7,5 (15Н, мультиплет), 7,98 (2Н, дублет, J=8,9 Гц), 8,16 (1Н, дублет, J=8,1 Гц), 8,29 (1Н, дублет, J=7,4 Гц), 9,16 (1Н, широкий синглет)
Пример 18
Целевое соединение (18)
т.пл.: 86-90oC
ИК (нуджол): 3300, 1720, 1610, 1595 см-1
ЯМР (ДМСО-d6, δ): 1,71 (4Н, широкий синглет), 2,22 (2Н, широкий синглет), 2,67 (1Н, двойной дублет, J=17,4 Гц, J=5,9 Гц), 3,05 (1Н, двойной дублет, J= 17,7 Гц, J=9,2 Гц), 3,7-4,2 (4Н, мультиплет), 4,52 (4Н, широкий синглет), 5,0-5,2 (6Н, мультиплет), 7,00 (2Н, дублет, J=8,3 Гц), 7,2-7,6 /21Н/, 7,99 /2Н, дублет, J=8,4 Гц/, 8,69 /1Н, дублет, J=7,4 Гц)
Пример 19
Целевое соединение /19/
т.пл.: 55-60oC
ИК (нуджол): 3260, 1725, 1645, 1600 см-1
ЯМР (ДМСО-d6, δ): 2,6-3,1 /4Н, мультиплет/, 2,77 и 2,96 /3Н, каждый синглет/, 3,56 /3Н, синглет/, 3,69 /3Н, синглет/, 3,97 и 4,01 /2Н, каждый синглет/, 4,4 /1Н, мультиплет/, 4,7-5,3 /7Н, мультиплет/, 6,80 /2Н, мультиплет/, 6,95-7,2 /4Н, мультиплет/, 7,35 /10Н, мультиплет/, 7,97 /2Н, дублет, J=7,9 Гц/, 8,2-8,3 /1Н, мультиплет/, 8,4-8,6 /1Н, мультиплет/
Пример 20
Целевое соединение /20/
т.пл.: 50-55oC
ИК (нуджол): 3250 /уширенный/, 1720, 1640, 1600 см-1
ЯМР (ДМСО-d6, δ): 2,4-3,1 /4Н, мультиплет/, 2,76 и 2,95 /3Н, каждый синглет/, 3,68 и 3,69 /3Н, каждый синглет/, 3,95 и 3,99 /2Н, каждый синглет/, 4,43 /1Н, мультиплет/, 4,6-5,3 /9Н, мультиплет/, 6,79 /2Н, мультиплет/, 6,99 /2Н, дублет, J= 8,9 Гц/, 7,08 /2Н, дублет, J=8,9 Гц/, 7,1-7,5 /15Н, мультиплет/, 7,95 /2Н, дублет, J=7,9 Гц/, 8,32 /1Н, мультиплет/, 8,53 /1Н, мультиплет/
Пример 21
Целевое соединение /21-А/ получили по методике, аналогичной методике Примера 1.
К смеси сырого исходного соединения /21-А/ /0,787 ммоль/ и анизола /1 мл/ добавили трифторуксусную кислоту /4 мл/ при комнатной температуре и перемешивали смесь при комнатной температуре в течение 1 ч. После выпаривания добавили к полученному веществу смесь 4 н. хлористоводородная кислота/диокса /5 мл/, затем смесь выпаривали в вакууме и растерли полученное вещество с диэтиловым эфиром, промыли диэтиловым эфиром, получив в результате целевое соединение /21-В/ /0,58 г/.
т.пл.: 105-110oC
ИК (нуджол): 1730, 1650 см-1
ЯМР (ДМСО-d6, δ): 0,80 /6Н, мультиплет/, 2,05 /1Н, мультиплет/, 2,65 и 2,75 /3Н, каждый синглет/, 2,6-2,9 /2Н, мультиплет/, 3,19 /2Н, мультиплет/, 3,6-4,4 /3Н, мультиплет/, 4,5-4,8 /2Н, мультиплет/, 5,09 /4Н, синглет/, 5,33 /2Н, синглет/, 7,2-7,6 /17Н, мультиплет/, 7,80 /2Н, дублет, J=8,0 Гц/, 8,17 и 8,36 /1Н, каждый дублет, J=8,1 Гц/, 8,2-8,8 /4Н, мультиплет/
Пример 22
К смеси 4-/4-(N-бензилоксикарбониламидино)-фенокси/масляной кислоты /1,18 г/, исходного соединения /22/ /2,00 г/ и 1-гидрокси-1Н-бензотиазола /0,51 г/ в N,N-диметилформамиде /30 мл/ при -20oC добавили 1-/3-диметиламинопропил/-3-этилкарбодиимид /0,61 мл/ и перемешивали смесь при комнатной температуре в течение 6 ч. Реакционную смесь вылили в смесь воды /300 мл/ и этилацетата /200 мл/, pH довели до 10,50 с помощью раствора гидроксида натрия. Отделенный органический слой промыли 0,5 н. хлористоводородной кислотой, насыщенным гидрокарбонатом натрия, водой и раствором соли и высушили над сульфатом магния. Полученный после фильтрации фильтрат выпарили в вакууме, осадок промыли диизопропиловым эфиром и получили целевое соединение /22/ /2,04 г/.
ИК (нуджол): 3300, 1730, 1650, 1600 см-1
ЯМР (ДМСО-d6, δ ): 1,92 /2Н, мультиплет/, 2,25 /2Н, триплет, J=6,4 Гц/, 2,54-2,78 /2Н, мультиплет/, 2,85-2,93 /2Н, мультиплет/, 4,01 /2Н, триплет, J=6,8 Гц/, 4,42 (1Н, мультиплет/, 4,70 /1Н, мультиплет/, 4,99 /2Н, синглет/, 5,03 /2Н, синглет/, 5,05 /2Н, синглет/, 5,10 /2Н, синглет/, 6,87 /2Н, дублет, J= 8,9 Гц/, 6,98 /2Н, дублет, J=8,6 Гц/, 7,08 /2Н, дублет, J=8,6 Гц/, 7,24-7,39 /20Н, мультиплет/, 7,98 /2Н, дублет, J=8,9 Гц/, 8,22 /1Н, дублет, J=8,1 Гц/, 8,31 /1Н, дублет, J=7,4 Гц/, 9,11 /2Н, широкий синглет/
МС (m/z): 905 /М+/
Следующие соединения /Примеры с 23 по 36/ были получены по методике, аналогичной методике Примера 22.
Пример 23
Целевое соединение /23/
ИК (нуджол): 3400, 1740, 1620, 1250 см-1
ЯМР (ДМСО-d6, δ): 1,92 /2Н, мультиплет/, 2,25 /2Н, триплет, J=6,4 Гц/, 2,54-2,78 /2Н, мультиплет/, 2,88-2,95 /2Н, мультиплет/, 3,60 /3Н, синглет/, 4,01 /2Н, триплет, J=6,8 Гц/, 4,45 /1Н, мультиплет/, 4,73 /1Н, мультиплет/, 4,79 /2Н, синглет/, 4,94 /2Н, синглет/, 5,10 /2Н, синглет/, 6,79 /2Н, дублет, J= 8,9 Гц/, 7,04 /2Н, дублет, J=8,6 Гц/, 7,08 /2Н, дублет, J=8,6 Гц/, 7,23-7,42 /15Н, мультиплет/, 7,99 /2Н, дублет, J=8,9 Гц/, 8,22 /1Н, дублет, J=8,1 Гц/, 8,31 /1Н, дублет, J=7,4 Гц/, 9,10 /2Н, широкий синглет/,
МС (m/z): 829 /М+ + 1/
Пример 24
Целевое соединение /24/
ИК (нуджол): 3400, 3300, 1730, 1700, 1650, 1250 см-1
ЯМР (ДМСО-d6, δ): 1,40-1,50 /4Н, мультиплет/2,08 /2Н, типа триплета/, 2,57 /2Н, типа триплета/, 2,66-2,76 /2Н, мультиплет/, 2,89-2,93 /2Н, мультиплет/, 3,69 /3Н, синглет/, 4,45 /1Н, мультиплет/, 4,41 /1Н, мультиплет/, 5,04 /2Н, синглет/, 5,10 /2Н, синглет/, 5,20 /2Н, синглет/, 6,78 /2Н, дублет, J= 8,9 Гц/, 7,07 /2Н, дублет, J=8,6 Гц/, 7,23-7,40 /17Н, мультиплет/, 7,91 /2Н, дублет, J=8,9 Гц/, 8,13 /1Н, дублет, J=8,1 Гц/, 8,26 /1Н, дублет, J=7,4 Гц/, 9,12 /2Н, широкий синглет/
Пример 25
Целевое соединение /25/
ИК (нуджол): 3300, 1740, 1700, 1650, 1600, 1250 см-1
ЯМР (ДМСО-d6, δ): 1,06-1,35 /4Н, мультиплет/, 1,39-1,51 /2Н, мультиплет/, 2,06 /2Н триплет, J=6,9 Гц/, 2,49-2,77 /2Н, мультиплет/, 2,85-2,93 /2Н, мультиплет/, 3,70 /3Н, синглет/, 3,99 /2Н, триплет, J=6,4 Гц/, 4,44 /1Н, мультиплет/, 4,71 /1Н, мультиплет/, 4,99 /2Н, синглет/, 5,01 /2Н, синглет/, 5,09 /2Н, синглет/, 6,78 /2Н, дублет, J=8,9 Гц/, 6,98 /2Н, дублет, J=8,6 Гц/, 7,07 /2Н, дублет, J=8,6 Гц/, 7,24-7,89 /15Н, мультиплет/, 7,97 /2Н, дублет, J=8,9 Гц/, 8,12 /1Н, дублет, J=8,1 Гц/, 8,25 /1Н, дублет, J=7,4 Гц/, 9,10 /2Н, широкий синглет/
МС (m/z): 857 /М+ + 1/
Пример 26
Целевое соединение /26/
ЯМР (ДМСО-d6, δ): 0,80 /3Н, дублет, J=6,0 Гц/, 0,85 /3Н, дублет, J=6,0 Гц/, 1,40-1,71 /7Н, мультиплет/, 1,99 /2Н, типа триплета/, 2,56-2,78 /4Н, мультиплет/, 4,30 /1Н, мультиплет/, 4,71 /1Н, мультиплет/, 5,04 /2Н, синглет/, 5,09 /2Н, синглет/, 5,10 /2Н, синглет/, 7,26-7,49 /17Н, мультиплет/, 7,91 /2Н, дублет, J=8,9 Гц/, 8,15 /1Н, дублет, J=8,1 Гц/, 8,30 /1Н, дублет, J=7,6 Гц/, 9,12 /2Н, широкий синглет/
МС (m/z): 763 /М+ + 1/
Пример 27
Целевое соединение /27/
ИК (нуджол): 3380, 3300, 1740, 1630, 1250 см-1
ЯМР (ДМСО-d6, δ): 1,87-2,02 /2Н, мультиплет/, 2,28 /2Н, триплет, J=7,0 Гц/, 2,64-2,83 /2Н, мультиплет/, 3,87 /2Н, дублет, J=6,5 Гц/, 4,02 /2Н, триплет, J=6,4 Гц/, 4,73 /1Н, мультиплет/, 5,06 /2Н, синглет/, 5,10 /2Н, синглет/, 5,11 /2Н, синглет/, 6,99 /2Н, дублет, J=8,9 Гц/, 7,31-7,37 /15Н, мультиплет/, 7,98 /2Н, дублет, J=8,9 Гц/, 8,27-8,34 /2Н, мультиплет/, 9,07 /2Н, широкий синглет/
МС (m/z): 709 /М+ + 1/
Пример 28
Целевое соединение /28/
ЯМР (ДМСО-d6, δ): 1,29 /3Н, дублет, J=7,3 Гц/, 1,92 /2Н, мультиплет/, 2,27 /2Н, триплет, J=7,3 Гц/, 2,55-2,78 /2Н, мультиплет/, 4,02 /2Н, триплет, J=6,3 Гц/, 4,31 /1Н, мультиплет/, 4,72 /1Н, мультиплет/, 5,05 /2Н, синглет/, 5,06 /2Н, синглет/, 5,10 /2Н, синглет/, 6,99 /2Н, дублет, J=8,9 Гц/, 7,34-7,40 /15Н, мультиплет/, 7,98 /2Н, дублет, J=8,9 Гц/, 8,24 /1Н, дублет, J=8,2 Гц/, 8,43 /1Н, дублет, J=7,2 Гц/, 9,10 /2Н, широкий синглет/
Пример 29
Целевое соединение /29/
ИК (нуджол): 3300, 1740, 1650, 1600, 1250 см-1
ЯМР (ДМСО-d6, δ): 1,88-1,99 /2Н, мультиплет/, 2,25 /2Н, триплет, J=7,1 Гц/, 2,52-2,60 /2Н, мультиплет/, 2,97-3,07 /2Н, мультиплет/, 4,03 /2Н, триплет, J=6,4 Гц/, 4,52 /1Н, мультиплет/, 4,73 /1Н, мультиплет/, 4,97 /2Н, синглет/, 4,99 /2Н, синглет/, 5,11 /2Н, синглет/, 6,99 /2Н, дублет, J=8,9 Гц/, 7,18-7,40 /20Н, мультиплет/, 8,00 /2Н, дублет, J=8,9 Гц/, 8,22 /1Н, дублет, J=8,1 Гц/, 8,36 /1Н, дублет, J=7,4 Гц/, 9,16 /2Н, широкий синглет/
МС (m/z): 799 /М++1/
Пример 30
Целевое соединение /30/
ИК (нуджол): 3300, 1740, 1650, 1600, 1250 см-1
ЯМР (ДМСО-d6, δ): 1,12 /3Н, триплет, J=7,1 Гц/, 1,56-1,64 /2Н, мультиплет/, 1,90-1,97 /2Н, мультиплет/, 2,18-2,30 /4Н, мультиплет/, 2,57-2,79 /4Н, мультиплет/, 3,90-4,06 /5Н, мультиплет/, 4,64 /1Н, мультиплет/, 5,06 /2Н, синглет/, 5,11 /2Н, синглет/, 7,00 /2Н, дублет, J=8,9 Гц/, 7,14-7,40 /15Н, мультиплет/, 7,68 /1Н, дублет, J=7,9 Гц/, 8,00 /2Н, дублет, J=8,9 Гц/, 8,16 /1Н, дублет, J=8,1 Гц/, 9,12 /2Н, широкий синглет/
МС (m/z): 765 /М++1/
Пример 31
Целевое соединение /31/
ЯМР (ДМСО-d6, δ): 0,68-0,95 /2Н, мультиплет/, 1,01-1,35 /5Н, мультиплет/, 1,39-1,61 /10Н, мультиплет/, 2,11 /2Н, типа триплета/, 2,60-2,75 /4Н, мультиплет/, 4,31 /1Н, мультиплет/, 4,71 /1Н, мультиплет/, 5,04 /2Н, синглет/, 5,07 /2Н, синглет/, 5,09 /2Н, синглет/, 7,26-7,37 /15Н, мультиплет/, 7,90 /2Н, дублет, J=8,9 Гц/, 8,15 /1Н, дублет, J=8,1 Гц/, 8,27 /1Н, дублет, J=7,4 Гц/, 9,11 /2Н, широкий синглет/
МС (m/z): 803 /М+/
Пример 32
Целевое соединение /32/
ЯМР (ДМСО-d6, δ): 0,84 /3Н, триплет, J=7,4 Гц/, 1,60-1,67 /2Н, мультиплет/, 1,95 /2Н, мультиплет/, 2,27 /2Н, триплет, J=6,4 Гц/, 2,57-2,80 /2Н, мультиплет/, 4,02 /2Н, триплет, J=6,8 Гц/, 4,20 /1Н, мультиплет/, 4,76 /1Н, мультиплет/, 5,00 /2Н, синглет/, 5,06 /2Н, синглет/, 5,07 /2Н, синглет/, 6,99 /2Н, дублет, J=8,9 Гц/, 7,24-7,44 /15Н, мультиплет/, 7,99 /2Н, дублет, J=8,9 Гц/, 8,25-8,29 /2Н, мультиплет/, 9,12 /2Н, широкий синглет/,
МС (m/z): 737 /М++1/
Пример 33
Целевое соединение /33/
ЯМР (ДМСО-d6, δ): 0,82 /3Н, триплет, J=7,3 Гц/, 1,23-1,34 /2Н, мультиплет/, 1,64 /2Н, мультиплет/, 1,92-2,10 /2Н, мультиплет/, 2,24 /2Н, триплет, J= 6,4 Гц/, 2,56-2,78 /2Н, мультиплет/, 4,05 /2Н, триплет, J=6,8 Гц/, 4,25 /1Н, мультиплет/, 4,72 /1Н, мультиплет/, 5,05 /2Н, синглет/, 5,06 /2Н, синглет/, 5,09 /2Н, синглет/, 6,99 /2Н, дублет, J=8,9 Гц/, 7,31-7,40 /15Н, мультиплет/, 7,98 /2Н, дублет, J=8,9 Гц/, 8,25 /1Н, дублет, J=8,0 Гц/, 8,32 /1Н, дублет, J=7,4 Гц/, 9,10 /2Н, широкий синглет/
Пример 34
Целевое соединение /34/
ЯМР (ДМСО-d6, δ): 0,62-0,97 /2Н, мультиплет/, 1,01-1,18 /5Н, мультиплет/, 1,42-1,69 /6Н, мультиплет/, 1,94 /2Н, мультиплет/, 2,24 /2Н, триплет, J= 6,4 Гц/, 2,56-2,76 /2Н, мультиплет/, 4,02 /2Н, триплет, J=6,8 Гц/, 4,32 /1Н, мультиплет/, 4,72 /1Н, мультиплет/, 5,05 /2Н, синглет/, 5,06 /2Н, синглет/, 5,08 /2Н, синглет/, 6,98 /2Н, дублет, J=8,9 Гц/, 7,23-7,39 /15Н, мультиплет/, 7,98 /2Н, дублет, J=8,9 Гц/, 8,23-8,38 /2Н, мультиплет/, 9,13 /2Н, широкий синглет/
МС (m/z): 805 /М++1/
Пример 35
Целевое соединение /35/
ЯМР (ДМСО-d6, δ): 2,52-2,98 /3Н, мультиплет/, 2,90 /3Н, синглет/, 3,70 /3Н, синглет/, 3,92 /2Н, мультиплет/, 4,43 /1Н, мультиплет/, 4,72 /1Н, мультиплет/, 5,04 /2Н, синглет/, 5,07 /2Н, синглет/, 5,10 /2Н, синглет/, 6,77 /1Н, мультиплет/, 7,09 /2Н, мультиплет/, 7,26-7,37 /19Н, мультиплет/, 7,82-7,95 /1Н, мультиплет/, 8,22-8,56 /1Н, мультиплет/, 9,18 /2Н, широкий синглет/
Пример 36
Целевое соединение /36/
ЯМР (ДМСО-d6, δ): 0,72-0,98 /2Н, мультиплет/, 1,01-1,38 /5Н, мультиплет/, 1,41-1,68 /6Н, мультиплет/, 2,60-2,88 /2Н, мультиплет/, 2,77 /3Н, синглет/, 3,98 /2Н, мультиплет/, 4,29 /1Н, мультиплет/, 4,80 /1Н, мультиплет/, 5,05 /2Н, синглет/, 5,06 /2Н, синглет/, 5,06 /2Н, синглет/, 5,09 /2Н, синглет/, 6,99 /2Н, дублет, J=8,9 Гц/, 7,33-7,37 /15Н, мультиплет/, 7,95 /2Н, дублет, J= 8,9 Гц/, 8,28-8,33 /1Н, мультиплет/, 8,46-8,60 /1Н, мультиплет/, 9,12 /2Н, широкий синглет/
МС (m/z): 848 /М++1/
Пример 37
Смесь исходного соединения /37/ /1,70 г/ и 10% Pd-C /0,80 г/ в смесь 1N хлористоводородной кислоты /2,25 мл/ и тетрагидрофурана /20 мл/ перемешивали в атмосфере H2 при комнатной температуре в течение 6 ч. После фильтрации фильтрат выпарили в вакууме. Конечное вещество промыли изотоническим раствором хлорида натрия и выделили целевое соединение /37/ /0,60 г/.
т.пл.: 180-183oC
ИК (нуджол): 3250, 1670, 1640, 1600, 1260 см-1
ЯМР (ДМСО-d6, δ): 1,94 /2Н, мультиплет/, 2,27 /2Н, типа триплета/, 2,63-2,72 /2Н, мультиплет/, 2,80-2,87 /2Н, мультиплет/, 4,08 /2Н, типа триплета/, 4,30 /1Н, мультиплет/, 4,62 /1Н, мультиплет/, 6,66 /2Н, дублет, J=8,9 Гц/, 6,97 /2Н, дублет, J=8,6 Гц/, 7,14 /2Н, дублет, J=8,6 Гц/, 7,85 /3Н, мультиплет/, 8,25 /1Н, дублет, J=7,4 Гц/, 9,05 /2Н, синглет/, 9,25 /3Н, мультиплет/, 12,51 /2Н, широкий синглет/
МС (m/z): 501 /М+/
Следующие соединения /Примеры 38 - 41/ получили по методике, аналогичной описанной в Примере 37.
Пример 38
Целевое соединение /38/
т.пл.: 204-206oC
ИК (нуджол): 3350, 3300, 1670, 1640, 1540, 1260 см-1
ЯМР (ДМСО-d6, δ): 1,94 /2Н, мультиплет/, 2,31 /2Н, триплет, J=6,4 Гц/, 2,45-2,62 /2Н, мультиплет/, 2,79-2,96 /2Н, мультиплет/, 3,70 /3Н, синглет/, 4,08 /2Н, триплет, J=6,8 Гц/, 4,35 /1Н, мультиплет/, 4,61 /1Н, мультиплет/, 6,81 /2Н, дублет, J= 8,9 Гц/, 7,10-7,16 /4Н, мультиплет/, 7,84-7,93 /3Н, мультиплет/, 8,26 /1Н, дублет, J= 7,8 Гц/, 9,09 /2Н, синглет/, 9,27 /2Н, синглет/, 12,00 /2Н, широкий синглет/
МС (m/z): 515 /М+/
Пример 39
Целевое соединение /39/
т.пл.: 163oC /разл./
ИК (нуджол): 3270, 1700, 1665, 1630, 1605, 1535, 1480 см-1
ЯМР (ДМСО-d6, δ): 0,84 /6Н, дублет, J=6,1 Гц/, 1,29-1,85 /6Н, мультиплет/, 1,91-2,23 /3Н, мультиплет/, 2,35-2,78 /2Н, мультиплет/, 3,98-4,2 /3Н, мультиплет/, 4,55-4,73 /1Н, мультиплет/, 7,14 /2Н, дублет, J=8,9 Гц/, 7,72 /1Н, дублет, J=8,7 Гц/, 7,83 /2Н, дублет, J=8,9 Гц/, 8,25 /1Н, дублет, J=7,7 Гц/, 8,94 /2Н, синглет/, 9,20 /2Н, синглет/
Элементный анализ C22H32N4O7•HCl•1H2O
Вычислено: C 50,91, H 6,79, N 10,79, Cl 6,83
Найдено: C 51,14, H 6,81, N 10,74, Cl 6,37
Пример 40
Целевое соединение /40/
ИК (нуджол): 3300, /широкая/, 1720, 1650 см-1
ЯМР (ДМСО-d6, δ): 0,83 /6Н, дублет, J=6,7 Гц/, 1,35-1,7 /4Н, мультиплет/, 1,9-2,25 /3Н, мультиплет/, 2,33-2,8 /4Н, мультиплет/, 4,03-4,2 /1Н, мультиплет/, 4,5-4,7 /1Н, мультиплет/, 7,44 /2Н, дублет, J=8,2 Гц/, 7,75 /1Н, дублет, J=8,3 Гц/, 7,77 /2Н, дублет, J=8,2 Гц/, 8,28 /1Н, дублет, =7,7 Гц/, 9,16 /2Н, синглет/, 9,34 /2Н, синглет/,
Пример 41
Целевое соединение /41/
т.пл.: 87-90oC
ИК (нуджол): 3200 /широкая/, 1640, 1595, 1530 см-1
ЯМР (ДМСО-d6, δ): 2,4-3,1 /4Н, мультиплет/, 2,77 и 2,97 /3Н, каждый синглет/, 3,69 и 3,70 /3Н, каждый синглет/, 3,96 и 4,02 /2Н, каждый синглет/, 4,33 /1Н, мультиплет/, 4,65 /1Н, мультиплет/, 4,93 и 5,06 /2Н, каждый синглет/, 6,82 /2Н, мультиплет/, 7,12 /4Н, дублет, J=8,8 Гц/, 7,80 /2Н, дублет, J=8,8 Гц/, 7,95 и 8,17 /1Н, каждый дублет, каждый J=7,7 Гц/, 8,28 и 8,59 /1Н, каждый дублет, каждый J=8,2 Гц/, 9,02 и 9,22 /4Н, каждый синглет/
МС (m/z): 558 /М++1/
Следующие соединения /Примеры 42 - 58/ получили по методике, аналогичной описанной в Примере 5
Пример 42
Целевое соединение /42/
т.пл.: 200-202oC
ИК (нуджол): 3300, 1640, 1270 см-1
ЯМР (ДМСО-d6, δ): 1,06-1,35 /4Н, мультиплет/, 1,39-1,51 /2Н, мультиплет/, 2,06 /2Н, триплет, J=6,9 Гц/, 2,49-2,77 /2Н, мультиплет/, 2,84-2,94 /2Н, мультиплет/, 3,70 /3Н, синглет/, 4,04 /2Н, триплет, J=6,4 Гц/, 4,38 /1Н, мультиплет/, 4,62 /1Н, мультиплет/, 6,80 /2Н, дублет, J=8,9 Гц/, 7,05-7,20 /4Н, мультиплет/, 7,76 /2Н, мультиплет/, 8,15 /1Н, дублет, J=7,4 Гц/, 8,91-9,80 /1Н, широкий синглет/, 9,10-9,21 /2Н, широкий синглет/
МС (M/z): 543 /М++1/
Пример 43
Целевое соединение /43/
т.пл.: 205-207oC
ИК (нуджол): 3280, 1640, 1550, 1210 см-1
ЯМР (ДМСО-d6, δ): 1,39-1,62 /4Н, мультиплет/, 2,10 /2Н, триплет, J=6,5 Гц/, 2,40-2,62 /2Н, мультиплет/, 2,64 /2Н, триплетоподобный/, 2,77-2,97 /2Н, мультиплет/, 3,71 /3Н, синглет/, 4,39 /1Н, мультиплет/, 4,58 /1Н, мультиплет/, 6,80 /2Н, дублет, J= 8,9 Гц/, 7,10 /2Н, дублет, J=8,6 Гц/, 7,43 /2Н, дублет, J=8,8 Гц/, 7,73 /2Н, дублет, J=8,9 Гц/, 7,83 /1Н, дублет, J=7,7 Гц/, 8,10 /1Н, дублет, J=8,0 Гц/, 9,18 /2Н, синглет/, 9,23 /2Н, синглет/, 12,54 /2Н, широкий синглет/
МС (m/z): 513 /М++1/
Пример 44
Целевое соединение /44/
т.пл.: ≈150oC /разлаг./
ИК (нуджол): 3300, 3100, 1720, 1670, 1610, 1540 см-1
ЯМР (ДМСО-d6, δ): 1,51-1,84 /4Н, мультиплет/, 2,16 /2Н, триплетоподобный/, 2,31-3,0 /4Н, мультиплет/, 3,58 /3Н, синглет/, 4,08 /2Н, триплетоподобный/, 4,35 /1Н, мультиплет/, 4,61 /1Н, мультиплет/, 6,66 /2Н, дублет, J= 8,4 Гц/, 6,97 /2Н, дублет, J=8,4 Гц/, 7,15 /2Н, дублет, J=8,9 Гц/, 7,82 /2Н, дублет, J=8,8 Гц/, 8,06 /1Н, дублет, J=7,4 Гц/, 8,13 /1Н, дублет, J=7,9 Гц/, 9,08 /2Н, синглет/, 9,14 /2Н, синглет/
МС (m/z): 529 /М++1/
Пример 45
Целевое соединение /45/
т.пл.: 208oC /разлаг./
ИК (нуджол): 3280, 3090, 1730, 1705, 1660, 1640, 1605, 1540 см-1
ЯМР (ДМСО-d6, δ): 1,51-1,96 /4Н, мультиплет/, 2,15 /2Н, триплетоподобный/, 2,32-3,0 /4Н, мультиплет/, 3,58 /3Н, синглет/, 3,70 /3Н, синглет/, 4,07 /2Н, триплетоподобный/, 4,38 /1Н, мультиплет/, 4,60 /1Н, мультиплет/, 6,82 /2Н, дублет, J=8,6 Гц/, 7,10 /2Н, дублет, J=8,6 Гц/, 7,15 /2Н, дублет, J=8,9 Гц/, 7,81 /2Н, дублет, J=8,9 Гц/, 8,11 /2Н, мультиплет/, 9,04 /2Н, синглет/, 9,14 /2Н, синглет/
МС (m/z): 543 /М++1/
Пример 46
Целевое соединение /46/
т.пл.: 173oC /разл./
ИК (нуджол): 3275, 1680, 1620, 1600, 1540 см-1
ЯМР (ДМСО-d6+TFA, δ): 1,5-1,8 /4Н, мультиплет/, 2,14 /2Н, триплетоподобный/, 2,25-3,10 /4Н, мультиплет/, 3,69 /3Н, синглет/, 4,05 /2Н, триплетоподобный/, 4,32 /1Н, мультиплет/, 4,59 /1Н, мультиплет/, 6,80 /2Н, дублет, J= 8,6 Гц/, 7,09 /2Н, дублет, J=8,6 Гц/, 7,13 /2Н, дублет, J=8,9 Гц/, 7,79 /2Н, дублет, J=8,9 Гц/, 7,85 /1Н, дублет, J=7,7 Гц/, 8,11 /1Н, дублет, J=7,9 Гц/, 8,90 /2Н, синглет/, 9,11 /2Н, синглет/
МС (m/z): 529 /М++1/
Пример 47
Целевое соединение /47/
т.пл.: 162-164oC
ИК (нуджол): 3300, 3100, 1660, 1270, 1200 см-1
ЯМР (ДМСО-d6, δ): 1,93-2,00 /2Н, мультиплет/, 2,31 /2Н, триплет, J=7,1 Гц/, 2,64-2,75 /2Н, мультиплет/, 3,73 /2Н, дублет, J=5,7 Гц/, 4,10 /2Н, триплет, J=6,5 Гц/, 4,64 /1Н, мультиплет/, 7,15 /2Н, дублет, J=8,9 Гц/, 7,81 /2Н, дублет, J=8,9 Гц/, 8,10 /1Н, триплет, J=5,7 Гц/, 8,23 /1Н, дублет, J= 8,1 Гц/, 9,01 /2Н, синглет/, 9,14 /2Н, синглет/
МС (m/z): 395 /М++1/
Пример 48
Целевое соединение /48/
т.пл.: 160-162oC
ИК (нуджол): 3300, 1670, 1600, 1270, 1200 см-1
ЯМР (ДМСО-d6, δ ): 1,25 /3Н, дублет, J=7,3 Гц/, 1,95 /2Н, мультиплет/, 2,29 /2Н, триплет, J=7,1 Гц/, 2,42-2,72 /2Н, мультиплет/, 4,09 /2Н, триплет, J= 6,4 Гц/, 4,14 /1Н, мультиплет/, 4,62 /1Н, мультиплет/, 7,15 /2Н, дублет, J= 8,9 Гц/, 7,81 /2Н, дублет, J=8,9 Гц/, 8,12 /1Н, дублет, J=7,3 Гц/, 8,19 /1Н, дублет, J=7,9 Гц/, 8,99 /2Н, синглет/, 9,14 /2Н, синглет/
МС (m/z): 409 /М++1/
Пример 49
Целевое соединение /49/
т.пл.: 118-120oC
ИК (нуджол): 3280, 1650, 1600, 1540 см-1
ЯМР (ДМСО-d6, δ): 1,70 /4Н, широкий синглет/, 2,19 /2Н, мультиплет/, 2,2-2,6 /1Н, мультиплет/, 2,70 /1Н, двойной дублет, J=16,6 Гц, J=5,0 Гц/, 3,67 /2Н, мультиплет/, 4,08 /2Н, широкий синглет/, 4,22 /1Н, мультиплет/, 4,65 /1Н, мультиплет/, 7,15 /2Н, дублет, J=8,9 Гц/, 7,7-7,9 /3Н, мультиплет/, 8,19 /1Н, дублет, J=7,8 Гц/, 9,00 и 9,14 /4Н, каждый синглет/
МС (M/z): 439 /М++1/
Пример 50
Целевое соединение /50/
т.пл.: 207-209oC
ИК (нуджол): 3300, 1720, 1640, 1270, 1200 см-1
ЯМР (ДМСО-d6, δ): 1,83-2,02 /2Н, мультиплет/, 2,25 /2Н, триплет, J=7,0 Гц/, 2,34-2,68 /2Н, мультиплет/, 2,92-3,02 /2Н, мультиплет/, 4,07 /2Н, триплет, J=6,3 Гц/, 4,38 /1Н, мультиплет/, 4,62 /1Н, мультиплет/, 7,12-7,26 /7Н, мультиплет/, 7,80 /2Н, дублет, J=8,9 Гц/, 7,94 /1Н, дублет, J=7,6 Гц/, 8,17 /1Н, дублет, J=7,9 Гц/, 8,90 /2Н, синглет/, 9,12 /2Н, синглет/, 12,55 /2Н, широкий синглет/
МС (m/z): 485 /М++1/
Пример 51
Целевое соединение /51/
т.пл.: 172-175oC
ИК (нуджол): 3300, 3100, 1660, 1550, 1200 см-1
ЯМР (ДМСО-d6, δ): 0,80 /3Н, дублет, J=6,2 Гц/, 0,85 /3Н, дублет, J=6,2 Гц/, 1,41-1,65 /7Н, мультиплет/, 2,13 /2Н, триплет, J=6,2 Гц/, 2,40-2,71 /4Н, мультиплет/, 4,16 /1Н, мультиплет/, 4,58 /1Н, мультиплет/, 7,44 /2Н, дублет, J=8,9 Гц/, 7,74 /2Н, дублет, J=8,9 Гц/, 7,97 /1Н, дублет, J=8,0 Гц/, 8,11 /1Н, дублет, J=7,9 Гц/, 9,13 /2Н, синглет/, 9,23 /2Н, синглет/
МС (M/z): 449 /М++1/
Пример 52
Целевое соединение /52/
т.пл.: 177-180oC
ЯМР (нуджол): 0,84 /3Н, триплет, J=7,4 Гц/, 1,26-1,34 /2Н, мультиплет/, 1,57-1,65 /2Н, мультиплет/, 1,90-2,10 /2Н, мультиплет/, 2,27 /2Н, триплет, J=6,5 Гц/, 2,51-2,70 /2Н, мультиплет/, 4,06-4,16 /3Н, мультиплет/, 4,63 /1Н, мультиплет/, 7,14 /2Н, дублет, J=8,9 Гц/, 7,80 /2Н, дублет, J=8,9 Гц/, 7,99 /1Н, дублет, J= 7,8 Гц/, 8,20 /1Н, дублет, J=7,9 Гц/, 8,87 /2Н, синглет/, 9,13 /2Н, синглет/, 12,4 /2Н, широкий синглет/
МС (m/z): 437 /М++1/
Пример 53
Целевое соединение /53/
т.пл.: 217-219oC
ЯМР (ДМСО-d6, δ): 0,71-0,98 /2Н, мультиплет/, 1,01-1,39 /5Н, мультиплет/, 1,47-1,71 /6Н, мультиплет/, 1,97 /2Н, мультиплет/, 2,25 /2Н, триплет, J=6,4 /, 2,62-2,70 /2Н, мультиплет/, 4,09 /2Н, триплет, J=6,8 Гц/, 4,21 /1Н, мультиплет/ 4,62 /1Н, мультиплет/, 7,14 /2Н, дублет, J=8,9 Гц/, 7,80 /2Н, дублет, J=8,9 Гц/, 7,99 /1Н, дублет, J=7,9 Гц/, 8,20 /1Н, дублет, J=7,9 Гц/, 8,95 /2Н, синглет/, 9,13 /2Н, синглет/, 12,43 /2Н, широкий синглет/
МС (m/z): 491 /М++1/
Пример 54
Целевое соединение /54/
т.пл.: 220-221oC
ИК (нуджол): 3300, 1670, 1650, 1250, см-1
ЯМР (ДМСО-d6, δ): 1,45-1,79 /2Н, мультиплет/, 1,92-2,01 /2Н, мультиплет/, 2,10-2,29 /4Н, мультиплет/, 2,37-2,68 /4Н, мультиплет/, 3,88 /1Н, мультиплет/, 4,09 /2Н, триплет, J=6,4 Гц/, 4,52 /1Н, мультиплет/, 7,12-7,24 /7Н, мультиплет/, 7,71 /1Н, дублет, J=8,5 Гц/, 7,81 /2Н, дублет, J=8,9 Гц/, 8,09 /1Н, дублет, J=7,9 Гц/, 8,99 /2Н, синглет/, 9,13 /2Н, синглет/, 12,13 /2Н, широкий синглет/
МС (m/z): 513 /М++1/
Пример 55
т.пл.: 186-188oC
ИК (нуджол): 3300, 1670, 1210 см-1
ЯМР (ДМСО-d6, δ): 0,72-0,98 /2Н, мультиплет/, 1,05-1,18 /5Н, мультиплет/, 1,39-1,71 /10Н, мультиплет/, 2,13 /2Н, типа триплета/, 2,61-2,71 /4Н, мультиплет/, 4,19 /1Н, мультиплет/, 4,59 /1Н, мультиплет/, 7,44 /2Н, дублет, J= 8,9 Гц/, 7,73 /2Н, дублет, J=8,9 Гц/, 7,95 /1Н, дублет, J=7,9 Гц/, 8,11 /1Н, дублет, J=7,9 Гц/, 9.07 /2Н, синглет/, 9,23 /2Н, синглет/, 12,43 /2Н, широкий синглет/
МС (m/z): 489 /М++1/
Пример 56
Целевое соединение /56/
т.пл.: 65-73oC
ИК (нуджол): 3270 /широкая/, 1650, 1610, 1510 см-1
ЯМР (ДМСО-d6, δ): 2,3-3,1 /4Н, мультиплет/, 2,78 и 2,98 /3Н, каждый синглет/, 3,56 /3Н, синглет/, 3,70 /3Н, синглет/ 3,96 и 4,02 /2Н, каждый синглет/, 4,37 /1Н, мультиплет/, 4,65 /1Н, мультиплет/, 4,93 и 5,05 /2Н, каждый синглет/, 6,82 /2Н, мультиплет/, 7,12 /4Н, мультиплет/, 7,77 /2Н, дублет, J=8,3 Гц/, 8,14 и 8,23 /1Н, каждый дублет, J=7,3 Гц (на 8,14), J=8,0 Гц /на 8,23), 8,37 и 8,53 /1Н, каждый дублет, J=7,6 Гц (на 8,37), J=8,0 Гц (на 8,53), 9,00 и 9,13 /4Н, каждый синглет/
Пример 57
Целевое соединение /57/
т.пл.: 90-92oC /разл./
ИК (нуджол): 1650, 1300, 1250 см-1
ЯМР (ДМСО-d6, δ): 2,58-2,98 /8Н, мультиплет/, 2,75 /3Н, синглет/, 3,71 /3Н, синглет/, 3,94 /2Н, мультиплет/, 4,32 /1Н, мультиплет/, 4,62 /1Н, мультиплет/, 6,81 /2Н, мультиплет/, 7,12 /2Н, мультиплет/, 7,47 /2Н, мультиплет/, 7,71 /2Н, мультиплет/, 7,90-8,18 /1Н, мультиплет/, 8,07-8,32 /1Н, мультиплет/, 9,94 /2Н, синглет/, 9,22 /2Н, синглет/
МС (m/z): 556 /М++1/
Пример 58
Целевое соединение /58/
т.пл.: 95-98oC
ИК (нуджол): 3300, 1650, 1250 см-1
ЯМР (ДМСО-d6, δ): 0,73-1,00 /2Н, мультиплет/, 1,01-1,39 /5Н, мультиплет/, 1,42-1,69 /6Н, мультиплет/, 2,63-3,02 /2Н, мультиплет/, 2,79 /3Н, синглет/, 4,00 /1Н, синглет/, 4,04 /1Н, синглет/, 4,22 /1Н, мультиплет/, 4,65 /1Н, мультиплет/, 4,94 /1Н, синглет/, 5,04 /1Н, синглет/, 7,13 /2Н, дублет, J=8,9 Гц/, 7,77 /2Н, дублет, J=8,9 Гц/, 8,00-8,18 /1Н, мультиплет/, 8,19-8,56 /1Н, мультиплет/, 8,86 /2Н, синглет/, 9,12 /2Н, синглет/
МС (m/z): 534 /М++1/
Пример 59
Целевое соединение /59-А/ получили аналогично методике Примера 5.
Лиофилизировали смесь этого целевого соединения /59-А/ и 1 н. хлористоводородной кислоты /200 мл/. Высушили полученный порошок, что дало целевое соединение /59-В/ /5,33 г/.
т.пл.: 198oC /разлаг./
ИК (нуджол): 3270, 1690, 1635, 1600, 1540 см-1
ЯМР (ДМСО-d6, δ): 0,84 /6Н, дублет, J=6,4 Гц/, 1,8-2,05 /3Н, мультиплет/, 2,3 /2Н, триплет, J=7 Гц/, 2,3-2,8 /2Н, мультиплет/, 3,97-4,22 /3Н, мультиплет/, 4,65 /1Н, мультиплет/, 7,14 /2Н, дублет, J=8,9 Гц/, 7,8 /1Н, дублет, J=8,5 Гц/, 7,85 /2Н, дублет, J=8,9 Гц/, 8,35 /1Н, дублет, J=7,7 Гц/, 9,04 /2Н, синглет/, 9,24 /2Н, синглет/, 12,51 /1Н, широкий синглет/
Элементный анализ: C20H28N4O7•HCl•1H2O
Вычислено: C 48,93 H 6,36 N 11,41 Cl 7,22
Найдено: C 48,77 H 6,52 N 11,22 Cl 6,98
Пример 60
Смесь исходного соединения /60/ /0,7 г/ в тетрагидрофуране /3,5 мл/ и 1 н. водного раствора гидроксида натрия /3,49 мл/ перемешивали при комнатной температуре в течение 2 ч. Реакционную смесь довели до pH 5,0, добавляя 10% хлористоводородную кислоту, и собрали образовавшийся осадок фильтрацией, получив целевое соединение /60/ /0,5 г/.
т.пл.: 220oC /разлаг./
ИК (нуджол): 3280, 1650, 1605, 1550, 1490 см-1
ЯМР (ДМСО-d6 + TFA, δ): 1,5-1,85 /4Н, мультиплет/, 2,19 /2Н, триплетоподобный/, 2,3-3,0 /4Н, мультиплет/, 4,08 /2Н, триплетоподобный/, 4,31 /1Н, мультиплет/, 4,61 /1Н, мультиплет/, 6,65 /2Н, дублет, J=8,4 Гц/, 6,97 /2Н, дублет, J=8,4 Гц/, 7,15 /2Н, дублет, J=8,9 Гц/, 7,81 /2Н, дублет, J=8,8 Гц/, 7,83 /1Н, дублет, J=7,8 Гц/, 8,15 /1Н, дублет, J=8 Гц/, 8,98 /2Н, синглет/, 9,13 /2Н, синглет/
МС /m/z/: 515 /М++1/
Элементный анализ: C25H30N4O8•2H2O
Вычислено: C 54,53 H 6,22 N 10,17
Найдено: C 54,32 H 6,04 N 10,08
Пример 61
К раствору исходного соединения /61/ /0,53 г/ и триэтиламина /0,20 мл/ в метиленхлориде /5 мл/ добавили уксусный ангидрид /0,066 мл/ при охлаждении льдом, и смесь перемешивали при комнатной температуре в течение 4 ч. Реакционную смесь разбавили водой и экстрагировали этилацетатом, отделенный органический слой промыли разбавленной хлористоводородной кислотой, насыщенным водным раствором бикарбоната натрия, водой и раствором соли, высушили над сульфатом магния и выпарили в вакууме, что дало целевое соединение /61-А/ /сырое/ /это соединение не выделяли/.
Из указанного соединения /61-А/ получили следующее целевое соединение /61-В/ по методике, аналогичной методике Примера 5.
т.пл.: 86-94oC
ИК (нуджол): 1640 /широкий синглет/, 1530 см-1
ЯМР (ДМСО-d6, δ): 0,86 /6Н, мультиплет/, 1,71 и 1,76 /3Н, каждый синглет/, 2,04 /1Н, мультиплет/, 2,80 и 3,03 /3Н, каждый синглет/, 2,4-3,2 /4Н, мультиплет/, 3,8-5,1 /5Н, мультиплет/, 7,49 /2Н, мультиплет/, 7,72 /2Н, мультиплет/, 7,6-8,6 /3Н, мультиплет/, 9,15 и 9,26 /4Н, каждый синглет/
МС (m/z): 535 /М++1/
Условия проведения ВЭЖХ
колонка: МС-РАСК P-ODS-15 S-15 120A ODS 50 ϕ х 250
элюирование: CH3CN : 0,1% трифторуксусная кислота /15:85/
поток: 118 мл/мин
время удерживания: 7,6 минут
Пример 62
Целевое соединение /62/ получили из исходного соединения /62/ по методике, аналогичной методике Примеров 37 и 13,
т.пл.: 175-177oC /разлаг./
ИК (нуджол): 3300, 1640, 1600, 1260 см-1
ЯМР (ДМСО-d6, δ): 0,75 /3Н, триплет, J=7,2 Гц/, 1,60-1,72 /2Н, мультиплет/, 1,94 /2Н, мультиплет/, 2,31 /2Н, триплетоподобный/, 2,60-2,68 /2Н, мультиплет/, 3,90 /1Н, мультиплет, 4,07 /2Н, триплетоподобный/, 4,56 /1Н, мультиплет/, 7,09 /2Н, дублет, J=8,9 Гц/, 7,56 /1Н, дублет, J=6,6 Гц/, 7,72 /2Н, дублет, J=8,9 Гц/, 8,38 /1Н, дублет, J=7,6 Гц/, 8,75 /2Н, широкий синглет/, 11,18 /2Н, широкий синглет/
МС (m/z): 423 /М++1/
Пример 63
Целевое соединение /63/ получили из исходных соединений /63-А/ и /63-В/ по методике, аналогичной методике Примера 22.
ИК (нуджол): 3300, 1720, 1640, 1250 см-1
ЯМР (ДМСО-d6, δ): 1,91 /2Н, мультиплет/, 2,24 /2Н, триплет, J=7,1 Гц/, 2,73-2,96 /2Н, мультиплет/, 3,11-3,15 /2Н, мультиплет/, 3,57 /3Н, синглет/, 3,98-4,04 /3Н, мультиплет/, 4,65-4,72 /1Н, мультиплет/, 5,06 /2Н, синглет/, 5,11 /2Н, синглет/, 6,99 /2Н, дублет, J=8,9 Гц/, 7,18-7,26 /2Н, мультиплет/, 7,34-7,40 /10Н, мультиплет/, 7,64-7,72 /1Н, мультиплет/, 7,99 /2Н, дублет, J= 8,9 Гц/, 8,24 /1Н, дублет, J=8,1 Гц/, 8,37 /1Н, дублет, J=7,6 Гц/, 8,46 /1Н, дублет, J=4,0 Гц/, 9,15 /2Н, широкий синглет/
МС (m/z): 724 /М++1/
Пример 64
Целевое соединение /64/ получили аналогично методике Примера 5.
т.пл.: 120-125oC
ИК (нуджол): 3300, 1740, 1660, 1200 см-1
ЯМР (ДМСО-d6, δ): 1,91 /2Н, мультиплет/, 2,28 /2Н, триплет, J=7,2 Гц/, 2,53-2,67 /2Н, мультиплет/, 3,20-3,33 /2Н, мультиплет/, 3,60 /3Н, синглет/, 4,07 /2Н, триплет, J=6,4 Гц/, 4,55 /1Н, мультиплет/, 4,72 /1Н, мультиплет/, 7,14 /21, дублет, J=8,9 Гц/, 7,55 /2Н, дублет, J=7,8 Гц/, 7,82 /2Н, дублет, J= 8,9 Гц/, 8,02 /1Н, мультиплет/, 8,19 /1Н, дублет, J=7,8 Гц/, 8,40 /1Н, дублет, J= 7,8 Гц/, 8,63 /1Н, дублет, J=4,9 Гц/, 9,13 /2Н, синглет/, 9,16 /2Н, синглет/
МС (m/z): 500 /М++1
Пример 65
Целевое соединение (65-А) получили из исходного соединения (65-А) и исходного соединения (65-В) по методике, аналогичной описанной в Примере 1.
Целевое соединение (65-В) получили из полученного таким образом целевого соединения (65-А) по методике, аналогичной описанной в Примере 5.
т.пл.: 50-54oC (разлаг.)
ИК (нуджол): 1640 (br), 1520 см-1
ЯМР (ДМСО-d6, δ): 0,84 (6Н, мультиплет), 2,07 (1Н, мультиплет), 2,4-2,8 (2Н, мультиплет), 2,79 и 3,00 (каждый - синглет), 3,8-4,2 (3Н, мультиплет), 4,7 (1Н, мультиплет), 4,94 и 5,06 ) (2Н, каждый - синглет), 7,13 (2Н, дублет, J=7,4 Гц), 7,78 (2Н, дублет, J=7,4 Гц), 7,78 и 8,05 (1Н, каждый дублет, каждый J= 8,8 Гц), 8,27 и 8,57 (1Н, каждый дублет, каждый J=8,0 Гц), 9,00 и 9,13 (4Н, каждый синглет).
Пример 66
Целевое соединение (66-А) получили из исходного соединения (66-А) и исходного соединения (66-В) по методике, аналогичной описанной в Примере 1.
Целевое соединение (66-В) получили из полученного таким образом целевого соединения (66-А) по методике, аналогичной описанной в Примере 5.
т.пл.: 67-72oC
ИК (нуджол): 1640 (br), 1530 см-1
ЯМР (ДМСО-d6, δ): 0,86 (6Н, мультиплет), 2,05 (1Н, мультиплет), 2,3-2,8 (2Н, мультиплет), 2,82 и 3,03 (3Н, каждый синглет), 3,74 и 3,89 (2Н, каждый синглет), 3,8-4,2 (3Н, мультиплет), 4,68 (1Н, мультиплет), 7,4 (2Н, мультиплет), 7,7 (2Н, мультиплет), 7,8 и 7,97 (1Н, мультиплет и дублет (J=8,5 Гц)), 8,3 и 8,52 (1Н, каждый дублет, J=7,9 Гц), 9,24 и 9,28 (4Н, каждый синглет)
МС (m/z): 464 (М++1/
Пример 67
Целевое соединение (67-А) получили из исходного соединения (67-А) и исходного соединения (67-В) по методике, аналогичной описанной в Примере 1.
Целевое соединение (67-В) получили из полученного таким образом целевого соединения (67-А) по методике, аналогичной описанной в Примере 5.
т.пл.: 52-56oC
ИК (нуджол): 1660 (br), 1540 см-1
ЯМР (ДМСО-d6, δ): 0,85 (6Н, мультиплет), 2,05 (1Н, мультиплет), 2,4-3,0 (6Н, мультиплет), 2,78 и 2,96 (3Н, каждый - синглет), 3,9-4,2 (3Н, мультиплет), 4,66 (1Н, мультиплет), 7,48 (2Н, мультиплет), 7,71 (2Н, мультиплет), 7,7 и 7,92 (1Н, мультиплет и дублет (J=8,56 Гц), 8,28 и 8,46 (1Н, каждый - дублет, J=7,9 Гц)), 9,15 и 9,24 (4Н, каждый синглет)
МС (m/z): 478 (М++1)
Пример 68
Целевое соединение (68-А) получили из исходного соединения (68-А) и исходного соединения (68-В) по методике, аналогичной описанной в Примере 1.
Целевое соединение (68-В) получили из полученного таким образом целевого соединения (68-А) по методике, аналогичной описанной в Примере 5.
т.пл.: 88-94oC
ИК (нуджол): 1610 (широкий синглет), 1510 см-1
ЯМР (ДМСО-d6, δ): 0,85 (6Н, мультиплет), 1,71 и 1,76 (3Н, каждый синглет), 2,08 (1Н, мультиплет), 2,80 и 3,03 (3Н, каждый синглет), 2,4-3,2 (4Н, мультиплет), 3,8-5,1 (5Н, мультиплет), 7,49 (2Н, мультиплет), 7,72 (2Н, мультиплет), 7,6-8,6 (3Н, мультиплет), 9,18 и 9,26 (4Н, каждый синглет)
МС (m/z): 535 (М++1)
Пример 69
Целевое соединение (69-А) получили из исходного соединения (69-А) и исходного соединения (69-В) по методике, аналогичной описанной в Примере 1.
Целевое соединение (69-В) получили из полученного таким образом целевого соединения (69-А) по методике, аналогичной описанной в Примере 5.
т.пл.: 84-91oC
ИК (нуджол): 1650 (уширенный), 1610, 1490 см-1
ЯМР (ДМСО-d6, δ): 1,05 (3Н, дублет, J=6,1 Гц), 2,4-2,8 /3Н, мультиплет/, 2,80 и 3,01 /3Н, каждый синглет/, 3,9-4,2 /3Н, мультиплет/, 4,7 /1Н, мультиплет/, 4,95 и 5,06 /2Н, каждый синглет/, 7,13 /2Н, дублет, J=8,9 Гц/, 7,58 и 7,74 /1Н, дублет, (J=8,5 Гц) и мультиплет/, 7,78 /2Н, дублет, J=8,9 Гц/, 8,38 и 8,70 /1Н, каждый дублет, J=8,1 Гц/, 9,0-9,3 /4Н, мультиплет/
МС /m/z/: 482 /М++1/
Пример 70
Целевое соединение /70-А/ получили из исходного соединения /70-А/ и исходного соединения /70-В/ по методике, аналогичной описанной в Примере 1.
Целевое соединение /70-В/ получили из целевого соединения /70-А/ по методике описанной в Примере 5
т.пл.: ≈170oC /разл./
ИК (нуджол): 3300, 3100, 1725, 1660, 1640, 1610, 1540, 1490 см-1
ЯМР (ДМСО-d6, δ): 0,85 /6Н, дублет, J=6,7 Гц/, 1,8-2,1 /3Н, мультиплет/, 2,29 /2Н, типа триплета/, 2,3-2,76 /2Н, мультиплет/, 3,63 /3Н, синглет/, 4,0-4,2 /3Н, мультиплет/, 4,65 /1Н, мультиплет/, 7,14 /2Н, дублет, J=8,8 Гц/, 7,81 /2Н, дублет, J=8,8 Гц/, 8,03 /1Н, дублет, J=8,2 Гц/, 8,27 /1Н, дублет, J=7,7 Гц/, 9,04 /2Н, синглет/, 9,14 /2Н, синглет/
FAB-MC: 451 /М++1/
Пример 71
Целевое соединение /71-А/ получили из исходного соединения /71-А/ и исходного соединения /71-В/ по методике, аналогичной описанной в Примере 1.
Целевое соединение /71-В/ получили из целевого соединения /71-А/, полученного таким образом по методике, аналогичной описанной в Примере 5.
т.пл.: ≈169oC /разл./
ИК (нуджол): 3280, 3100, 1710, 1660, 1600, 1540, 1490 см-1
ЯМР (ДМСО-d6, δ): 0,84 (6Н, дублет, J=6,8 Гц), 1,16-1,8 (10Н, мультиплет), 1,94-2,2 (3Н, мультиплет), 2,33-2,8 (2Н, мультиплет), 3,9-4,25 (3Н, мультиплет), 4,65 (1Н, мультиплет), 7,15 (2Н, дублет, J=8,9 Гц), 7,70 (1Н, дублет, J=8,7 Гц), 7,81 (2Н, дублет, J=8,9 Гц), 8,21 (1Н, дублет, J=7,8 Гц, 8,97 (2Н, синглет)), 9,13 2Н, синглет.
Пример 72
Целевое соединение (72-А) получено из исходного соединения (72-А) и исходного соединения (72-В) по методике, аналогичной описанной в Примере 1.
Целевое соединение (72-В) получили из полученного таким образом целевого соединения (72-А) по методике, аналогичной описанной в Примере 5.
т.пл.: ≈210oC /разл./
ИК (нуджол): 3300, 3080, 1660, 1630, 1540, 1510 см-1
ЯМР (ДМСО-d6, δ): 1,3 (3Н, триплет, J=6,9 Гц), 1,51 (4Н, мультиплет), 2,1 (2Н, типа триплета), 2,3-3,1 (6Н, мультиплет), 3,97 (2Н, квартет J=6,9 Гц), 4,34 (1Н, мультиплет), 4,59 (1Н, мультиплет), 6,79 (2Н, дублет, J=8,6 Гц), 7,08 (2Н, дублет, J=8,8 Гц), 7,43 (2Н, дублет, J=8,3 Гц), 7,74 (2Н, дублет, J=8,3 Гц), 7,83 (1Н, дублет, J=7,7 Гц), 8,11 (1Н, дублет, J=7,9 Гц), 9,24 (4Н, синглет)
Пример 73
Целевое соединение /73-А/ получили их исходного соединения /73-А/ и исходного соединения /73-В/ по методике, аналогичной описанной в Примере 1.
Целевое соединение /73-В/ получили из целевого соединения /73-А/, полученного таким образом по методике, аналогичной описанной в Примере 5.
т.пл.: 145oC /разл./
ИК (нуджол): 3320, 3100, 1660, 1610, 1530, 1490 см-1
ЯМР (ДМСО-d6, δ): 1,02 (3Н, дублет, J=6,3 Гц), 1,97 (2Н, мультиплет), 2,31 (2Н, типа триплета), 2,35-2,8 (2Н, мультиплет), 3,95-4,25 (4Н, мультиплет), 4,68 (1Н, мультиплет), 7,15 (2Н, дублет, J=8,9 Гц), 7,55 (1Н, дублет, J= 8,6 Гц), 7,81 (2Н, дублет, J=8,9 Гц), 8,34 (1Н, дублет, J=7,9 Гц), 8,98 (2Н, синглет), 9,13 (2Н, синглет)
Пример 74
Целевое соединение /74-А/ получили из исходного соединения /74-А/ и исходного соединения /74-В/ по методике, аналогичной описанной в Примере 1.
Целевое соединение /74-В/ получили из полученного таким образом целевого соединения /74-А/ по методике, аналогичной описанной в Примере 5.
т.пл.: 136oC /разл./
ИК (нуджол): 3300, 3100, 1720, 1670, 1540, 1490 см-1
ЯМР (ДМСО-d6, δ): 1,02 (3Н, дублет, J=6,3 Гц), 1,53 (4Н, мультиплет), 2,15 (2Н, типа триплета), 2,35-2,9 (4Н, мультиплет), 4,0-4,2 (2Н, мультиплет), 4,65 (1Н, мультиплет), 7,45 (2Н, дублет, J=8,3 Гц), 7,51 (1Н, дублет, J= 8,6 Гц), 7,74 (2Н, дублет, J=8,3 Гц), 8,24 (1Н, дублет, J=7,9 Гц), 9,15 (2Н, синглет), 9,23 (2Н, синглет)
Пример 75
Целевое соединение /75-А/ получили из исходного соединения /75-А/ и исходного соединения /75-В/ по методике, аналогичной описанной в Примере 1.
Целевое соединение /75-В/ получили из полученного таким образом целевого соединения /75-А/ по методике, аналогичной описанной в Примере 5.
т.пл.: 198oC /разл./
ИК (нуджол): 3280, 1630, 1600, 1540, 1480 см-1
ЯМР (ДМСО-d6, δ): 0,84 (6Н, мультиплет), 1,34-1,72 (3Н, мультиплет), 1,97 (2Н, мультиплет), 2,15-2,8 (4Н, мультиплет), 3,9-4,27 (3Н, мультиплет), 4,57 (1Н, мультиплет), 7,11 (2Н, дублет, J=8,8 Гц), 7,68 (1Н, дублет, J=7,8 Гц), 7,75 (2Н, дублет, J=8,7 Гц), 8,29 (1Н, дублет, J=7,8 Гц), 8,82 (1,5H, синглет), 10,9 (1,5Н, синглет)
Пример 76
Целевое соединение /76-А/ получили из исходного соединения /76-А/ и исходного соединения /76-В/ по методике, аналогичной описанной в Примере 1.
Целевое соединение /76-В/ получили из целевого соединения /76-А/, полученного таким образом по методике, аналогичной описанной в Примере 5.
т.пл.: 204oC /разл./
ИК (нуджол): 3275, 1625, 1535, 1490 см-1
ЯМР (ДМСО-d6, δ): 0,7-1,0 (6Н, мультиплет), 1,0-1,57 (2Н, мультиплет), 1,74 (1Н, мультиплет), 1,98 /2Н, мультиплет/, 2,34 (2Н, типа триплета), 2,3-2,8 (2Н, мультиплет), 3,97 (1Н, мультиплет), 4,09 (2Н, типа триплета), 4,56 (1Н, мультиплет), 7,10 (2Н, дублет, J=8,8 Гц), 7,48 (2Н, дублет, J=7,8 Гц), 7,73 (2Н, дублет, J=8,6 Гц), 8,39 (1Н, дублет, J=7,6 Гц), 8,73 (1,5H, синглет), 11,29 (1,5H, синглет)
Пример 77
Целевое соединение /77-А/ получено из исходного соединения /77-А/ и исходного соединения /77-В/ по методике, аналогичной описанной в Примере 1.
Целевое соединение /77-В/ получено из целевого соединения /77-А/, полученного таким образом по методике, аналогичной описанной в Примере 5.
ИК (нуджол): 3275, 3080, 1700, 1630, 1600, 1540, 1480 см-1
ЯМР (ДМСО-d6, δ): 0,7-1,0 (6Н, мультиплет), 1,0-1,51 (2Н, мультиплет), 1,7 (5Н, мультиплет), 2,19 (2Н, типа триплета), 2,25-2,79 (2Н, мультиплет), 3,97-4,25 (3Н, мультиплет), 4,63 (1Н, мультиплет), 7,14 (2Н, дублет, J=8,9 Гц), 7,76 (1Н, дублет, J=9,5 Гц), 7,80 (2Н, дублет, J=8,9 Гц), 8,24 (1Н, дублет, J=7,7 Гц), 9,02 (2Н, синглет), 9,13 (2Н, синглет), 12,52 (1,5H, синглет)
Пример 78
Целевое соединение /78-А/ получили из исходного соединения /78-А/ и исходного соединения по методике, аналогичной описанной в Примере 1.
Целевое соединение /78-В/ получили из целевого соединения /78-А/, полученного таким образом по методике, аналогичной описанной в Примере 5.
т.пл.: ≈118oC /разл./
ИК (нуджол): 3300, 3080, 1655, 1600, 1530, 1480 см-1
ЯМР (ДМСО-d6, δ): 0,7-0,92 (6Н, мультиплет), 1,0-1,8 (9Н, мультиплет), 2,14 (2Н, типа триплета), 2,35-2,77 (2Н, мультиплет), 3,94-4,27 (3Н, мультиплет), 4,63 (1Н, мультиплет), 7,14 (2Н, дублет, J=8,9 Гц), 7,73 (1Н, дублет, J= 8,5 Гц), 7,80 (2Н, дублет, J=8,9 Гц), 8,12 (1Н, дублет, J=7,7 Гц), 8,83 (2Н, синглет), 9,13 (2Н, синглет)
Пример 79
Целевое соединение /79-А/ получили из исходного соединения /79-А/ и исходного соединения /79-В/ по методике, аналогичной описанной в Примере 1.
Целевое соединение /79-В/ получили из целевого соединения /79-А/, полученного таким образом по методике, аналогичной описанной в Примере 5.
т.пл.: 196-200oC
ИК (нуджол): 3300, 1710, 1640, 1615, 1540, 1490 см-1
ЯМР (ДМСО-d6, δ): 0,83 (3Н, широкий синглет), 1,22 (4Н, мультиплет), 1,62 (2Н, мультиплет), 1,96 (2Н, мультиплет), 2,29 (2Н, мультиплет), 2,2-2,8 (2Н, мультиплет), 4,09 (3Н, мультиплет), 4,62 (1Н, мультиплет), 7,13 (2Н, дублет, J=8,5 Гц), 7,81 (2Н, дублет, J=8,5 Гц), 7,80 (1Н, мультиплет), 8,24 (1Н, мультиплет), 9,10 и 9,40 (4Н, каждый синглет)
Пример 80
Целевое соединение /80-А/ получили из исходного соединения /80-А/ и исходного соединения /80-B/ по методике, аналогичной описанной в Примере 1.
Целевое соединение /80-В/ получили из целевого соединения /80-А/, полученного таким образом по методике, аналогичной описанной в Примере 5.
т.пл.: 216oC /разл./
ИК (нуджол): 3275, 1680, 1630, 1600, 1540, 1480 см-1
ЯМР (ДМСО-d6, δ): 0,81 (3Н, типа триплета), 1,19 (4Н, мультиплет), 1,4-1,8 (2Н, мультиплет), 1,85-2,1 (2Н, мультиплет), 2,2-2,9 (4Н, мультиплет), 3,93 (1Н, мультиплет), 4,08 (2Н, мультиплет), 4,56 (1Н, мультиплет), 7,09 (2Н, дублет, J=8,9 Гц), 7,57 (1Н, дублет, J=6,9 Гц), 7,72 2Н, дублет, J=8,8 Гц), 8,37 (1Н, дублет, J=7,9 Гц), 8,75 (2Н, синглет), 11,19 (2Н, синглет)
Пример 81
Целевое соединение /81-А/ получили из исходного соединения /81-А/ и исходного соединения /81-В/ по методике, аналогичной описанной в Примере 1.
Целевое соединение /81-В/ получили из целевого соединения /81-А/, полученного таким образом по методике, аналогичной описанной в Примере 5.
т.пл.: ≈175oC /разл./
ИК (нуджол): 3300, 3100, 1660, 1600, 1530, 1480 см-1
ЯМР (ДМСО-d6, δ): 0,87 (9Н, синглет), 1,45-1,71 (2Н, мультиплет), 1,94 (2Н, мультиплет), 2,27 (2Н, типа триплета), 2,3-2,8 (2Н, мультиплет), 4,09 (2Н, типа триплета), 4,21 (1Н, мультиплет), 4,59 (1Н, мультиплет), 7,14 (2Н, дублет, J=8,9 Гц), 7,82 (2Н, дублет, J=8,9 Гц), 8,02 (1Н, дублет, J=8,2 Гц), 8,16 (1Н, дублет, J=8,0 Гц), 9,06 (2Н, синглет), 9,14 (2Н, синглет)
Пример 82
Целевое соединение /82-А/ получили из исходного соединения /82-А/ и исходного соединения /82-В/ по методике, аналогичной описанной в Примере 1.
Целевое соединение /82-В/ получили из целевого соединения /82-А/, полученного таким образом по методике, аналогичной описанной в Примере 5.
т.пл.: ≈202oC /разл./
ИК (нуджол): 3270, 3075, 1690, 1640, 1600, 1530, 1490 см-1
ЯМР (ДМСО-d6, δ): 1,68 (4Н, мультиплет), 2,15 (2Н, типа триплета), 2,3-2,75 (2Н, мультиплет), 2,78-3,15 (2Н, мультиплет), 4,07 (2Н, типа триплета), 4,39 (1Н, мультиплет), 4,6 (1Н, мультиплет), 7,05-7,37 (7Н, мультиплет), 7,81 (2Н, дублет, J=8,9 Гц), 7,92 (1Н, дублет, J=7,7 Гц), 8,13 (1Н, дублет, J=8 Гц), 9,1 (2Н, синглет), 9,14 (2Н, синглет), 12,58 (1Н, синглет)
FAB-MC: 499 /М++1/
Пример 83
Целевое соединение /83-А/ получили из исходного соединения /83-А/ и исходного соединения /83-В/ по методике, аналогичной описанной в Примере 1.
Целевое соединение /83-В/ получили из целевого соединения /83-А/, полученного таким образом по методике, аналогичной описанной в Примере 5.
т.пл.: 168-170oC /разл./
ИК (нуджол): 3300, 1670, 1200 см-1
ЯМР (ДМСО-d6, δ): 0,83 (3Н, триплет, J=7,4 Гц), 1,21-1,38 (2Н, мультиплет), 1,40-1,68 (4Н, мультиплет), 2,12 (2Н типа триплета), 2,63-2,71 (6Н, мультиплет), 4,15 (1Н, мультиплет), 4,61 (1Н, мультиплет), 7,44 (2Н, дублет, J= 8,9 Гц), 7,73 (2Н, дублет, J=8,9 Гц), 7,92 (1Н, дублет, J=7,9 Гц), 8,11 (1Н, дублет, J= 7,8 Гц), 9,01 (2Н, синглет), 9,22 (2Н, синглет), 12,41 2Н, широкий синглет)
МС (m/z): 435 /М++1/
Пример 84
Целевое соединение /84-А/ получили из исходного соединения /84-А/ и исходного соединения /84-В/ по методике, аналогичной описанной в Примере 1.
Целевое соединение /84-В/ получили из целевого соединения /84-А/, полученного таким образом по методике, аналогичной описанной в Примере 5.
ИК (нуджол): 3280, 3100, 1650, 1605, 1530, 1490 см-1
ЯМР (ДМСО-d6, δ): 0,88 (6Н, дублет, J=6,8 Гц), 1,6-2,44 (9Н, мультиплет), 3,9-4,2 (3Н, мультиплет), 4,38 (1Н, мультиплет), 7,14 (2Н, дублет, J= 8,9 Гц), 7,81 (2Н, дублет, J=8,9 Гц), 7,95 (1Н, дублет, J=8,3 Гц), 8,08 (1Н, дублет, J=8,Гц), 9,05 (2Н, синглет), 9,14 (2Н, синглет)
Пример 85
Целевое соединение /85-А/ получили из исходного соединения /85-А/ и исходного соединения /85-В/ по методике, аналогичной описанной в Примере 1.
Целевое соединение /85,В/ получили из целевого соединения /85-А/, полученного таким образом по методике, аналогичной описанной в Примере 5.
т.пл.: ≈199oC /разл./
ИК (нуджол): 3320, 3100, 1700, 1660, 1610, 1530, 1490 см-1
ЯМР (ДМСО-d6, δ): 0,85 (6Н, дублет, J=6,6 Гц), 2,05 (1Н, мультиплет), 2,5-2,8 (2Н, мультиплет), 4,12 (1Н, мультиплет), 4,68 (2Н, синглет), 4,74 (1Н, мультиплет), 7,15 (2Н, дублет, J=8,9 Гц), 7,81 (2Н, дублет, J=8,9 Гц), 7,96 (1Н, дублет, J=9,5 Гц), 8,48 (1Н, дублет, J=8, Гц), 9,04 (2Н, синглет), 9,16 (2Н, синглет), 12,54 (1Н, синглет)
Пример 86
Целевое соединение /86-А/ получили из исходного соединения /86-А/ и исходного соединения /86-В/ по методике, аналогичной описанной в Примере 1.
Целевое соединение /86-В/ получили из целевого соединения /86-А/, полученного таким образом по методике, аналогичной описанной в Примере 5.
т.пл.: ≈150oC /разл./
ИК (нуджол): 3300, 3100, 1660, 1610, 1540, 1490 см-1
ЯМР (ДМСО-d6, δ): 0,82 (3Н, дублет, J=6,2 Гц), 0,87 (3Н, дублет, J=6,2 Гц), 1,25-1,85 (9Н, мультиплет), 2,13 (2Н, типа триплета), 2,3-2,75 (2Н, мультиплет), 4,07 (2Н, типа триплета), 4,19 (1Н, мультиплет), 4,61 (1Н, мультиплет), 7,14 (2Н, дублет, J=8,9 Гц), 7,81 (2Н, дублет, J=8,9 Гц), 7,95 (1Н, дублет, J= 8,0 Гц), 8,11 (1Н, дублет, J=8,0 Гц), 8,96 (2Н, синглет), 9,13 (2Н, синглет)
Пример 87
Целевое соединение /87-А/ получили из исходного соединения /87-А/ и исходного соединения /87-В/ по методике, аналогичной описанной в Примере 1.
Целевое соединение /87-В/ получили из целевого соединения /87-А/, полученного таким образом по методике, аналогичной описанной в Примере 5.
т.пл.: 189-191oC
ИК (нуджол): 1665, 1615, 1525, 1495 см-1
ЯМР (ДМСО-d6, δ): 0,91 (9Н, синглет), 1,97 (2Н, мультиплет), 2,2-2,6 (3Н, мультиплет), 2,70 (1Н, двойной дублет, J=16,7 Гц, J=5,9 Гц), 4,0-4,2 (3Н, мультиплет), 4,66 (1Н, мультиплет), 7,14 (2Н, дублет, J=8,9 Гц), 7,66 (1Н, дублет, J=9,2 Гц), 7,83 (2Н, дублет, J=8,9 Гц), 8,40 (1Н, дублет, J=7,6 Гц), 9,16 и 9,21 (4Н, каждый синглет)
МС (m/z): 451,2 /М++1/
Пример 88
Целевое соединение /88-А/ получено из исходного соединения /88-А/ и исходного соединения /88-В/ по методике, аналогичной описанной в Примере 1.
Целевое соединение /88-В/ получили из целевого соединения /88-А/, полученного таким образом по методике, аналогичной описанной в Примере 5.
т.пл.: 76-82oC
ИК (нуджол): 1640, 1520 см-1
ЯМР (ДМСО-d6, δ): 0,92 и 0,93 (9Н, каждый синглет), 2,3-2,8 (2Н, мультиплет), 2,80 и 3,00 (3Н, каждый синглет), 3,8-4,2 (3Н, мультиплет), 4,73 (1Н, мультиплет), 4,94 и 5,06 (2Н, каждый синглет), 7,13 (2Н, дублет, J=8,9 Гц), 7,78 (2Н, дублет, J=8,9 Гц), 7,6-8,0 (1Н, мультиплет), 8,37 и 8,65 (1Н, каждый дублет, J=7,8 Гц и 7,7 Гц), 9,08 и 9,14 (4Н, каждый синглет)
МС (m/z): 494 /М++1/
Пример 89
Целевое соединение /89-А/ получили из исходного соединения /89-А/ и исходного соединения /89-В/ по методике, аналогичной описанной в Примере 1.
Целевое соединение /89-В/ получили из целевого соединения /89-А/, полученного таким образом по методике, аналогичной описанной в Примере 5.
т.пл.: ≈170oC /разл./
ИК (нуджол): 3320, 1700, 1660, 1610, 1540, 1480 см-1
ЯМР (ДМСО-d6, δ): 0,87 (6Н, дублет, J=6,7 Гц), 2,05 (1Н, мультиплет), 2,34 (2Н, типа триплета), 2,35-2,8 (2Н, мультиплет), 3,34 (2Н, мультиплет), 4,12 (1Н, мультиплет), 4,61 (2Н, синглет), 4,64 (1Н, мультиплет), 7,15 (2Н, дублет, J=8,9 Гц), 7,81 (2Н, дублет, J=8,9 Гц), 7,82 (1Н, дублет, J=8,5 Гц, 8,2 (1Н, типа триплета)), 8,32 (1Н, дублет, J=7,7 Гц), 9,03 (2Н, синглет), 9,16 (2Н, синглет)
Пример 90
Целевое соединение /90/ получили из исходного соединения /90/ по методике, аналогичной описанной в Методе получения 18.
т.пл.: ≈210oC /разл./
ИК (нуджол): 3300, 1730, 1650, 1600, 1550 см-1
ЯМР (ДМСО-d6, δ): 0,83 (6Н, дублет, J=6,4 Гц), 1,82 (2Н, типа триплета), 2,05 (1Н, мультиплет), 2,4-2,8 (2Н, мультиплет), 3,14 (2Н, мультиплет), 4,05 (2Н, типа триплета), 4,23 (1Н, мультиплет), 4,6 (1Н, мультиплет), 5,06 (2Н, синглет), 5,10, (2Н, синглет), 6,25-6,4 (2Н, мультиплет), 7,13 (2Н, дублет, J= 8,9 Гц), 7,34 (10Н, мультиплет), 7,79 (2Н, дублет, J=8,9 Гц), 8,16 (1Н, дублет, J=8,3 Гц),
FAB-MC: 632 /М+1/
Пример 91
Целевое соединение /91/ получили из исходного соединения /91/ по методике, аналогичной описанной в Методе получения 18
т.пл.: 190oC /разл./
ИК (нуджол): 3300, 3100, 1725, 1670, 1630, 1610, 1550, 1490 см-1
ЯМР (ДМСО-d6, δ): 0,83 (6Н, дублет, J=5,7 Гц), 1,53 (2Н, мультиплет), 1,71 (2Н, мультиплет), 2,06 (1Н, мультиплет), 2,4-2,8 (2Н, мультиплет), 3,06 (2Н, мультиплет), 4,07 (2Н, триплет, J=6,1 Гц), 4,22 (1Н, мультиплет), 4,62 (1Н, мультиплет), 5,06 (2Н, синглет), 5,11 (2Н, синглет), 6,2-6,4 (2Н, мультиплет), 7,14 (2Н, дублет, J= 8,9 Гц), 7,35 (10Н, мультиплет), 7,81 (2Н, дублет, J= 8,9 Гц), 8,16 (1Н, дублет, J=8,3 Гц), 9,03 (2Н, синглет), 9,14 (2Н, синглет)
Следующие соединения /Примеры 92 и 93/ получили по методике, аналогичной описанной в Примере 5.
Пример 92
Целевое соединение /92/
т.пл.: ≈188oC /разл./
ИК (нуджол): 3300, 1710, 1650, 1600, 1550 см-1
ЯМР (ДМСО-d6, δ): 0,84 (6Н, дублет, J=5,4 Гц), 1,85 (2Н, триплет, J=6,4 Гц), 1,9-2,28 (1Н, мультиплет), 2,35-2,72 (2Н, мультиплет), 3,17 (2Н, мультиплет), 4,05 (1Н, мультиплет), 4,10 (2Н, типа триплета), 4,49 (1Н, мультиплет), 6,42 (2Н, мультиплет), 7,15 (2Н, дублет, J=8,8 Гц), 7,75 (1Н, дублет, J= 8,8 Гц), 7,84 (2Н, дублет, J=8,8 Гц), 9,0 /2Н, синглет/, 9,23 /2Н, синглет/
МС: 452 /М+1/
Пример 93
Целевое соединение /93/
т.пл.: ≈183oC /разл./
ИК (нуджол): 3310, 1700, 1650, 1635, 1600, 1560, 1540, 1480 см-1
ЯМР (ДМСО-d6, δ): 0,84 /6Н, дублет, J=5,7 Гц/, 1,4-1,8 /4Н, мультиплет/, 2,04 /1Н, мультиплет/, 2,3-2,5 /2Н, мультиплет/, 3,07 /2Н, мультиплет/, 4,0-4,2 /3Н, мультиплет/, 4,48 /1Н, мультиплет/, 6,2-6,45 /2Н, мультиплет/, 7,14 /2Н, дублет, J=8,8 Гц/, 7,73 /1Н, дублет, J=8,9 Гц/, 7,81 /2Н, дублет, J= 8,8 Гц/, 9,02 /2Н, синглет/, 9,14 /2Н, синглет/, 12,51 /1Н, широкий синглет/
Пример 94
Исходное соединение /94/ /6,89 г/ растворили в 1N хлористоводородной кислоты /116 мл/ и полученный раствор лиофилизировали. Полученный порошок высушили и выделили целевое соединение /94/ /4,34 г/.
т.пл.: 133-140oC.
ИК (нуджол): 1620-1660 /широкая/, 1530 см-1
ЯМР (ДМСО-d6, δ): 0,86 /6Н, дублет, J=6,8 Гц/, 2,04 /1Н, мультиплет/, 2,2-2,8 /2Н, мультиплет/, 2,80 и 3,0 /3Н, каждый синглет/, 3,8-4,2 /3Н, мультиплет/, 4,6 /1Н, мультиплет/, 5,06 и 5,41 /2Н, каждый синглет/, 7,13 /2Н, дублет, J=8,8 Гц/, 8,00 /2Н, дублет, J=8,8 Гц/, 7,80-8,20 /1Н, мультиплет/, 8,27 и 8,68 /1Н, каждый дублет, J=7,8 Гц/, 9,05 и 9,25 /4Н, каждый синглет/
МС (m/z): 480 /М++1/
Пример 95
Смесь исходного соединения /95/ /19,61 г/ и воды /50 мл/ довели до pH 6,05 водным раствором аммиака и смесь лиофилизировали. Полученный порошок высушили и выделили целевое соединение /95/ /19,17 г/.
Т.пл.: 167-170oC
ИК (нуджол): 3260, 1640 широкая/, 1540, 1485 см-1
ЯМР (ДМСО-d6, δ): 0,80 /6Н, дублет, J=4,9 Гц/, 2,03 /1Н, мультиплет/, 2,2-2,8 /2Н, мультиплет/, 2,80 и 3,03 /3Н, каждый синглет/, 3,8-4,7 /4Н, мультиплет/, 4,94 и 5,04 /2Н, каждый синглет/, 7,10 /2Н, дублет, J=8,2 Гц/, 7,59 /1Н, мультиплет/, 7,73 /2Н, мультиплет/, 8,45 и 8,72 /1Н, мультиплет/
МС (m/z): 480 /М++1/
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ИНДОЛИЛПИПЕРИДИНА ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ | 1991 |
|
RU2039056C1 |
| ПРОИЗВОДНЫЕ ИНДОЛА ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1991 |
|
RU2045518C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ТИАЗОЛА ИЛИ ИХ СОЛЕЙ С ГАЛОИДВОДОРОДНОЙ КИСЛОТОЙ | 1990 |
|
RU2010026C1 |
| Способ получения производных тиазола или их аддитивных солей с кислотами | 1988 |
|
SU1753948A3 |
| СПОСОБ ПОЛУЧЕНИЯ СОЕДИНЕНИЙ ЦЕФЕМА ИЛИ ИХ КИСЛОТНО-АДДИТИВНЫХ СОЛЕЙ | 1988 |
|
RU2017744C1 |
| Способ получения бензоконденсированного гетероциклического соединения | 1986 |
|
SU1426454A3 |
| ПРОИЗВОДНЫЕ ТИАЗОЛА | 1991 |
|
RU2048468C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ АЛКАНСУЛЬФОНАНИЛИДА ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫХ СОЛЕЙ | 1988 |
|
RU2012557C1 |
| Способ получения производных хиназолина или их солей | 1986 |
|
SU1588283A3 |
| АМИДЫ КИСЛОТ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2000 |
|
RU2211215C2 |









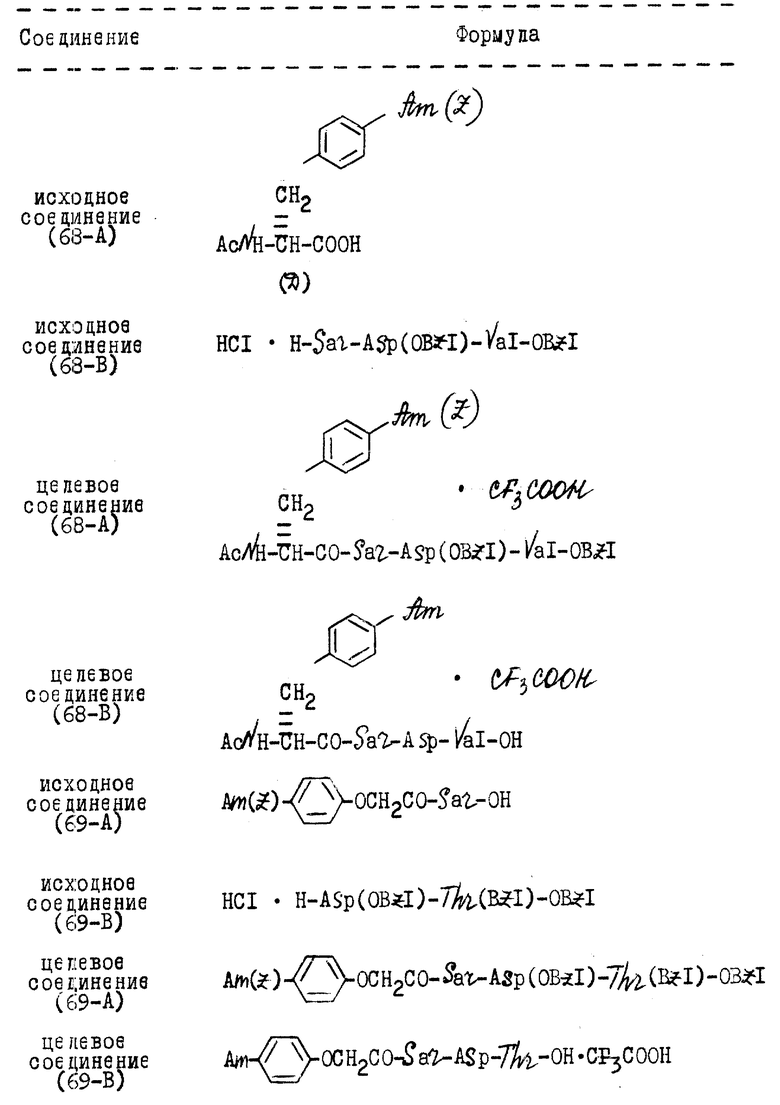
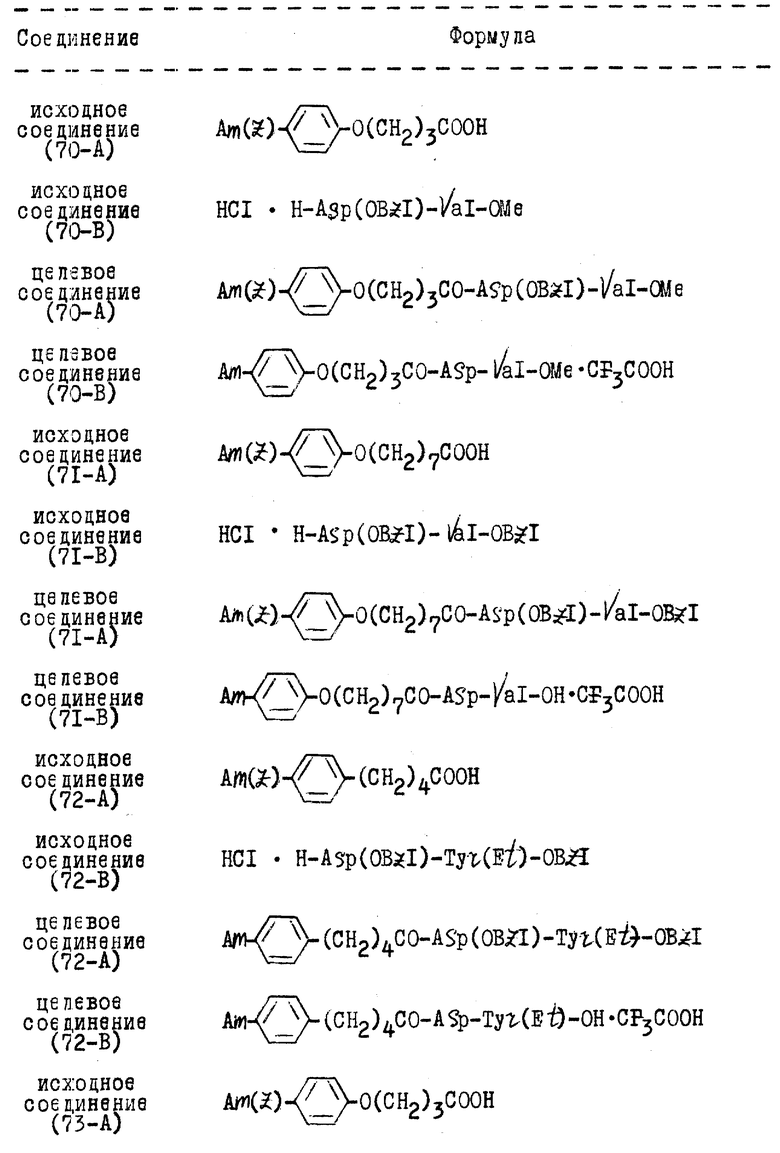





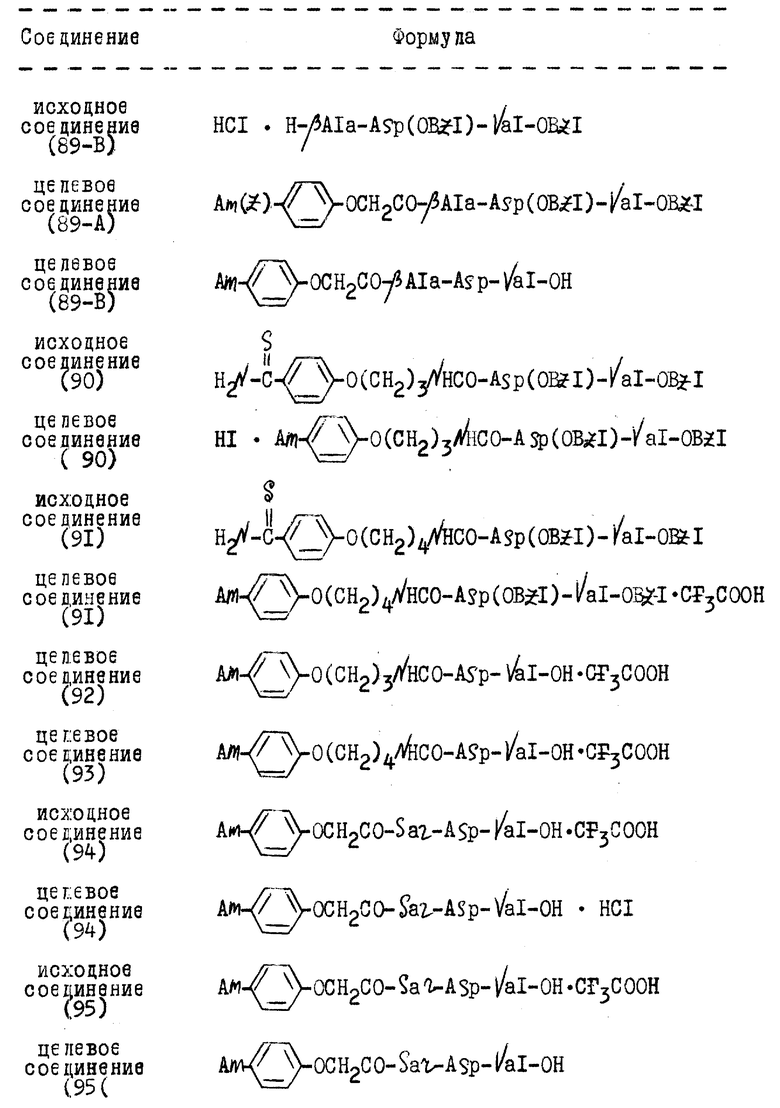
Использование: в медицине для предупреждения и устранения образования тромбов. Сущность изобретения: производные пептидов общей формулы I: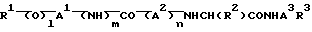
где R1 - арил, который может содержит 1-3 заместителя, выбранных из амидино- и защищенной амидиногруппы; R2 - карбокси /низший/ алкил или защищенный карбокси /низший/ алкил; R3 - карбокси или защищенная карбоксигруппа, A1 - алкилен, который может содержит 1-3 заместителя, выбранного из амино и защищенной аминогруппы; A2 - -N(R4)CH2CO-, где R4 - низший алкил или A2 группа -NHCH2CH2CO-; A3 - низший алкилен, содержащий 1-3 заместителя, выбранного из низшего алкила, моно-, ди- или три фенил /низшего/ алкила, содержащего 1-3 заместителя, выбранного из группы гидрокси, низшего алкокси, защищенного гидрокси, гидрокси /низшего/ алкила; защищенного гидрокси /низшего/ алкила; [цикло /низший/ алкил]-/низшего/ алкила, пиридил /низшего/ алкила, l, m и n одинаковые или разные и представляют собой целое число 0 или 1, при условии, что A2 не может быть группой -NHCH2CH2CO-, если l = 0, или фармацевтические соли; пептиды могут быть получены двумя путями; а/ взаимодействием соединений II:  или их реакционноспособных производных с соединениями формулы
или их реакционноспособных производных с соединениями формулы  и от полученного продукта конденсации отщепляют защитные группы; или б/ взаимодействием соединений IV:
и от полученного продукта конденсации отщепляют защитные группы; или б/ взаимодействием соединений IV:  с соединениями формулы V: H2NCHR2CONHA3R3 или их реакционноспособными по аминогруппе производными; фармацевтическая композиция, содержащая в качестве активного ингредиента производные пептидов формулы I в эффективном количестве, и способ предупреждения и устранения тромбоза у млекопитающих путем введения производных формулы I в суточной дозе 0,001-200 мг/кг веса в 2-4 приема. 5 с. и 7 з.п.ф-лы, 3 табл.
с соединениями формулы V: H2NCHR2CONHA3R3 или их реакционноспособными по аминогруппе производными; фармацевтическая композиция, содержащая в качестве активного ингредиента производные пептидов формулы I в эффективном количестве, и способ предупреждения и устранения тромбоза у млекопитающих путем введения производных формулы I в суточной дозе 0,001-200 мг/кг веса в 2-4 приема. 5 с. и 7 з.п.ф-лы, 3 табл.

где R1 арил, который может содержать от 1 до 3 заместителей, выбранных из группы, состоящей из амидино- и защищенной амидиногруппы;
R2 карбокси(низший)алкил или защищенный карбокси(низший)алкил;
R3 карбокси- или защищенная карбоксигруппа;
А1 алкилен, который может содержать от 1 до 3 заместителей, выбираемых из амино- и защищенной аминогруппы;
А2 группа формулы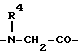
где R4 низший алкил, или А2 группа формулы -NH-CH2-CH2-CO-;
А3 низший алкилен, который может содержать 1 3 подходящих заместителя, выбираемых из низшего алкила, моно-, или ди-, или трифенил(низшего)алкила, содержащего 1 3 заместителя, выбираемого из группы, состоящей из гидрокси, низшего алкокси и защищенного гидрокси, гидрокси(низшего)алкила, защищенного гидрокси(низшего)алкила, (цикло)низший(алкил) (низшего)алкила, пиридил(низшего)алкила;
l, m и n одинаковые или различные, целое число 0 или 1, при условии, что А2 не является группой формулы
-NHCH2CH2CO-,
если l целое число, равное 0,
или фармацевтически приемлемые их соли.
или их фармацевтически приемлемых солей, значения радикалов указаны в п. 1, отличающийся тем, что соединения общей формулы II
где R1, А1, l и m имеют указанные значения,
или их реакционноспособные производные по карбоксигруппе,
или их соли вводят во взаимодействие с соединениями общей формулы III
где R2 R3, А2, А3 и n имеют указанные значения,
или их солями и от полученных при этом производных формулы I, где R1 арил, содержащий амидиногруппу, отщепляют амидинозащитную группу, или от полученного производного формулы I, где R2 защищенный карбокси(низший)алкил, отщепляют карбоксизащитную группу с получением соединений общей формулы I, где R2 карбокси(низший)акил, или от полученных соединений формулы I, где А3 низший алкилен, содержащий моно(или ди-, или три-) (защищенный гидрокси)-фенил(низший) алкил, или солей, или от полученных соединений формулы I, где R3 защищенная карбоксигруппа, или их солей отщепляют карбоксизащитную группу с образованием соединений формулы I, где R3 карбоксигруппа, или их солей.
где значения радикалов указаны в п. 1,
или их фармацевтически приемлемых солей, отличающийся тем, что соединения формулы IV
R1-(O)l-A1-(NH)m-CO-A2- OH,
где R1, А1, А2, l, m имеют указанные в п. 1 значения,
или их соли вводят во взаимодействие с соединениями формулы V
где R2, R3 и А3 имеют указанные в п. 1 значения,
или с их реакционноспособными по аминогруппе производными, или их солями.
Авторы
Даты
1998-01-27—Публикация
1992-05-12—Подача