Изобретение относится к нефтепереработке и нефтехимии и может быть использовано в нефтеперерабатывающей, нефтехимической и газовой промышленности. Получаемые дикетосульфиды представляют практическую ценность и могут эффективно использоваться в качестве абсорбента диоксида серы.
Известно получение дикетосульфидов, например 2,21-дициклогексаннонилсульфида при взаимодействии 2-хлорциклогексанона с избытком сульфида натрия в водно-метанольной среде при 15оС.
Недостатком известного способа является использование труднодоступного 2-хлорциклогексанона, низкий выход целевого продукта.
Наиболее близким к предлагаемому способу по технической сущности и достигаемому результату является способ получения 4-меркапто-2-бутанона на основе метилвинилкетона и сульфида натрия в водной среде. Процесс протекает в среде метанола при (-12) (-15)оС по схеме
CH3-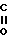 -CH=CH2
-CH=CH2 CH
CH CH2CH2SH+(CH
CH2CH2SH+(CH CH2CH2)2S
CH2CH2)2S
В результате получают 4-меркапто-2-бутанон. Это основной продукт реакции. Дикетосульфид является побочным продуктом и является нежелательной примесью. Недостатком известного способа является низкий выход дикетосульфида и использование труднодоступного винилкетона. Применение дикетосульфидов, синтезированных по известным способам связано, в основном, с их биологической активностью и органолептическими свойствами. Использование же их в качестве абсорбентов диоксида серы неизвестны.
Известно применение в качестве абсорбента сернистого ангидрида аминокетосульфидов общей формулы -
- где R пиперидино, морфолино или диэтиламино.
где R пиперидино, морфолино или диэтиламино.
Недостатком известного поглотителя является недоступность и токсичность исходных азотистых соединений и меркаптанов.
Целью изобретения является повышение выхода дикетосульфида, использование доступных кетонов, расширение ассортимента веществ, поглощающих диоксид серы.
Поставленная цель достигается тем, что кетон (ацетофенон, циклогексанон, метилэтилкетон) подвергают взаимодействию со смесью формальдегида и сульфида натрия в водно-спиртовой или водно-щелочной средах.
Сущность предлагаемого изобретения заключается в том, что тиометилированию подвергают ацетофенон, циклогексанон, метилэтилкетон смесью формальдегида и водно-спиртового или водно-щелочного раствора сульфида натрия.
Процесс тиометилирования идет при температуре 20±5оС в течение 1-7 ч при молярном соотношении компонентов равном (1,5-2,5):)1,5-2,5):1, предпочтительно 2,2:2,5:1. При уменьшении соотношения реагентов и времени реакции уменьшается выход дикетосульфидов до 50,9% увеличение реагентов более 2,5 моль нецелесообразно, так как не наблюдается увеличение выхода целевого продукта и степени превращения.
Отличительным признаком предлагаемого способа является получение дикетосульфида путем осуществления реакции конденсации кетона с сульфидом натрия в присутствии формальдегида при молярном соотношении: кетона, формальдегида и серы (1,5:2,5):(1,5-2,5):1.
Преимуществом предлагаемого способа является высокий выход целевого продукта (76-92%), доступность кетонов.
Следует отметить, что в качестве серусодержащего реагента наряду с реактивным сульфидом натрия может быть использован отработанный щелочной раствор, образующийся при очистке газов от сероводорода. В результате реакции отработанный щелочной раствор регенерируется и может возвращаться в процесс очистки газов от сероводорода, что является также значительным преимуществом способа. Использование предлагаемого способа позволит в комплексе решить вопросы регенерации щелочного раствора, а также очистки газов от сероводорода и диоксида серы.
Целевой продукт-дикетосульфиды представляют собой вязкие жидкости от светло-желтого до светло-коричневого цвета, характеристика которых приведена в табл. 2. Выход дикетосульфидов из расчета на серу сульфидную составляет 76-92 отн.
Общая формула дикетосульфидов, получаемых на основе различных кетонов следующая:
R2-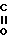 -CH2-CH2-S-CH2CH2-
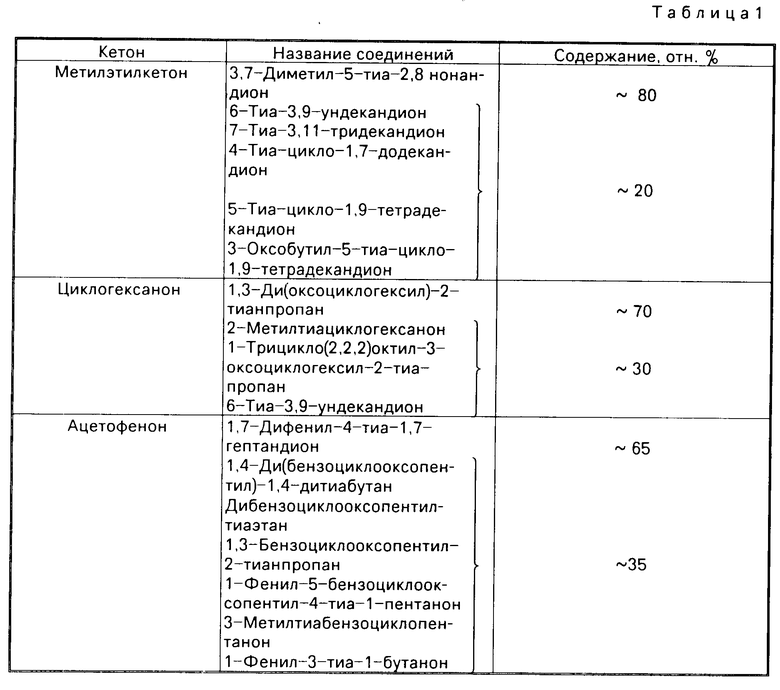
-CH2-CH2-S-CH2CH2-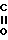 -R1 где R1 R2 CH3, C2H5, C5H10, C6H6. Продукт реакции представляет собой смесь, состав которой для используемых кетонов приведен в табл.1.
-R1 где R1 R2 CH3, C2H5, C5H10, C6H6. Продукт реакции представляет собой смесь, состав которой для используемых кетонов приведен в табл.1.
Проведенные испытания показали, что дикетосульфиды, полученные на основе кетонов (метилэтилкетон, циклогексанон, ацетофенон) эффективно поглощают диоксид серы. Емкость дикетосульфидовв в зависимости от используемого кетона составляет 277-306 мг/г (см.табл.3).
П р и м е р 1. Получение концентрата кетосульфидов на основе ацетофенона.
В круглодонную колбу, снабженную механической мешалкой, вносят 50 г сульфида натрия, растворенного в 100 г дистиллированной воды. Содержание сульфид ионов составляет 2,930 мас. что соответствует 4,395 г или 0,137 молей серы в растворе. Затем в колбу при перемешивании подают 75 мл (59,52 г) спирта, 27,4 г 30%-ного раствора формалина, содержащего 8,22 г (0,274 моль) чистого формальдегида и 32,6 г (0,274 моль) ацетофенона. Соотношение кетона, формальдегида и серы составляет 2:2:1 (моль). Смесь перемешивают в течение 5 ч. Контроль на полноту реакции проводят методом потенциометрического титрования аммиакатом азотнокислого серебра. Результаты анализа свидетельствуют, что через 5 ч перемешивания конверсия серы составляет 86,3%
Остаточное содержание серы в растворе составляет 0,402 мас.
Затем реакционную смесь переносят в делительную воронку и после отстоя ( ≈1 ч) отделяют органический слой.
Водный слой экстрагируют хлороформом (50-100 мл), сушат над сульфатом магния. Затем хлороформный экстракт объединяют с органическим слоем.
После удаления растворителя получают 34,03 г целевого продукта (см. N 8 табл.4), характеристика которого приведена в табл.2.
П р и м е р 2. Получение дикетосульфидов на основе метилэтилкетона.
В круглодонную колбу, снабженную механической мешалкой, вносят 50 г сульфида натрия, растворенного в 100 мл дистиллированной воды. Содержание сульфид ионов составляет 2,930 мас. Содержание серы в растворе составляет 4,395 г или 0,137 моль.
В колбу при перемешивании подают 5 г едкого натрия, 27,4 г 30%-ного раствора формалина, содержащего 8,22 г (0,274 моль) чистого формальдегида и 19,7 г (0,274 моль) метилэтилкетона. Смесь перемешивают в течение 7 ч. Контроль на полноту реакции проводят методом потенциометрического титрования аммиаком азотнокислого серебра. Результаты анализа свидетельствуют, что через 7 ч перемешивания конверсия серы составляет 58,8%
Остаточное содержание серы составляет 1,207 мас.
После перемешивания смесь переносят в делительную воронку. После отстоя (1 ч) отделяют органический слой. Водный слой экстрагируют хлороформом (50-100 мл). Хлороформный экстракт сушат над сульфатом магния и объединяют с органическим слоем. После удаления растворителя получают 13.0 г целевого продукта (см. N 12 табл.4). Характеристика продукта приведена в табл.2.
П р и м е р 3. Получение дикетосульфида на основе циклогексанона.
Дикетосульфид получают в условиях примера 1, используя 75 мл (59.52 г) спирта, 27,4 мл 30% -ного раствора формалина, содержащего 8,22 г чистого формальдегида (0,274 моль) и 26,9 г (0,274 моль) циклогексанона.
Реакционную смесь перемешивают в течение 7 ч. В этих условиях достигается 81,7% конверсия серы. Остаточное содержание сульфид-ионов не превышает 0,536 мас.
Выход продукта составляет 34,28 г (см. N 21, табл.4). Характеристика продукта приведена в табл.2.
П р и м е р 4. Емкость дикетосульфидов по диоксиду серы определяли в абсорбенте типа Дрекселя при парциальном давлении диоксида серы 745±5 мм рт. ст. при 20±5оС. В абсорбер загружали 9,2041 г дикетосульфидов (масса абсорбера с дикетосульфидами 68.6477, масса пустого 59,4436), полученных в условиях примера 1 на основе ацетофенона и сульфида натрия. После этого в абсорбер подавали диоксид серы. Поглощение диоксида серы определяли по привесу абсорбера. Опыты показывают, что через два часа наступает насыщение абсорбента и масса абсорбера 71,2006 г. Увеличение массы абсорбента составляет 71,2006 г 68,6477 г 2,5529 г. Таким образом, емкость (мг О2 на 1 г абсорбента) составляет 2,5529 г9,2041 г 0,2774 г/г (277,4 мг/г). В аналогичных условиях емкость кетосульфидов по сероводороду и диоксиду азота составляет 7,9 и 8,2 мг/г, соответственно.
В указанных условиях оксид азота предлагаемым образцом кетосульфидов практически не поглощается. После насыщения газом абсорбент продувают воздухом или азотом при 20±30оС в течение 5-10 мин, в результате чего диоксид серы отдувается и абсорбент полностью регенерируется. Масса абсорбера равна 73,7826 г. Аналогично определена емкость дикетосульфидов, полученных на основе метилэтилкетона и циклогексанона. Данные по емкости приведены в табл.3.
Таким образом, предлагаемый способ позволяет увеличить выход продукта (дикетосульфидов), который может эффективно использоваться в качестве абсорбента диоксида серы.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ЭКСТРАГЕНТА АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ ИЗ ИХ СМЕСЕЙ С НОРМАЛЬНЫМИ УГЛЕВОДОРОДАМИ | 1992 |
|
RU2043338C1 |
| СПОСОБ ПОЛУЧЕНИЯ АБСОРБЕНТА ДИОКСИДА СЕРЫ | 1992 |
|
RU2028177C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭКСТРАГЕНТА АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ ИЗ ИХ СМЕСЕЙ С НОРМАЛЬНЫМИ УГЛЕВОДОРОДАМИ | 1992 |
|
RU2041207C1 |
| АБСОРБЕНТ ДИОКСИДА СЕРЫ | 1992 |
|
RU2026721C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОНЦЕНТРАТОВ ГАММА-КЕТОСУЛЬФИДОВ | 2004 |
|
RU2278110C2 |
| Способ очистки газоконденсата от меркаптанов | 1988 |
|
SU1579927A1 |
| СПОСОБ ПОЛУЧЕНИЯ СУЛЬФОКСИДОВ | 1998 |
|
RU2139275C1 |
| СПОСОБ ПОЛУЧЕНИЯ МИКРОКРИСТАЛЛИЧЕСКОЙ ЦЕЛЛЮЛОЗЫ | 2000 |
|
RU2163945C1 |
| Способ получения экстрагента палладия из кислых растворов | 1989 |
|
SU1744086A1 |
| Способ очистки газа от сероводорода | 1990 |
|
SU1699546A1 |



Сущность изобретения: продукт абсорбент серы. Реагент 1: метилэтилкетон или циклогексанон или ацетофенон. Реагент 2: смесь формальдегида и водно-щелочного или водно-спиртового раствора сульфида натрия. Условия реакции: молярное соотношение кетона, формальдегида и серы равно (1,5 2,5) 1 и массовое соотношение спирта (или щелочи) и сульфида натрия поддерживают равным 19,84 71,42 или (2,5 7,5) 50. 1 з. п. ф-лы, 5 табл.
| Аминокетосульфиды в качестве абсорбентов сернистого ангидрида | 1982 |
|
SU1052508A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1995-09-10—Публикация
1992-05-28—Подача