Изобретение относится к биологии и медицине и предназначено для отбора веществ, обладающих противовоспалительной активностью, содержащих в составе молекулы группу NH, связанную с фенильным радикалом.
Наиболее близким к изобретению по технической сущности и достигаемому результату является известный способ изучения возможной зависимости антиаритмической активности от величины химического сдвига (химсдвига) протона амидной группы, снятые в СDCl3 в концентрации 2,5% относительно эталона гексаметилдисилоксан. Изучение ведется в гомологическом ряду ариламидов N-замещенных аминоуксусных кислот. В работе отмечено, что биологическая активность не коррелируется с химсдвигом протона группы NH. Недостатком данного способа является использование в качестве растворителя CDCl3, что ограничивает круг исследуемых веществ, а также высокая концентрация исследуемого вещества в образце 2,5%
Задача изобретения повышение достоверности и расширение круга исследуемых веществ.
Патентуемый способ предусматривает связи ПМР-спектроскопии с электронным строением молекул, а именно, с помощью снятия ПМР-спектров исследуемых веществ в трихлориде мышьяка и регистрации химических сдвигов NH-группы, причем концентрацию исследуемых веществ берут в пределах 0,95-0,98 мол.
Для отбора биологической активности представлены химические соединения, содержащие в молекуле группу NH, а именно: производные антраниловой кислоты, хиназолина и ортофен производное фенилуксусной кислоты.
Выбор ориентации на группу NH обусловлен тем, что процесс циклообразования в гетероциклические соединения (хиназолины, акридоны и др.), а также метаболизм их по кинурениновому пути сопряжен с электронным эффектом на атоме азота группы NH.
На электронный эффект атома азота группы NH, а следовательно, и в целом на структурные особенности молекул и хим-сдвиг протона группы NH значительное влияние оказывают подбор растворителя и концентрация вещества.
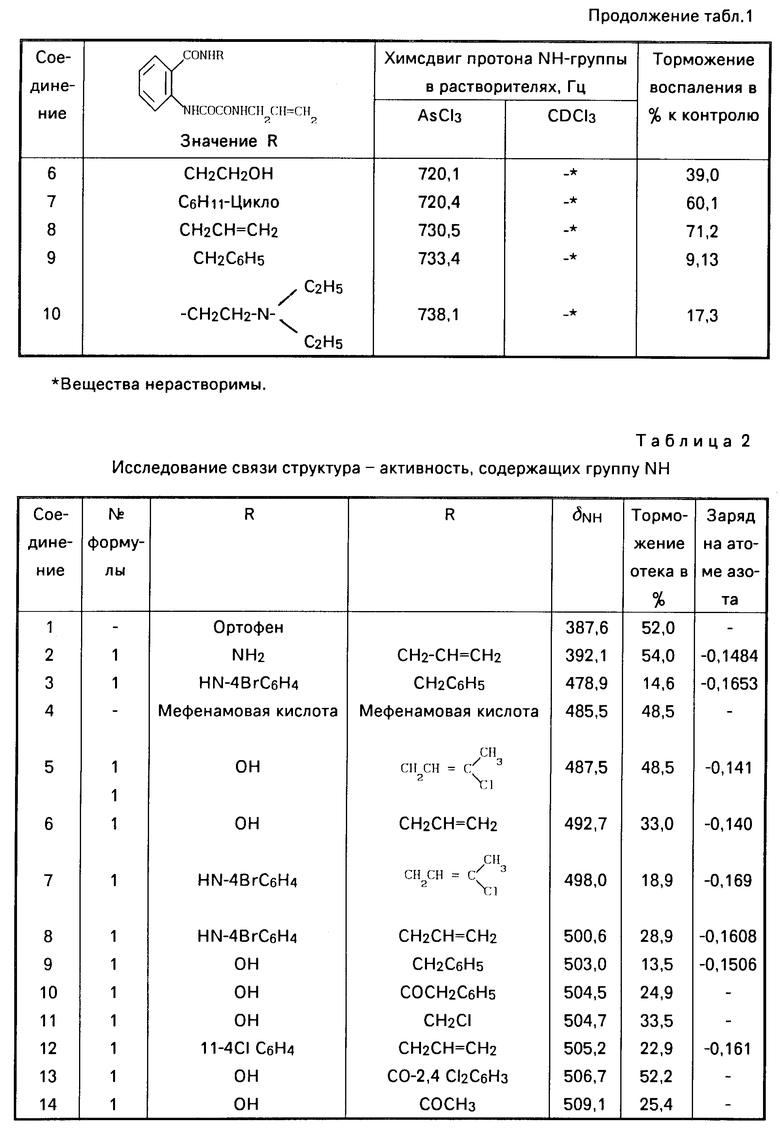
С целью расширения круга исследуемых веществ необходимо было подобрать соответствующий растворитель. В качестве растворителей использовали AsCl3 и CDCl3 (табл.1).
Как видно из табл.1, дейтерированный хлороформ как растворитель значительно снижает круг исследуемых веществ.
Изменение концентрации вещества в растворителе отражается на точности измерения химсдвига. Так, например, при концентрации вещества N 49 (табл.2) от 0,5 до 2,6 мол. наблюдалось увеличение хим-сдвига протона группы NH на 2,4 Гц. Снижение концентрации вещества до 0,5 мол. затрудняет регистрацию химсдвига протона группы NH. Поэтому для испытуемых веществ наиболее приемлемая концентрация 0,95-0,98 мол. Концентрация до 1% способствует ослаблению межмолекулярной ассоциации молекул, что повышает достоверность результатов исследований.
Таким образом, AsCl3 является универсальным растворителем для испытуемых веществ, является апротонным растворителем и менее полярным, чем CDCl3, а также способствует уменьшению межмолекулярной водородной связи, как одного из факторов изучения связи структура-активность. Использование трихлорида мышьяка в ПМР-спектроскопии для отбора веществ с противовоспалительным дей-ствием не является очевидным для специалистов, что подтверждается патентными исследованиями заявителя.
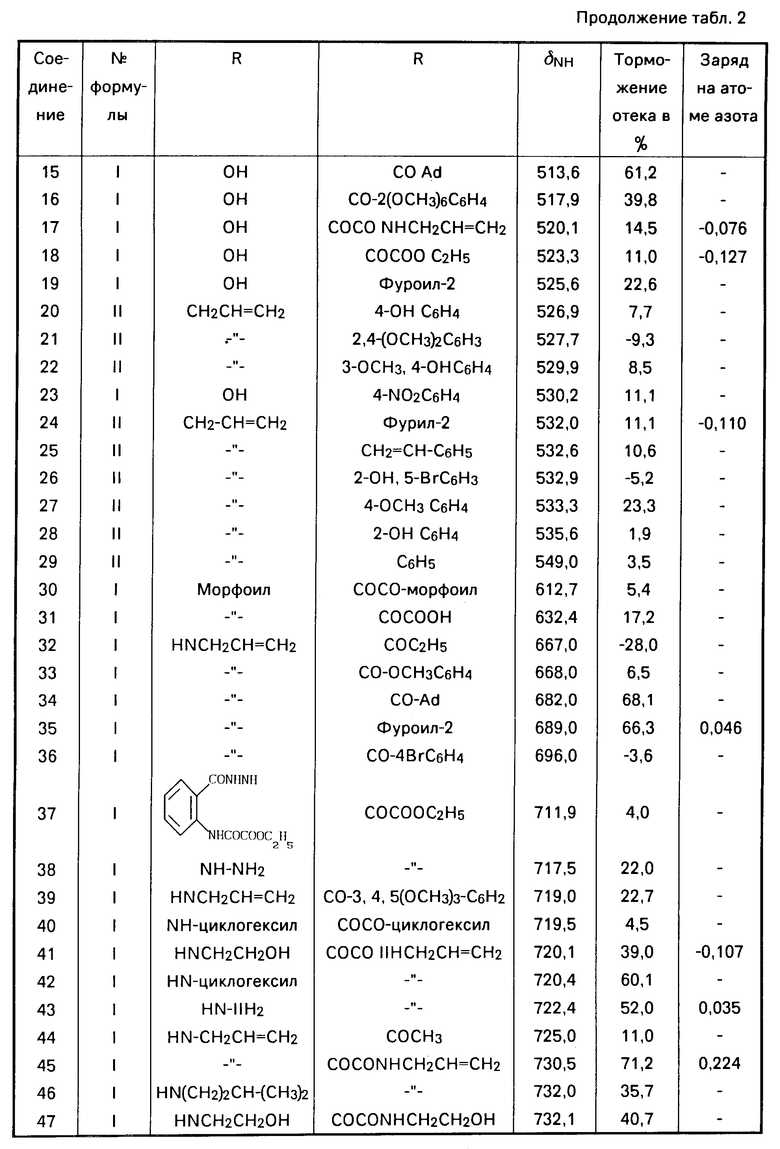
Из исследуемых 57 веществ обнаружено, что химический сдвиг протона группы NH коррелирует с зарядом на атоме азота у 15 соединений (r=0,789 при доверительной вероятности 99%). Квантово-химические расчеты по расширенному методу Хюккеля и их корреляционная связь с химическим сдвигом подтверждает достоверность экспериментальных данных ПМР-спектроскопии. Предварительная регистрация химического сдвига протона группы NH позволяет проводить отбор биологически активных веществ. Результатом исследований и изучения связи химсдвига протона группы NH и противовоспалительного действия испытуемых веществ способствовало выявлению активных в противовоспалительном отношении (торможение отека 30%) областей химсдвига протона группы NH для веществ различных химических рядов соединений, снятых в AsCl3 в концентрации 0,97±0,03 мол. эталон тетраметилсилан, выраженная в Гц: (387.392; 485.495; 505.518; 680.690; 720.732; 740,5±0,3 Гц. ±0,3 Гц это погрешность измерения химсдвига протона группы NH, поэтому погрешность каждого интервала составляет ±0,3 Гц.
Из 57 соединений, использованных нами, 17 попали в интервал биологически активной области химсдвига протона, это составило 30% Из этих 17 соединений 15 проявили в эксперименте биологическую активность, что составило 88,3%
Это послужило основанием для анализа противовоспалительной активности веществ с определенным химсдвигом протона группы NH, попадающим в определенные интервалы. В дальнейшем это нашло подтверждение при предварительном экспериментальном исследовании веществ не только среди производных антраниловой кислоты и хиназолина, но и производного ряда фенилуксусной кислоты (ортофена). Предлагаемый способ работает в том случае, если у синтезированных соединений имеется протон при атоме азота, а амино-группа непосредственно связана с фенильным радикалом.
Примеры 1 и 2 новые вещества, пример 3 известное вещество.
П р и м е р 1. 2,4-Дихлорбензоилантраниловая кислота (соединение 10). 0,0202 г вещества растворили в AsCl3 и получили 0,97 мол. раствор. Снимали ПМР-спектр на спектрометре РС-60 с частотой прибора 60 МГц при 25оС. Внутренний стандарт тетраметилсилан (ТМС). Химические сдвиги измеряли методом боковых сигналов. За наблюдаемый химсдвиг принимали среднее арифметическое 6-8 измерений. Погрешность измерения химсдвигов не превышала ±0,3 Гц (0,005 м.д.). Химический сдвиг протона NH-группы составил 506,7 Гц.
Противовоспалительное действие изучали на модели острого асептического воспаления, вызванного субплантарным введением в заднюю лапу крысы 0,1 мл 1% -ного раствора каррагенина. Изменение объема лапы оценивали онкометрически через 4 ч после введения каррагенина. Исследуемое вещество вводили внутрибрюшинно в виде взвеси в 2%-ной крахмальной слизи в дозе 50 мг/кг за 1 ч до флогенного агента. Активность соединений оценивали в процентах торможения отека по сравнению с контролем. Торможение отека соединения 13 составило 52,2%
П р и м е р 2. Гидразид-N-этоксалилантраниловой кислоты (соединение 38). 0,0163 г вещества растворили в AsCl3 и получили 0,95 мол. раствор, снимали ПМР-спектр аналогично примеру 1. Химсдвиг протона NH-группы соединения 38 составил 717,5 Гц. Исследования на противовоспалительную активность показали торможение отека на 22%
П р и м е р 3. Аллиламид N-этоксалилантраниловой кислоты (соединение 55). 0,0183 г вещества растворили в AsCl3 до получения концентрации 0,98 мол. ПМР-спектроскопические и биологические исследования проводили аналогично примеру 1. Химический сдвиг протона группы NH соединения 55 740,6 Гц, торможение отека 60,1%
Сравнение данных табл.1 и 2 показывает, что проведение анализа по предлагаемому способу расширяет круг анализируемых веществ (за счет подбора универсального растворителя АsCl3), повышает точность измерений за счет концентрации 0,95-0,98 мол. и позволяет определить наиболее активные области химсдвига протона NH-группы, а группа NH непосредственно связана с фенильным радикалом для отбора веществ, обладающих противовоспалительным действием.


Использование: биология, медицина, для отбора противовоспалительных средств. Сущность: исследуемое вещество растворяют в трихлориде мышьяка и регистрируют ПМР-спектр, затем расчитывают величину химического сдвига NH-групп, связанных с фенильным радикалом и по его величине осуществляют отбор. 2 з.п. ф-лы, 2 табл.
| Хим.фарм.журн | |||
| Пуговица для прикрепления ее к материи без пришивки | 1921 |
|
SU1992A1 |
| Способ запрессовки не выдержавших гидравлической пробы отливок | 1923 |
|
SU51A1 |
Авторы
Даты
1995-09-10—Публикация
1992-09-10—Подача