Изобретение относится к новым химическим соединениям, в частности к N-ацилмоногидразидам малеиновой кислоты, которые проявляют противосудорожную активность.
Вышеуказанное свойство предполагает их использование в медицинской практике в качестве противосудорожных средств.
Известен N-ацетилмоногидразид малеиновой кислоты формулы I
СН3СОNHNHCOCH = CHCOOH,
который является ближайшим структурным аналогом предложенных соединений.
Однако биологическая активность или какое-либо назначение этого вещества не указаны.
В настоящее время в медицинской практике в качестве противосудорожного препарата используют гексамидин формулы II
H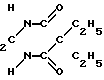
Однако гексамедин обладает замедленным противосудорожным действием и высокой токсичностью (см. таблицу).
Целью изобретения является расширение ассортимента производных моногидразидов малеиновой кислоты, проявляющих высокую противосудорожную активность и обладающих низкой токсичностью.
Поставленная цель достигается предложенным соединением общей формулы III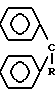 -CONHNHCOCH = CHCOOH , где R-H(a), OH(б).
-CONHNHCOCH = CHCOOH , где R-H(a), OH(б).
Способ получения соединений общей формулы III, основанный на известной реакции взаимодействия амида кислоты с соответствующим ангидридом, заключается в том, что гидразид дифенилуксусной кислоты или бензиловой кислоты подвергают взаимодействию с эквимолярным количеством малеинового ангидрида в среде бензола при комнатной температуре.
Реакцию осуществляют по следующей схеме: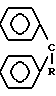 -CONHNH
-CONHNH
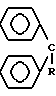 -CONHNHCOCH=CHCOOH, где R имеет указанные значения.
-CONHNHCOCH=CHCOOH, где R имеет указанные значения.
Выход целевых продуктов составляет 92,8-98,0%.
Соединения формулы III представляют собой бесцветные кристаллические вещества, растворимые в спирте, ацетоне, хлороформе и трудно растворимые в воде.
П р и м е р 1. N-Дифенилацетилмоногидразид малеиновой кислоты.
К раствору 6,78 г (0,03 моль) гидразида дифенилуксусной кислоты в 400 мл бензола добавляют при перемешивынии раствор 2,94 г (0,03 моль) малеинового ангидрида в 200 мл бензола.
Полученную реакционную смесь выдерживают в течение 1 ч, затем бензол испаряют и остаток перекристаллизовывают из спирта. Получают 9,0 г (92,8%) кристаллического продукта с Т.пл. = 191-192оС (с разложением).
Вычислено,%: N 8,64; С 66,66; Н 4,97.
Найдено,%: N 8,85; С 66,45; Н 4,72.
П р и м е р 2. N-Бензилоилмоногидразид малеиновой кислоты.
К раствору 7,26 г (0,03 моль) гидразида бензиловой кислоты в 400 мл бензола добавляют при перемешивании раствор 2,94 г (0,03 моль) малеинового ангидрида в 200 мл бензола. Полученную реакционную смесь выдерживают в течение 1 ч, затем бензол испаряют и остаток перекристаллизовывают из водного спирта. Получают 10,0 г (98,0%) кристаллического продукта с Т.пл. = =171-172оС (с разложением).
Вычислено,%: N 8,23; С 63,53; Н 4,74.
Найдено,%: N 8,37; С 63,70; Н 4,62.
В ИК-спектре N-дифенилацетилмоногидразида малеиновой кислоты (IIIa) присутствует полоса поглощения при 1703 см-1, обусловленная валентными колебаниями карбонила карбоксильной группы, полоса при 1670 см-1, обусловленная колебаниями амидных карбонилов, а также полоса при 3180-3170 см-1, соответствующая колебаниям NH-групп.
В спектре ПМР соединения IIIa, снятом в растворе дейтерированного диметилсульфоксида, присутствуют синглет протона СН-группы при 5,08 м.д., синглет протонов двух СН-групп малеинового остатка при 6,32 м.д., мультиплет десяти протонов фенильных радикалов и протонов двух NH-групп с центром около 7,32 м.д., а также синглет протона карбоксильной группы при 10,68 м. д.
В ИК-спектре N-бензилоилмоногидразида малеиновой кислоты (IIIб) присутствует полоса поглощения при 1705 см-1, обусловленная валентными колебаниями карбонила карбоксильной группы, полоса при 3215-3205 см-1, соответствующая колебаниям NH-групп, а также полоса при 3338 см-1, обусловленная колебаниями гидроксильной группы.
В спектре ПМР соединения IIIб, снятом в растворе дейтенированного ацетона, присутствуют два дублета протонов двух СН-групп при 6,28 и 6,63 м.д., мультиплет десяти протонов фенильных радикалов и протонов двух NH-групп с центром около 7,42 м.д., а также синглет протона гидроксильной группы при 10,05 м.д.
Противосудорожную активность предложенных соединений изучают на белых мышах при внутрибрюшинном введении по тесту максимального электрошока.
Острую токсичность N-ацилмоногидразидов малеиновой кислоты изучают на белых мышах при внутрибpюшинном введении.
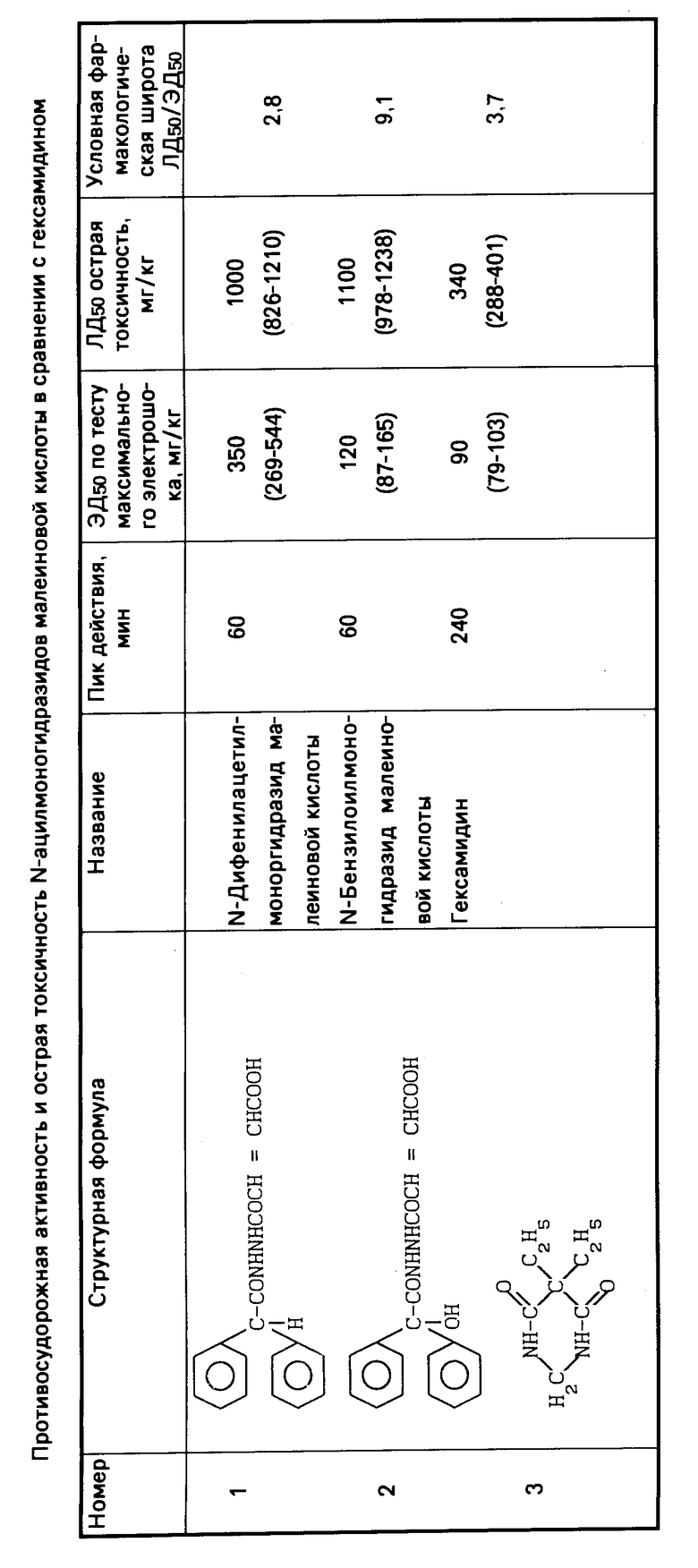
Как видно из таблицы, предложенные соединения проявляют максимальную противосудорожную активность через 60 мин, действие гексамидина проявляется через 240 мин. Первое соединение уступает гексамидину по силе действия в 3,8 раза, второе в 1,3 раза, но они менее токсичны, чем гексамидин соответственно в 2,9 и 3,2 раза.
Важным показателем ценности лекарственного препарата, позволяющим судить о его безвредности, является условная фармакологическая широта - отношение средней летальной дозы ЛД50 к средней эффективной дозе ЭД50.
Условная фармакологическая широта N-бензилоилмоногидразида малеиновой кислоты в 2,5 раза больше, чем у гексамидина, а у N-дифенилацетилмоногидразида малеиновой кислоты незначительно ему уступает.
Противосудорожное действие предложенных соединений развивается в 4 раза быстрее, чем у гексамидина.
Таким образом, N-ацилмоногидразиды малеиновой кислоты проявляют противосудорожную активность, менее токсичны, чем гексамидин, и действуют быстрее, они могут найти применение в медицинской практике в качестве лекарственных препаратов.
N-Ацилмоногидразиды малеиновой кислоты формулы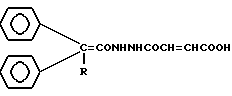

где R - H, OH,
проявляющие противосудорожную активность.
| Бюдер К., Пирсон Д | |||
| Органические синтезы | |||
| М.: Мир, ч.2, 1973, с.389-390. |
Авторы
Даты
1994-11-15—Публикация
1982-04-28—Подача