Изобретение относится к способу получения новых со формулы NHNHC(o)c - : . R где 5 - R Н; ,jHf; R -ен,; II - ,H,; R C2Hy; Ю - R H; ,H7; IV- R 4-Br: ,Hl; V- R-A-CH O; .a . которые могут найти примен исходные вещества для синт гически активных соединени Соединения (I)-(V) отно классу арилгидраэидов «1, ных алифатических кислот. Известен способ получен « гидразидов «i ,|3-непредельны заключающийся во взаимодей 02 нилгидразина со свободными кислотами l . Однако этот способ неудобен тем, что реакция проводится в запаянной трубке при 200°С, а таюте ограничен доступностью некоторых непредельных кислот, в частности оС-бутил-й-пропилакриловой кислоты. Целью изобретения является разработка нового способа получения новых арилгидразидов oi , й-дизамещенных акриловых кислот, которые могут быть использованы в качестве исходных для синтеза биологически активных веществ, исходя из легко доступных арилгидразидов диалкилгликолевых кислот 2 , Поставленная цель достигается предлагаемым способом, заключающимся во взаимодействии одного эквивалента арилгидразвда диалкилгликолевой кислоты с эквивалентным количеством пятихлористого фосфора в диоксане при комнатной температуре, последующей обработке реакционной смеси фенолом с вьщелением промежуточного продукта - кристаллического комплекса арилгидразида хлордИалкилуксусной кислоты с фенолом - и нагревании его в течение 3-5 мин при 120-130 С с последующим вьщелением целевого продукта. Процесс проходит по схеме:
i
К
(0)с:(к )гХСбН50Н(,2)У1-Х /j
t I ly-JldT T7-NHNHC(0)-Cl CiHR -PhOn / .K
Образующиеся арилгидразиды X ,дизамещенных акриловых кислот не описаны в литературе.50
Промежуточные комплексы арилгидразидов хлордиалкилуксусных кислот с фенолом (Vi)-(X) представляют собой бесцветные кристаллические вещества ,55 (табл. 1), нерастворимые в воде, хорошо растворимые в органических растворителях (эфире, бензоле, хлороформе, этилацетате). Их состав и структура подтверждаются данными элементного анализа на азот и хлор, ИК- и ПМР-спектрами. В ИК-спектрах соединений (V1)-(X), снятых на приборах Specord-IR-75 и ИКС-22 в вазелиновом маслр, в области 3100-3300 см наблнщается широкая полоса двух NH-rpynn гидразида и ОН-группы фенола, Ьвязанных водородными связями; поглощение карбонильной группы - в области 1640-1660 , В ИК-спектрах 0,003 М растворов в четыреххлористом углероде, снятых на приборе UR-20, наблюдаются полосы свободного фенольного гидроксила 3610-3615 см , хорошо разрешенные полосы,двух NHгрупп 3400-3450 и 3320-3350 см .полоса карбонила при 1670-1680 см. В ПМР-спектре вещества (УШ), снятом на приборе, Tesla BS-487-C в СС1 , присутствуют сигналы этильной группы So,9 (6Н,т, СН-) и 1,9 (4Н, KB, ) М.Д., сигнал oi -Ш-группы при 8,63 (1Н, с) и сигналы ароматических протонов 6,45-7,20 м.д., по интеграл ной интенсивности равные 17 протонам так как протоны й-Ш-группы и феноль ного гидроксила резонируют в этой же области. Арилгидразиды о ,/ -дизамещенных акриловых кислот (1)-(V) (табл. 2) это бесцветные кристаллические вещества, нерастворимые в воде, хорошо растворимые в органических растворителях. ИК-спектры соединений (1)-(V) снятые в вазелиновом масле, содержат широкие полосы поглощения двух NHгрупп, связанных водородными связями с карбонильными группами, с максимумом поглощения 3200-3250 , а также полосы 1650-1660 () и 16101660 () . В ПМР-спехтрах веществ (1)-(1V) наблюдаются триплеты олефинового протона для 5-10%-ных растворов в CCl;j 85,88-6,09(вещества (1), (Ш) или дейтероацетоне 6,20-6,23 м.д. (вещества (П), (V) с константой Гц. Вещества (1)-(V) получены в виде смеси цис- и трансизомеров. Разность химических сдвигов олефиновых протонов, вычисленная для цис- и транс-форм по известному методу , составляет всего 0,03 м.д., или 2,4 Гц, чем объясняется некоторая размытость триплетов олефиновых протонов в .ПМР-спектрах этих соединений. Крометого, в ПМР-спектре, в СС1д, напри- ,мер5 соединения (1) наблнщакггся следующие сигналы: 8 0,79 (ЗН, т, СН,, ,5 Ги), 1,55 (ЗН, д, СН,,-СН, Гц), 2,14 (2Н, KB, СН,, Гц), 6,35-7,08 (5Н, м, ароматические протоны), 9,14 м.д. (1Н, с,об- NH), сиг нал 1 -NH-группы - в области резонан са ароматических протонов. Пример 1. Комплекс фенилгидразида хлордиэтилуксусной кислоты с фенолом (VI). 22,0 г (0,1 моль) фенилгидразида диэтилгликолевой кислоты pQ растворяют в 100 мл абсолютного диоксана, прибавляют порциямипри перемешивании 20,85 г (0,1 моль) порошкообразного пятихлористого фосфора, оставляют на 12 ч, прибавляют г (0,8 моль) фенола, выпивают в чашку для удаления растворителя под тягой, через 1 сут ставят на холод, через 2сут отфильтровывают 22,5 г комплекса, кристаллизуют из гексана, получают 20,2 г (52%) вещества (VI), т.пл. 73-74 С. Аналогично получают (vn)-(x). П р и м е р 2. Фенилгидразид сС-этилкротоновой Кислоты (1). 2,38 г (0,0071 моль) вещества VI нагревают до 105 С (начало экзотермической реакции), затем вьщерживают 3мин при 120°С, после чего перегоняют с паром. Остаток растворяют в 50 МП эфира, супГат сульфатом натрия, после удаления эфира остаток хроматографируют на колонке с 20 г силикагеля L 100/400, элюируют 250 мл бензола, бензол отгоняют, остаток кристаллизуют из смеси спирт - гексан 1:1. Выход вещества (1) 0,48 г (33%), т.пл. 101-102°С. Увеличение продолжительности реакции до 10 мин и более приводит к значительному осмолению. Примерз. Фенилгидразид л бутил-р-пропилакриловой кислоты (Ш). , 3,91 г (0,01 моль) вещества (VDI) расплавляют в фарфоровой чашке и выдерживают 5 мин при 130 С. Отгоняют фенол с паром, остаток экстрагируют 100 МП эфира, сушат сульфатом натрия, после удаления растворителя кристаллизуют из смеси гексан - спирт 4:1, получают 1,66 г (64%) вещества (Ш), т.пл. 103-104с,. Аналогично получают соединения (П), (1V)-(V). Таким образом, данный способ получения арилгидразидов о ,-дизамещенных акриловых кислот прост, осуществляется в две стадии из арилгидразидов дизамещенных гликолевых кислот и не требует труднодоступных реактиво. $1142470 Комплексы арилгидразидов хлордиалкилуксусных
Г
NHNHC(0)C (К )2 ХСбНйОН 6 Таблица 1 кислот с фенолом .(,2)

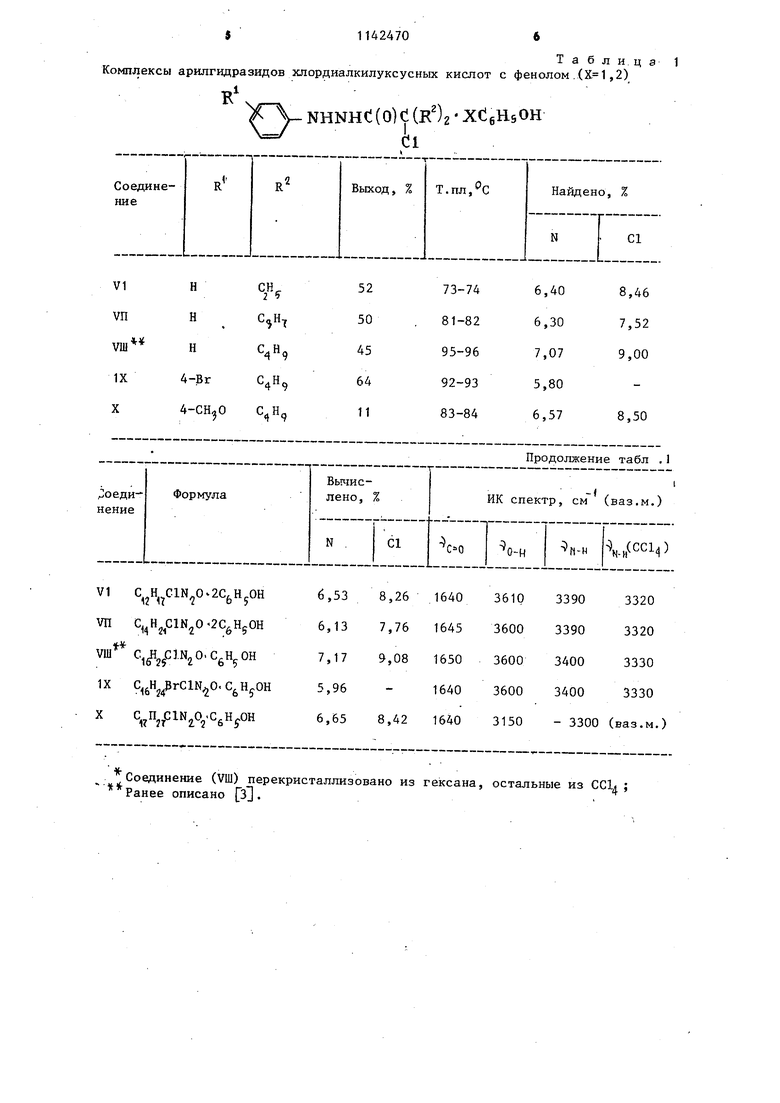
СПОСОБ ПОЛУЧЕНИЯ АРИЛгидрАзвдов oi ./НШЗАМЕЩЕННЬК АКРИЛОВЫХ кислот формулы rV NHNHt 
Соединение (УШ) перекристаллизовано из Ранее описано зЗ.
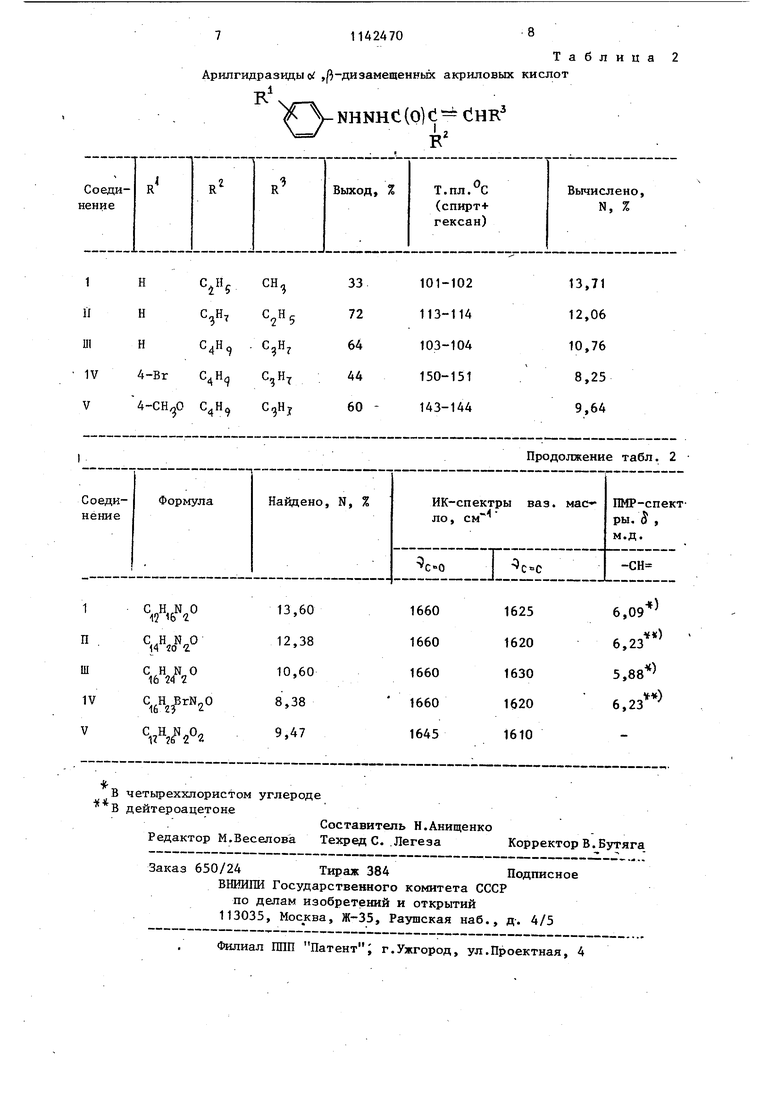
Продолжение табл ,1 гексана, остальные из CCL ; 71142470 Арилгидразиды 0 ,р-дизамещенньк акриловых
Л-кнынс(о)с; с1нк / .
Продолжение табл. 2 в Таблица 2 кислот
Авторы
Даты
1985-02-28—Публикация
1983-06-28—Подача