Изобретение касается содержащих серебро катализаторов на носителе, служащих для окисления алкена, в частности этилена, и соответствующую окись алкилена, например окись этилена, которые заключают содержащий марганец компонент в количестве, обеспечивающем повышение стабильности и/или эффективности и/или активности.
Окись этилена получается в промышленных условиях путем эпоксидирования этилена над содержащим серебро катализатором при повышенной температуре. Проведены работы, имеющие целью получение катализаторов, которые повышают эффективность или избирательность процесса получения окиси этилена.
Известен процесс получения окиси этилена путем реакции кислорода или кислородсодержащего газа с этиленом в присутствии серебряного катализатора. Так, например, известно получение окиси этилена путем реакции кислорода с этиленом в присутствии серебряных катализаторов, содержащих класс металлических промоторов. Известно, что окислы олефина могут быть получены путем смешивания олефинов непосредственно с молекулярным кислородом в присутствии серебряного катализатора. Ввиду этого основные усилия были направлены на улучшение эффективности катализатора для получения окиси этилена.
В данном изобретении используются понятия "конверсия", "избирательность" и "выход".
Серебряные катализаторы, используемые для получения окиси этилена, претерпели существенные изменения, начиная с первоначального периода их разработки. Частицы серебра первоначально осаждались на материалы носителя, при этом не уделялось большого внимания свойствам носителя, таким как удельная поверхность, объем пор и химическая инертность. По мере дальнейших разработок появились специальные технологии, касающиеся носителей или подложек, содержащих серебро, которые более эффективны в реакциях этилена с кислородом с образованием окиси этилена. В настоящее время большинство носителей серебряных катализаторов имеют форму частиц, которые могут вводиться внутрь реактора, в котором реагирующие газы и газообразные продукты реакции способны проходить внутрь и вокруг этих частиц, проходя через реактор и регенерируясь. Размер и форма носителя являются переменными параметрами и размер и форма частиц выбираются в зависимости от используемого реактора и перепада давления в реакторе с учетом других факторов.
Носители, которые должны использоваться для катализаторов, обычно изготавливаются из неорганических материалов, как правило минерального происхождения. В большинстве случаев предпочтительный носитель изготавливается из альфа-окиси алюминия.
Носители, используемые для получения большинства промышленно применяемых катализаторов для получения окиси этилена изготавливаются фирмами, которые не производят эти катализаторы. Для изготовления носителя, обеспечивающего уникально желаемые характеристики для производства успешного катализатора, критически важными могут быть ряд факторов, таких как чистота и другие физические/химические свойства сырьевых материалов, служащих для получения этого носителя, и способ получения носителя.
Серебро, осаждаемое на этих носителях, имеет форму небольших частиц. Известно, что размер частиц серебра является фактором, обусловливающим эффективность катализатора, и в большинстве случаев тонкие частицы серебра получаются с помощью общеизвестных приемов.
Используются частицы серебра размерами 150-400 А), а также диаметром менее 1000 А. Усовершенствования микроскопических методов исследования серебряных катализаторов дают возможность наблюдать, что размеры частиц могут достигать еще меньших значений.
Осаждение серебра на носитель может осуществляться различными способами, но два способа, используемые наиболее часто, включают в одном случае пропитку носителя раствором серебра с последующей термической обработкой пропитанного носителя для осаждения серебра на носителе, и в другом случае покрытие носителя серебром путем осаждения серебра или предварительного перевода серебра в суспензию с тем, чтобы частицы серебра осаждались на носителе и адгезионно связывались с поверхностью носителя, когда этот носитель или подложка нагревается с целью удаления присутствующей там жидкости.
Удельная поверхность, создаваемая за счет носителя, является предметом, представляющим большой интерес для разработки серебряных катализаторов. Известно, что вполне подходящей является удельная поверхность 0,002-10 м2/г. Известны патенты США, в которых указывается значение пористости 35-65% и диаметр пор 80-200 мкм, удельная поверхность менее 1 м2/г и средний диаметр пор 10-15 мкм, а также использование носителя, имеющего среднюю пористость примерно 30% с количеством пор менее 90% которые имеют диаметр в пределах 1-30 мкм, и со средним значением таких диаметров в пределах 4-10 мкм. В одном из известных патентов используется носитель катализатора, имеющий удельную поверхность менее 1 м2/г, объем 0,23 мл/г и размер частиц 0,074-0,30 мм). Согласно известным способам успешно используется альфаокись алюминия с низкой удельной поверхностью.
Известно, что примеси, присутствующие в катализаторе и/или в газовой фазе, могут существенно повлиять на ход реакции. В первоначальных разработках не существовало способа идентификации или определения таких примесей, ввиду чего нельзя было выяснить, какую роль играют эти примеси. Однако даже в ранние периоды разработок было хорошо известно использование щелочных металлов в качестве промоторов получения окиси этилена, катализированного серебром. В известных патентах США описывается использование щелочных металлов в серебряных катализаторах, в также говорится, что очень желательным в качестве промотора является литий, но калий и цезий оказывают вредное действие на окись серебра, используемую при приготовлении катализатора, при использовании гидрата окиси калия или гидрата окиси цезия в количестве 10 мас. В более поздних патентах США говорится, что натрий и литий являются эффективными промоторами для данной реакции. Кроме того, щелочные металлы в форме их сульфатов эффективны в качестве промоторов для таких серебряных катализаторов. В частности, в качестве промоторов могут использоваться сульфаты натрия, калия, лития, рубидия или цезия.
Известна предварительная обработка носителя разбавленным раствором хлорсодержащего соединения (такие хлористые соединения должны быть неорганическими продуктами). Иллюстрированные примеры подходящих соединений хлора включают хлорид натрия, хлорид лития и хлорат калия. Количество неорганического хлорсодержащего соединения, осаждаемого на носителе катализатора, составляет 0,0001-0,2 мас. в расчете от весового количества носителя. Известно использование галоида металла для обработки катализатора на носителе, такие галоиды могут быть галоидами щелочного металла лития, натрия, калия и цезия. Галоид металла присутствует в пределах 0,01-50 мас. в расчете от весового количества металлического серебра. Для улучшения или увеличения периода до разрушения новой катализаторной композиции могут использоваться смеси отдельных галогенидов металла, которые одновременно сохраняют умеренную, но постоянную активность катализатора в течение увеличенного периода времени в ходе нормальной рабочей операции. Так, например, катализатор, обработанный одним галогенидом металла, обеспечивает кратковременную высокую начальную активность, в то время катализатор, обработанный другим галогенидом металла, обеспечивает длительную умеренную активность действия. Определено, что галогениды металла, используемые в катализаторе, ингибируют сжигание этилена до двуокиси углерода. Таким образом данные материалы относятся к катализаторным депрессантам или к противокатализаторным материалам.
Известно использование серебряного катализатора для получения окиси этилена, где одновременно с вводом серебра в твердый носитель предусматриваются любые галогениды щелочного металла, такие как литиевые, натриевые, калиевые и рубидиевые соединения хлора, брома и йода, для повышения общего выхода окиси этилена. Определены небольшие количества этих соединений "желательны количества менее чем ≈ 0,5%". В частности, наиболее предпочтительны пропорции галогенида щелочного металла в пределах 0,0001-0,1% В известном патенте говорится, что "хотя предпочтительная катализаторная композиция содержит отдельный промотор, он не всегда обязателен, поскольку в ходе получения катализатора галогенид щелочного металла может быть в некоторой степени превращен в соответствующую окись металла, которая действует как промотор". Кроме того, цезий и калий оказывают вредное действие на серебряные катализаторы, полезными промоторами являются натрий и литий. Однако в другом патенте США говорится, что натрий, калий и литий являются промоторами в случае их использования в серебряных катализаторах и рекомендуется также предварительная обработка носителя разбавленными растворами хлорида натрия, хлорида лития или хлората калия.
В известных патентах США рекомендуется, чтобы содержание неорганического галогенида как компонента катализатора поддерживалось в пределах 0,01-5 мас. предпочтительно в пределах 0,01-0,1 мас. в расчете на весовое количество серебряного компонента катализатора окисления, т.е. соль серебра, превращаемую в элементарное серебро. Указывается ряд металлов в качестве промоторов и одним из этих металлов является цезий. Рекомендуется использование щелочных металлов, таких как литиевые соединения в качестве промоторов. Предпочтительное количество промотирующего материала примерно 0,03-0,5 мас. (окиси металла) в расчете на весовое количество носителя. В известных патентах США говорится, что хлориды щелочного металла "противодействуют образованию двуокиси углерода" и "могут быть введены в катализатор", а также описывается серебряный катализатор на носителе, содержащий сопутствующе осажденный щелочной металл, выбранный из числа платины, рубидия и цезия в определенном грамм-атомном соотношении с серебром. Весовое количество серебра предпочтительно 2-5 мас. от катализатора. Данный катализатор характеризуется как наиболее подходящий для реакции окиси азота с пропиленом. Этот же катализатор получается согласно известным способам, которые позволяют использовать их для получения окиси этилена. Катализатор используется также для получения окиси этилена. В известном патенте США описывается совместное осаждение щелочного металла и серебра на носителе, причем щелочные металлы находятся на носителе в их конечной форме форме оксида и этот оксид состоит из оксида цезия, рубидия и их смесей при желании в комбинации с незначительным количеством оксида калия. Количество такого оксида составляет от 4 х 0 х 10-5 диб /кг до 8,0 х 10-3 диб/ кг от суммарного количества катализатора. Описывается использование этого катализатора. Известны также некоторые интересные данные, заслуживающие пояснений. Согласно примеру 2, в котором описываются некоторые сравнительно эксперименты, осуществляется получение катализатора, содержащего 310 ч. на миллион (вес) совместно введенного калия, и этот катализатор при использовании его как катализатора окисления этилена неактивен для получения окиси этилена.
В описании известного немецкого патента в примерах иллюстрируется серебряный катализатор получения окиси этилена, содержащий натрий и либо калий, либо рубидий, либо цезий.
Описание известной японской патентной заявки касается способа получения окиси этилена с использованием катализаторной композиции, содержащей серебро, барий, калий и цезий в определенных атомных отношениях.
Известен катализатор для получения окиси этилена, содержащий серебро, олово, сурьму, таллий, калий, цезий и кислород в определенных атомных отношениях.
В известном бельгийском патенте описываются серебряные катализаторы, содержащие различные смеси натрия с цезием. В патентной заявке Великобритании приводятся серебряные катализаторы на носителе, содержащие различные смеси цезия и таллия, из которых некоторые дополнительно содержат калий или сурьму. В известном патенте США дается широкое описание серебряных катализаторов получения окиси алкилена, содержащих серебро "вместе с промотирующим количеством по меньшей мере одного промотора, выбранного из числа следующих: литий, калий, натрий, рубидий, цезий, медь, золото, магний, цинк, кадмий, стронций, кальций, ниобий, тантал, молибден, вольфрам, хром, ванадий и барий.". В известных патентах США описываются катализаторы и способы эпоксидирования олефинов в присутствии многометаллического компонента. Катализатор включает незначительное количество одного или более чем одного из металлов: палладий, рутений, рений, железо и платина со значительным количеством серебра. Описывается получение катализатора из способной к разложению соли металла группы 7b, 1b или подгруппы железа группы 8 периодической таблицы элементов. Эта соль выбирается предпочтительно из группы солей золота, меди, рения, марганца и железа. Хотя в этих патентах говорится, что данные металлы находятся в условиях эпоксидирования может происходить окисление с одним или более чем одним из этих металлов, например с рением, образованием оксианионов, содержащих данный металл.
Известно использование окиси бериллия в качестве промотора. Предлагаются другие металлические промоторы, такие как медь, алюминий, марганец, кобальт, железо, магний, золото, торий, никель, цезий и цинк. Эти металлические промоторы вводятся в катализатор путем механического смешивания или совместного осаждения.
В известных патентах описываются содержащие серебро катализаторы, которые включают смеси калия с цезием, и катализатор, содержащий натрий и цезий, а также серебряные катализаторы на носителе, содержащие взятый в эффективном количестве литий и несколько меньшее количество щелочного металла, выбранного из числа следующих: цезий, рубидий и/или калий. Описываются также серебряные катализаторы на носителе для получения окиси этилена, содержащие определенное количество калия и по меньшей мере один щелочной металл, выбранный из числа следующих: рубидий или цезий.
Известно использование синергетической комбинации цезия и по меньшей мере одного другого щелочного металла в сочетании с серебром на инертном носителе с образованием катализаторов, которые превосходят известные на указанный момент времени катализаторы. Эти катализаторы находят широкое промышленное применение.
Щелочной металл как компонент катализатора наносится на носитель различными приемами. Щелочной металл может наноситься на носитель в виде соли и описываются многие соли щелочного металла. Иллюстрируется использование сульфатов щелочного металла как одного из многих применяемых соединений щелочного металла.
Известен катализатор получения окиси этилена, в котором осуществляется "химическая абсорбция" цезия и/или бериллия на катализаторный носитель путем спиртовой промывки.
Известны также катализаторы, содержащие молибдат цезия или вольфрамат цезия или борат цезия. Этот катализатор имеет носитель в форме окиси алюминия с содержанием натрия менее чем 0,07 мас. и состоящий главным образом из альфа-окиси алюминия с удельной поверхностью 1-5 м2/г. Этот носитель пропитывается раствором разлагающейся соли серебра, содержащим комплекс щелочной металл бор, комплекс щелочной металл-молибден и/или комплекс щелочной металл-вольфрам. Не дается ни одного примера смесей анионов. Описываются содержащие таллий катализаторы, в которых таллий может находиться в форме боратной или титановой соли.
Известны катализаторы, содержащие щелочной металл и/или барий, которые могут иметь форму соли. Эти соли включают нитраты, сульфаты и галогениды. Описываются катализаторы, содержащие рениевый компонент, например окись рения, рениевый катион или ренат, или перренатный анион.
Как установлено, ренат повышает эффективность, особенно в присутствии некоторых "со-промоторов", таких как сульфатный анион. Кроме того, когда количество рената увеличивается или используется со-промотор, который увеличивает эффективность, то в большинстве случаев температура, необходимая для степени конверсии кислорода 40% ("Т40, оС), также увеличивается. Присутствие 55 ч/мин Mn в виде KMnO4 оказывает небольшое или даже совсем не оказывает действия на избирательность при степени конверсии кислорода 40 мол. или Т40.
Хотя желательны повышенные степени конверсии окиси этилена, сопутствующее увеличение температуры (т.е. потеря активности) может быть нежелательным для промышленно доступных катализаторов. Установки промышленного получения окиси этилена обычно работают таким образом, что обеспечивают желаемый баланс и эффективности. Таким образом менее активные катализаторы функционируют при более высоких температурах для достижения желаемого выхода. Однако верхний температурный предел катализатора является ограниченным. Следовательно, катализаторы, имеющие высокую начальную температуру для данной степени конверсии, могут иметь менее продолжительный срок службы. Для владельца установки основную статью расхода составляет не только катализатор, но и необходимость отключения установки на значительные периоды времени для выгрузки отработанного катализатора и загрузки нового катализатора в типичный трубчатый реактор с неподвижным слоем окиси этилена. Следовательно, при использовании катализатора, не имеющего желаемого срока службы, а именно 2 года или более, преимущество, достигаемое в отношении повышенной эффективности, быстро теряется за счет расходов, связанных с заменой катализатора и отключением установки.
Известно использование марганца в катализаторе, например, оксихлорирование алканов в присутствии твердой порошкообразной катализаторной композиции, включающей: (1) металлическое серебро и/или его соединение, и (2) одно или более соединений марганца, кобальта или никеля. В известной японской патентной заявке описываются катализаторы разложения озона. Данные катализаторы приготавливаются путем ввода 0,1 20 мас. серебра и 1-20 мас. окиси кобальта (рассчитано как атомный процент кобальта) в двуокись марганца. Известны марганцево-серебряные катализаторы каталитического окисления окиси углерода, например, один из патентов США касается катализаторов системы нитрат нитрат для отделения кислорода от кислородсодержащих газов, таких как воздух. Этот катализатор включает оксид переходного металла из группы, включающей оксиды марганца, рутения, рения, осьмия, родия, иридия и их смесей.
Проводятся поиски способов, обеспечивающих активность и/или стабильность содержащих серебро нанесенных на носитель катализаторов получения окиси этилена, которые промотированы с целью повышения эффективности. Они, обеспечивая желаемые эффективности, обычно менее активны и должны функционировать при более высоких температурах в промышленных установках. Эти высокие температуры могут чрезмерно сократить срок службы катализатора настолько, что эти катализаторы станут нежелательными для использования в промышленных установках.
Согласно изобретению предусматриваются содержащие серебро нанесенные на носитель катализаторы получения окиси алкилена, пригодные для эпоксидирования алкена в окись алкена, имеющие повышенную активность и/или эффективность действия и/или стабильность. Эти катализаторы содержат достаточное количество осажденного на них по меньшей мере одного марганцевого компонента, обеспечивающего увеличение по меньшей мере одной из характеристик активности и/или эффективности и/или стабильности катализатора по сравнению с аналогичным катализатором, но не содержащим марганцевого компонента в идентичных во всех других отношениях условиях. Часто марганцевый компонент присутствует в количестве не менее чем примерно 20 или 60, например примерно 70-1000, предпочтительно 80-500 ч/млн (по весу) в расчете на весовое количество всего катализатора. Количество марганца, обеспечивающего повышенную активность и/или эффективность и/или стабильность, обычно изменяется в зависимости от природы и количества других компонентов в катализаторной композиции.
Катализаторы, отвечающие изобретению, содержат количество повышающего активность марганцевого компонента по меньшей мере достаточное для увеличения активности катализатора при определении в стандартных условиях процесса получения окиси этилена (определено в данном описании), при температуре не менее 5оС, предпочтительно не менее 10оС.
Когда активность катализатора повышается, то температура, требуемая для получения в заданных условиях заданного количества окиси алкилена (обычно выражаемая через увеличение концентрации окиси алкилена в слое катализатора), снижается. Стабильность катализатора может быть непосредственно связана со скоростью снижения по меньшей мере либо эффективности его действия, либо активности его действия. В случае более стабильного катализатора скорость снижения эффективности и/или активности окисления меньше, чем в случае менее активного катализатора.
Под используемым термином "соединение" имеется в виду комбинация одного элемента с одним или более другими элементами, получаемая за счет поверхностного и/или химического связывания, например за счет ионного и/или ковалентного и/или координационного связывания. Термин "ионный" или "ион" охватывает электрически химически заряженную группу; "катионный" или "катион" является положительным и "анионный" или "анион" является отрицательным. Под термином "оксианионный" или "оксианион" имеется в виду отрицательно заряженная группа, содержащая не менее чем один атом кислорода в комбинации с другим элементом. Таким образом, оксианион является кислородсодержащим анионом. Понятно, что ионы отсутствуют в вакууме и находятся в комбинации с уравновешивающими заряд противоионами.
Данный катализатор содержит предпочтительно не менее чем один промотор в количестве, достаточном для повышения эффективности данного катализатора по сравнению с аналогичным катализатором, но не содержащим промотора. Часто этот промотор включает соединение элемента иного чем марганец, который выбран из групп от 1а и/или 2а и/или групп 3b-7b или групп 3а-7а периодической таблицы элементов. (Ссылки на периодическую таблицу элементов в публикации Chemical Rubber Company, Кливлэнд, Огайо, в CRC Handbook of Chemistry and Physics, 46 изд. внутри задней части обложки). Предпочтительные промоторы включают оксианионы иных элементов чем кислород, имеющих молекулярный вес 5-83, из группы 3b-7b и 3а-7а периодической таблицы. Наиболее предпочтительно, когда промоторы являются одним или несколькими из оксианионов азота, серы, тантала, молибдена, вольфрама и рения. Многие из этих промоторов характеризуются как повышенной эффективностью, так и пониженной активностью действия катализаторов. Катализаторы, содержащие комбинации промоторов, таких как сульфат, с одним или более оксианионами из числа элементов группы 3b-7b периодической таблицы, например молибден и рений, часто имеют значительно увеличенные активности за счет присутствия в них марганцевого компонента.
Согласно другому предпочтительному аспекту изобретения катализаторы содержат рениевый компонент, который может иметь форму катиона или аниона, например рената.
Согласно одному из предпочтительных аспектов изобретения эпоксидирование алкена в присутствии кислородсодержащего газа включает контактирование алкена с катализатора в условиях эпоксидирования в присутствии по меньшей мере одного повышающего эффективность действия газового компонента пары окислительно-восстановительной полуреакции. Катализатор включает в качестве промотора повышающее эффективность количество по меньшей мере одной повышающей эффективность соли компонента пары окислительно-восстановительной полуреакции.
Согласно другому предпочтительному аспекту изобретения, катализатор включает нитрат щелочного металла, особенно нитрат калия и/или рубидия, особенно в количествах, превышающих примерно 400 или 500 частей на млн. (ppm) (по весу) в расчете на весовое количество калия. Согласно этому аспекту изобретения азото- и кислородсодержащее соединение, например окись азота, двуокись азота, закись азота, и т.д. могут вводиться в реакционную зону, содержащую катализатор как сопромотор, для повышения по меньшей мере одной активности, эффективности или стабильности катализатора.
Согласно следующему аспекту изобретения катализатор содержит менее чем примерно 50 ч/млн (вес) и более предпочтительно менее чем 25 ч/млн (вес) выщелачиваемого калия. При таких низких содержаниях калия усиливающий эффект марганцевого компонента в некоторых случаях может быть более явным.
Один из аспектов изобретения касается использования указанных катализаторов в процессе эпоксидирования алкена с образованием окиси алкена, особенно эпоксидирования этилена в окись этилена.
Окислы алкилена, получаемые с использованием катализаторов, отвечающих изобретению, характеризуются структурной формулой
R1- 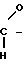
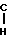 R2 в которой R1 и R2 представляют собой низший алкил, например метил или этил, или предпочтительно водород. Наиболее предпочтительно окись алкилена представляет собой окись этилена. Окислы алкилена получаются из соответствующего алкена, например из R1HC=CHR2. Для лучшего представления данной картины дается нижеследующее разъяснение в отношении окиси этилена и этилена.
R2 в которой R1 и R2 представляют собой низший алкил, например метил или этил, или предпочтительно водород. Наиболее предпочтительно окись алкилена представляет собой окись этилена. Окислы алкилена получаются из соответствующего алкена, например из R1HC=CHR2. Для лучшего представления данной картины дается нижеследующее разъяснение в отношении окиси этилена и этилена.
Катализаторы, отвечающие изобретению, характеризуются комбинацией их с достаточным количеством по меньшей мере одного марганцевого компонента, обеспечивающего повышение активности и/или эффективности и/или стабильности катализатора по сравнению с аналогичным катализатором, который не содержит марганцевого компонента. Хотя эти катализаторы могут использоваться в процессах с широко изменяющимися пределами условий для определения того, достаточное ли количество марганца введено в катализатор, могут использоваться стандартные условия процесса.
Стандартные условия процесса получения окиси этилена (АБР, "Условия") для определения характеристик катализаторов, отвечающих изобретению, заключают в себе использование стандартного автоклава с противоточным смешиванием с полным газовым рециклом, включающим использование двуокиси углерода. Эти условия могут заключать в себе некоторые непостоянства подачи этилена, кислорода и газофазного ингибитора. Иллюстрируются два случая условия воздушного процесса, которые в реакторе с противоточным смешиванием воспроизводят типичные условия, используемые в промышленных процессах получения окиси этилена в воздушных условиях, где источником молекулярного кислорода служит воздух; и условия кислородного процесса, которые в реакторе с противоточным смешиванием воспроизводят типичные условия, используемые в промышленных процессах получения окиси этилена в кислородных условиях, где используется молекулярный кислород как таковой. В каждом случае достигается различная эффективность, но как правило практически во всех случаях, где используется воздух как источник кислорода, использование меньших количеств кислорода и этилена приводит к эффективности получения окиси этилена примерно на 2-4% ниже, чем тогда, когда используется непосредственно молекулярный кислород. Когда катализатор содержит соль окислительно-восстановительной реакционной пары и предназначен для использования в сочетании с соответствующим повышающим эффективность газовым компонентом пары окислительно-восстано тельной полуреакции, то условия включают присутствие такого газового компонента. Согласно этим условиям в выходном газе из реактора используется 1,0 мол. смеси этилена при следующих стандартных условиях на входе (см. табл. 1).
При этих условиях используются хорошо известные автоклавы "Magnedrive" с противоточным донным смешиванием, представленным на рисунке 2 статьи J.M. Berty, "Реактор для изучения парофазных каталитических процессов", в журнале Chemical Engineering Progress, том 70, N 5, с. 78-84, 1974.
Давление поддерживается постоянным, равным 275 pri (17,25 атм) и общая скорость потока на выходе поддерживается 22,6 SCFH (0,632 м3/ч). SCFH означает число куб. футов в 1 ч при стандартных температуре и давлении, а именно при 0оС и одной атмосфере. Концентрация окиси этилена на выходе поддерживается равной 1,0% за счет регулирования температуры реакции. Температура (оС) и эффективность катализатора получаются как характеристики, описывающие эксплуатационные свойства катализатора.
Используемая в данных условиях процедура испытания катализатора включает следующие этапы:
1. 80 см3 катализатора вводится в автоклав противоточного смешивания. Объем катализатора измеряется в калиброванном цилиндре внутренним диаметром 1 дюйм (25,4 мм) после нескольких подсочек цилиндра для тщательной набивки катализатора. Объем катализатора может быть рассчитан по плотности набивки носителя и по количеству серебра и присадок. Фиксируется вес катализатора.
2. Автоклав противоточного смешивания нагревается примерно до температуры реакции в потоке азота 20 SCFH (0,560 м3/ч) с использованием вентилятора, работающего со скоростью 1500 об/мин. Поток азота затем прерывается и описанный выше питательный поток вводится в реактор. Общая скорость выходящего потока газа доводится до 22,6 SCFH (0,6328 м3/ч). В течение следующих нескольких часов температура регулируется таким образом, чтобы концентрация окиси этилена в выходящем газе составляла ≈ 1,0%
3. В течение следующих 4-6 дней концентрация выходящей окиси регулируется так, чтобы была абсолютная уверенность, что катализатор достиг его максимального устойчивого состояния. Температура периодически регулируется таким образом, чтобы концентрация окиси на выходе достигала 1% Таким образом достигается избирательность действия катализатора в отношении окиси этилена.
Стандартное отклонение результата одного испытания, показывающего эффективность катализатора согласно описанной выше процедуре, составляет примерно 0,7% единиц эффективности. Стандартное отклонение результата одного испытания, показывающего активность катализатора согласно описанной выше процедуре, составляет ≈ 1,2оС. Стандартное отклонение безусловно зависит от качества оборудования и точности методов испытания, в связи с чем оно неодинаково. Представленные результаты испытания находятся в пределах стандартного отклонения (на корень квадратный от числа испытаний).
Количество марганцевого компонента обычно достаточно для повышения активности в стандартных условиях процесса получения окиси этилена, т.е. при температуре не менее 5оС, предпочтительно не менее 10оС. Наиболее желательно использование условий кислородного процесса. При определении повышения активности процесс и катализатор должны находиться в установившемся состоянии и часто она может быть быстро определена при достижении установившихся состояний. В некоторых случаях катализатор активируется в течение определенного периода времени, часто даже в течение недели и более, перед тем как достигается начальная пиковая активность. Причина указанного времени активации в случае некоторых катализаторов неизвестна, и она может быть связана с химическим и/или физическим кондиционированием катализатора. Следовательно, активность обычно определяется после того, как катализатор находился в потоке в течение не менее 24 ч, предпочтительно в течение ≈ 120-170 ч.
Оптимальное количество марганцевого компонента может изменяться в зависимости от содержания серебра, количества и типа других присутствующих промоторов и от химических и физических свойств носителя. Однако марганцевый компонент часто присутствует в количестве не менее 60 мас.ч/млн в расчете на весовое количество марганца. Если используется слишком большое количество марганцевого компонента, то это отрицательно скажется на рабочие характеристики катализатора. При определении желаемых количеств марганцевого компонента могут быть определены концентрации марганцевого компонента катализаторной композиции для катализаторов, которые подвергаются оценке на рабочие характеристики. В некоторых случаях может быть желательным варьирование количеств других компонентов, например серебра и других промоторов, таким образом, чтобы достигались желаемые комбинации эффектов и оптимальных рабочих характеристик катализатора. Обычно количество марганцевого компонента находится в пределах примерно 70-1000, предпочтительно 80-500 мас.ч./млн в расчете на весовое количество марганца.
Марганцевый компонент может находиться в различных формах, например в форме ковалентного соединения, такого как двуокись марганца, в виде катиона или аниона, например марганатного аниона. Марганцевые компоненты, обеспечивающие повышенную активность и/или стабильность, не имеют определенной формы и могут представлять собой компонент вводимый или компонент, образуемый либо в процессе получения катализатора, либо в процессе использования катализатора. Хотя марганцевые компоненты, обеспечивающие улучшенные свойства катализаторов, не имеют определенной формы, обычно лучшие результаты получаются, когда марганцевый компонент вводится в катализатор в форме перманганата (MnO2- ). Марганец может использоваться в более высоко окисленном состоянии, например в форме манганата (MnO2), а также в форме катиона, например Mn(NO3)2, но при этом требуется некоторый период активации. Кроме того, различные вводимые марганцевые компоненты могут иметь также различные оптимальные концентрации для достижения указанных результатов. Часто марганец и марганцевый компонент имеют окисленное состояние +2, +3, +4 и/или +7, предпочтительно +3, +4 и/или +7.
Марганцевый компонент включает (но не ограничивается ими) ацетат марганца, сульфат марганца аммония, цитрат марганца, дитионат марганца, оксалат марганца, нитрат марганца, сульфат марганца и марганцевый анион, например перманганатный анион, манганатный анион, и др. В случае формы аниона марганцевый компонент может вводиться в виде кислоты или наиболее часто в форме соли металла, например группы 1а, 2а 1b или 2b или аммониевой соли, соли щелочного или щелочноземельного металла, например соли лития, натрия, калия, рубидия, цезия, бериллия, марганца, кальция, стронция, бария и т.д. Могут использоваться также смеси марганатных компонентов.
Как и у любого катализатора получения окиси этилена, который имеет оптимальные рабочие характеристики, существует взаимосвязь между многими факторами. Часто принимаемые в расчет факторы включают:
(i) тип носителя;
(ii) количество серебра на или в носителе;
(iii) компоненты и их количества в или на носителе;
(iv) примеси или загрязнения, источником которых является серебро или другие компоненты;
(v) процедура получения катализатора;
(vi) условия, при которых используется катализатор при получении окиси этилена.
Однако при попытке определить любой катализатор должен быть основополагающий показатель, из которого определяются другие факторы, особенно когда эти факторы являются переменными величинами, каждый из которых зависит от основополагающего фактора. Основополагающим фактором может быть количество серебра или комбинация количества серебра и типа носителя. В большинстве случаев указана комбинация количества серебра и типа носителя. Указанная комбинация должна быть основополагающим фактором. Поскольку основополагающий показатель, определяющий рабочие характеристики катализатора, включает не менее двух величин, то корреляционные зависимости между такими комбинациями и другими факторами могут быть довольно сложными. Нет никакой общей логической нити, которая объединяет все эти три комбинации и/или фактора.
Практическое осуществление изобретения требует проведения экспериментов для достижения всех или почти всех указанных преимуществ изобретения. Специалисты в данной области могут легко достигнуть оптимальные рабочие характеристики катализаторов, отвечающих изобретению. Следует иметь ввиду, что практически данный способ могут легко осуществить специалисты, имеющие опыт в изготовлении любых промышленно используемых катализаторов получения окиси этилена. Отдельные элементы данной процедуры зависят от технологии, используемой для получения катализатора.
Концентрация серебра в конечном катализаторе может находиться в пределах ≈ 2-45 мас. или более, часто в пределах ≈ 2-40 мас. и более (предпочтительный предел содержания серебра составляет ≈ 6-35 мас. В экономическом отношении предпочтительны более низкие концентрации серебра. Однако, оптимальная концентрация серебра для любого типа катализатора будет зависеть как от экономических факторов, так и от рабочих характеристик, таких как эффективность катализатора, скорость старения катализатора и температура реакции.
В некоторых катализаторах, отвечающих изобретению дискретные частицы серебра на готовом к использованию катализаторе и/или на отработанном катализаторе имеют угловую или неправильную конфигурацию, которая иногда может иметь форму параллелепипеда или кубическую форму в противоположность обычно сферической или полусферической форме известных катализаторов. Эти частицы часто имеют основной размер менее чем примерно 0,2, часто менее чем примерно 0,1 мкм.
Носитель, или подложка, используемая в этих катализаторах, в их самых широких аспектах выбирается из большого числа пористых огнестойких катализаторных материалов посетителей или материалов подложки, которые относительно инертны в присутствии исходных материалов процесса эпоксидирования этилена, продуктов реакции и условий реакции. Многие такие материалы уже известны для специалистов в данной области и могут быть естественными или синтезированными и они имеют предпочтительно пористую структуру.
Химический состав носителя не имеет критически узких пределов. Носители могут состоять, например, из альфа-окиси алюминия, карбида кремния, двуокиси кремния, двуокиси циркония, окиси магния и различных глин. Предпочтительными носителями являются частицы альфа-окиси алюминия, часто связанные вместе посредством связывающего агента, и имеют очень высокую степень чистоты, т.е. содержать не менее чем 98 мас. альфа-окиси алюминия, и остальную часть составляют двуокись кремния, оксиды щелочного металла (например, оксид натрия) и следовые количества других содержащих металл или не содержащих металл присадок или примесей; или они могут иметь более низкую степень чистоты, т.е. содержать ≈ 80 мас. альфа-окиси алюминия с остальной частью баланса, приходящейся на смесь двуокиси кремния, оксидов различных щелочных металлов, оксидов щелочноземельных материалов, оксидов железа и оксидов других металлов и неметаллов. Эти носители приготавливаются в форме рецептуры, которая инертна в условиях получения катализатора и в условиях протекания процесса. Промышленностью выпускается множество таких носителей. Носители из окиси алюминия изготавливаются фирмой "United Catalysts Inc." Лаусвилль, Кэнтуки, фирмой Norton Company, Акрон, Огайо.
В случае носителей, содержащих альфа-окись алюминия, предпочтение отдается тем, которые имеют удельную поверхность, измеренную методом БЭТ, примерно 0,03-10 м2/г, предпочтительно ≈ 0,05-5 м2/г, еще более предпочтительно ≈ 0,1-3 м2/г, и которые имеют объем пор, измеренный методом абсорбции воды, в пределах примерно 0,1-0,85 см3/г (по объему). Метод БЭТ определения удельной поверхности подробно описывается Брюнауэром, Эмметом и Толлером, см. J.Am.Chem.Soc. 60, 309-316, 1938.
Некоторые типы носителей, содержащих альфа-окись алюминия, особенно предпочтительны. Эти носители на основе альфа-окиси алюминия имеют относительно равномерные диаметры пор и имеют следующие характеристики. Удельная поверхность по БЭТ примерно 0,1-3,0 м2/г, предпочтительно ≈ 0,1-2,0 м2/г; объем пор (по абсорбции воды) ≈ 0,10-0,85 см3/г, предпочтительно ≈ 0,25-0,75 см3/г. Средние диаметры пор указанных выше носителей находятся в пределах ≈ 0,01-100 мкм, более предпочтительно в пределах ≈ 0,5-50 мкм. Носители могут иметь мономодальное, бимодальное или мультимодальное распределение пор. Типичные свойства некоторых носителей даются в табл. 2, где
(а) метод Брюнауэра, Эммета и Тайлора;
(b) прочность на раздавливание на плоской пластине, одна гранула;
(с) определяется по просачиванию ртути до давления 55 000 psi
(d) определяется использованием микрометрического аутопоромера 9200 или 9210 (контактный угол 130о, поверхностное натяжение ртути 0,473 Н/м).
(е) средний диаметр пор отражает диаметр пор, где 50% пор от общего объема пор имеют диаметр меньший или больший среднего.
Независимо от характера носителя или подложки они обычно имеют форму частиц, кусочков, обломков, шариков, колец, сфер, ободов и т.д. размером, позволяющим использовать их в реакторах с неподвижным слоем катализатора. Обычно промышленные реакторы окисления этилена с неподвижным слоем катализатора имеют форму параллельно вытянутых трубок (в соответствующей оболочке) внешним диаметром примерно 0,7-2,7 дюйма (17,78 мм) (68,5 мм) и внутренним диаметром 0,5-2,5 дюйма (12,7 мм) (63,5 мм) и длиной 15-45 футов (4,57 футов (4, 57 м) (13,76 м), заполненных катализатором. В таких реакторах желательно использовать носитель, имеющий закругленную форму, например форму сфер, гранул, колец, шариков и т.д. диаметрами примерно 0,1-0,8 дюйма (2,54 мм 20,32 мм).
Как и у любого катализатора на носителе, оптимальные его рабочие характеристики зависят от оптимизации носителя в отношении его химического состава (включая примеси), удельной поверхности, пористости и объема пор. Однако согласно изобретению улучшение рабочих характеристик является особенно явным в случае использования менее чем оптимизированных носителей. Так, в примерах, иллюстрирующих изобретение, используются различные типы носителей.
Катализаторы, отвечающие изобретению, содержат наряду с марганцевым компонентом по меньшей мере один промотор или модификатор для улучшения рабочих характеристик катализатора, например для повышения эффективности или снижения горения окиси этилена или воздействия на активность. Эти промоторы или модификаторы обычно имеют форму химических соединений.
Для облегчения понимания далее промоторы называются катионными промоторами, например щелочного и щелочноземельного металлов, и анионными промоторами. Такие соединения как оксиды щелочного металла или МоО3, хотя и не ионные, но могут превращаться в ионные соединения, например в процессе приготовления катализатора или в процессе его использования. Независимо от того, происходит или не происходит такая конверсия, они будут называться в данном описании катионными или анионными промоторами, например промоторы щелочного металла или молибдата.
Часто катализаторы содержат щелочной металл и/или щелочноземельный металл как катионный промотор. Примерами щелочного металла и/или щелочноземельных металлов являются литий, натрий, калий, рубидий, цезий, бериллий, магний, кальций, стронций и барий. Другие катионные промоторы включают ионы металлов группы 3b, включая скандий, иттрий, лантан и металлы из серии лантанидов. В некоторых случаях промотор включает смеси катионов, например цезия, и по меньшей мере одного другого щелочного металла, в результате чего достигается синергическое повышение эффективности. Катионный промотор может безусловно являться противоионом манганатному анионному компоненту. Очень часто используются цезиевые соли либо как таковые, либо в комбинации с другими солями.
Во многих случаях катализатор предпочтительно включает соль (или соли) по меньшей мере одного оксианиона элемента (иного чем кислород), имеющего атомное число 5-83 и относящегося к группам 3b-7b или к группам 3а-7а включительно, периодической таблицы элементов. В некоторых случаях желательно вводить большее количество аниона, чем требуется для связывания с щелочным металлом или щелочноземельным металлом, вводимым в катализатор. Причина того, что ввод дополнительного аниона дает положительный эффект в данных условиях, не ясна. Дополнительный анион может вводиться в форме кислоты, аммониевой соли, аминовой соли и т.д. или порция щелочного металла и/или щелочноземельного металла может быть введена в форме кислотной соли, например бисульфата цезия.
Концентрация соли (или солей) (включая соли любого другого щелочного металла или щелочноземельного металла) в готовом для использования катализатора не находится в критически узких диапазонах и может изменяться в широких пределах. Оптимальная концентрация соли в катализаторе зависит от рабочих характеристик катализатора, таких как эффективность катализатора, скорость старения катализатора и температура реакции.
Концентрация соли (в расчете на весовое количество катиона, например цезия) в готовом к применению катализатора может изменяться в пределах ≈ 0,0005-1,0 мас. предпочтительно ≈ 0,005-0,1 мас. Предпочтительное количество катионного промотора, осажденного на или присутствующего на поверхности носителя или катализатора, обычно находится в пределах ≈ 20-2500 ч/млн (мас) катиона от общего количества материала носителя. Часто наиболее предпочтительны количества в пределах ≈ 50-2000 ч/млн. Когда цезий используется в смеси с другими катионами, то отношение цезиевой соли к соли (солям) любого другого щелочного металла и щелочноземельного металла, если они используются для достижения желаемых рабочих характеристик, не находится в критически узких пределах и может изменяться в широких пределах. Отношение цезиевой соли к другой соли (солям) может составлять ≈ 0,0001 1 10000: 1, предпочтительно ≈ 0,001 1 до 1.000 1. Цезий не менее чем примерно 10, более предпочтительно ≈ 20-100 мас. вводимого щелочного металла и щелочноземельного металла в готовом к применению катализаторе.
В некоторых предпочтительных случаях осуществления изобретения, особенно при использовании иных катализаторов, чем катализатор окислительно-восстановительной пары, количество выщелачиваемого калиевого катиона, определяемое путем выщелачивания в минеральной кислоте, в частности в азотной кислоте концентрацией ≈ 10 об. при ≈ 90оС в течение 1 ч с последующей промывкой дистиллированной водой, составляет менее чем ≈ 50, предпочтительно менее чем ≈ 25, например 0-25 частей на млн (мас) от весового количества катализатора. В некоторых случаях низкая концентрация выщелачиваемого калия в комбинации с марганцевым компонентом усиливает или позволяет марганцевому компоненту значительно повысить активность и/или стойкость катализатора. Кроме того, во многих случаях предпочтительные катализаторы, отвечающие изобретению, содержат менее чем примерно 100, например менее чем примерно 50 ч/млн (мас) выщелачиваемого натриевого катиона, который определяется как описано выше.
Типы анионных промоторов или модификаторов, пригодных для использования в катализаторах, отвечающих изобретению, включают, например, оксианионы, такие как сульфат, SO4-2, фосфаты, например PO4-3, титанаты, например TiO3-2, танталаты, например Ta2O6, молибдаты, например MoO4-2, ванадаты, например V2O4-2, хроматы, например CrO4-2, пирконаты, например ZrO3-2, полифосфаты, нитраты, хлораты, броматы, бораты, силикаты, карбонаты, вольфраматы, тиосульфаты, цераты и другие. Галогенидные ионы также могут присутствовать в анионах и они включают фторид, хлорид, бромид и иодид.
Хорошо известно, что многие анионы имеют комплексную химическую структуру и могут существовать в одной или нескольких формах, например ортованадат и метаванадат; и различные молибдатные оксианионы, такие как MoO4-2, Mo7O24-6 и Mo2O7-2. Оксианионы могут включать также смешанные металлосодержащие оксианионы, включающие иодиоксианионные структуры. Так, например, марганец и молибден могут образовывать смешанный металлический оксианион. Аналогично этому другие металлы, независимо от того, какую форму они образуют, анионную, катионную, элементную или ковалентную, могут входить в анионные структуры.
Поскольку как оксианион, так и источник оксианиона могут использоваться в растворах, пропитывающих носитель, то возможно, что в процессе получения катализатора и/или в процессе его использования, оксианион или присутствующий вначале его источник могут превращаться в другую форму. Данный элемент может быть превращен в катионную или ковалентную форму. Данный элемент предпочтительно ассоциируется с кислородом, то есть образует оксианион, ковалентный оксид или кислородосодержащий анион. Во многих случаях существующие методы анализа не в состоянии точно идентифицировать присутствующие формы. Изобретение не ограничивается точно теми формами, которые могут в конечном виде присутствовать в катализаторе в ходе его использования; приведенная ссылка на оксианионы имеет целью лишь дать лучшее представление и возможности практического осуществления данного изобретения.
Особенно предпочтительные анионные промоторы включают сульфаты и оксианионы рения, молибдена, вольфрама и/или хрома. Примерами анионов серы, которые могут успешно использоваться, являются сульфат, сульфит, бисульфит, бисульфат, сульфонат, надсульфат, тиосульфат, дитионат, дитионит, галоидсульфат, например фторсульфат, и т.д. Предпочтительными используемыми соединениями являются сульфат аммония и сульфаты щелочного металла. Примерами анионов молибдена, вольфрама и хрома, которые могут успешно использоваться, являются молибдат, димолибдат, димолибдат парамолибдат, другие изо- и гетерополимолибдаты, и т. д. вольфрамат, паравольфрамат, метавольфрамат, другие изо-, и гетерополивольфраматы, и т.д. и хромат, бихромат, хромит, галоидхромат, и т.д. Предпочтительными являются сульфаты, молибдаты, вольфраматы и хроматы.
Когда катализатор включает рений, этот рениевый компонент может иметь различные формы, например форму металла, ковалентного соединения, катиона или аниона. Рениевые компоненты, которые дают повышенную эффективность и/или активность, не имеют определенной формы, и могут представлять собой вводимый компонент или компонент, образующийся в процессе получения катализатора или в процессе использования катализатора. Примерами рениевых соединений являются соли рения, такие как галогениды рения, оксигалогениды рения, ренаты, перренаты, оксиды и рениевые кислоты. Однако могут успешно использоваться также перренаты щелочного металла, перренаты щелочноземельного металла, перренаты серебра, другие перренаты и семиоксид рения. Семиокись рения, Re2O7 при растворении ее в воде гидролизуется до перрениевой кислоты, HReO4, или кислой соли рениевой кислоты. Так, например, в данном описании семиокись рения может рассматриваться как перренат (соль рениевой кислоты), т.е. ReO4. Аналогичные химические структуры могут быть представлены другими металлами, такими как молибден и вольфрам.
Количество анионного промотора может изменяться в широких пределах, например ≈0,0005-2 мас. предпочтительно ≈ 0,001-0,5 мас. от общего количества катализатора. Рениевый компонент в случае его использования часто находится в количествах не менее чем 1 ч/млн (мас.), например не менее 5 ч/млн (мас), например ≈ 10-2000, часто в пределах 20-1000 ч/млн (мас) в расчете на весовое количество рения от общего весового количества катализатора.
Катализаторы по изобретению могут включать по меньшей мере одну повышающую активность соль компонента пары окислительно-восстановительной полуреакции и предназначены для использования в процессах эпоксидирования, в которых присутствует по меньшей мере один повышающий эффективность газовый компонент окислительно-восстановительной пары (описано ниже). Термин "окислительно-восстановительная полу-реакция" означает полуреакции типа тех реакций, которые воспроизводятся уравнениями, приведенными в таблицах стандартных потенциалов окисления или восстановления, известных как стандарты одиночных электродных потенциалов, как разъясняется, например, в Handbook of Chemistry, N.A. Lange, изд. Mc. Graw-Нill Book Company, Inc. стр. 1213-1218 (1961 г. ), или в "CRC Handbook of Chemistry and Physics", 65-е изд. CRC Press, Inc. Boca Raton, Флорида, стр. D155-162 (1984 г.). Термин параокислительно-восстановительной полу-реакции" означает пары атомов, молекул или ионов или их смесей, которые претерпевают окисление или восстановление в таких уравнениях полуреакции. Используемые здесь термины, такие как пары окислительно-восстановительной полуреакции включают те же компоненты указанного класса веществ, которые обеспечивают желаемое повышение рабочих характеристик, а не механизм химических процессов. Такие соединения, когда они находятся в сочетании с катализатором в виде солей компонента пары, полуреакции, представляют собой соли, в которых анионами являются оксианионы, предпочтительно оксианион многовалентного атома, а именно атом аниона, с которым связан кислород, способен существовать при связывании его с другим атомом в других валентных состояниях. Предпочтительным катионом является калий, хотя эффективными могут быть также рубидий и цезий, и предпочтительными анионами являются нитрат, нитрит и другие анионы, способные претерпевать замещение или другую химическую реакцию и образующие нитратные анионы в условиях эпоксидирования. Предпочтительные соли включают KNO3 и KNO2, причем предпочтительна KNO3.
Соль компонента пары окислительно-восстановительной пары полуреакции вводится в количестве, достаточном для повышения эффективности реакции эпоксидирования. Точное количество будет изменяться в зависимости от таких переменных, как повышающий эффективность газовый компонент пары окислительно-восстановительной полуреакции и концентрация этого компонента, концентрация других компонентов в газовой фазе, количество серебра, содержащегося в катализаторе, удельная поверхность носителя, условия процесса, например объемная скорость и температура, и морфология носителя. Обычно подходящий предел концентрации вводимой повышающей эффективность соли, рассчитанной по катиону, составляет ≈ 0,01-5 мас. предпочтительно ≈ 0,02-3 мас. от общего весового количества катализатора. Наиболее предпочтительно данная соль вводится в количестве ≈ 0,03-2 мас.
В любом случае катионный и/или анионный промоторы предусматриваются в промотирующем количестве. Под используемым здесь термином "промотирующее количество" определенного компонента катализатора имеется ввиду такое количество этого компонента, которое обеспечивает эффективное улучшение одного или более каталитических свойств катализатора по сравнению с катализатором, не содержащим этого компонента. Примеры каталитических свойств включают (наряду с другими свойствами) эксплуатационную способность (стойкость к уносу), избирательность, активность, степень конверсии, стабильность и выход. Для специалистов должно быть ясно, что за счет "промотирующего количества" могут быть улучшены одно или более каталитических свойств, в то время как другие каталитические свойства могут быть улучшены, но могут быть и не улучшены или могут быть даже ухудшены. Промотор безусловно может повышать эффективность, но снижать активность катализатора, как определено в стандартных условиях процесса получения окиси этилена. Кроме того, различные каталитические свойства могут быть улучшены при различных рабочих условиях. Так, например, катализатор, имеющий повышенную избирательность при одном диапазоне рабочих условий, может функционировать при другом диапазоне условий, при которых улучшение проявляется в активности, а не в избирательности действия, и оператор установки получения окиси этилена будет намеренно изменять рабочие условия для того, чтобы обеспечить преимущество в отношении определенных каталитических свойств даже за счет других каталитических свойств для того, чтобы обеспечить максимальные преимущества в отношении стоимости исходного сырья, энергетических расходов, стоимости удаления побочных продуктов и т.д.
Промотирующий эффект, создаваемый за счет промоторов, может зависеть от ряда переменных, например таких как условия реакции, способы приготовления катализатора, удельная поверхность и пористая структура и поверхностные химические свойства носителя, содержание серебра и сопромотора катализатора, присутствие других катионов и анионов в катализаторе. Присутствие других активаторов, стабилизаторов, промоторов, усилителей или других модификаторов, улучшающих характеристики катализатора, также оказывает влияние на промотирующие эффекты.
Для получения катализаторов согласно изобретению может быть использован ряд способов. Предпочтительный способ включает пропитку пористого носителя катализатора раствором, включающим растворитель или растворяющий агент, комплекс серебра в количестве, достаточном для осаждения желаемого весового количества серебра, и указанные выше анионные и/или катионные промоторы на носителе; последующую обработку пропитанного носителя с целью превращения соли серебра в металлическое серебро и осаждения серебра и анионных и/или катионных промоторов на внешних и внутренних поверхностях носителя. Для воспроизводимости при использовании и повторном использовании пропитывающих растворов желательно, чтобы носитель не содержал чрезмерных количеств ионов, которые растворимы в пропитывающем растворе и/или которые способны к обмену с промотором, наносимом на катализатор, либо при получении, либо при использовании катализатора, так чтобы обеспечивался верхний предел количества промотора, позволяющего получить желаемое усиление каталитического действия. Если носитель содержит такие ионы, то эти ионы должны, как правило, удаляться стандартными химическими приемами, такими как выщелачивание. Осаждение серебра и промотора обычно осуществляется путем нагревания носителя при повышенных температурах с целью испарения жидкости внутри носителя и осаждения серебра и промоторов на внутреннюю и наружную поверхности носителя. Пропитка носителя является предпочтительным способом осаждения серебра, поскольку она более эффективна, чем процедура покрытия; процедура покрытия не в состоянии обеспечивать желаемое осаждение серебра на внутреннюю поверхность носителя. Кроме того, катализаторы с покрытием более чувствительны к потере серебра за счет механического абразивного воздействия.
Последовательность пропитки или осаждения на поверхность носителя серебра и промоторов является произвольной. Так, например, пропитка и осаждение серебра и солей могут осуществляться совместно или последовательно, т.е. промоторы могут осаждаться до, в процессе или после осаждения серебра на носитель. Промоторы могут осаждаться вместе или последовательно. Так например, сначала могут осаждаться одна или несколько солей с последующим совместным или последовательным осаждением серебра и с дополнительным осаждением других солей. Пропитка носителя катализатора осуществляется с использованием одного или более растворов, содержащих серебро и промоторы согласно хорошо известным процедурам для совместного или последовательного осаждений. Для совместного осаждения после пропитки пропитанный носитель нагревается или химически обрабатывается для восстановления соединения серебра в металлическое серебро и осаждения этих солей на поверхности катализатора.
Для последовательного осаждения носитель сначала пропитывается серебром или промотором (в зависимости от осуществляемой последовательности) и затем нагревается или химически обрабатывается, как описано выше. За этим следует второй этап пропитки и соответствующие нагрев или химическая обработка и в результате получается готовый к применению катализатор, содержащий серебро и промоторы.
При изготовлении катализаторов согласно изобретению некоторые промоторы, такие как соли щелочных и щелочноземельных металлов, имеют такие высокие температуры плавления, что при осаждении их на носитель с соединением серебра и при нагреве с целью превращения из соединения серебра в металлическое серебро, эти соли могут оставаться практически неизменными. Безусловно, как это должно быть ясно для специалистов, соли щелочного и щелочноземельного металла, имеющие нежелательное окислительное состояние, превращаются в устойчивое окислительное состояние или, например, в сульфиты или сульфаты. Так например, когда щелочной или щелочноземельный металл осаждается в форме гидроокиси или карбоната, он может быть превращен в присутствии аминов, которые могут быть использованы при пропитке катализатора, в другую солевую форму (например, нитрат) в процессе этапа нагревания (обжига) в зависимости от условий обжига.
Раствор серебра, используемый для пропитки носителя, состоит из соединения серебра в растворителе или комплексобразующего/солюбилизирующего агента, например раствора серебра, описанного в известной литературе. Используемое для данной цели соединение серебра может быть выбрано, например, из числа комплексов серебра, нитратов, оксидов или карбоксидатов серебра, таких как ацетат серебра, оксалат серебра, цитрат серебра, фталат серебра, лактат серебра, пропионат серебра, бутират серебра и соли более высокомолекулярных жирных кислот. При практическом осуществлении изобретения предпочтительной формой серебра является комплексное соединение оксида серебра с аминами.
Для растворения серебра до желаемой концентрации в пролитывающей среде используется большое разнообразие растворителей или комплексообразующих/солюбилизирующих агентов. Из числа описанных в литературе как пригодных для данной цели являются следующие: молочная кислота (патенты США NN 2477436, Aries; и 3501417, De Maio); аммиак (патент США N 2463228, West и др. ); спирты, такие как этиленгликоль (патенты США NN 2825701, Endler и др. и 3563914, Wattimina); и амины и водные смеси аминов (патенты США NN 2459896, Schwarz; 3563914, Wattimina; 3215750, Benisi, 3702259, Nielsen; и 4097414; 4374260; и 4321206, Cavitt).
Особенно предпочтительный способ получения катализаторов с высоким содержанием серебра заключается в последовательных прожитках серебром, с промоторами или без промоторов, где каждая из пропиток может сопровождаться обжигом или другими процедурами, благодаря которым серебро превращается в нерастворимое состояние. Желательно, чтобы носитель имел большой объем пор и высокоудельную поверхность при высоком наполнении серебром.
После пропитки носителя катализатора серебром и промотором пропитанные частицы носителя отделяются от любого остаточного неабсорбированного раствора. Обычно это осуществляется путем удаления избытка пропитывающей среды или как возможный вариант путем использования способов разложения, таких как фильтрация, или центрифугирование. Пропитанный носитель затем, как правило, подвергается термической обработке (например, обжигу) с целью разложения и восстановления соединения серебра (в большинстве случаев комплексных соединений) в металлическое серебро и осаждения солей щелочного металла и щелочноземельного металла. Такой обжиг осуществляется при температуре ≈ 100-900оС, предпочтительно 200-700оС, в течение времени, достаточном для превращения практически всей соли серебра в металлическое серебро. Обычно чем выше температура, тем меньше время, требуемое для восстановления. Так, например, при температуре ≈ 400-900оС восстановление может осуществляться примерно 1-5 мин. Хотя в общепринятой практике для термической обработки пропитанного носителя может быть предложен широкий диапазон периодов нагрева (например, предлагается нагревание в течение менее чем 300 с для сушки, но не для обжига с целью восстановления катализатора. Известно описание процесса нагрева 2-8 ч при 100-375оС с целью восстановления соли серебра в катализаторе, в другом известном патенте США предлагается термообработка в течение 1/2-8 ч в том же температурном диапазоне, очень важно, чтобы время восстановления находилось в корреляционной связи с температурой так, чтобы полностью завершилось восстановление соли серебра в металлическое серебро. Для данной цели желателен непрерывный или ступенчатый режим нагрева. Непрерывный обжиг катализатора в течение короткого периода времени, например не более чем 1/2 ч, является предпочтительным, и он эффективно осуществляется при изготовлении катализаторов, отвечающих изобретению.
Термообработка осуществляется предпочтительно в воздухе, но может использоваться также атмосфера азота или двуокиси углерода. Оборудование, используемое для такой термообработки, может использовать статическую атмосферу или текучую атмосферу (струю таких газов) для осуществления восстановления, но наиболее предпочтительна текущая атмосфера.
Очень важным фактором при изготовлении катализаторов, отвечающих изобретению, является исключение использования сильно кислотных или щелочных растворов, которые могут оказывать воздействие на носитель и осаждать примеси, отрицательно влияющие на рабочие характеристики катализатора. Предпочтительной процедурой пропитки согласно известному патенту Великобритании является процедура, включающая в себя высокую температуру обжига, причем незначительная продолжительность воздействия температуры приводит к минимальному загрязнению данного катализатора. Однако применение солей, отвечающих изобретению, в сочетании с носителями высокой степени чистоты позволяет использовать более низкие температуры, хотя предпочтительно непродолжительное время воздействия температуры.
Как определено уже имеющейся практикой в данной области, размер частиц металлического серебра, осажденного на носитель, является функцией используемой процедуры получения катализатора. Это может быть связано с ограниченной возможностью существующих технических приемов тщательно изучить поверхность катализатора. Так, например, пространство между частицами катализатора на носителе не может быть охарактеризовано достаточно хорошо, чтобы можно было сказать, заключают ли такие частицы серебра все серебро на носителе. Однако, конкретный выбор растворителя и/или комплексообразующего агента, соединения серебра, условий термообработки и носителя катализатора может в различной степени повлиять на диапазон размеров полученных частиц серебра на носителе. Для носителей, представляющих общий интерес для получения окиси этилена, обычно получается распределение частиц серебра по размеру в пределах 0,005-2,0 мкм. Однако роль размера частиц серебряного катализатора в эффективности катализатора в процессе получения окиси этилена не очень понятна. Ввиду того, что частицы серебра мигрируют на поверхности катализатора при использовании в каталитической реакции, приводящей к значительному изменению их размера и формы, пока катализатор еще достаточно высоко эффективен, предполагается, что размер частиц серебра, наблюдаемых на носителе, не может быть существенным фактором, влияющим на рабочие характеристики катализатора.
Серебряные катализаторы по изобретению особенно пригодны для получения окиси этилена путем аэрофазного окисления этилена молекулярным кислородом. Условия реакции для осуществления такого окисления хорошо известны. Это относится к таким условиям реакции, как температура, давление, время обработки, концентрация реагентов, газофазные разбавители (например, азот, метан и СО2), газофазные ингибиторы (например, хлористый этилен и дихлорид этилена), и т.д.
Газы, подаваемые в реактор, могут содержать модификаторы или ингибиторы, или присадки. В частности, используются катализаторы, включающие не менее чем одну повышенную эффективность соль компонента пары окислительно-восстановительной полуреакции в сочетании с по меньшей мере одним повышающим эффективность газовым компонентом пары окислительно восстановительной полуреакции. Термин "газовый компонент пары окислительно-восстановительной полуреакции", "повышающий эффективность газовый компонент пары окислительно-восстановительной полуреакции и другие аналогичные термины имеют те же значения, что и "соль компонента пары окислительно-восстановительной полуреакции" и другие термины, которые определены выше. Эти термины относятся к компонентам полуреакций, представленных в таблицах стандартных или одиночных электродных потенциалов в справочной литературе или в описании стандартов, которые находятся в газовом состоянии и представляют собой вещества, которые в реакционных уравнениях, представленных в указанных текстах, либо окисляются, либо восстанавливаются. Предпочтительными газообразными повышающими эффективность веществами являются соединения, содержащие элемент, способный существовать более чем в двух валентных состояниях, предпочтительно азот и другой элемент, который представляет собой предпочтительно кислород. Примерами предпочтительных повышающих эффективность компонентов пары окислительно-восстановительной пары полуреакций являются по крайней мере одно из следующих соединений: NO, NO2, N2O4, N2O3 или любое газообразное вещество, способное образовывать любой из указанных выше газов, особенно NO и NO2 в условиях эпоксидирования и их смеси с одним или более чем одним соединением из числа следующих: PH3, CO, SO3, SO2, P2O5 и P2O3. В качестве повышающего эффективность газообразного соединения часто предпочтителен NO.
Хотя в некоторых случаях нежелательно использование компонентов той же самой полуреакционной пары в данной реакционной системе, т.е. как повышающего эффективность солевого компонента, связанного с катализатором, так и газового компонента в подаваемом потоке, например, с предпочтительной комбинацией нитрата калия и окиси азота, для достижения удовлетворительных результатов это совсем необязательно. В этой же системе могут использоваться также другие комбинации, такие как KNO3/N2O4, KNO3/SO2, KNO2/NO, KNO2/NO2 и KNO3/смесь SO2 и NO.
В некоторых случаях соль и газовые компоненты могут быть обнаружены в различных полуреакциях, являющихся первой и последней реакциями последовательности полуреакций общей реакции. Повышающий эффективность газовый компонент пары окислительно-восстановительной полуреакции также присутствует в количестве, достаточном для повышения рабочих характеристик катализатора, таких как активность катализатора и особенно эффективность реакции эпоксидирования. Точное количество определяется отчасти повышающей эффективность солью компонента пары окислительно-восстановительной полуреакции, используемой в данном процессе, и ее концентрацией, в частности подвергающемся окислению алкеном, и другими факторами, указанными выше, которые влияют на количество повышающей эффективность соли компонента пары окислительно-восстановительной полуреакции. Обычно желаемая концентрация газового компонента окислительно восстановительной пары полуреакции для эпоксидирования большинства алкенов, включая пропилен, составляет примерно 0,1-2000 об. частей на миллион, подаваемого газового потока, когда N2 используется как балласт. В случае, когда используется предпочтительный газовый компонент пары окислительно-восстановительной полуреакции, такой как NO, в процессе эпоксидирования пропилена, предпочтительная концентрация составляет примерно 2000 ч/млн (по объему) с балластом N2. Однако, когда происходит окисление этилена, подходящая концентрация этилена составляет ≈ 0,1-100 ч/млн (по объему) от компонентов данного газового вводимого потока. Повышающий эффективность газовый компонент окислительно-восстановительной пары полуреакции присутствует в количестве примерно 1-80 ч/млн в случае, когда в реакционной смеси присутствует ≈ 3 об. СО2. При использовании окиси азота в качестве повышающего эффективность газового соединения в системе эпоксидирования этилена он присутствует в количестве примерно 0,1-60 ч/млн предпочтительно в количестве ≈1-40 ч/млн, когда СО2 присутствует в реакционной смеси в количестве, например, ≈ 3 об.
Желательность рецикла непрореагировавшего исходного материала или использования одноциклической системы или использования последовательных реакций для повышения конверсии этилена за счет использования последовательно установленных реакторов может быть легко определена специалистами в данной области. Выбранный прием осуществления операций обычно диктуется экономическими критериями.
Обычно принятие в промышленных условиях процессы осуществляются путем непрерывного ввода исходного потока, содержащего этилен и кислород, в реактор при температуре примерно 200-300оС, и давление может изменяться в пределах 5-30 атмосфер в зависимости от массовой скорости и желаемого выхода. Время пребывания в промышленных реакторах обычно составляет примерно 1-5 с. Кислород может подаваться на реакцию в кислородсодержащем потоке, например в форме воздуха или получаемого производственного кислорода. Полученная окись этилена отделяется и извлекается из продуктов реакции общепринятыми приемами. Однако для целей данного изобретения процесс получения окиси этилена осуществляется с использованием нормального газового рецикла, включающего рецикл двуокиси углерода с нормальными концентрациями, например ≈ 0,5-6 об.
В нижеследующих примерах описываются процессы в стандартных условиях получения окиси этилена. При осуществлении процессов в производственных условиях типичные рабочие условия могут изменяться и количество используемых ингредиентов может регулироваться таким образом, чтобы достигались наилучшие эффективности. В частности, количества этана, двуокиси углерода и органического хлорида могут изменяться таким образом, чтобы оптимизировались эффективность получения окиси этилена. Этан является примесью, содержащейся в различных количествах в сырьевом материале. Этан также может вводиться в производственный реактор, что обеспечивает лучший контроль действия хлоридного ингибитора. Обычно количество этана, используемого в производственных процессах, может изменяться ≈ 0,001-5 мол. для достижения оптимизации как кислородных процессов, так и воздушных процессов. По мере того как концентрация этана увеличивается в реакторе, эффективная поверхностная концентрация хлорида на катализаторе снижается, приводя таким образом к снижению способности хлорида (промотировать) ингибировать реакции, которые увеличивают эффективность получения окиси этилена. Количество хлорида, например этилхлорида или этилендихлорида, также может изменяться, приводя к требуемому действию промотора/ингибитора, соотносящемуся с концентрациями этана в конкретном процессе и с типом промоторов или модификаторов, используемых в катализаторе. Количество органического хлорида, используемого в осуществляемых в производственных условиях процессах, может обычно изменяться примерно от 1,0 ч/млн до 100 ч/млн для достижения оптимизации как в условиях воздушного процесса, так и в условиях кислородного процесса. Двуокись углерода обычно рассматривается как ингибитор, и этот ингибирующий эффект двуокиси углерода на эффективность процесса может изменяться с его концентрацией. При использовании различных типов промоторов или модификаторов для получения катализаторов, отвечающих изобретению, в некоторых промышленно осуществляемых процессах могут быть более желательны различные концентрации двуокиси углерода. Обычно количество двуокиси углерода, используемое в промышленных процессах, может изменяться примерно от 2 до 15 мол. для достижения оптимизации как в условиях воздушного процесса, так и в условиях кислородного процесса. Количество двуокиси углерода зависит от размера и типа системы промывки двуокиси углерода. Оптимизация количеств этана, двуокиси углерода и органического хлорида обеспечивает катализаторы наиболее пригодные для достижения желаемых эффективностей при получении в промышленных условиях окиси этилена. В частности, в процессах эпоксидирования с использованием по меньшей мере одного повышающего эффективность газового компонента пары окислительно-восстановительной полуреакции в сочетании с по меньшей мере одной солью компонента пары окислительно-восстановительной полуреакции на катализаторе, концентрация двуокиси углерода поддерживается предпочтительно ниже чем ≈ 1,5, например ниже чем ≈ 1,0 или даже ≈ 0,5 об.
Катализаторы, подвергнутые воздействию условий процесса получения окиси этилена, например стандартных условий процесса получения окиси этилена, рассматриваются как важный аспект изобретения.
П р и м е р ы.
Носитель, как указывается в описании примеров, пропитывается в условиях вакуума раствором комплекса серебра и солей щелочного металла и щелочноземельного металла. Компоненты, содержащие щелочной и/или щелочноземельный металл, не обязательно вводятся как соли. Так, например, гидрат окиси цезия может использоваться в сочетании с солью аммония (например, сульфатом аммония) или кислотой (например, серной кислотой) или органическим соединением (например, этилсульфонатом) и в условиях получения или использования катализатора осуществляется конверсия в желаемое соединение. Пропитывающий раствор приготавливается такой концентрации, чтобы готовый к применению катализатор содержал желаемые количества серебра и промотора или модификатора. Требуемая концентрация серебра и промотора в растворе для данного носителя рассчитывается по истинной плотности (г/см3) и объему пор носителя, которые либо известны, либо могут быть легко определены. Это соотношение может изменяться в зависимости от типа носителя, например, объем пор может влиять на количества серебра, осажденного из данного раствора. Требуемая концентрация промотора в растворе получается путем деления концентрации серебра в растворе на желаемое отношение серебра к промотору в готовом к применению катализаторе. При получении катализатора обычно желаемое количество этилендиамина (высокочистого качества) смешивается с указанными количествами дистиллированной воды. Затем в раствор медленно вводится дигидрат щавелевой кислоты (химически чистого качества) при комнатной температуре 23оС при непрерывном перемешивании. В ходе этого ввода щавелевой кислоты температура раствора обычно повышается примерно до 40оС в результате экзотермической реакции. Затем в диаминовую соль щавелевой кислоты вводится порошок серебра при поддержании температуры раствора ниже чем ≈ 40оС. И, наконец, для завершения растворения вводятся моноэтаноламин, водный раствор (растворы) соли щелочного металла и дистиллированная вода. Плотность образующегося раствора часто составляет примерно 1,3-1,4 г/мл.
Носитель может быть пропитан в стеклянном цилиндрическом сосуде длиной 12 дюймов (304,8 мм) внутренним диаметром 2 дюйма (50,8 мм), снабженном специальным краном для отвода носителя после пропитки, однако могут использоваться и другие колбы подходящих размеров и типов. Разделительная воронка подходящего размера для пропитывающего раствора вставляется через стеклянную пробку, снабженную металлической трубкой для подвода вакуумной линии к верхней части пропитывающего сосуда. Пропитывающий сосуд, содержащий носитель, вакуумируется до остаточного давления примерно 2 дюйма рт.ст. (50,8 мм Hg) в течение примерно 20 мин, после чего пропитывающий раствор медленно вводится в носитель путем открытия крана между разделительной воронкой и пропитывающим сосудом до тех пор, пока носитель не будет полностью погружен в раствор, при этом давление в сосуде поддерживается равным ≈ 2 дюйма рт.ст. (50,8 мм рт.ст.). После ввода данного раствора сосуд открывается, сообщаясь с атмосферой, и достигается атмосферное давление. Далее носитель остается погруженным в пропитывающий раствор при комнатных условиях в течение ≈ 1 ч и после этого избыток раствора удаляется в течение ≈ 30 мин. Пропитанный носитель затем подвергается термической обработке указанным ниже образом (если нет других указаний) с целью восстановления соли серебра и осаждения промотора на поверхности. Пропитанный носитель распределяется с образованием одного слоя на непрерывной ленте из нержавеющей стали шириной 2 5/8 дюйма (66,8 мм) (в виде спиральных волнистостей) и проходит через нагревательную зону размерами 2 х 2 дюйма (50,8 х 50,8 мм) в течение 2,5 мин, причем эта нагревательная зона поддерживается при 500оС за счет пропускания вверх горячего воздуха через ленту и вокруг частиц катализатора со скоростью 266 SCFH. Горячий воздух образуется за счет пропускания его через трубку из нержавеющей стали длиной 5 футов (1,5 м) и внутренним диаметром 2 дюйма (50,8 мм), которая снаружи нагревается электрической печью (трубчатая печь с горячей зоной внутренним диаметром 2 1/2 дюйма (63,5 мм), длиной 3 футов (76,2 мм)), способной развивать мощность 5400 Вт. Нагретый воздух в трубке выпускается из выходного отверстия квадратного сечения 2 х 2 дюйма (50,8 х 50,8 мм), расположенного непосредственно под движущейся лентой, несущей носитель катализатора. После обжига в зоне нагрева готовый к употреблению катализатор взвешивается и на основе привеса носителя и известных отношений серебра к промотору в пропитывающем растворе рассчитывается мас. серебра и желаемого промотора.
Анализ на серебро осуществляется следующим образом. Примерно 50 г образца катализатора превращается в порошок в измельчающей мельнице и берется 10 граммовая навеска этого образца, который взвешивается с точностью до 0,1 мг. Серебро в образце катализатора растворяется в горячем (80оС) растворе азотной кислоты концентрацией 50 об. Нерастворимые частицы окиси алюминия фильтруются и промываются дистиллированной водой и удаляются, сливаясь с нитратными солями серебра, цезия и других металлов. Раствор доводится до 250 мл в волюмометрической колбе с использованием дистиллированной воды. Аликвота этого раствора объемом 25 мл титруется путем стандартных процедур с использованием 1-нормального раствора тиоцианата аммония и нитрата трехвалентного железа как индикатора. Определяемое таким образом количество серебра в 250 мл раствора используется для расчета весового процента серебра в образце катализатора.
Концентрации серебра и промотора для всех приведенных в данном описании катализаторов являются рассчитанными величинами, как описано выше.
Носители имеют номинально кольцевую форму размерами примерно 1/8 x 5/16 x x 5/16 дюйма (3,2 x 8 x 8 мм) или примерноx x1/8 x 1/4 x 1/4 дюйма (3,2 x 6,3 х 6,3 мм).
Носитель "J" представляет собой носитель на основе альфа-окиси алюминия, полученный путем обжига гамма-окиси алюминия (N-6573) до максимальной температуры ≈ 1025оС, который пропитывается водным раствором фторида аммония концентрацией 3,44 мас. Носитель содержит не менее 99 мас. альфа-окиси алюминия, примерно 0,2 мас. фторида и выщелачиваемые водой следующие компоненты, мас. ч. /млн: Алюминий 118 Кальций 68 Магний 7 Калий 3 Натрий 36 Фторид 375 Нитрат 4 Фосфат 30 Фторфосфат 3 Сульфат 2 Кремний 6
Физические свойства носителя "J":
Удельная поверх- ность 1,09 м2/г Объем пор 0,668 см3/г Средний диаметр пор 1,85 мкм Истинная плотность 0,53 г/мл
Распределение пор по размеру, от общего объема пор Размер пор, мкм от общего
объема пор Р1 (< 0,1) 0 Р2 (0,1-0,5) 1 Р3 (0,5-1) 6 Р4 (1,0-10) 88,5 Р5 (10-100) 1,5 Р6 (> 100) 3
Носитель "К" представляет собой носитель J, который был подвергнут пятикратной промывке деионизированной водой (с температурой ≈ 70оС).
Химический состав носителя "N". Альфа-окись алюминия содержится в количестве не менее 98 мас.
Выщелачиваемые кислотой примеси.
Шнилок от выщелачивания содержит 378 ч/млн натрия и 330 ч/млн калия.
Физические свойства носителя "N"
Удельная поверх- ность (К) (1) 1,166 м2/г Объем пор (2) 0,697 см3/г
Истинная плот- ность (3) 34,2 фунт/
/фут3
(550 кг/м3)
Средний диаметр пор (4) 15 мкм
Кажущаяся порис- тость, 72 Абсорбция воды, 65,4 Объемная плотность 1,2 г/см3
Носитель "О" представляет собой носитель на основе альфа-окиси алюминия, полученный путем обжига гамма-окиси алюминия (N-6573), пропитанного примерно 3,4 мас. раствором фторида аммония до максимальной температуры примерно 1025оС.
Химический состав носителя "О", мас.ч. Альфа-окись алюминия 99 Фторид 0,28
Выщелачиваемые водой примеси, ч/млн:
алюминий 64; кальций 9; магний 5; калий 2; натрий 12; кремний 2; фторид 173; нитрат 11; фосфат 3,2; сульфат 2.
Физические свойства носителя "О":
Удельная поверх- ность (1) 1,10 м2/г Объем пор (2) 0,69 см3/г
Истинная плот- ность (3) 52,38 г/мл
Средний диаметр пор (4) 2,3 мкм
Распределение пор по размеру, от общего объема пор (4) Размер пор, мкм от общего
объема пор Р1 (< 0,1) 0 Р2 (0,1-0,5) 1 Р3 (0,5-1,0) 5 Р4 (1,0-10,0) 89,2 Р5 (10,0-100) 1,8 Р6 (> 100) 3
Носитель "Р" представляет собой носитель на основе альфа-окиси алюминия без связующего
Химический состав носителя "Р": Альфа-окись 99 мас.
Выщелачиваемые водой примеси, ч/млн:
алюминий 168; кальций 30; магний 1,3; калий 102; натрий 197; кремний 148; ванадий 0,8; фосфор 2,8; хлорид 1; нитрат 2; фосфат 5; сульфат 1; фторид 3; ацетат 4; формат 1.
Физические свойства носителя "Р":
Удельная поверх- ность (1) 1,35 м2/г Объем пор (2) 0,561 см3/г
Средний диаметр пор (4) 6,3 мкм
Истинная плот- ность (3) 0,61 г/мл
Распределение пор по размеру, от общего объема пор (4) Размер пор, мкм от общего
объема пор Р1 (< 0,1) 0,5 Р2 (0,1-0,5) 16,0 Р3 (0,5-1,0) 17,0 Р4 (1,0-10,0) 18,5 Р5 (10,0-100) 38,5 Р6 (> 100) 8,5
Носитель "О" получается путем пропитки носителя "Р" в 10%-ном растворе HF при 25оС в течение 1 ч и промывки деионизированной водой при 25оС пять раз с последующей сушкой в воздухе при 300оС в течение 1 ч.
Выщелачиваемые водой примеси, ч/млн:
алюминий 266; кальций 313; магний 5,4; калий 128; натрий 106; кремний 16; ванадий 0,2; цинк 0,3; фосфор 1,8; хлорид 1; нитрат 10; сульфат 1 и фторид 1011.
Носитель "R" получается путем промывки носителя "О" пятикратно горячей деионизированной водой (при ≈ 70оС)
Носитель "S" представляет собой носитель на основе альфа-окиси алюминия, полученный путем прокаливания смеси боэмита бифторида аммония, содержащей 3 мас. бифторида аммония, сначала при 600оС и затем при 1025оС.
Химический состав носителя "S", мас. Альфа-окись алюминия 99 Фторид 0,25
Выщелачиваемые водой примеси, ч/млн:
алюминий 6; кальций 9; магний 5; калий 1; натрий 13; фторид 36; сульфат 1.
Физические свойства носителя "S":
Удельная поверх- ность 1,24 м2/г Объем пор 0,77 см3/г
Истинная плот- ность 0,50 г/мл
Средний диаметр пор 1,7 мкм Распределение пор от общего по размеру объема пор: Р1 (< 0,1) 0,5 Р2 (0,1-0,5) 3 Р3 (0,5-1,0) 9,5 Р4 (1,0-10) 81 Р5 (10-100) 2 Р6 (> 100) 4
Носитель "Т" является носителем на основе альфа-окиси алюминия, полученным путем обжига смеси боэмита бифторида аммония, содержащей 3 мас. бифторида аммония, сначала при 600оС и затем с повторным обжигом при температуре ≈ 1025оС.
Химический состав носителя "Т", мас. Альфа-окись алюминия 99 Фторид 0,25
Выщелачиваемые водой примеси, ч/млн:
алюминий 8; кальций 17; магний 8; калий 5; натрий 6; фторид 55; сульфат 1.
Физические свойства носителя "Т": Удельная поверх- ность 1,13 м2/г Объем пор 0,75 см3/г Истинная плот- ность 0,51 г/мл Средний диаметр пор 2,1 мкм
Распределение пор по размеру от общего объема пор Размер пор, мкм: от общего
объема пор Р1 (< 0,1) 0 Р2 (0,1-0,5) 1 Р3 (0,5-1,0) 4,5 Р4 (1,0-10) 90,5 Р5 (10-100) 1,5 Р6 (> 100) 2,5
Носитель "И" представляет собой носитель "Т", подвергнутый пятикратной пропитке горячей деионизированной водой (примерно с температурой 70оС)
(1) Метод измерения, описанный в публикации "Удельная поверхность и пористость, измеренные путем абсорбции", S. Gregg и K.S.W. Sing, Academic Press, 1967 г. стр. 316-321.
(2) Метод измерения, описанный в стандарте АСТМ С20-46.
(3) Рассчитанная величина на основе обычных измерений веса носителя в емкости известного объема.
(4) Метод измерения, описанный в публикации: "Применение ртутной порометрии (проницаемости по ртути) для анализа материалов", C. Orr, Ir. Powder Technology, том 3, стр. 117-123, 1970 г.
Потеря при трении и средняя величина и пределы прочности на раздавливание определяются согласно испытанию N 45 и испытанию N 5 соответственно как описано в Бюллетене СС-11, 1974 г. Catalyrt Carriers Norton Company, Акрон, Огайо. Испытание с падением капли (25 футов) осуществляется путем падения частиц носителя в вертикальной трубке с расстояния 25 футов (7,6 м) на стальную пластину и наблюдения за тем как происходит их разбивание. Неразбившиеся частицы носителя показывают процент прохождения. Выщелачиваемые кислотой примеси определяются путем контактирования частиц носителя с 10%-ной азотной кислотой в течение 1 ч при ≈ 90оС и измерения экстрагируемых катионов методами стандартной атомно-абсорбционной спектроскопии. Для данных измерений могут также использоваться методы индуктивно сопряженной плазменной спектроскопии.
Идентичность и количества выщелачиваемых водой компонентов носителей могут быть определены любым существующим аналитическим методом. Обычно носители нагреваются в дистиллированной воде при ≈ 50-95оС, часто при 90оС, в течение примерно 0,5-2 ч, например 1 ч. Затем жидкость подвергается анализу методами ионной хроматографии или индуктивно сопряженной плазменной спектроскопии.
П р и м е р 1 является сравнительным. В табл. 3 суммированы данные о катализаторе и эффективности при указанных условиях. Следует иметь в виду, что рабочие характеристики катализатора в данном примере не отражают оптимизации рецептуры катализатора.
Данные катализаторы приготавливаются с использованием общепринятых процедур, изложенных ниже.
Пропитка раствором осуществляется следующим образом.
1. Этилендиамин (высокой степени чистоты) смешивается с дистиллированной водой.
2. Щавелевая кислота (дигидрат щавелевой кислоты химически чистый) медленно вводится в водный раствор этилендиамина при комнатных условиях. Происходит экзотермическая реакция и температура раствора повышается примерно до 40оС.
3. Окись серебра (Порошок из Met Z) затем медленно вводится в раствор, приготовленный в этапе 2.
4. В раствор этапа 3 вводится моноэтаноламин (свободный от Fe и Cl). (Примечание: этапы 1-4 осуществляются периодически 3 раза как указано выше, и затем раствор делится на три аликвоты, одна из которых используется для последующих этапов).
5. Затем вводятся соли щелочного металла.
6. Вводится дистиллированная вода для доведения объема до 150 мл.
При пропитке носителя носитель вакуумируется при комнатной температуре и указанный выше пропитывающий раствор А вводится в носитель в вакууме. Избыточный раствор удаляется.
При обжиге катализатора пропитанный носитель обжигается в горячем воздухе с использованием ленточного обжигового устройства при ≈ 500оС в течение 2,5 мин на ленточном обжиговом устройстве. Скорость потока воздуха составляет 66 SCFH/дюйм2.
Катализаторы примеров 1 и 2 представлены в табл. 3.
П р и м е р ы 3-5
Для приготовления катализаторов 3-5 осуществляется нижеследующая общая процедура.
В 100-миллилитровый химический стакан из стекла Пирекс при постоянном перемешивании вводятся 7,5 г этилендиамина, 7,0 мл воды, 7,51 г щавелевой кислоты, 13,16 г окиси серебра и 2,63 г моноэтаноламина.
Химический состав накрывается часовым стеклом между вводами.
Температура раствора после каждого ввода составляет от 25-60% Затем данная смесь разбавляется дистиллированной водой до объема 35 мл.
Приготавливается стандартный раствор перрената цезия, содержащий 0,00531 г цезия на граммы раствора путем ввода равномолярного количества гидрата окиси цезия и перрената аммония в дистиллированную воду. Приготавливается стандартный раствор сульфата цезия, содержащий 0,015 г цезия на 1 г раствора, и затем добавления сульфата цезия в дистиллированную воду.
Эти стандартные растворы вводятся в содержащий окись серебра раствор с образованием желаемого пропитывающего раствора. Раствор перрената цезия нагревается до 75оС с той целью, чтобы вся соль растворилась, и пропитывающий раствор нагревается ≈ до 40оС с целью, чтобы перренат цезия растворился.
В пропитывающую камеру из стекла Пирекс вводится 10 г носителя. Давление в камере снижается примерно до 2,0-5,0 мм рт.ст. Пропитывающий раствор медленно вводится в камеру. Давление в камере снова доводится до атмосферного. Пропитывающий раствор удаляется по прошествии 20 минут. Слитый раствор остается в стакане с покрытием. Пропитанный носитель обжигается в обжиговом устройстве при 500оС в течение 3 мин. Этапы пропитки и обжига повторяются с использованием слитого раствора для пропитки.
В табл. 4 суммированы данные для данных катализаторов.
Катализаторы из примеров 3, 4 и 5 используются в микрореакторе для определения рабочих характеристик. Для испытания в микрореакторе катализатор раздавливается в ступке с пестиком и просеивается до желаемого размера (30-70 меш) (0,59-0,21 мм).
Два грамма измельченного катализатора вводятся в трубку из нержавеющей стали диаметром 1/4 дюйма (6,3 мм), длиной 51/2 дюйма (139,7 мм). Трубка располагается внутри испытательной печи и подсоединяется к системе подвода газа. Температура печи контролируется посредством контроллера температуры, и давление на выходе реактора поддерживается равным 150 psi посредством обратного клапана Грува. Скорость потока газа доводится до желаемого значения (12 л в 1 ч при стандартных температуре и давлении). Температура реакции измеряется с помощью двух термопар внутри реактора. Одна погружается в слой катализатора, на глубину примерно 2 дюйма от верхней части реактора (50,8 мм) и другая располагается на выходе реактора. Среднее значение двух измерений записывается как температура реакции. Исходная подаваемая композиция включает 30 об. этилена, 8 об. кислорода, 6,5 об. двуокиси углерода, этан и хлориды, как указано в табл. 5. Остальная часть баланса приходится на азот.
П р и м е р ы 6-23.
Катализаторы 6-23 приготавливаются аналогично описанию примеров 3-5. В каждом случае катализаторы приготавливаются путем двукратной пропитки нижеследующим образом.
Носитель пропитывается раствором, содержащим желаемые концентрации солей серебра и промоторов с помощью цилиндрического сосуда, оборудованного для пропитки в вакууме. Избыточный пропитывающий раствор удаляется из сосуда после контактирования этого раствора с носителем в течение 30-60 мин. Пропитанный носитель затем обжигается в потоке воздуха при 500оС в течение 2,5 мин. Описанная процедура повторяется однократно и получается готовый к употреблению катализатор.
Весовое наполнение приготовленного катализатора серебром и концентрации промотора зависят от концентрации пропитывающего раствора и общего объема пор носителя. Для каждого моля серебра в растворе используются 1,05 моль этилендиамина (ЕДА), 0,525 моль щавелевой кислоты (ОА), 0,378 моль моноэтаноламина (МЕА) и подходящие количества воды и промоторов. Для получения пропитывающего раствора ЕДА смешивается с соответствующим количеством дистиллированной воды. Затем медленно вводится щавелевая кислота при непрерывном перемешивании раствора при нормальных условиях. Однако введение ОА вызывает экзотермическую реакцию, температура раствора повышается примерно до 40оС. Окись серебра и МБА затем вводятся в водный раствор ЕДА-ОА. И, наконец, вводятся раствор промотора и балансная вода и получаются желаемые концентрации серебра и промоторов.
Для получения катализатора носитель вакуумируется при комнатной температуре в пропитывающем сосуде. Пока носитель находится под вакуумом пропитывающий раствор вводится в сосуд и контактирует с носителем. Избыток раствора удаляется из сосуда в течение 30-60 мин после пропитки. Пропитанный носитель затем распределяется в виде монослоя на куске из нержавеющей стали и высушивается при 500оС в течение 2,5 мин в потоке горячего воздуха со скоростью 244 SCFH в горячей зоне 2 х 2 дюйма (50,8 х 50,8 мм).
Все катализаторы являются двукратно пропитанным. Ввиду этого описанные процедуры повторяются однократно с использованием пропитывающего раствора желаемой концентрации. Готовый к употреблению катализатор взвешивается, и по привесу носителя может быть рассчитано наполнение серебром готового к употреблению катализатора. Некоторые промоторы, вводимые при первой пропитке, могут снова растворяться в ходе второй пропитки. Ввиду этого концентрация промотора в пропитывающем растворе должна регулироваться с учетом таких потерь для того, чтобы была достигнута его желаемая концентрация в готовом к употреблению катализаторе.
В табл. 6 представлено конечное содержание каждого компонента в каждом этапе пропитки и конечное содержание их в катализаторе.
В табл. 7 даются рабочие характеристики каждого катализатора в миниавтоклавном реакторе. Миниавтоклавный реактор представляет собой рецикловый реактор Берти из нержавеющей стали диаметром 2 дюйма (50,8 мм) (изготавливается Autodave Engineers Inc. Erie, Пенсильвания, США). Реактор состоит из сосуда давления, емкости с катализатором, крыльчатки и системы магнитного привода Магн-Драйв. Сосуд давления имеет внутренний диаметр 2 дюйма (50,8 мм), и в нем предусмотрено пространство для емкости с катализатором и крыльчатки. Емкость для катализатора представляет собой цилиндр из нержавеющей стали внутренним диаметром 1,25 дюйма (31,7 мм) и длиной 1,06 дюйма (26,9 мм). Дно сетчатого цилиндра изготовлено из кусочка сетки из нержавеющей стали подложки для образца катализатора и для свободного прохождения газа. Шесть стальных полос, приваренных к боковой стороне емкости, служат в качестве дефлекторов, которые определяют направление газового потока внутри сосуда давления и поддерживают цилиндрическую емкость при вводе ее в сосуд давления. Крыльчатка располагается над цилиндрической емкостью и присоединяется к внутреннему валу системы привода Магн-Драйв. Внутренний вал подсоединяется к верхней части сосуда давления и образует закрытое пространство в сосуде давления. Внутренний вал приводится в движение посредством магнитной силы от внешних магнитов, которые приводятся воздухом или электрическим мотором. Вращение крыльчатки, обычно со скоростью 1500 об/мин вызывает циркуляцию газа внутри сосуда давления через цилиндр с катализатором. Реакционный газ подается в сосуд давления сверху и выходит снизу. Температура внутри сосуда регулируется и измеряется термопарой, вставленной в сосуд давления снизу. Катализаторы обычно испытываются в стандартных условиях кислородного процесса с содержанием 1,7-2 ч/млн этилхлорида в автоклаве противоточного смешивания размером 2 дюйма (50,8 мм) при давлении 275 psi (19,25 атм). Процедура испытания, используемая в стандартных условиях, заключает в себе нижеследующие этапы:
1. Примерно 8 см3 катализатора вводится в автоклав противоточного смешивания. Объем катализатора рассчитывается по истинной плотности носителя и количеству серебра и присадок.
2. Автоклав противоточного смешивания нагревается до ≈ 230оС в потоке азота движущегося со скоростью 2 SCFH при скорости вращения 1500 об/мин. Затем поток азота прекращается и в реактор вводится поток исходного продукта эпоксидирования. Общая скорость газового потока на выходе составляет 2,2 SCFH (скорость потока регулируется таким образом, чтобы обеспечивалась желаемая объемная скорость, дающая фактическое количество вводимого катализатора). Температура постепенно увеличивается в течение следующих четырех дней таким образом, что концентрация окиси этилена в выходящем газе составляет примерно 2%
3. Катализатор функционирует при постоянной температуре в течение примерно 1-4 недель после его полной активации. Скорость старения катализатора рассчитывается по изменению концентрации окиси этилена (мол.) при работе его при постоянной температуре. Поскольку эффективность катализатора является функцией концентрации окиси этилена, и концентрация окиси этилена обычно не остается постоянной при постоянной температуре испытания, то скорость потери эффективности (старения катализатора) рассчитывается по изменению регулируемой эффективности с учетом концентрации окиси этилена.
Регулируемая эффективность (%) измеренная эффективность (%) + 3,75 (мол. ) х (измеренная концентрация окиси этилена, мол.) 2,0 (мол.).
а. 6% двуокиси углерода, ΔЕО 1,43.
b. Затруднения с реакционной системой.
с. Температура и эффективность, рассчитанные путем интерполяции или экстраполяции из полученных данных, обеспечивающие основание для сравнения при дельта окиси этилена 2,0%
d. Рассчитанные скорости потери активности катализатора при постоянных температурах.
е. Рассчитанные скорости потери эффективности катализатора по изменению эффективности при 2 мол. окиси этилена.
П р и м е р ы 24-26. Основные растворы приготавливаются нижеследующим образом: Основной раствор 88: 11,47 мас.ч.
этилендиа-
мина
22,00 мас.ч.
воды
11,60 мас.ч. ща-
велевой кис-
лоты
19,82 мас.ч.
окиси серебра
4,01 мас.ч. мо-
ноэтаноламина Основной раствор 115: 11,43 мас.ч. этилендиа-
мина
24,0 мас.ч.
воды
11,60 мас.ч. ща-
велевой кис-
лоты
19,82 мас.ч.
окиси серебра
4,00 мас.ч. мо-
ноэтанола-
мина
При получении основных растворов скорость подачи исходных щавелевой кислоты и окиси серебра таковы, что температура раствора не повышается за пределы более чем ≈ 42оС.
Из порции основных растворов получаются три пропитывающие раствора, составы которых приведены в табл. 8.
Катализатор приготавливается с осуществлением способа двукратной пропитки, в котором взвешенное количество носителя вводится в пропитывающий сосуд. Сосуд, содержащий носитель, вакуумируется как в примере 1, и вводится указанный основной раствор. Затем вакуум сбрасывается и устанавливается атмосферное давление. Носитель затем удаляется и обжигается, как и в примере 1, на ленточном обжиговом устройстве. Катализатор снова возвращается в сосуд пропитки для вторичной пропитки. Указанный пропитывающий раствор вводится в сосуд пропитки при поддержании в сосуде вакуума, как в примере 1. При приготовлении пропитывающих растворов сначала вводится нитрат калия при интенсивном перемешивании. Затем вводится содержащее марганец соединение при перемешивании, и пропитывающий раствор сразу же используется. Давление в сосуде давления доводится до атмосферного. Катализатор выгружается и обжигается, как описано выше. Эти подробности процедур получения катализатора суммированы в табл. 9.
Каждый приготовленный катализатор оценивался в автоклавах, как описано выше с использованием ≈ 80 см3 образцов катализатора.
Подаваемый в автоклав газ содержит 8 об. кислорода, 30 об. этилена, примерно 5 ч/млн этилхлорида, примерно 5 об.ч. млн NO и балансный азот. С момента начала действия катализаторов температура повышается в течение четырех дней (220о, 230о, 240о и 255оС) до конечной температуры 255оС. Концентрации хлорида этилена и окиси азота оптимизируются для комбинации характеристик активности и эффективности. После работы в течение 25 дней активность катализатора в отношении получения окиси этилена в примере 24 снижается примерно до 70% от значения активности пяти дней работы, в то время как активность катализаторов из примеров 25 и 26 остается такой же, как и при пяти днях работы, т.е. примерно 5% активностей пяти дней работы.
П р и м е р ы 27-43. Процедуры приготовления и оценки катализаторов осуществляются в основном как и в примерах 6-23 с той разницей, что все соли цезия вводятся во второй пропитке, и катализаторы обжигаются при 300оС в течение 5 мин после каждой пропитки. Для данных катализаторов используется носитель И. Составы катализаторов и их рабочие характеристики суммированы в табл. 10.
П р и м е р ы 44-50.
В табл. 11 суммированы данные о катализаторе и его эффективности в стандартных условиях. Следует отметить, что рабочей характеристикой катализатора в данных примерах является не показатель оптимизации катализаторной рецептуры.
Катализаторы получаются путем принятых процедур, как описано ниже.
Пропитывающий раствор приготавливают следующим образом.
1. Этилендиамин (высокой степени чистоты) смешивается с дистиллированной водой.
2. Щавелевая кислота (дигидрат щавелевой кислоты, химически чистый) медленно вводится в водный раствор этилендиамина при комнатных условиях. Происходит экзотермическая реакция, и температура раствора повышается примерно до 40оС.
3. Затем в раствор этапа 2 вводится медленно окись серебра.
4. В раствор этапа 3 вводится моноэтаноламин (свободный от Fe и Cl). Этапы 1-4 осуществляются в больших объемах в промышленной установке получения катализатора. Затем небольшие порции пропитывающего раствора используются в лаборатории для получения катализаторов. Весовые соотношения этилендиамина, щавелевой кислоты (дигидрата), окиси серебра и моноэтаноламина составляют 0,6 0,6 10,2. Вводится достаточное количество воды для доведения концентрации серебра до 25,60 мас. В лаборатории используются небольшие порции этого раствора для приготовления катализаторов.
5. Затем вводятся соли щелочного металла.
Пропитку носителя осуществляют следующим образом.
Носитель вакуумируется при комнатной температуре и указанный выше пропитывающий раствор вводится в носитель в вакууме. Используется носитель Т. Избыточный раствор удаляется.
Пропитанный носитель обжигается в горячем воздухе с использованием ленточного обжигового устройства при температуре ≈ 500оС в течение 2,5 мин. Расход потока воздуха 66 SCFH/дюйм2.
Катализаторы испытываются в стандартных условиях процесса получения окиси этилена в воздушной среде.
Данные примеров 44-50 представлены в табл. 10. Как видно из данных этой таблицы, если используется слишком много или слишком мало марганцевого компонента, рабочие характеристики катализатора могут быть ухудшены.
П р и м е р ы 51 и 52. Для получения катализаторов примеров 51 и 52 (для сравнения) используется нижеследующая общая процедура.
В 150-миллилитровый химический стакан при постоянном перемешивании вводятся
36,72 г этилендиамина
25,00 мл воды
36,83 г щавелевой кислоты
63,94 г окиси серебра
13,57 г моноэтаноламина
Стакан накрывается часовым стеклом. Температура раствора после каждых диапазонов повышается от 25 до 60оС при приготовлении смеси. Затем эта смесь разбавляется дистиллированной водой до объема 125 мл.
В пропитывающую камеру вводится 10 г носителя О. Давление в камере снижается до абсолютного давления примерно 2,0-5,0 мм рт.ст. В камеру медленно вводится примерно 31,25 мл пропитывающего раствора. Давление в камере снова повышается до атмосферного. Через 30 мин пропитывающий раствор удаляется. Пропитанный носитель обжигается в ленточном обжиговом устройстве, как описано выше, при температуре выше 500оС в течение 2,5 мин. Этапы пропитки и обжига повторяются с использованием аликвоты (31,25 мл) среднего пропитывающего раствора, который также содержит рубидий. Катализатор примера 51 приготавливается из раствора, содержащего 0,8217 г нитрата рубидия и 0,0854 г перманганата рубидия, и катализатор примера 52 приготавливается из раствора, содержащего 0,8217 г нитрата рубидия. Готовый к употреблению катализатор примера 51 содержит примерно 40 мас. серебра и 9273 мас.ч./млн нитрата рубидия в расчете на рубидий. Готовый к употреблению катализатор примера 52 содержит примерно 40 мас. серебра и 8340 мас.ч./млн нитрата рубидия в расчете на рубидий.
Данные катализаторы используются в микрореакторе для оценки их рабочих характеристик. Для испытания в микрореакторе частицы катализатора раздавливаются с помощью ступки и пестика и просеиваются до желаемого размера (14-28 меш) (0,16-0,58 мм). Примерно 0,9 г измельченного катализатора вводится в трубку из нержавеющей стали диаметром 1/4 дюйма (6,3 мм) и длиной 5 1/2 дюймов (139,7 мм). Эта трубка помещается внутри испытательной печи и подсоединяется к системе подвода газа. Температура печи регулируется с помощью контроллера температуры, и выходное давление реактора регулируется с помощью регулятора обратного давления Грува. Скорость потока газа доводится до желаемого значения (6 л в 1 ч при нормальных условиях температуры и давления). Температура реакции измеряется с помощью ступки и пестика и просеиваются до желаемого размера (14-28 меш) (0,16-0,58 мм). Примерно 0,9 г измельченного катализатора вводится в трубку из нержавеющей стали диаметром 1/4 дюйма (6,3 мм) и длиной 5 1/2 дюймов (139,7 мм). Эта трубка помещается внутри испытательной печи и подсоединяется к системе подвода газа. Температура печи регулируется с помощью контроллера температуры и выходное давление реактора регулируется с помощью регулятора обратного давления Грува. Скорость потока газа доводится до желаемого значения (6 л в 1 ч при нормальных условиях температуры и давления). Температура реакции измеряется с помощью двух термопар, помещаемых внутри реактора. Одна термопара измеряет температуру газа на входе, другая температуру газа на выходе. Реакция регулируется по значению температуры газа на входе.
Вводимый в систему исходный продукт содержит 30 об. этилена, 8 об. кислорода, примерно 5-6 об.ч./млн этилхлорида и примерно 6 об.ч./млн NO. При температуре реактора 220оС на 12-й день работы катализатор из примера 52 имеет активность примерно 1/3 от активности катализатора из примера 51.
П р и м е р 53. Катализатор аналогичный катализатору, полученному в примере 24, работает в тех же условиях, что определены в примере 24, в течение примерно 11 дней при температуре реакции ≈ 255оС. Катализатор деактивируется в ходе работы. Затем катализатор удаляется из реакционного оборудования и обрабатывается KMnO4, растворенным в этилендиамине по принятому способу смачиваемости таким образом, чтобы катализатор содержал примерно 200 мас.ч./млн марганца от общего весового количества катализатора. Катализатор снова подвергается воздействию условий реакции получения окиси этилена, которые определены в примере 24. Активность и эффективность, проявляемые катализатором, меньше чем в случае, когда катализатор удаляется из реакционного оборудования; однако активность стабилизируется и после дополнительных 15 дней работы его активность сопоставима с активностью катализатора, который не был подвергнут обработке перманганата калия.
Компонент может вводиться в процессе получения катализатора или в предварительно приготовленный катализатор или даже в использованный катализатор.
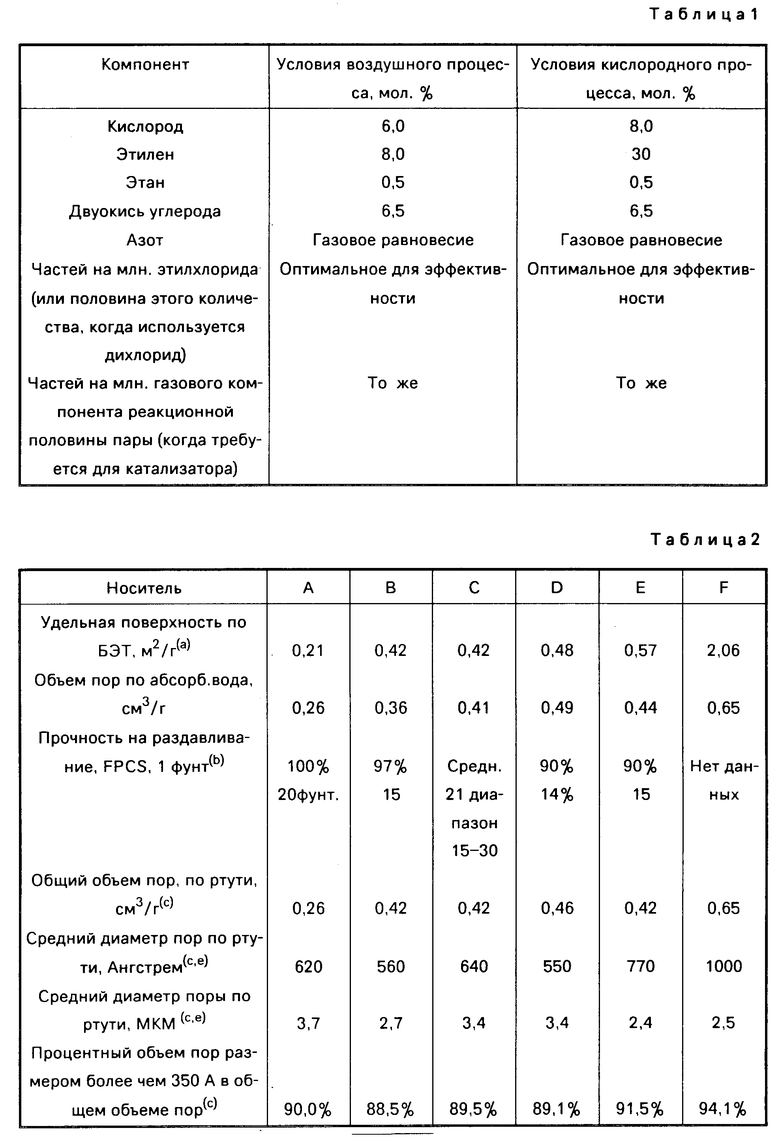
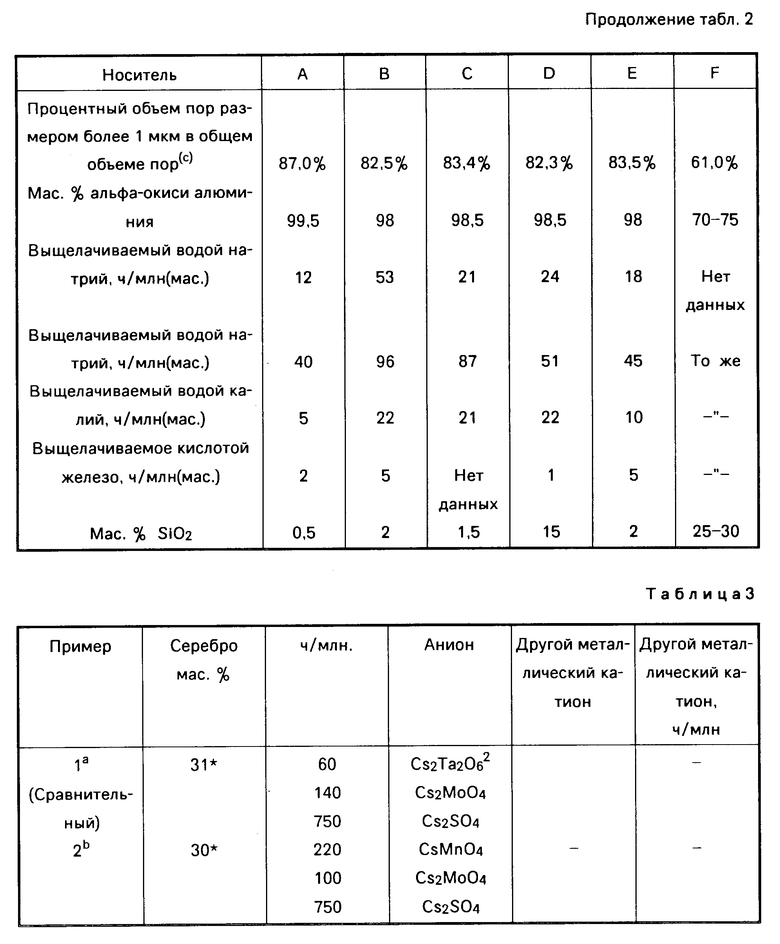
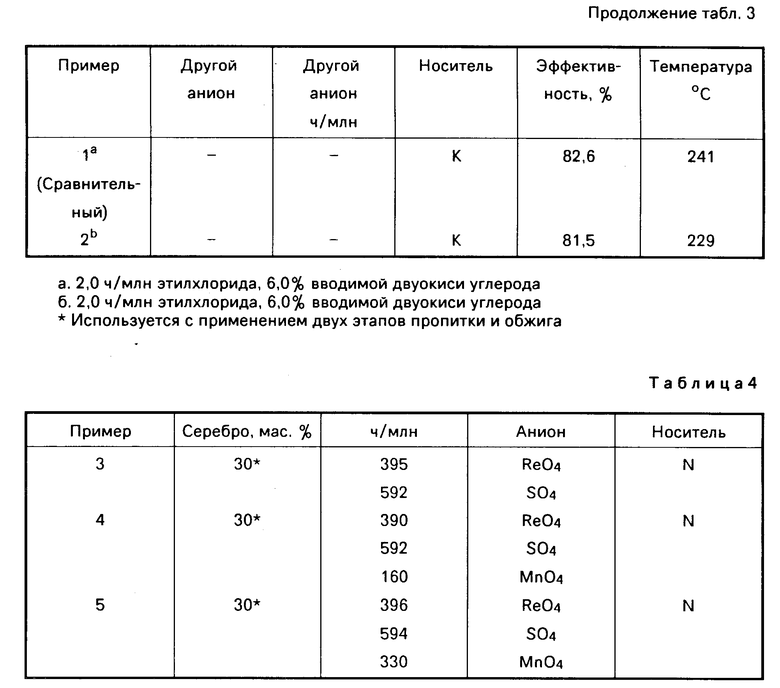
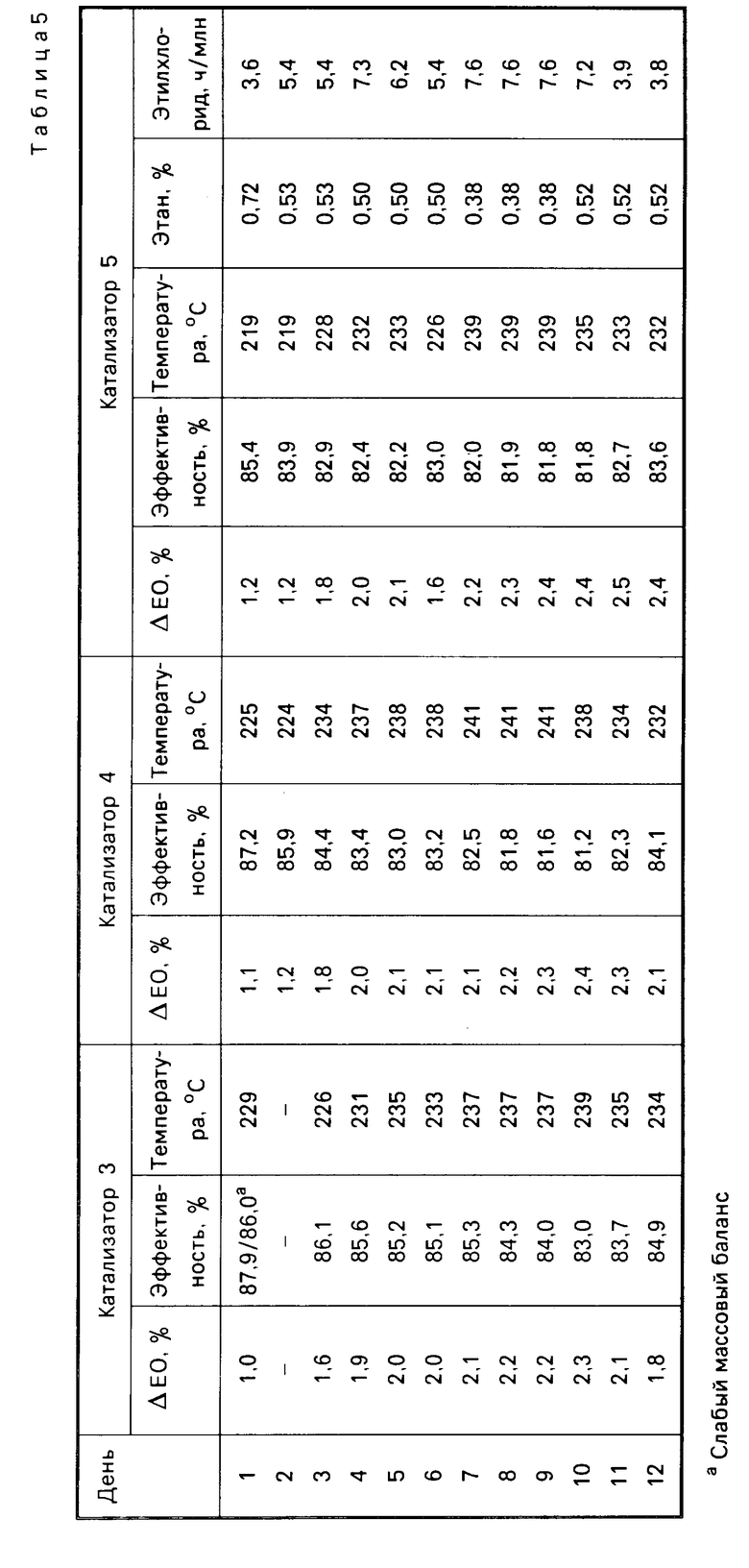

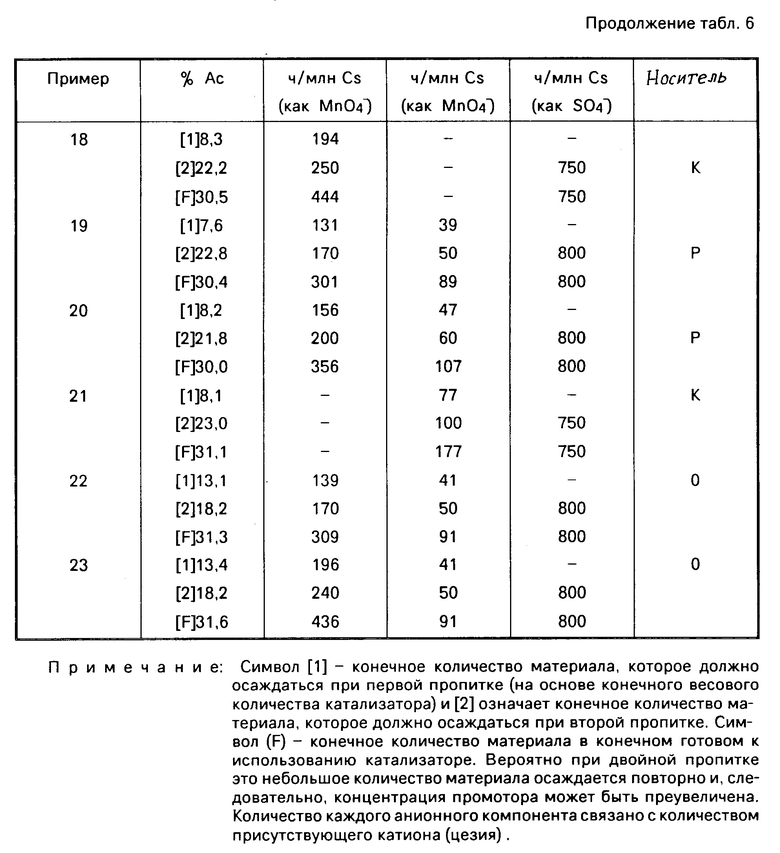
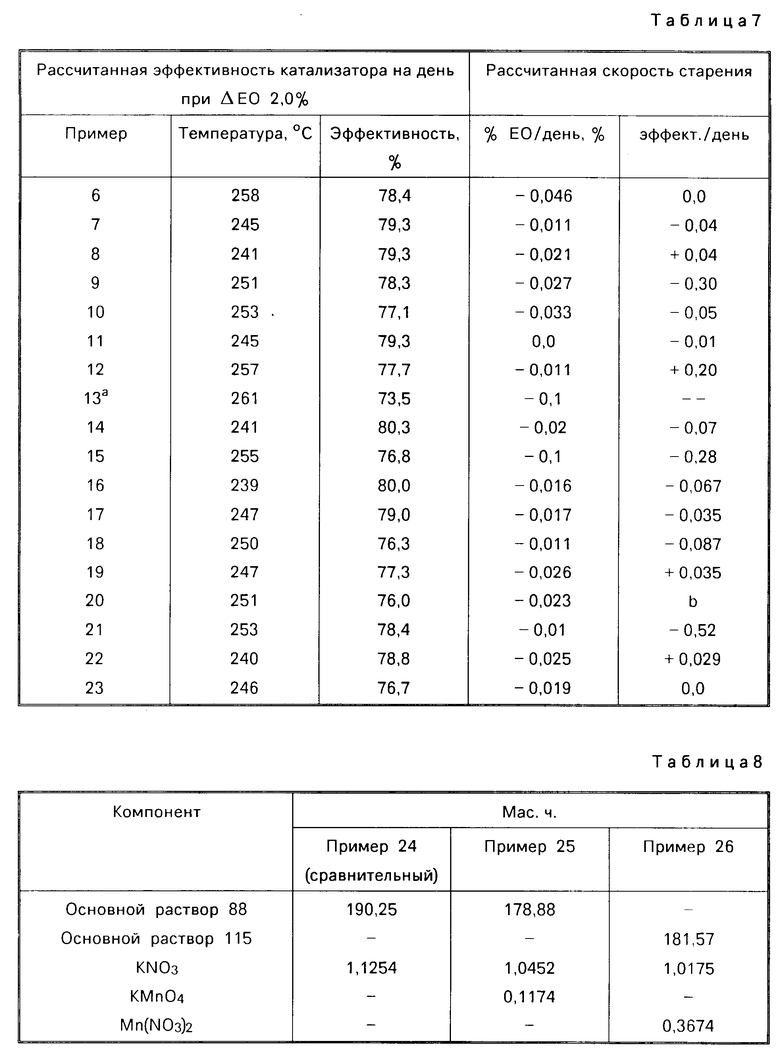
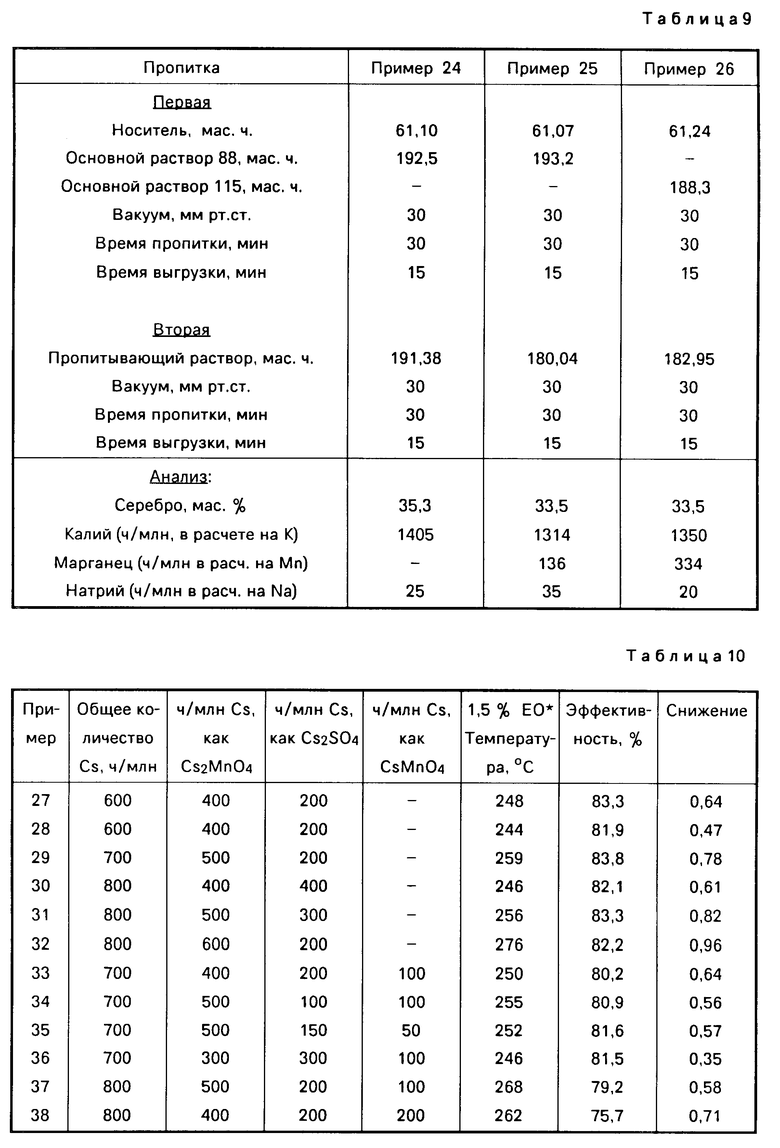
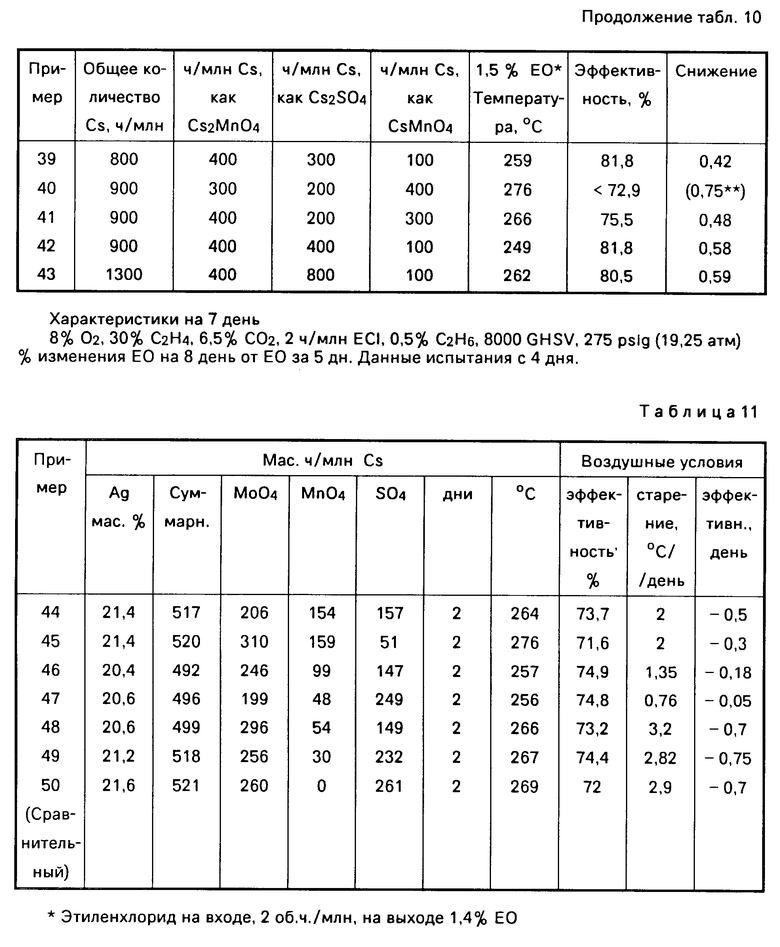
Использование: в нефтехимии, в частности в составах катализаторов для производства эпоксидированного этилена. Сущность изобретения: катализатор содержит, ( мас. ): серебро 20,4 33,5, щелочной металл 0,002 0,135, рений 0,01 5,0, дополнительно марганец 0,006, сопромотор, выбранный из серы, молибдена или их смеси, 0,0005 2,0 и инертный термостойкий твердый носитель остальное. При этом лучше, когда катализатор содержит марганец в виде оксианиона, сопромотор в виде сульфата или молибдата, а также вышелачиваемый калий менее 50 мас.ч на млн мас.ч катализатора. В другом составе катализатор содержит, мас. серебро 2 45, щелочной металл 0,001 0,4, сопромотор, выбранный из группы оксианионов молибдена или их смеси, 0,0005 2, дополнительно марганец 0,006 и инертный термостойкий носитель остальное. Лучше, когда катализатор содержит серу в виде сульфата и молибден в виде оксимолибдена. 6 з. п. ф-лы, 10 табл.
Серебро 20,4 33,5
Щелочной металл 0,002- 0,135
Рений 0,01 5,0
Марганец 0,006
Сопромотор 0,0005 2,0
Носитель Остальное
2. Катализатор по п.1, отличающийся тем, что он содержит марганец в виде оксианиона марганца.
Серебро 2,0 45,0
Щелочной металл 0,001 0,4
Сопромотор 0,0005 2,0
Марганец 0,006
Носитель Остальное
6. Катализатор по п. 5, отличающийся тем, что он содержит серу в виде сульфата.
| Патент США N 4766105, кл | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
1995-10-10—Публикация
1990-04-17—Подача