Изобретение относится к биотехнологии и может быть использовано для получения моноклональных антител (мкАТ) к дигоксину.
Сердечный глигозид дигоксин обладает узким терапевтическим интервалом, из-за чего при его применении возможны нежелательные побочные токсические явления. Для повышения безопасности и эффективности терапии необходим контроль за концентрацией препарата в организме больного и индивидуальный подбор дозы. Это стало возможным после появления доступных иммуноаналитических методов для измерения концентрации этого препарата в крови. Для иммуноанализа дигоксина необходимы высокоспецифические антитела, которые при этом должны быть и высокоаффинными. Поэтому получение антител к дигоксину нужного качества является довольно сложной задачей. Свойства поликлональных антител варьируют от животного к животному и только некоторые антидигоксиновые сыворотки оказываются пригодными для анализа, например из 30 кроликов только один давал сыворотку нужного качества (Butler V P, 1977 Pharmacological Reviews 29(2) 103-184). Большие возможности для получения антител с заданными свойствами открываются при использовании гибридомной технологии. Поэтому в нескольких лабораториях было предпринято несколько попыток получения моноклональных антител к дигоксину (J. Immunol. 129,3,1165-1172, (1982); Int. J. Immunol. 5,5,397-402, (1983); Methods Find. Exp. Clin. Pham. 12,4,265-271 (1990); Molecular Immunology, 22,4,477-488 (1985), US Patent 4803167, 1989).
Во всех работах для получения конъюгатов дигоксина с белками использовали один и тот же метод, который еще ранее показал свою эффективность при получении поликлональных антител к дигоксину (Smith T.W. Biochemistry 9/2, 331-337, 1970). Используемые линии мышей и миеломных линий варьировались. Описаны моноклональные антитела с аффинностью от 10 до 10 М. Однако при описании антител не всегда дается полная характеристика их специфичности и тем более пригодности для иммуноанализа.
Наиболее полно охарактеризованы антитела, полученныe группой американских исследователей Mudgett-Hunter M, Anderson W, Haber E, Margolies M N, (J. Immunol. 129,3,1165-1172, (1982); US Patent 4803167, 1989), поэтому их способ выбран нами в качестве прототипа.
В качестве прототипа выбран способ получения моноклональных антител к дигоксину, в котором для получения гибридом авторы иммунизировали мышей линии А/J конъюгированным антигеном дигоксина с человеческим сывороточным альбумином и спленоциты сливали с клетками миеломной линии SP2/0-Ag14 (Патент США 4803167, 1989). Полученные моноклональные антитела имеют константу аффинности 1,3˙109 М-1 и дают значительные перекрестные реакции с другими гликозидами, заявленные антитела взаимодействуют с дигоксигенином только в 2,7 раза слабее, чем с дигоксином, т.е. перекрест составляет 37%
Между тем для целей иммуноанализа особенно важно отсутствие перекрестных реакций с метаболитом дигоксина дигоксигенином.
Целью данного технологического решения было получение гибридных культивируемых клеток мыши линии BALB/с, продуцирующих мкАТ, обладающие высокой аффинностью и специфичностью и пригодные для разработки иммуноаналитических тест-систем для определения концентрации дигоксина в биологических жидкостях.
Для получения гибридомных клеток, продуцирующих мкАТ, сливали клетки мышиной миеломной линии Х63.Ag 865.3 и сплентоциты мыши линии BALB/c, иммунизированной конъюгированным антигеном дигоксина с гемоцианином из моллюска keyhole limpet.
Мыши иммунизировались в течение 3-4 месяцев, периодически сыворотка животных анализировалась на присутствие антител к дигоксину.
Анализ осуществляли твердофазным иммуноферментным методом, в качестве антигена использовали конъюгированный антиген дигоксина с бычьим сывороточным альбумином. У животных с высоким титром антител к дигоксину брали селезенки и выделяли из них клетки для слияния.
Миеломная линия Х63.Ag8.653. стабильная миеломная линия, не секретирующая иммуноглобулины, была выбрана в качестве второго партнера для слияния. Слияние клеток проводили с использованием полиэтиленгликоля. Отношение числа селезеночных клеток к числу миеломных клеток варьировали от 5:1 до 1:1. После слияния клетки разбавлялись и культивировались в селективной среде, содержащей аминоптерин, гипоксантин и тимидин до появления растущих клонов. Супернатанты анализировали твердофазным иммуноферментным методом, в качестве антигена использовали конъюгат дигоксин-БСА, антитела обнаруживали с помощью кроличьих антител к IgG мыши, меченных пероксидазой хрена, так что выявились только клоны, продуцирующие антитела класса G.
Дополнительный анализ синтезируемых антител производили по ингибированию дигоксином и его аналогами связывания антител с сорбированным конъюгатом дигоксин-БСА. Положительные клоны повторно клонировали. Из положительных клонов был выбран клон D22, продуцирующий антитела наиболее аффинные и с минимальной перекрестной реактивностью по отношению к аналогам дигоксина. Кафф антител D22 составляет 5 10 М, что превышает Кафф аналога. Клон продуцирует антитела, относящиеся к подклассу IgG1. Важной характеристикой гибридомы D22 является ее стабильность и способность расти в асцитных опухолях.
Для получения больших количеств антител гибридные клетки вводили внутрибрюшинно мышам, предварительно сенсибилизированным пристаном. Антитела из асцитных жидкостей выделяли ионообменной хроматографией на ДЕАЕ-целлюлозе. На основе полученных мкАт был разработан метод иммуноферментного определения дигоксина, позволяющий определять дигоксин в 10 мкл сыворотки крови с большой точностью и специфичностью.
Кроме того пригодность полученных антител для иммуноанализа оценивали, используя их в ките фирмы Boehringer Mannhaim, где они также продемонстрировали хорошие результаты.
Штамм получают следующим образом.
1. Иммунизация.
Мышей линии ВАLB/c, самок, иммунизировали внутрибрюшинно 100 мкг конъюгированного антигена дигоксин-гемоцианин, полученного известным способом (Smith T. W. Biochemistry 9/2, 331-337, 1970), суспендированного в 100 мкл физиологического раствора и 200 мкл полного адъюванта Фрейнда. Инъекцию повторяли через 6 недель и далее через 2-4 недели с неполным адъювантом. Через 7 дней после последней иммунизации у мышей брали кровь и сыворотки анализировали на присутствие антител твердофазным иммуноферментным методом. Для завершающей иммунизации отбирали мышей, в сыворотках которых обнаруживали наибольший титр антител к дигоксину. За 3 дня до гибридизации таким мышам вводили по 100 мкг антигена без адъюванта.
2. Твердофазный иммуноферментный метод обнаружения антител к дигоксину.
Конъюгированный антиген дигоксин-БСА, полученный по тому же методу, что и дигоксин-гемоцианин, растворяли в 0,05 М карбонат-бикарбонатном буфере, pH 9,6 в концентрации 0,3 мкг/мл и сорбировали на полистироловых 96-луночных планшетах по 100 мкл на лунку, при 4оС в течение ночи, затем твердую фазу отмывали 0,05% -ным раствором тритона Х-100 и водой. В лунки вносили по 90 мкл 0,01 М натрий-фосфатного буфера, содержащего 0,15 М NaCl, 0,05% твин-20 и 0,2% БСА (буфер А). В первую лунку вносили 10 мкл сыворотки и далее делали серию десятикратных разведений до конца ряда. После инкубации в течение 1 ч при комнатной температуре планшет промывали и вносили в каждую лунку по 90 мкл кроличьих антител против иммуноглобулинов мыши, меченых пероксидазой хрена, растворенных в буфере А. Планшет инкубировали 45 мин, отмывали и для измерения ферментной активности добавляли субстратный раствор (4 мкл 30% Н2О2 и 4 мг ортофенилендиамина на 100 мл 0,1 М натрий цитратного буфера pH5), по 90 мкл, через 10 мин для остановки ферментативной реакции добавляли по 45 мкл 10%-ного раствора серной кислоты и измеряли поглощение при 492 нм.
3. Гибридизация.
У иммунизированной мыши брали селезенку в стерильных условиях и готовили суспензию спленоцитов. Клетки миеломной линии Р3-Х63.Ag8.653 отмывали средой без сыворотки и сливали со спленоцитами в соотношении 1:1, используя 30%-ный полиэтиленгликоль 6000, 1 мл. Слившиеся клетки отмывали бессывороточной средой, суспендировали в 50 мл среды RPMI 1640, содержащей 10% эмбриональной телячьей сыворотки, 2 мМ глутамина, 5-10 5 М 2-меркаптоэтанола, 1 мМ пируват натрия, 100 единиц пенициллина и стрептомицина, 4-10-7 М аминоптерина, 10-4 М гипоксантина, 1,6 10-5 тимидина и разливали в 96-луночные планшеты, содержащие фиддерный слой мышиных перитониальных макрофагов по 50 мкл в лунку. Через неделю планшеты начинали сканировать ежедневно, супернатанты от активно растущих клонов отбирали и анализировали на присутствие антител к дигоксину. Активные клоны переносили в 24-луночные планшеты, часть клеток замораживали.
4. Отбор положительных клонов.
Для отбора положительных клонов использовали твердофазный иммуноферментный метод. Конъюгированный антиген дигоксин-БСА сорбировали в 96-луночных планшетах, как описано в п.2. В качестве положительных контролей использовали сыворотки мышей, содержащие антитела к дигоксину (разведение 1:200), в качестве отрицательных контролей сыворотки неиммунизированных мышей и супернатанты от миеломных линий. Было выявлено 17 положительных клонов. Далее была изучена способность антител, продуцируемых этими клонами, связывать свободный дигоксин. Сродство антител к дигоксину определяли по ингибированию связывания антител с иммобилизованным антигеном в присутствии свободного дигоксина. Было отобрано 3 клона, активно секретирующих антитела к дигоксину. Эти клоны были проанализированы аналогичным образом на способность связывать аналоги дигоксина.
Для дальнейшей работы был выбран клон D22, обладающий наименьшей перекрестной реакцией по отношению к дигоксигенину.
5. Клонирование методом предельных разведений.
Клетки выбранного клона клонировали методом предельных разведений в 96-луночном планшете, содержащем фиддерный слой макро-фагов, из расчета 0,3 клетки на лунку. После появления клонов супернатанты тестировали на присутствие моноклональных антител. Все выросшие клоны продолжали продуцировать антитела к дигоксину.
6. Производство моноклональных антител в виде асцита.
Для получения больших количеств антидигоксиновых антител гибридомные клетки вводили внутрибрюшинно мышам линии ВАLB/с, за 10 дней до того получившим инъекции 0,5 мл пристана, по 3х10 клеток на животное. После появления у мышей асцитных опухолей (через 5-14 дней) собирали асцитную жидкость, клетки удаляли центрифугированием, асцитную жидкость замораживали и хранили при -20оС. От каждой мыши получали по 5-10 мл асцита, содержащего от 5 до 8 мг/мл антител.
Полученный штамм гибридных культивируемых клеток D22 хранится в Специализированной коллекции перевиваемых соматических клеток позвоночных Всесоюзной коллекции клеточных культур под номером ВСКК(П) 623 Д.
Штамм характеризуется следующими признаками:
Культуральные свойства клона D22.
Клетки культивируются в монослое в концентрации 5-10 клеток/мл, время субкультивирования составляло около 48 ч.
Криоконсервирование гибридомы осуществляется в смеси равных объемов среды RPMI 1640 и телячьей эмбриональной сыворотки, содержащей 15% диметилсульфоксида по 10 клеток в ампуле. Первые трое суток ампулы хранили при -70оС, затем переносили в жидкий азот. После размораживания клетки не теряли своих ростовых свойств.
Характеристика моноклональных антител:
Антитела из асцитов выделялись солевым осаждением сульфатом аммония и последующей хроматографией на ДЕАЕ-целлюлозе в 0,01 М фосфатном буфере, pH 8,2 с использованием градиента NaCl от 0 до 0,5 М NaCl. Гомогенность выделенных антител проверялась с помощью электрофореза в полиакриламидном геле в присутствии додецилсульфата натрия. Антитела, синтезируемые клоном D22, относятся к подклассу IgG1, что определено твердофазным иммуноферментным методом с использованием козьих антител к подклассам мышиного IgG.
Изучение специфичности моноклональных антител D-22.
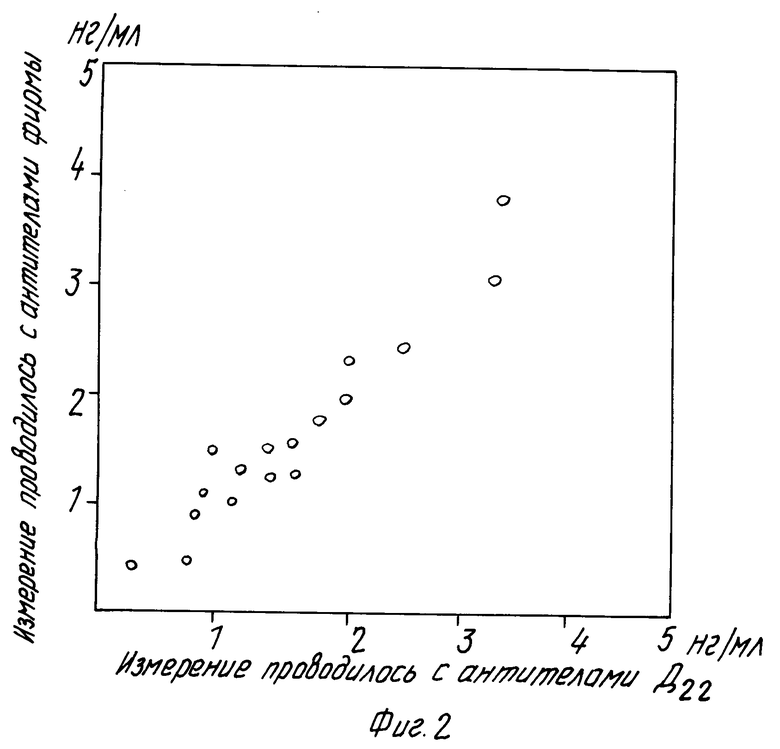
В планшете с иммобилизованным конъюгатом дигоксин-ЧСА готовили ряд последовательных разведений аналогов дигоксина в буфере А от 10-6 до 10-12 М по 50 мкл в лунке. Добавляли к ним по 50 мкл разведения асцита D-22 в буфере А в разведении 1:10 000. Инкубировали 24 ч при 4оС, отмывали планшет водой и заканчивали анализ как описано в п.2. Перекрестные реакции оценивали по отношению концентраций аналога и дигоксина, вызывающих 50% ингибирование связывания антител с конъюгатом (таблица).
Таким образом, концентрация дигоксигенина, необходимая для 50% ингибирования, превышает концентрацию дигоксина, необходимую для этой цели, в 11,2 раз, или перекрест составляет 8.9% он значительно ниже, чем перекрест антител аналога (37%).
Константа аффинности антител D22 равна 5˙109 М-1, что превышает Кафф антител аналога (1,3˙109 М-1).
Использование штамма иллюстрируется следующими примерами.
П р и м е р 1. Использование полученных моноклональных антител для определения дигоксина в сыворотке иммуноферментным методом.
Конъюгированный антиген дигоксин-БСА растворяли в 0,05 М натрий карбонат-бикарбонатном буфере (pH 9,6) в концентрации 0,3 мкг/мл и сорбировали на полистироловых 96-луночных планшетах фирмы NUNK, по 120 мкл/лунку, при 4оС в течение ночи, затем твердую фазу трижды отмывали 0,05%-ным раствором тритона Х-100 и высушивали.
Очищенные ионообменной хроматографией на DEAE-целлюлозе моноклональные антитела окисляли периодатом натрия и метили пероксидазой хрена. Для этого 1 мг пероксидазы растворяли в 0,1 мл воды и добавляли 1 мг периодата натрия в 25 мкл воды. Смесь инкубировали 2 ч в темноте при комнатной температуре, пропускали через 0,5 см слой сефадекса G-25 и смешивали с 4 мг антител в 0,1 М карбонат-бикарбонатного буфера, pH 9,5. Через 3 часа добавили 0,1 мг боргидрида натрия, инкубировали 1 ч и диализовали конъюгат против воды. Затем конъюгат был осажден 75%-ным раствором сульфата аммония, отцентрифугирован и растворен в воде. После диализа против физиологического раствора конъюгат хранили в ЗФР в концентрации 10 мг/мл с добавлением 0,01% мертиолята.
Стандартные растворы дигоксина в сыворотке готовили следующим образом.
Пул донорских сывороток или лошадиную сыворотку 100 мл центрифугировали при 15 т. об/мин, инактивировали при 56оС, затем пропускали через колонку 1/5 см с активированным углем. Приготовленную таким образом сыворотку фильтровали через мембрану с диаметром пор 3,0 нм. Дигоксин растворяли в ДМСО в концентрации 1 мг/мл и готовили из него стандартные растворы в сыворотке в концентрации 0; 0,5; 1; 2; 5 нг/мл. Стандартные сыворотки разливали в пробирки и лиофильно высушивали, перед использованием стандарты разводили дистиллированной водой.
Анализ проводили следующим образом.
Аликвоты по 10 мкл из сывороток крови больных, получавших дигоксин, и стандартных растворов дигоксина в донорской сыворотке, содержащих известное количество препарата, вносили в лунки планшета и добавляли по 100 мкл раствора конъюгата пероксидаза-антитела в 0,1 М натрий-фосфатном буфере, содержащем 0,15 М NaCl, 0,05% твин-20 и 0,2% БСА, разведение из концентрации 10 мг/мл 1: 20 000. Смесь вpащательно встряхивали, инкубировали 30 мин при комнатной температуре, твердую фазу отмывали и приливали в каждую лунку по 100 мкл раствора субстрата (4 мкл 30% Н2О2 и 4 мг ортофенилендиамина на 10 мл 0,1 М натрий-цитратного буфера, pH 5,0), инкубировали 10 мин в темноте, детекция при 492 нм. На основании значений поглощения, полученных для стандартных растворов, строилась калибровочная кривая (фиг.1). Все измерения выполнялись в дубликатах. Концентрацию дигоксина в сыворотках больных определяли по калибровочной кривой. Например, величине поглощения 1,0 соответствует значение концентрации дигоксина 1,3 нг/мл. Коэффициент вариабельности для 20 параллельных измерений составлял 6,8% Метод позволяет определять дигоксин в интервале от 0 до 5 нг/мл, минимально определяемая концентрация 0,1 нг/мл. Предложенным методом были проанализированы сыворотки 23 больных, получавших дигоксин. Измеренные концентрации препарата находились в терапевтической области и соответствовали терапевтическому эффекту. Для 10 сывороток был проведен параллельный анализ с использованием набора фирмы Boehringer Mannhaim, коэффициент корреляции результатов 0,94.
П р и м е р 2. Использование антител D22 в наборе для иммуноферментного определения дигоксина фирмы Boehringer Mannhaim.
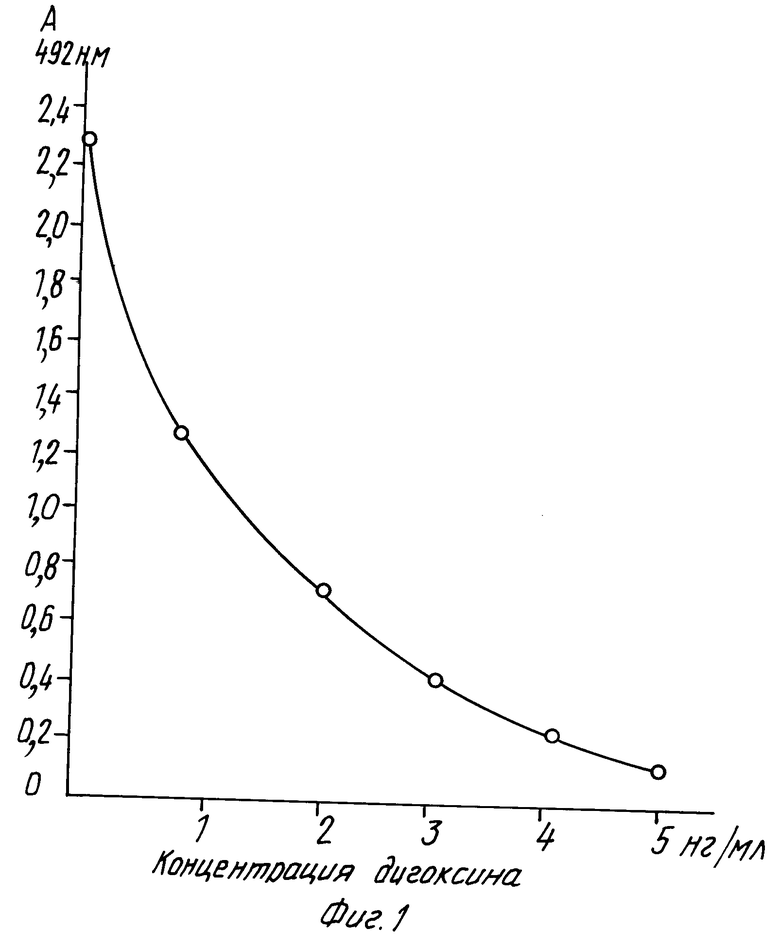
Использовался набор реагентов фирмы Boehringer Mannhaim для иммуноферментного определения дигоксина. В наборе используются антитела к дигоксину, сорбированные на полистироловые пробирки и конъюгат дигоксин-пероксидаза. Мы заменяли антитела из набора нашими антителами. Для этого антитела, выделенные ионообменной хроматографией, сорбировали на полистироловые пробирки в натрий карбонат-бикарбонатном буфере (pH 9,6) в концентрации 0,3 мкг/мл по 1 мл/пробирку, при 4оС в течение ночи, затем трижды отмывали 0,05%-ным раствором тритона Х-100 и высушивали. Далее проводили анализ по инструкции фирмы. Параллельно анализ проводился также с использованием набора фирмы. Было измерено 17 сывороток больных, получавших дигоксин. Коэффициент корреляции между измерениями очень высок, 0,98 (фиг.2).
Эти примеры подтверждают возможность использования полученных нами антител для иммуноанализа дигоксина.
Использование: клиническая биотехнология, разработка иммуноаналитических систем для определения дигоксина в крови. Сущность изобретения: получение штамма гибридных культивируемых клеток мыши Mus musculus, который продуцирует моноклональные антитела (МКА) к дигоксину. Штамм D-22 получают гибридизацией спленоцитов мышей линии BALB/с с клетками миеломы Х63 Ag. 865.3. МКА относятся к подклассу IgGI, константа аффинности антител составляет 5·109M-1 МКА специфически связываются с дигоксином, их перекрестная реактивность с аналогами данного лекарственного препарата составляет 8,9% 2 ил. 1 табл.
Штамм гибридных культивируемых клеток мыши Mus musculus L. ВСКК (II) N 623, D, используемый для получения моноклональных антител к дигоксину.
| Патент США N 4803167, кл | |||
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| Механизм для сообщения поршню рабочего цилиндра возвратно-поступательного движения | 1918 |
|
SU1989A1 |
Авторы
Даты
1995-12-10—Публикация
1993-04-05—Подача