Изобретение относится к биотехнологии и может быть использовано для получения моноклональных антител (МКА) к белку теплового шока 70 (БТШ 70).
Белки теплового шока играют важную роль для обеспечения гомеостаза организма на всех стадиях его развития и в экстремальных для него условиях, таких как воздействие стресса, отравляющих и наркотических веществ, радиации, сублетальной температуры и других.
В настоящее время достаточно подробно изучены основные функции внутриклеточных БТШ, связанные с участием этих молекул в процессах синтеза, фолдинга, транспорта, репарации внутриклеточных протеинов (шаперонные функции) [1] и важной ролью БТШ в системе защиты клеток от повреждающих воздействий (протективные функции) [2]. Зарегистрирована поверхностная локализация БТШ у ряда линий опухолевых клеток, у вирус-инфецированных лимфоцитов, у активированных макрофагов и Т-лимфоцитов [3], а также обнаружено существование свободного БТШ в межклеточном пространстве [4]. На основе иммуноадъювантных свойств БТШ интенсивно ведутся исследования по разработке вакцин для иммунотерапии злокачественных опухолей [5, 6].
Одним из важных подходов определения БТШ 70 в биологических организмах является использование MKA, продуцируемых гибридомами.
Известно, любая белковая структура несет на своей поверхности определенное количество эпитопов, в том числе и структурных. Как правило, чем выше молекулярный вес белка, тем больше эпитопов. Они имеют разную иммуногенность и определяют уникальность той или иной белковой молекулы в осуществлении ее функциональных свойств. Поэтому, чем больше панель гибридом, антитела каждой из них работают только с одним из эпитопов белка, тем больше инструментов для исследования этих свойств. Следовательно, получение новых гибридом всегда актуально. Моноклональные антитела, продуцируемые гибридомами, используются как важный инструмент для выявления основных структурно-функциональных свойств белков, в том числе и БТШ 70.
За рубежом некоторые фирмы, например, Sigma, Cayman chemical, Biocompare (США), StressGen (Канада), HyTest (Финляндия) продают моноклональные антитела к БТШ 70 [7].
Известен штамм гибридных культивируемых клеток животных Mus musculus SPA 810 (фирма StressGen, Канада), продуцирующий МКА к БТШ 70. Коммерческие МКА, продуцируемые гибридомой SPA 810 слабо окрашивают при непрямом иммунофлуоресцентном анализе живые клетки (например, клетки лимфомы EL-4), что ограничивает их использование для определения БТШ 70 при воздействии стрессовых факторов на живые клетки [8].
Задача изобретения - получение штамма гибридных культивируемых клеток, продуцирующих моноклональные антитела, специфичные к БТШ 70 и пригодные для определения БТШ 70 при воздействии стрессовых факторов.
Поставленная задача решается тем, что предложен новый штамм гибридных культивируемых клеток животных Mus musculus 2Е4 - продуцент моноклональных антител к БТШ 70.
Штамм депонирован в коллекции микроорганизмов Государственного научного центра прикладной микробиологии и биотехнологии (ГНЦ МПБ) коллекционный номер - H1.
Штамм гибридомы получают путем иммунизации мышей линии BALB/c бычьим БТШ 70 в течение 78 суток. На третьи сутки после последней бустер-инъекции проводят гибридизацию спленоцитов иммунных мышей (108 клеток) с клетками мышиной миеломы РЗ-Х63 Ag/8-653 (107 клеток). В качестве агента для слияния применяют полиэтиленгликоль с молекулярным весом 1500 (Merk, Германия). После гибридизации проводят селекцию, скрининг, клонирование и криоконсервацию гибридомы.
Характеристика гибридомы 2Е4.
Морфологическая характеристика. Культура гибридных клеток состоит из слабоприкрепленных к подложке округлых клеток с размером с исходную миеломную клетку.
Культуральные свойства. Культивирование штамма гибридомы 2Е4 ведут при температуре 37°С в атмосфере, содержащей 5% углекислого газа. Средой культивирования является среда DMEM или RPMI - 1640, содержащая 10% эмбриональной телячьей сыворотки, 2 мМ/L-глутамина, 50 мкг/мл гентамицина. Клетки культивируют в виде стационарной суспензии в пластиковых матрацах "Costar". Пассирование клеток гибридомы проводят 2 раза в неделю с кратностью разведения 1:2 - 1:3. Посевная концентрация клеток составляет 105 в 1 мл среды. Максимальная концентрация гибридных клеток при культивировании составляет 105 на 1 мл среды. Гибридный клон не теряет способности синтеза антител при 15 пассажах in vitro (срок наблюдения).
Культивирование гибридомы в организме животного. Вид животного - инбредные мыши линии BALB/c. Доза клеток при прививке составляет 106 на одну мышь при первичном введении и 105 на одну мышь при вторичном введении из иммуноасцитной жидкости. За 14 суток до введения клеток гибридомы, мышам внутрибрюшинно вводят 0,5 мл 2, 6, 10, 14-тетраметиленпентадекана (пристана). Иммуноасцитическая жидкость образуется на 14-20 сутки в объеме 3-5 мл. Синтез иммуноглобулина, продуцируемого гибридомой, определяют методом непрямого иммуноферментного анализа (ИФА).
Характеристика полезного продукта. Гибридома 2Е4 продуцирует специфичные моноклональные антитела к БТШ 70, титр которых составляет в культуральной жидкости (КЖ) 1:1000, в иммуноасцитической жидкости (ИАЖ) 1:128000. Моноклональные антитела из КЖ и ИАЖ выделяют с помощью осаждения сульфатом аммония с последующей аффинной хроматографией на белок А или G сефарозе. Гомогенность выделенных антител проверяется с помощью электрофореза в полиакриламидном геле в присутствии додецилсульфата натрия.
Продуктивность штамма. Продукция МКА в среде культивирования составляет 20-50 мкг/мл, в асцитической жидкости - 2-4 мг/мл. Продукция МКА в культуральной жидкости сохраняется на протяжении 15 пассажей (срок наблюдения) и 5 пассажей при культивировании в виде асцитных опухолей на мышах (срок наблюдения).
Контаминация штамма. Контаминанты гибридной линии, включая бактерии, дрожжи, грибы не выявлены. Микроплазмы не определяли.
Криоконсервация. Среда замораживания содержит эмбриональной телячьей сыворотки - 90%, диметилсульфоксида -10%. Режим криоконсервации и отогрева. Гибридные клетки вносят в криопробирки, помещают в контейнер из пенопласта с толщиной стенок не менее 1 см и оставляют на 16-24 часа в кельвинаторе при температуре - 70°С и затем опускают в жидкий азот.
Размораживание проводят быстро на водяной бане при температуре 37°С.Ампулы содержат 1,0 мл криозащитной среды с концентрацией гибридных клеток 106. Жизнеспособность восстанавливаемых гибридом после криоконсервации составляет 65-75%.
Свойства полезного продукта. Гибридома продуцирует моноклональные антитела, относящиеся к lgG3 подклассу иммуноглобулинов мыши. Моноклональные антитела специфичны к БТШ 70 быка, человека, мышей, дрожжей (с другими видами животных и микроорганизмами не проверялись).
Пример 1. Получение гибридомы.
Иммунизацация.
Мышей линии BALB/c иммунизируют препаратом БТШ 70 быка по схеме:
- подкожное введение мышам 45 мкг БТШ 70 в несколько точек в полном адъюванте Фрейнда;
- через 28 суток повторное введение мышам 45 мкг БТШ 70 в несколько точек в неполном адъюванте Фрейнда;
- через 28 суток внутривенная инъекция мышам 15 мкг БТШ 70 в физиологическом растворе;
- через 14 суток внутривенная инъекция мышам 10 мкг БТШ 70 в физиологическом растворе;
- через 7 суток внутривенная инъекция мышам 10 мкг БТШ 70 в физиологическом растворе;
- через 7 суток внутривенная инъекция мышам 10 мкг БТШ 70 в физиологическом растворе;
- через 7 суток внутривенная инъекция мышам 10 мкг БТШ 70 в физиологическом растворе.
Кровь у иммунных мышей отбирают на третий день после инъекции БТШ 70 согласно Animal protocol №P 02-19 стр.7.
Титры специфических антител в сыворотках животных определяют с помощью непрямого твердофазного ИФА.
Гибридизация.
Через 3 суток после последней внутривенной инъекции извлекают селезенку мыши и проводят гибридизацию 108 спленоцитов мыши с 107 клетками миеломной линии РЗ-Х63 Ag/8-653 в присутствии 1 мл 50% раствора полиэтиленгликоля (Sigma) с молекулярным весом 1500 в течение 1 минуты.
Селекция.
После отмывки полиэтиленгликоля клетки высевают на 96-луночные планшеты на слой перитонеальных макрофагов, взятых у мышей линии BALB/c. Селекцию гибридных клеток проводят на селективной среде с содержанием гипоксантина-аминоптерина-тимидина (HAT). Через 21 сутки из среды убирают аминоптерин. В последующем культивирование проводят на среде DMEM "Sigma" с 15% эмбриональной телячьей сыворотки, 2 мМ/L-глутамина, 50 мкг/мл гентамицина.
Скрининг гибридных клонов.
Для отбора положительных гибридных клонов, продуцирующих МКА, используют непрямой твердофазный ИФА.
Для проведения непрямого варианта ИФА в лунки 96 - луночного полистироловой планшета для иммуноферментного анализа вносят по 100 нг БТШ 70, приготовленного на 0,01 М карбонатном буфере pН 9,6 в объеме 100 мкл и затем выдерживают при температуре 6°С в течение 16 ч. Лунки планшета отмывают забуференным физиологическим раствором, содержащим 0,05% Твина-20 (ЗФР-Тв). Вносят в лунки по 100 мкл 0,5% раствор бычьего сывороточного альбумина (БСА), проверенного на отсутствие пероксидазной активности, и инкубируют при температуре 37°С в течение 45 мин. Три раза отмывают ЗФР-Тв и вносят в лунки супернатант культуральной жидкости в объеме 100 мкл. Планшет инкубируют при температуре 37°С в течение 1 часа. После этого лунки планшета трижды отмывают раствором ЗФР-Тв и добавляют в лунки антитела против иммуноглобулинов мыши, меченные пероксидазой хрена в рабочем разведении. Планшет инкубируют при температуре 37°С в течение 40 минут, затем 5 раз отмывают лунки раствором ЗФР-Тв. Положительную реакцию оценивают по появлению желто-коричневого окрашивания продукта хромогена - ортофениплендиамина (4 мкл 30% Н2O2 4 мг ортофенилендиамина на 100 мл 0,1 М натрий цитратного буфера pH 5,0). Реакцию останавливают добавлением в лунки по 50 мкл 8 N серной кислоты. Планшеты сканируют на планшетном ридере Пикон (Россия), измеряя поглощение при 492 нм.
Клонирование.
Клонирование гибридных клеток проводят методом лимитирующих разведений в 96-луночных планшетах на слое перитонеальных макрофагов из расчета 104 клеток на лунку. Скрининг клонов проводят непрямым твердофазным ИФА, как описано выше.
Культивирование.
Культивирование клонов гибридомы ведут при температуре 37°С в атмосфере, содержащей 5% углекислого газа. Средой культивирования является среда RPMI - 1640, содержащая 15% эмбриональной телячьей сыворотки, 2 мМ/L-глутамина, 50 мкг/мл гентамицина.
Криоконсервация.
Клоны гибридомы криоконсервируют на среде замораживания, состоящей из эмбриональной телячьей сыворотки - 90%, диметилсульфоксида - 10%. Клоны гибридомы хранят в сосудах Дюара с жидким азотом.
Проверка специфичности МКА.
Пример 2. Непрямой твердофазный иммуноферментный анализ.
Для проведения твердофазного ИФА в лунки 96 - луночного полистиролового планшета для иммуноферментного анализа вносят БТШ 70 в разведениях от 100 нг до 1,5 нг, приготовленных на 0,01 М карбонатном буфере (рН 9,6) в объеме 100 мкл и выдерживают при температуре 6°С в течение 16 часов. Последующие стадии анализа проводят аналогично стадиям, описанным для скрининга гибридных клонов.
Моноклональные антитела вносят в лунки в концентрации 100 нг/мл.
Отрицательный контроль - сыворотка интактной мыши в разведении 1/1000.
В непрямом твердофазном ИФА моноклональные антитела гибридомы 2Е4 специфически взаимодействуют с БТШ 70 и определяют до 3 нг белка в анализируемом образце (фиг.1).
Пример 3 Иммуноблот.
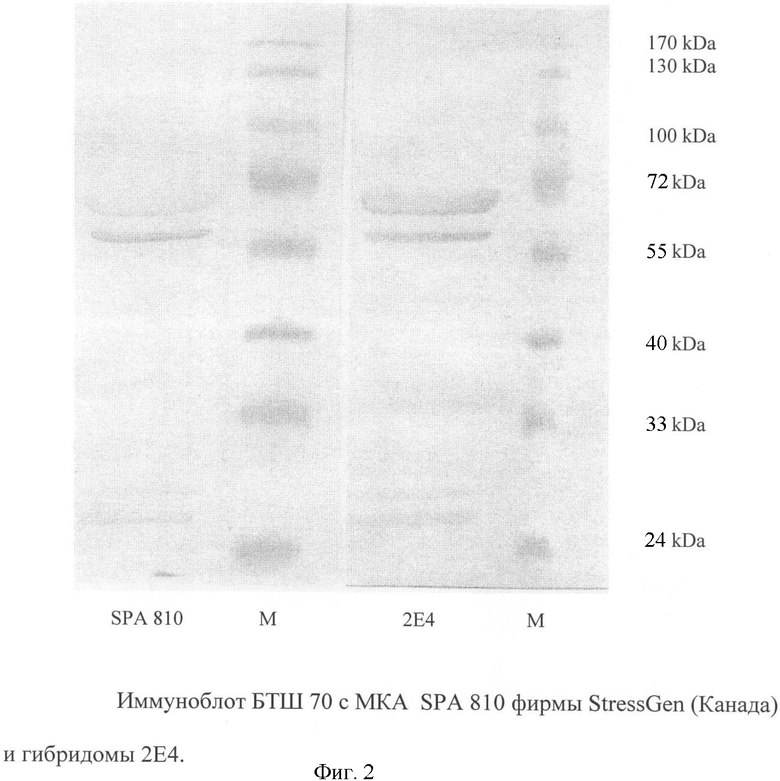
Для проверки специфичности МКА гибридомы 2Е4 к БТШ 70 проводят СДС-электрофорез в 10% полиакриламидном геле (ПААГ) в течение 2 часов при 220 В, 20 мА. Белки из ПААГ переносят на нитроцеллюлозную мембрану (Hybond-P) в течение 1 час при силе тока 380 мА. После завершения переноса мембрану блокируют, погружая в 1% раствор БСА в 20 мМ трис-буфер, pH 7,4 на 1 час при комнатной температуре. Для промывок мембран и разведения белков использовали 20 мМ трис-буфер, pН 7,4, содержащий 150 мМ NaCl и 0,5% твин 20. Блокированные и промытые мембраны разрезают на полосы. Каждую полосу инкубируют отдельно в растворах МКА гибридомы 2Е4 и МКА SPA 810 с концентрацией 1 мкг/мл в течение 1 часа при температуре 37°С. После промывки буфером полоски обрабатывают раствором антимышиных антител конъюгированных с пероксидазой хрена (Sigma) в рабочем разведении при тех же условиях, промывают буфером и окрашивают раствором диаминобензидина (0,5 мг/мл 3.3'-диаминобензидина с 0,1 мг/мл NiCl2, 0,1 мг/мл СоС12, 0.03% Н2O2) в ЗФР pН 7,2. Реакцию останавливают промывкой дистиллированной водой.
Отрицательный контроль - сыворотка интактной мыши в разведении 1/1000.
Моноклональные антитела, продуцируемые гибридомой 2Е4, взаимодействуют с БТШ 70 в иммуноблоте и выявляют те же белковые полосы, что и коммерческие МКА SPA 810 (фиг.2).
Пример 4. Дот-блот.
Дот-блот проводят на нитроцеллюлозной мембране (Hybond-P). Посадочная доза для БТШ 70 и его фрагментов составляет 50 нг в точку диаметром 2 мм. Нитроцеллюлозную мембрану блокируют в 1% растворе БСА в ЗФР в течение 1 часа при комнатной температуре, погружают в раствор МКА гибридомы 2Е4 в концентрации 1 мкг/мл в ЗФР-Тв, инкубируют в течение 1 часа при температуре 37°С и промывают ЗФР-Тв. Затем мембраны помещают в раствор пероксидазного конъюгата (Sigma) в ЗФР-Тв в рабочем разведении на 1 час при температуре 37°С и промывают ЗФР-Тв. В качестве субстрата для пероксидазы хрена используют раствор диаминобензидина (0,5 мг/мл 3.3'-диаминобензидина с 0,1 мг/мл NiCl2, 0,1 мг/мл CoCl2, 0.03% Н2O2) в ЗФР pН 7,2. Реакцию останавливают промывкой дистиллированной водой.
Отрицательный контроль - мембраны, обработанные сывороткой интактной мыши в разведении 1/1000. Положительный контроль - мембраны, обработанные сывороткой иммунной мыши в разведении 1/1000.
Моноклональные антитела, продуцируемые гибридомой 2Е4, специфически взаимодействуют в дот-блоте с цельным БТШ 70 и его С-концевым фрагментом (аа386-641) и не взаимодействуют с его N-концевым фрагментом (aal-437) (фиг.3).
Пример 5. Цитометрическое тестирование МКА.
Измерение уровня экспрессии поверхностных БТШ 70 производят методом проточной цитометрии после непрямого иммунофлуоресцентного окрашивания клеток с использованием тестируемых моноклональных антител к БТШ 70 (2Е4, SPA 810 - «первые» антитела, титр 1:500) и «вторых» антител - конъюгат антител против Fab-фрагментов мышиных IgG с флуоресцеинизотиоционатом (ФИТЦ) ("Sigma", США) в рабочем разведении. Для этого клетки после центрифугирования при 200g в течение 10 минут переводят в ЗФР, содержащий 0,1%) NaN3 и 0,5% BSA, и инкубируют в течение 30 мин при температуре 4°С с первыми антителами. Затем клетки дважды отмывают ЗФР с использованием центрифугирования при 200g в течение 10 мин и инкубируют в течение 30 мин при 4°С со вторыми антителами. После инкубации клетки опять дважды отмывают в ЗФР центрифугированием в том же режиме. Окрашенные образцы анализируют на проточном цитофлуориметре (EPICS XL, "Coulter Corporation", США). В каждом образце проводят измерение уровня флуоресценции не менее 10000 клеток.
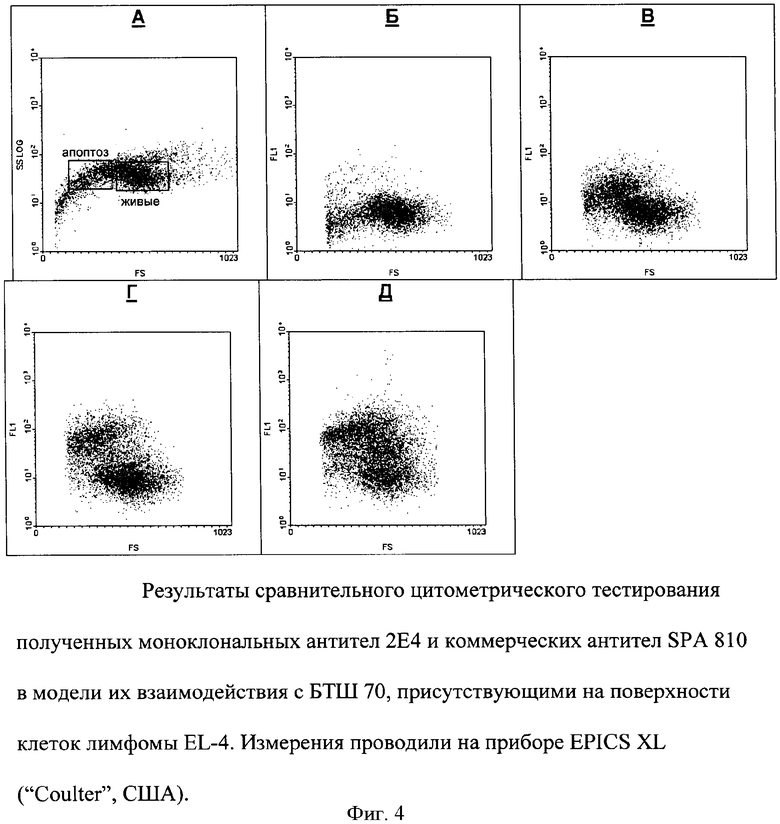
На фиг.4 представлены результаты сравнительного цитометрического тестирования полученных моноклональных антител гибридомы 2Е4 и коммерческих антител SPA 810 в модели их взаимодействия с БТШ 70, присутствующим на поверхности клеток лимфомы EL-4. В качестве контролей используют типичное распределение клеток EL-4 по параметрам переднего (FS) и бокового (SS) светорассеяния, выявляющее пулы живых и апоптозных клеток (фиг.4, А); контроль аутофлуоресценции (фиг.4, Б) и контроль окрашивания вторыми, ФИТЦ - мечеными антителами (фиг.4, В).
Коммерческие моноклональные антитела SPA 810 слабо окрашивают живые клетки, но хорошо связываются с поверхностью апоптозных клеток (фиг.4, Г). В то же время МКА гибридомы 2Е4 характеризуются гораздо более выраженным взаимодействием с пулом живых клеток и примерно равноценным связыванием с апоптозными клетками (фиг.4, Д).
Пример 6. Определение БТШ 70 при воздействии теплового шока.
Суспензию живых клеток лимфомы EL-4 инкубируют в течение 10 мин при температуре 43°С с последующим непрямым иммунофлуоресцентным окрашиванием внутриклеточных БТШ 70 с использованием МКА SPA810 и МКА гибридомы 2Е4. Контрольная группа образцов клеток не подвергалась тепловому шоку.
Непрямое иммунофлуоресцентное окрашивание клеток EL-4 первыми и вторыми антителами для оценки внутриклеточного содержания БТШ 70 осуществляют по описанному выше протоколу (пример 5). Однако перед окрашиванием проводят префиксацию клеток и перфорирование их плазматических мембран для обеспечения проникновения антител во внутриклеточное пространство. Для фиксации к клеткам добавляют 2% раствор параформальдегида в ЗФР и инкубируют в течение 30 мин при комнатной температуре и дважды отмывают ЗФР. Для перфорирования плазматических мембран клетки обрабатывают 0,5% раствором Triton-X100 в течение 30 мин при комнатной температуре. После этого клетки дважды отмывают ЗФР, переводят в раствор ЗФР и проводят процедуру непрямого иммунофлуоресцентного окрашивания. Полученные образцы анализируют на проточном цитофлуориметре (EPICS XL, "Coulter Corporation", США). В каждом образце проводят измерение уровня флуоресценции не менее 10000 клеток.
В таблице представлены результаты, полученные при использовании различных антител для проточно-цитометрического анализа изменения содержания БТШ 70 в клетках EL-4, подвергнутых тепловому шоку.
Результаты проточно-цитометрического анализа изменения содержания БТШ70 в клетках EL-4, подвергнутых тепловому шоку, с помощью МКА.
Из таблицы видно, что МКА гибридомы 2Е4 дают более высокий уровень флуоресценции по сравнению с МКА SPA810 как в контрольных клетках, так и в клетках, подвергнутых тепловому шоку. Кроме того, зарегистрированные протестированными МКА эффекты гипертермии различаются по величине. Тепловой шок приводит не только к усилению синтеза БТШ 70, но и к существенным изменениям его состояния и конформации. В частности, такое воздействие может вызывать образование прочных комплексов БТШ 70 с другими внутриклеточными протеинами и их агрегацию, что отражается на детектируемом МКА уровне БТШ 70. Моноклональные антитела гибридомы 2Е4 выявляют более высокий процент увеличения синтеза БТШ70 в клетке, чем МКА SPA810, что позволяет получить более полную картину количественного изменения синтеза этого белка в ответ на воздействие теплового шока.
Преимущество гибридомы 2Е4 по сравнению с гибридомой SPA810 заключается в том, что она продуцирует МКА, которые более выражено определяют БТШ 70 на поверхности пула живых клеток как в норме, так и при воздействии на клетки теплового шока (стрессовый фактор).
Моноклональные антитела гибридомы 2Е4 специфичны к БТШ 70.
Эти свойства гибридомы 2Е4, а также взаимодействие ее МКА с целым БТШ 70 и с его С-концевым фрагментом свидетельствует о возможности использования МКА как компонента тест-систем для определения БТШ 70.
Источники информации
1. Craig E.A., Weissman J.S., Horwich A.L. Heat shock proteins and molecular chaperones: mediators of protein conformation and turnover in the cell // Cell - 1994. - Vol.78. - P.365-372.
2. Parsell D.A., Lindquist S. The function of heat-shock proteins in stress tolerance: degradation and reactivation of damaged proteins // Annu. Rev. Genet. - 1993. - Vol.27. - P.437-496.
3. Multhoff G. and Hightower LE. Cell surface expression of heat shock proteins and the immune response. // Cell Stress & Chaperones - 1996. - Vol.1. - P.167-176.
4. Hightower L.E., Guidon P.T. Selective release from cultured mammalian cells of heat-shock (stress) proteins that resemble glia-axon transfer proteins. //J. Cell. Physiol. - 1989. - Vol.138. - P.257-266.
5. Udono H. and Srivatstava P.K. Heat shok protein 70-associated peptides elicit specific cancer immunity // J. Exp.Med. - 1993. - Vol.178. - P.1391-1396.
6. Li Y., Yang G., Repasky E., Wang X.-Y. Generation of anti-tumor immunity using mammalian heat shok protein 70 DNA vaccines for cancer immunotherapy // Vaccine - 2006. - Vol.24. - P.5360-5370.
7. /www.caymanchem.com, www.biocompare.com. www.stressgen.ru. www.abcam.com. /
8. Sapozhnikov A.M., Gusarova G.A., Ponomarev E.D., Telford W.G. Translocation of cytoplasmic HSP70 onto the surface of EL-4 cells during apoptosis.//Cell Proliferation - 2002. - Vol.35. - P.193-206.


Изобретение относится к биотехнологии. Штамм гибридомы получают путем иммунизации мышей линии BALB/c бычьим БТШ 70 в течение 78 суток. На третьи сутки проводят гибридизацию спленоцитов иммунных мышей (10 клеток) с клетками мышиной миеломы РЗ-Х63 Ag/8-653 (10 клеток). В качестве агента для слияния применяют полиэтиленгликоль с молекулярным весом 4000 (Merk, Германия). После гибридизации проводят селекцию, скрининг, клонирование и криоконсервацию гибридомы. Изобретение может быть использовано для получения моноклональных антител (МКА) к белку теплового шока 70 (БТШ 70). 4 ил., 1 табл.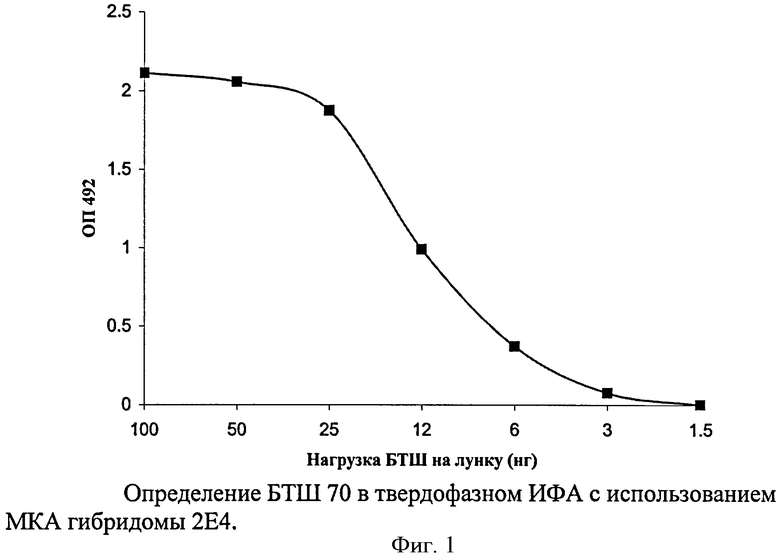
Штамм гибридных культивируемых клеток животных Mus musculus 2E4 - продуцент моноклональных антител, специфичных к белку теплового шока 70, депонирован в коллекции микроорганизмов Государственного научного центра прикладной микробиологии и биотехнологии (ГНЦ ПМБ), коллекционный номер Н-1.
| ШТАММ ГИБРИДНЫХ КУЛЬТИВИРУЕМЫХ КЛЕТОК ЖИВОТНЫХ MUS MUSCULUS - ПРОДУЦЕНТ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ К ГИПОГЛИКОЗИЛИРОВАННЫМ И ДЕГЛИКОЗИЛИРОВАННЫМ ИЗОФОРМАМ ОПУХОЛЬ-АССОЦИИРОВАННОГО АНТИГЕНА MUC I ЧЕЛОВЕКА | 2006 |
|
RU2319743C1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
Авторы
Даты
2010-02-10—Публикация
2008-07-10—Подача