Изобретение относится к медицине и может быть использовано в радиобиологических экспериментальных исследованиях на млекопитающих для изучения механизма действия радиации на организм, а также в практическом здравоохранении для лечения костномозговой формы острой лучевой болезни.
Известен способ лечения острой лучевой болезни, включающий однократное парентеральное введение в организм животного в течение первых суток после облучения высокомолекулярного соединения полисахаридной природы - фармакопейного препарата продигиозана [1]
Продигиозан представляет собой полимерный липополисахаридный комплекс, выделенный из микроорганизма B. prodigiosum и используемый в медицинской практике для повышения неспецифической резистентности при различных заболеваниях. Препарат эффективен при однократном внутримышечном введении через 3 5 ч после облучения в дозах, вызывающих гибель до 95% контрольных животных. Использование продигиозана позволяет увеличить выживаемость леченых животных на 25-34%
Однако наличие острой токсичности и развитие побочных явлений в виде рвоты, снижения пищевой возбудимости, угнетения двигательной активности и судорожных подергиваний в ответ на введение облученным животным продигиозана в оптимальных эффективных лечебных дозах ограничивают широкое применение данного способа лечения в медицинской практике.
Задача изобретения состоит в исключении, без ущерба для лечебной эффективности, острой токсичности и побочных реакций в ответ на введение средств, используемых в известном способе раннего лечения острой лучевой болезни.
Для решения поставленной задачи предложено в качестве лечебного средства использовать 1 ___→ 3; 1 ___→ 6 - β -D-глюкан транслам.
Известно применение предлагаемого 1___→3;1___→6-β-D-глюкана транслама в качестве иммуностимулятора, повышающего уровень антителообразующих клеток, фагоцитарную активность полиморфноядерных лейкоцитов при колисепсисе.
Авторами обнаружено новое качество 1 ___→ 3; 1 ___→ 6 - β -D-глюкана транслама при введении в ранние сроки после радиационного поражения препарат оказывает выраженное лечебное действие, проявляющееся в существенном облегчении клинических признаков радиационного поражения и повышении выживаемости подопытных животных. Применение транслама для лечения острой лучевой болезни неизвестно.
Высокая эффективность препарата 1 ___→ 3; 1 ___→ 6 - β -D-глюкана при использовании его в качестве лечебного средства радиационных поражений, подтвержденное на многих видах лабораторных животных (в том числе и на обезьянах), технологичность его производства, полное отсутствие токсичного и побочного действия при достаточно простой схеме назначения позволяют утверждать, что данный способ лечения найдет широкое практическое применение в здравоохранении.
Транслам представляет собой 1 ___→ 3; 1 ___→ 6 - β -D-глюкан (молекулярная масса (М. м. ) 8000), полученный ферментативным синтезом из ламинарана-полисахарида дальневосточных бурых водорослей Laminaria cichorioides.
Ламинаран представляет собой 1 ___→ 3; 1 ___→ 6 - β -D глюкан с М. м. 5 кДа. В ламинаране 1 ___→ 6- связанная глюкоза (около 10%) находится в виде ответвленной от основной цепи 1 ___→ 3 - β -D-глюкана. Около 80% восстанавливающих концов молекул закрыто маннитом.
Транслам получают из продуктов трансформации ламинарана под действием эндо- 1 ___→ 3; - β -D-глюканазы Ло, выделенной из Chlamys albidus. Структура транслама отличается от ламинарана тем, что он имеет более высокую М. м. (8 против 5 кДа), содержит примерно в 2,5 раза больше количество 1 ___→ 6-связанных остатков глюкозы, сосредоточенных, в основном, на невосстанавливающем конце молекулы. Помимо разветвлений, 1 ___→ 6 связанные остатки D глюкозы включены также в основную цепь 1 ___→ 3; - β -D-глюкана или транслама. Восстанавливающие концы молекул транслама не гликозилированы маннитом.
Структуру транслама устанавливали с помощью 13С-ЯМР-спектроскопии, деградации по Смиту, определения М. м. методами концевого анализа и гель-фильтрации.
Вещество водорастворимо, легко стерилизуется кипячением, нетоксично (при внутривенном введении мелким лабораторным животным транслама в дозах до 10 г/кг не зарегистрировано летальных эффектов).
Способ получения транслама.
Раствор ламинарана (5 10 мг/мл) в ацетатном буфере (0,05 М; pH 5,5), содержащем 0,1 М NaCl, обрабатывают эндо- 1 ___→ 3 - β -D-глюканазой Ло из Chlamis albidus при 25oC. Полученную смесь разделяют на полихроме-1, используя ступенчатый градиент вода-спирт: 11 12%-ным водным этанолом элюируют низкомолекулярные олиго- и полисахариды, 13 15%-ным продукт ферментативный синтеза- 1 ___→ 3; 1___→ 6- β -D-глюкан, именуемый трансламом.
Пример 1. Сравнительная эффективность предлагаемого способа и прототипа в опытах на облученных мышах.
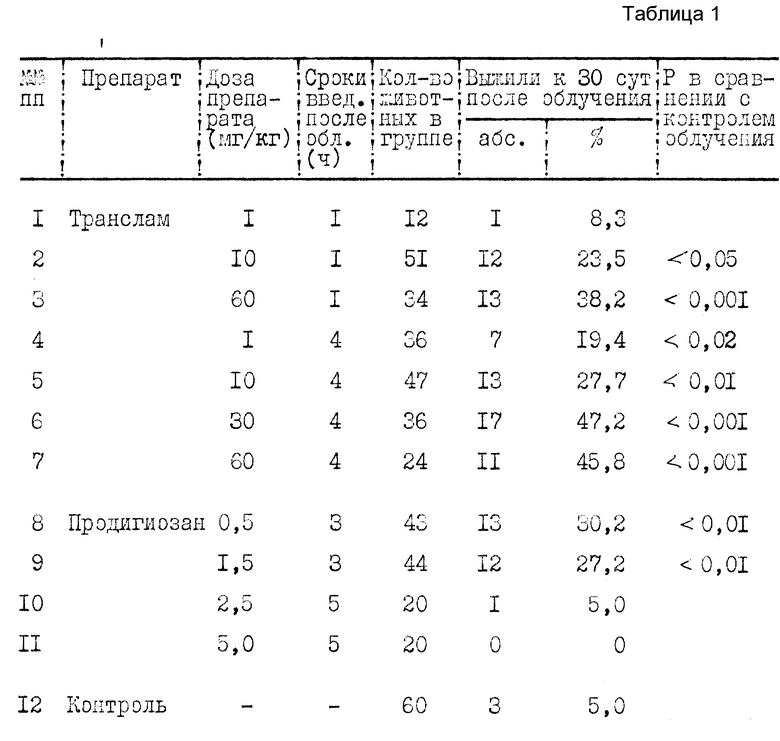
Транслам вводят мышам F1 (CBAxC57BL) подкожно в дозе в дозе 30 - 60 мг/кг, а продигиозан внутримышечно в дозе 0,5 1,5 мг/кг через 3 5 ч после гамма-облучения 137Cs в дозе 8,25 г (табл. 1).
Приведенные данные свидетельствуют, что предлагаемый способ в экспериментах на мелких лабораторных животных не уступает прототипу по выраженности лечебного действия и, по-видимому, обладает более длительным периодом эффективного применения в качестве средства раннего радиационного поражения.
Пример 2. Сравнительная оценка показателей острой токсичности транслама и продигиозана и их угнетающего влияния на дезинтоксикационную функцию печени в опытах на мелких лабораторных животных (мыши F1 (CBAxC57BL)).
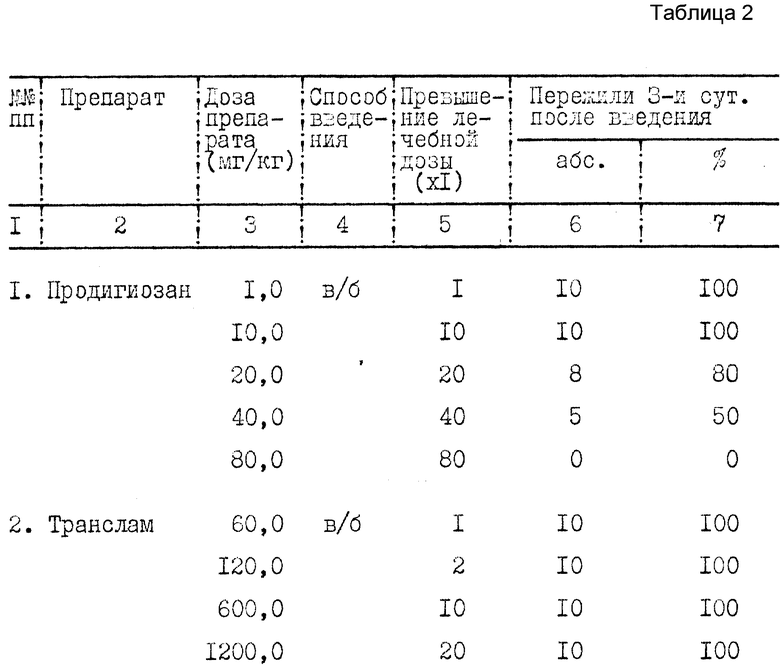
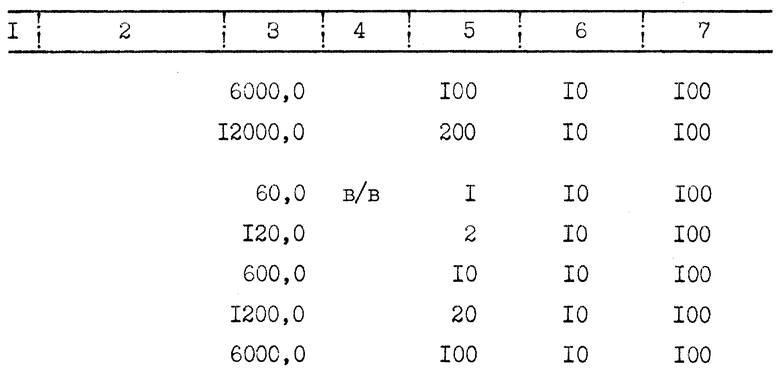
Острую токсичность определяли по гибели животных в течение 3 сут после парентерального введения препаратов в дозах, превышающих в 1 200 раз оптимальную лечебную (табл. 2).
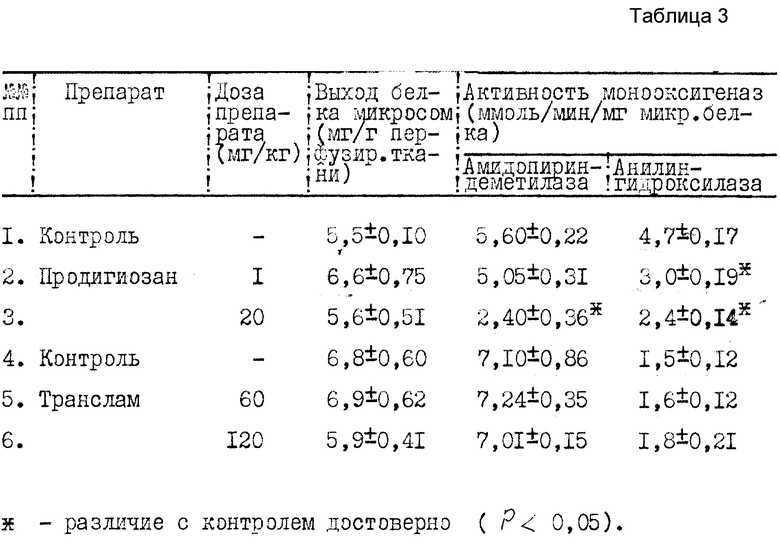
Влияние препаратов на дезинтоксикационную функцию печени оценивали по угнетению активности монооксигеназ (система метаболизма ксенобиотиков) в гепатоцитах мышей, получивших препараты за 24 ч до исследования (табл. 3).
Полученные результаты свидетельствуют о том, что в опытах на мелких лабораторных животных введение транслама в дозах до 10 12 г/кг (включая внутривенный способ) не вызывает их гибели, а при введении продигиозана регистрируются острые летальные эффекты ЛД50/3 для этого полисахарида составляет 39,6 мг/кг.
Кроме того, у животных, получавших транслам в дозах 60 120 мг/кг, не отмечено угнетение активности монооксигеназ системы метоболизма ксенобиотиков в печени, в то время как введение аналогичных оптимальных эффективных доз ородигиозана, выбранного в качестве прототипа, оказывает подавляющее действие на ферментные системы гепатоцитов, что свидетельствует о нарушении детоксикационной функции печени.
Пример 3. Сравнительная эффективность транслама и продигиозана в опытах на собаках, облученных γ квантами 60Co.
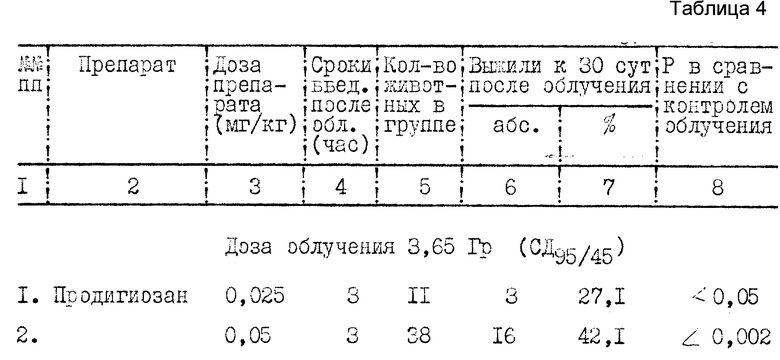
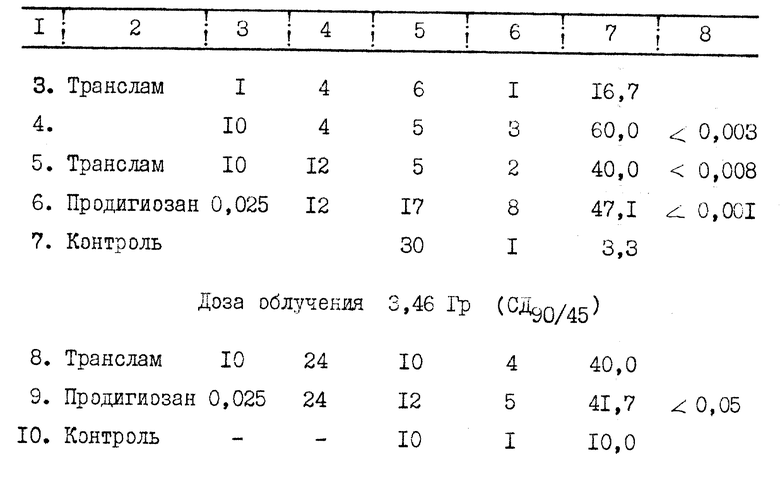
Группам беспородных собак, рандомизированным по массе, полу и общим гематологическим показателям, препараты вводили внутримышечно через 3 4, 12 и 24 ч после облучения (табл. 4).
Следовательно, и в опытах на собаках использование транслама в течение 1-х суток после облучения в дозах, близких к минимальной абсолютно летальной, нисколько не уступает прототипу в выраженности лечебных свойств, обеспечивая повышение выживаемости более чем на 40% Однако следует особо подчеркнуть, что при применении предлагаемого вещества не отмечено никаких побочных эффектов, в то время как после введения продигиозана у животных в течение нескольких часов наблюдали угнетение двигательной активности, судорожные подергивания, единичные акты рвоты и дефекации.
Пример 4. Лечебная эффективность транслама в сочетании со схемой комплексной антибиотикотерапии в опытах на обезьянах Масса fascicularis облученных g квантами 237Cs в дозе, близкой к минимальной абсолютно смертельной.
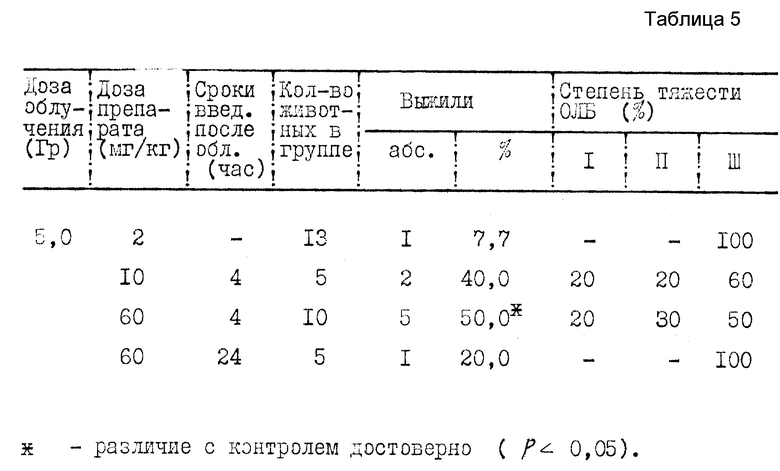
Препарат (10 или 60 мг/кг) вводили внтуримышечно через 4 или 24 ч после облучения, с 8-х суток ОЛБ животные опытной и контрольной групп получали терапию антибиотиками и витаминами по упрощенной комплексной схеме (табл. 5).
Таким образом, в результате предпринятых исследований на 3 видах лабораторных животных была продемонстрирована высокая терапевтическая эффективность препарата 1 ___→ 3; 1___→ 6- β -D-глюкана транслама при использовании его в качестве лечебного средства радиационных поражений.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОФИЛАКТИКИ ЗАБОЛЕВАНИЯ ИКРЫ И МОЛОДИ РЫБ САПРОЛЕГНИЕЙ | 1995 |
|
RU2081575C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ЛУЧЕВОЙ БОЛЕЗНИ | 1997 |
|
RU2141833C1 |
| СРЕДСТВО ДЛЯ ПРЕДУПРЕЖДЕНИЯ ЛУЧЕВОЙ БОЛЕЗНИ | 1998 |
|
RU2161973C2 |
| КРИОПРОТЕКТОР ЖИВОТНЫХ КЛЕТОК | 1993 |
|
RU2034026C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ | 2001 |
|
RU2184556C1 |
| СПОСОБ ПОЛУЧЕНИЯ УГЛЕВОД-БЕЛКОВОГО КОМПЛЕКСА ИЗ ПРИМОРСКОГО ГРЕБЕШКА | 1996 |
|
RU2121844C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1 -> 3, 1 -> 6-БЕТА-D-ГЛЮКАНА, ОБЛАДАЮЩЕГО ИММУНОСТИМУЛИРУЮЩЕЙ АКТИВНОСТЬЮ | 1993 |
|
RU2095417C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОФИЛАКТИЧЕСКИМ И ЛЕЧЕБНЫМ ДЕЙСТВИЕМ ПРИ ЗАРАЖЕНИИ ВИРУСОМ КЛЕЩЕВОГО ЭНЦЕФАЛИТА | 2003 |
|
RU2242238C1 |
| ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКАЯ ПИЩЕВАЯ КОМПОЗИЦИЯ "ЖЕНСОЛАР", ОБЛАДАЮЩАЯ АЛКОПРОТЕКТОРНЫМ ДЕЙСТВИЕМ (ВАРИАНТЫ) | 1996 |
|
RU2095080C1 |
| КАЛИЕВАЯ СОЛЬ КАУЛОЗИДА C, СТИМУЛИРУЮЩАЯ РЕПАРАТИВНУЮ РЕГЕНЕРАЦИЮ КОЖИ | 1994 |
|
RU2078086C1 |
Изобретение относится к медицине и может быть использовано в радиобиологических экспериментальных исследованиях на млекопитающих для изучения механизма действия радиации на организм и в практическом здравоохранения для лечения костно-мозговой формы острой лучевой болезни. Предложено в качестве лечебного средства использовать 1 ___→ 3; 1 ___→ 6 - β -D-глюкан - транслам. Препарат не вызывает побочных явлений, имеет низкую токсичность. 5 табл.
Способ лечения костно-мозговой формы острой лучевой болезни, включающий введение в организм после облучения высокомолекулярного соединения полисахаридной природы, отличающийся тем, что в качестве высокомолекулярного соединения используют 1 __→ 3; 1 __→ 6 - β - D -глюкан-транслам в дозе 10 60 мг/кг.
| Чертков К.С | |||
| и др | |||
| Лечение облученных морских свинок полисахаридом продигиозаном | |||
| - Радиобиология, 1976, т.16 вып | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Шланговое соединение | 0 |
|
SU88A1 |
Авторы
Даты
1997-11-27—Публикация
1993-08-31—Подача