Изобретение относится к медицине, хирургии, конкретно к способам пластики кровеносных сосудов.
Известен способ пластики кровеносных сосудов, заключающийся в закрытии дефекта аорты или магистральных артерий трансплантатом из вены пуповины человека, который закрепляют на области дефекта обвивным швом из шелковой или синтетической нити [2, 3] Однако данный способ имеет следующие недостатки: необходимо полное выделение сосуда в экстремальных условиях, наличие консервированного трансплантата, частое образование аневризм в месте анастомоза или прорезывание швов с последующим кровотечением, что чревато геморрагическим шоком или летальным исходом.
Наиболее близким по технической сущности является способ пластики, включающий замещение дефекта с помощью аутотрансплантата выкроенного из височного апоневроза [1] Однако данный способ имеет недостатки: необходимо дополнительное время для выкраивания лоскута из височного апоневроза, полное выделение сосуда в условиях обильного кровотечения, частое тромбирование сосудистой конструкции по причине контакта тромбоцитов с инородной поверхностью трансплантата, рубцовое сужение сосуда.
Новый технический результат сокращение времени и снижение осложнений за счет упрощения способа достигают новым способом пластики кровеносных сосудов, включающим закрытие дефекта трансплантатом и последующее его закрепление в области дефекта, причем в качестве трансплантата используют пластину из пористого никелида титана толщиной 0,39-0,4 мм с диаметром пор 180 микрон, частотой пор 60% а закрепляют ее с помощью спирали, выполненной из металла с памятью формы диаметром витков 8-12 мм, шагом 2-3 мм, толщиной проволоки 0,4-0,55 мм, имеющей конфигурацию элементов в форме "меандра".
Способ осуществляют следующим образом: на область пораженного сосуда накладывают пористую пластину из никелида титана, моделированную по диаметру сосуда (фиг. 1) и закрепляют ее спиралью из металла с памятью формы. В течение 1-2 минут поры пластины заполняются фибрином, тромбируются, кровотечение останавливается.
Для подтверждения осуществления изобретения при указанных выше технических результатах проведены испытания ан 16 беспородных собаках весом от 15 до 20 кг. Операцию проводили в одно и то же время суток, натощак. В качестве вводного и базисного наркоза применяли 1% раствор тиопентала Na вводимого интраплеврально. Эксперимент проводили на абдоминальном отделе аорты, а именно: заброшенным доступом слева выделялась аорта дистальнее отхождения почечных артерий и до трифуркации аорты. Остроконечным скальпелем наносился разрез по передней стенке аорты длинной от 10 до 15 мм. Заранее приготовленную пористую пластину из никелида титана, размером превышающим площадь дефекта в аорте, накладывали на сосуд. Стерилизацию пластины осуществляли методом тиндализации с последующей стерилизацией в сухожаровой камере и помещали для хранения в раствор 96o спирта. В день операции пластину вынимали и поджигали для выпаривания спирта, затем помещали в раствор антибиотиков широкого спектра действия.
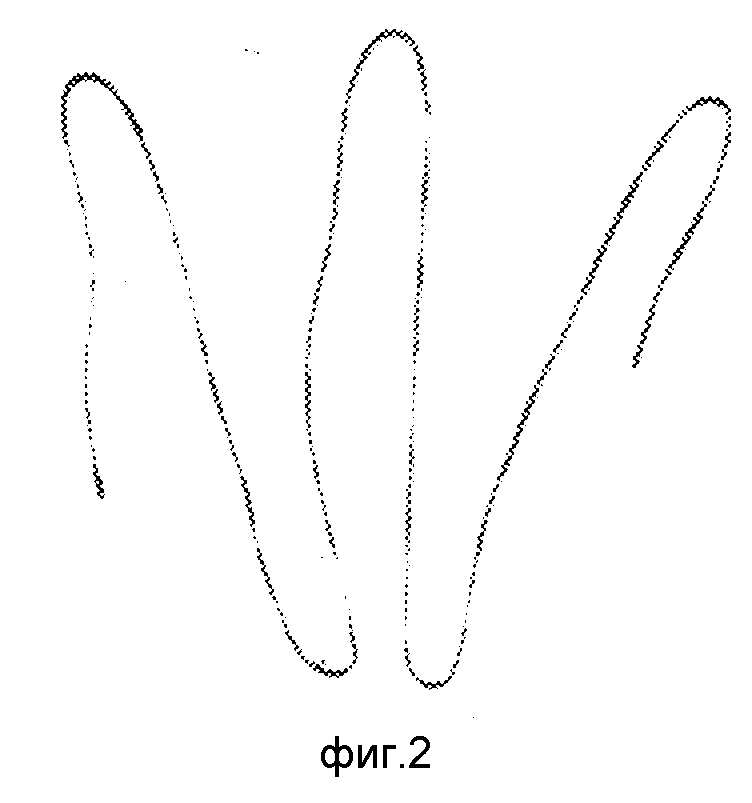
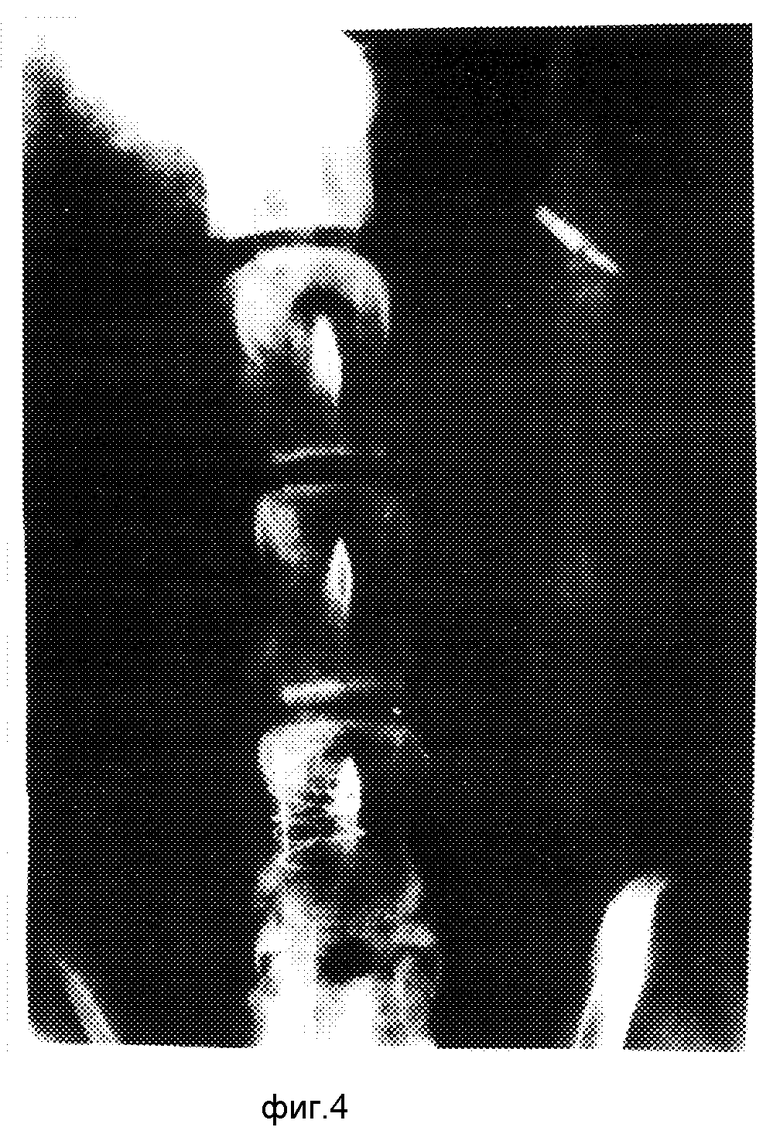
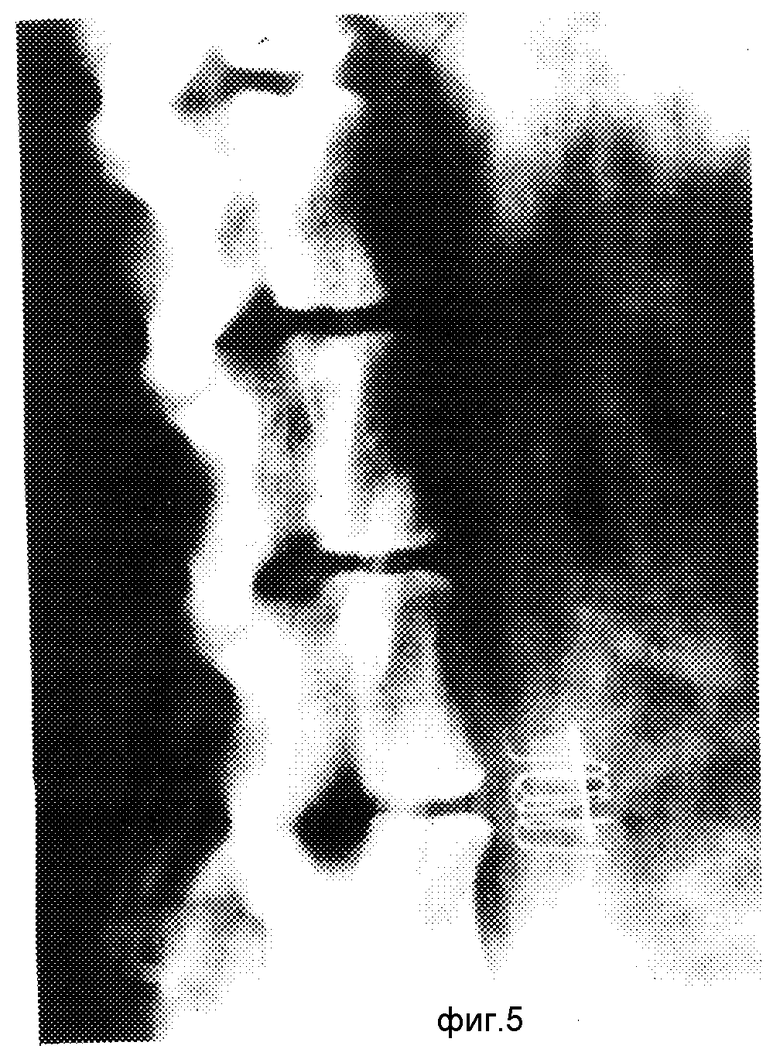
Пластину закрепляют с помощью спирали из металла с памятью формы. Спираль проходила аналогичную стерилизацию и хранение. Перед употреблением спираль помещают в хлорэтил и при этом все ее дуги выпрямлялись и располагались в одной плоскости (фиг. 2). При фиксации спирали на сосуде под действием температуры ткани происходило формовосстановление (фиг. 3), что позволило быстро, надежно зафиксировать пластину на сосуде (фиг. 4, 5). Материал спирали является биоинертным, нетоксичным и при надежном закреплении исключает излишнюю деформацию сосуда. Это обусловлено конфигурацией элементов в форме "меандра", внутренний диаметр 8-12 мм соответствует диаметру сосуда. Диаметр проволоки 0,4-0,55 мм используется с целью сохранения эластичности и предупреждению пролабирования стенки сосуда. Шаг витков спирали 2-3 мм достаточен для придания эластичности пружины и удержания пластины на аорте.
При величине пор более 180 микрон время образования тромба увеличивается. Через поры пластины устремляется кровь и в течение 1-2 минут отверстия заполняются кровяными сгустками, останавливается кровотечение. После остановки аортального кровотечения и после тщательного гемостаза рану ушивали послойно, наглухо. В ближайшем послеоперационном периоде (до 10 суток) осложнений не наблюдалось. Кормить начинали на вторые сутки жидкой пищей.
Животных выводили из эксперимента в различные сроки после пластики кровеносных сосудов. Повторную операцию осуществляли под эндотрахеальным эфирным наркозом. После срединной лапаротомии производили резекцию терминального отдела брюшной аорты, отступали 10-15 мм дистально и проксимально от сосудистой конструкции из никелида титана. Забор материала осуществляли через 1, 2, 4, 6 месяцев от момента сосудистой пластики соответственно у 4 собак после каждого указанного срока. Резецированную аорту помещали в раствор формалина с последующей окраской препаратов гематоксилин-эозином, по ван-Гизону, орсеином, серебром.
Полученные данные исследования реконструированной аорты выявили различную морфологическую картину в зависимости от срока реконструкции. К двум месяцам функционирования сосуда происходит заполнение пор пластины из никелида титана незрелой соединительной тканью, образование неоинтимы с эндотелиоподобной выстилкой. К этому времени исследуемая ткань достаточно снабжена кровеносными капиллярами и имеются нервные образования. К 4 месяцам выявляется дифференциация тканей, четко выражена зрелая соединительная ткань, обилие сосудов с четкой эндотелиоподобной выстилкой.
Таким образом, преимущество предлагаемого способа пластики артериального сосуда с помощью трансплантата из пористого никелида титана заключается в следующем.
1. Увеличивается скорость закрытия дефекта.
2. Достигается полная остановка кровотечения из пораженного сосуда в течение 1-2 минут вследствие заполнения пор пластины фибрином и в последующем на ней формируется неоинтима.
3. Материал обладает тромборезистентностью, биоинертен, подвижен, в результате чего не происходит деформации сосуда и связанных с ней осложнений.
4. Материал является нетоксичным, не отторгается тканями, более того становится основой для формирования внутренней поверхности сосуда.
5. Закрепление пластины на области дефекта с помощью спирали из металла с памятью формы позволяет быстро, надежно зафиксировать трансплантат. Материал спирали также является биоинертным, подвижным, способен моделировать форму, обладает тромборезистентностью, при надежном закреплении исключает деформацию сосуда.
Литература.
1. Авторское свидетельство СССР N 935084, 1982.
2. Беличенко И.А. Кунгурцев В.В. Шиманко А.И. Возможности применения вены пупочного канатика в реконструктивной хирургии артерий нижних конечностей /Хирургия, 1980, N 8, с. 8-11.
3. Чирьев А.И. Возможности использования вены пуповины в восстановительной хирургии сосудов /Автореферат дис. канд. мед. наук. Томск, 1986, 13 с.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПЛАСТИКИ МАГИСТРАЛЬНЫХ ВЕН | 2006 |
|
RU2305506C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ ВЕН | 1994 |
|
RU2116051C1 |
| СПОСОБ ПРОТЕЗИРОВАНИЯ МАГИСТРАЛЬНЫХ АРТЕРИАЛЬНЫХ СОСУДОВ | 2018 |
|
RU2705910C2 |
| СПОСОБ ПРОФИЛАКТИКИ АНЕВРИЗМ ПРИ РЕКОНСТРУКЦИЯХ АОРТЫ И МАГИСТРАЛЬНЫХ АРТЕРИЙ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2003 |
|
RU2245109C1 |
| КЛИПСА ДЛЯ ПРОФИЛАКТИКИ ТРОМБОЭМБОЛИИ ЛЕГОЧНОЙ АРТЕРИИ | 2001 |
|
RU2211675C2 |
| СПОСОБ ЗАМЕЩЕНИЯ ЦИРКУЛЯРНЫХ ДЕФЕКТОВ ТРАХЕИ | 2010 |
|
RU2445008C1 |
| СПОСОБ ПЛАСТИЧЕСКОГО ЗАМЕЩЕНИЯ ДЕФЕКТА ПЕРИКАРДА | 2009 |
|
RU2400152C1 |
| КОСТНЫЙ ИМПЛАНТАТ | 1998 |
|
RU2157151C2 |
| СПОСОБ ЗАМЕЩЕНИЯ ПРОТЯЖЕННОГО ЦИРКУЛЯРНОГО ДЕФЕКТА ТРАХЕИ | 2011 |
|
RU2449740C1 |
| СПОСОБ ОСТАНОВКИ КРОВОТЕЧЕНИЯ ИЗ ПРЕСАКРАЛЬНОГО ВЕНОЗНОГО СПЛЕТЕНИЯ | 2012 |
|
RU2493804C1 |

Изобретение относится к медицине, а именно к хирургии и может быть использовано для пластики кровеносных сосудов. Сущность изобретения: для закрытия дефекта сосуда используют трансплантат - пластину из пористого никелида титана толщиной 0,34-0,4 мм, с диаметром пор 180 микрон, частотой пор 60%, а закрепляют ее с помощью спирали, выполненной из металла с памятью формы диаметром витков 8-12 мм, шагом 2-3 мм, толщиной проволоки 0,4-0,55 мм, имеющей конфигурацию элементов в форме "меандра". Технический результат: упрощение операции за счет исключения этапа формирования трансплантата на операции. 5 ил.
Способ пластики кровеносных сосудов, включающий закрытие дефекта трансплантатом и последующее его закрепление на области дефекта, отличающийся тем, что в качестве трансплантата используют пластину из пористого никелида титана толщиной 0,39 0,4 мм с диаметром пор 180 мкм, частотой пор 60% а закрепляют ее с помощью спирали, выполненной из металла с памятью формы, с диаметром витков 8 12 мм, шагом 2 3 мм, толщиной проволоки 0,4 0,55 мм, имеющей конфигурацию элементов в форме меандра.
| SU, авторское свидетельство, 935084, кл | |||
| Устройство для сортировки каменного угля | 1921 |
|
SU61A1 |
Авторы
Даты
1997-12-20—Публикация
1996-05-14—Подача