Предлагаемое изобретение относится к нефтегазодобывающей промышленности, в частности к области кислотной обработки терригенных коллекторов и разглинизации пластов.
Известно, что на терригенные коллекторы воздействуют смесью соляной и плавиковой кислот [1]
Взаимодействие плавиковой кислоты с силикатными материалами, кварцем и каолином терригенного коллектора происходит по следующей схеме:
SiO2 + 4НF SiF4 + 2H2O (1)
Н4Al2Si2O9 + 14НF 2AlF3 + 2SiF4 + 9H2O (2)
Образовавшийся в результате реакции плавиковой кислоты и терригенной породы фтористый кремний, реагируя с водой, в свою очередь образует гидрат окиси кремния, который по мере снижения кислотности раствора превращается из золя в гель, запечатывающий поровое пространство. Для предупреждения образования в поровом пространстве геля кремниевой кислоты плавиковая кислота при обработке терригенных коллекторов применяется только в смеси с соляной. Оптимальным считают содержание в смеси 3-5% НF и 8-10% НCl. По другим источникам рекомендуемый состав раствора 6-10% НF и 10% НCl [2]
При этом следует учесть, что даже в терригенном пласте из-за своей высокой реакционной способности, реагируя с сульфатами и глинами, соляная кислота быстро нейтрализуется, а это приводит к повышению рН и выпадению осадков. При этом также происходит быстрое истощение и самой HF на реакцию с цементом, карбонатами и глиной с накоплением новых трудноизвлекаемых осадков СаF2 и геля кремниевой кислоты.
Температурный режим пластов влияет на скорость реакции кислот с породой, при повышении температуры более 60oС необходимо применение кислотных составов с замедленными сроками нейтрализации с целью повышения охвата пластов.
Возможно использование в качестве кислотного состава для обработок скважин с терригенными коллекторами смеси сульфаминовой кислоты и бифторида аммония [3] Но при этом в смеси с бифторидом аммония сульфаминовая кислота действует аналогично соляной, что предполагает избыток сульфаминовой кислоты, образует раствор грязевой кислоты, и подобный состав возможно использовать до температуры 50oС во избежание образования осадков сульфатов, получаемых за счет гидролиза сульфаминовой кислоты.
В прототипе [4] определены рабочие концентрации бифторида аммония в смеси с сульфаминовой кислотой для обработок в призабойной зоне скважин в терригенных коллекторах не более, чем 1 часть бифторида аммония на 4 части сульфаминовой кислоты исходя из того, что при таком соотношении происходит максимум и замедление скорости растворения при воздействии смеси на карбонаты. Замедление скорости реакции происходит за счет образования на поверхности известняка труднорастворимой коркой фтористого кальция.
Предлагаемый состав смеси имеет ряд недостатков: невозможность использования состава при повышенных (выше 50oС) температурах из-за образования в результате гидролиза сульфаминовой кислоты сульфат-ионов; высокая скорость реакции при повышенных температурах; высокая коррозионная активность; повышенный расход сульфаминовой кислоты, что экономически нецелесообразно.
Целью изобретения является: увеличение температуры возможного использования состава до 85oС за счет уменьшения осадкообразования; снижение скорости реакции с породой и коррозионной активности кислотного состава; уменьшение расхода сульфаминовой кислоты и стоимости кислотного состава.
Поставленная цель достигается тем, что кислотный состав для обработки терригенных коллекторов, включающий сульфаминовую кислоту и пресную воду, дополнительно содержит фторид аммония, или бифторид аммония, или бифторид-фторид аммония в количестве 0,56-18,50 мас. 0,43-14,25 мас. 0,51-17,00 мас. соответственно, а сульфаминовую кислоту в количествах не более эквимолекулярного. При этом смесь может содержать водорастворимый ПАВ - Неонол АФ9-25 или Нефтенол ВВД в количестве 0,05-0,5 мас.
Нижний предел концентраций фторида аммония, или бифторида аммония, или бифторид-фторида аммония соответствует минимальному количеству плавиковой кислоты, получающейся в результате реакции между компонентами, взятыми в эквимолекулярных количествах согласно следующим уравнениям:
H4F + NH2SO3H NH4SO3NH2 + HF (3)
NH4F•HF + NH2SO3H NH4SO3NH2 + 2HF (4),
которое используется для обработок пластов, в частности для разглинизации и составляет 0,3 мас. а верхний предел определяется максимальным количеством плавиковой кислоты, выше которого может начаться пескопроявление 10 мас.
Фторид аммония NH4F представляет собой бесцветное вещество, которое обладает следующими свойствами: молекулярная масса 37,04; плотность при 25•С 1010 кг/куб.м.
В промышленном масштабе выпускается бифторид аммония, который представляет собой кристаллическую соль с содержанием 96-97 мас. (NH4F•HF) и бифторид-фторид аммония, также кристаллическая соль, которая состоит из смеси двойной соли бифторида аммония (NH4F•HF) и фторида аммония (NH4F), воды и некоторого количества примесей, обычно он содержит 56 мас. фтора и 23 мас. кислотности.
Сульфаминовая кислота это кристаллический порошок с концентрацией HSO3NH2 96 мас. Реагент относится к достаточно сильным кислотам и обладает следующими свойствами:
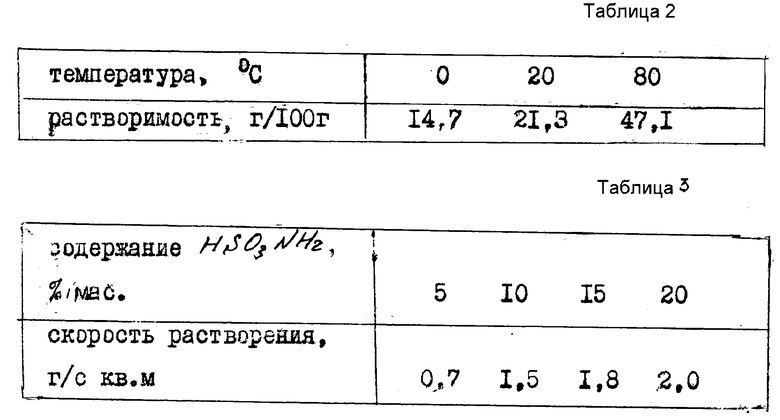
1. Растворимость сульфаминовой кислоты в воде приведена в табл. 2.
2. Скорость растворения мрамора в растворе HSO3NH2 приведена в табл. 3.
3. Коррозионная активность по стали 3 при температуре 30oС составляет 2,18 г/кв.м ч.
4. Водные растворы сульфаминовой кислоты подвергаются гидролизу при повышенных температурах, например, 10%-ный раствор кислоты при нагревании до 80oС за 8 ч гидролизуется на 44% по реакции
NH2SO3H + H2O NH4OSO3H NH4HSO4 (5)
5. В целом этот реагент обладает пониженной (в 5-6 раз) реакционной способностью и более низкой (в 3-3,5 раза) коррозионной активностью по сравнению с соляной кислотой.
В зависимости от наличия в составе того или иного фторсодержащего реагента реакция между компонентами смеси будет протекать по уравнению 3 (для фторида аммония), по уравнению 4 (для бифторида аммония) и по уравнениям 3 и 4 (для бифторид-фторида аммония). При разработке состава нет необходимости в избытке сульфаминовой кислоты для поддержания рН кислотного раствора. В среде, содержащей большое количество ионов аммония, возможно образование аммиакатов, координационных (комплексных) соединений, содержащих в качестве лигандов одну или несколько молекул NH3 (Химическая энциклопедия, М. Советская энциклопедия, т. 1, 1988). При этот рН раствора уменьшается:
NH
но аммиакаты комплексные соединения, не выпадающие в осадок (ионы аммония ингибируют образование осадков), также в свою очередь снижают рН, так как для них характерна внутрисферная амидореакция, например:
[Ca(NH3)2]F2 Ca(NH3)NH2F + HF (7).
Литературные данные подтверждают эксперименты. Испытанию на вторичное осадкообразование подвергались образцы, содержащие 93 мас. песка, 5 мас. глины, 2 мас. карбоната кальция (модель породы терригенного пласта).
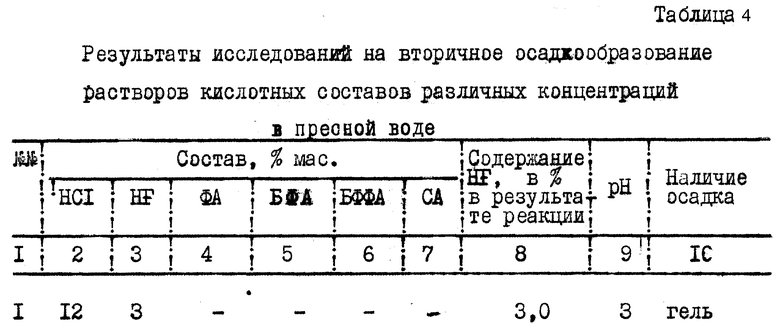
Образцы заливались растворами кислотного состава различных концентраций, наблюдения проводились визуально при температуре 85oС, в конце наблюдения измерялся рН раствора. Время наблюдения 6 ч. Результаты исследований представлены в табл. 4.
Как видно из табл. 4, предлагаемый состав не образует осадков при воздействии на образцы при температуре 85oС, в то время как раствор глинокислоты (п. 1) и раствор, содержащий избыток сульфаминовой кислоты (п. 11 прототип) при этой температуре образуют осадки, в первом случае за счет быстрой нейтрализации НСl, а во втором за счет образования сульфат-ионов в процессе гидролиза.
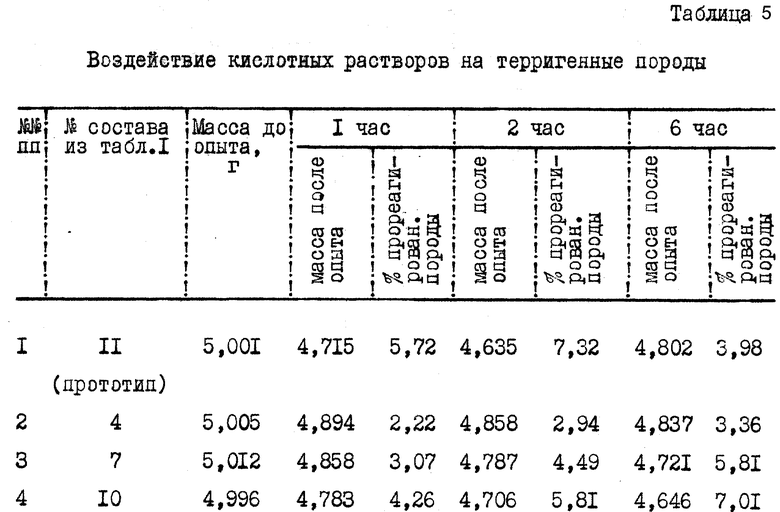
Исследования растворяющей способности кислотного состава при воздействии на образцы породы (модель терригенного пласта), содержащие 93 мас. кварцевого песка, 5 мас. бентонитовой глины, 2 мас. карбонатов, проводились по следующей методике. Навески образцов породы (около 5 г) высушивали до постоянной массы, после чего заливали кислотными растворами (количество кислотного раствора составляло 25 мл), устанавливали в термостат при температуре 85oС и выдерживали при этой температуре в течение 1,2 и 6 ч. Через заданное время кислотный раствор сливали, осадок промывали водным раствором щелочи до рН 9-10 (для лучшего удаления с поверхности остаточной кислотности), высушивали до постоянной массы и по разности масс определяли процент прореагированной породы. Результаты исследований представлены в табл. 5.
Из табл. 5 видно, что при использовании предлагаемого состава (опыты 2-4) процесс растворения породы более замедленный по сравнению с составом, содержащим избыточное количество сульфаминовой кислоты (опыт 1), при одном и том же содержании в составах HF 3 мас. При использовании предлагаемого состава не происходит также и прироста массы, что наблюдается в опыте 1 за счет образования осадка.
Коррозионная активность проверялась по стандартной методике на металлических пластинках (сталь 3). Коррозионную активность рабочего состава определяли при комнатной температуре и атмосферном давлении.
Пластинку из стали 3 размером 20х60х4 промывали в теплой воде, обезжиривали ацетоном или спиртом и высушивали до постоянного веса. Подготовленная таким образом пластинка подвешивалась на капроновой нити в стакане так, чтобы при заполнении стакана раствором кислоты торец пластинки оказался примерно на 10 мм под уровнем жидкости. Реакционный стакан заполнялся раствором кислотного состава, и пластинка оставлялась в этом растворе на определенное время. После истечения заданного времени пластинку вынимали из кислоты, погружали в стакан с водой, тщательно промывали в проточной воде мягкой щеткой и многократно ополаскивали горячей дистиллированной водой. Влагу с поверхности пластинки удаляли фильтровальной бумагой и пластинку сушили до постоянного веса.
Скорость коррозии вычисляли по формуле
V q•10-4•St
где V скорость коррозии, г/кв.м ч;
q потеря в массе пластинки от коррозии, г;
S поверхность, подвергающаяся коррозии, кв.м;
t время испытания, час.
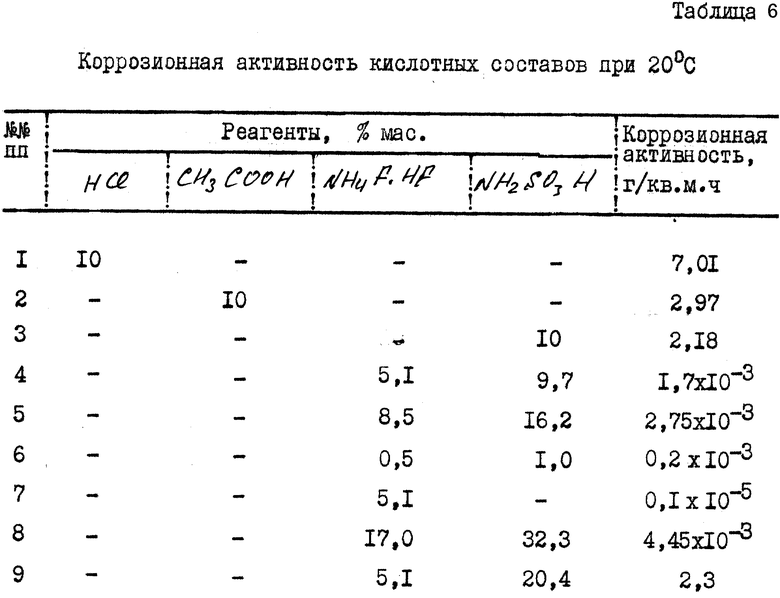
Результаты исследования приведены в табл. 6.
Как видно из табл. 6, предлагаемый состав (опыты 4-8) обладает наиболее низкой коррозионной активностью, по сравнению с используемыми в процессе кислотной обработки кислотами (опыты 1-3), так и по сравнению с прототипом (опыт 9).
В результате химической реакции между компонентами смеси образуется фтористоводородная кислота и аммониевая соль сульфаминовой кислоты, которая за счет гидролиза и сложных процессов комплексообразования позволяет поддерживать рН 1-2 до полной нейтрализации фтористоводородной кислоты. Это позволяет предотвратить образование геля гидрата окиси кремния, который запечатывает поровое пространство и сводит результат кислотной обработки на нет. Отсутствие в составе в свободном виде сульфаминовой кислоты позволяет избежать образование осадков сульфатов, которые могли бы образоваться за счет гидролиза сульфаминовой кислоты при повышенных температурах.
Состав обладает низкой коррозионной активностью, которая также обуславливается отсутствием в нем в свободном виде сульфаминовой кислоты.
Для улучшения смачиваемости и отмывающей способности состава в него дополнительно вводится водорастворимый ПАВ Неонол АФ9-25 или Нефтенол ВВД в количестве 0,05-0,5 мас.
| название | год | авторы | номер документа |
|---|---|---|---|
| КИСЛОТНЫЙ СОСТАВ ДЛЯ ОБРАБОТКИ ТЕРРИГЕННЫХ КОЛЛЕКТОРОВ И СПОСОБ КИСЛОТНОЙ ОБРАБОТКИ ПРИЗАБОЙНОЙ ЗОНЫ ПЛАСТА | 2003 |
|
RU2242605C1 |
| КИСЛОТНЫЙ СОСТАВ ДЛЯ ОБРАБОТКИ ТЕРРИГЕННЫХ КОЛЛЕКТОРОВ И СПОСОБ КИСЛОТНОЙ ОБРАБОТКИ ПРИЗАБОЙНОЙ ЗОНЫ ПЛАСТА | 2003 |
|
RU2244816C1 |
| КИСЛОТНЫЙ СОСТАВ ДЛЯ ОБРАБОТКИ НИЗКОПРОНИЦАЕМЫХ ТЕРРИГЕННЫХ КОЛЛЕКТОРОВ И СПОСОБ КИСЛОТНОЙ ОБРАБОТКИ ПРИЗАБОЙНОЙ ЗОНЫ ПЛАСТА С ЕГО ПРИМЕНЕНИЕМ | 2003 |
|
RU2243369C1 |
| КИСЛОТНЫЙ СОСТАВ ДЛЯ ОБРАБОТКИ НИЗКОПРОНИЦАЕМЫХ ТЕРРИГЕННЫХ КОЛЛЕКТОРОВ И СПОСОБ КИСЛОТНОЙ ОБРАБОТКИ ПРИЗАБОЙНОЙ ЗОНЫ ПЛАСТА С ЕГО ПРИМЕНЕНИЕМ | 2003 |
|
RU2242604C1 |
| СПОСОБ УДАЛЕНИЯ КОЛЬМАТИРУЮЩИХ ОБРАЗОВАНИЙ ИЗ ПРИЗАБОЙНОЙ ЗОНЫ ТЕРРИГЕННОГО ПЛАСТА | 2004 |
|
RU2283952C2 |
| СПОСОБ УДАЛЕНИЯ КОЛЬМАТИРУЮЩИХ ОБРАЗОВАНИЙ ИЗ ПРИЗАБОЙНОЙ ЗОНЫ ТЕРРИГЕННОГО ПЛАСТА | 2004 |
|
RU2272127C1 |
| СОСТАВ ПОЛИСАХАРИДНОГО ГЕЛЯ ДЛЯ ГИДРАВЛИЧЕСКОГО РАЗРЫВА ПЛАСТА | 1999 |
|
RU2173772C2 |
| СОСТАВ И СПОСОБ ПРИГОТОВЛЕНИЯ РЕАГЕНТА ДЛЯ СШИВКИ РАСТВОРОВ ПОЛИСАХАРИДОВ | 1998 |
|
RU2139424C1 |
| КИСЛОТНЫЙ СОСТАВ ДЛЯ ОБРАБОТКИ НИЗКОПРОНИЦАЕМЫХ ТЕРРИГЕННЫХ КОЛЛЕКТОРОВ С ВЫСОКОЙ КАРБОНАТНОСТЬЮ И СПОСОБ КИСЛОТНОЙ ОБРАБОТКИ ПРИЗАБОЙНОЙ ЗОНЫ ПЛАСТА С ЕГО ПРИМЕНЕНИЕМ | 2009 |
|
RU2407769C1 |
| БАЗОВАЯ ОСНОВА СОСТАВА ДЛЯ КИСЛОТНОЙ ОБРАБОТКИ ТЕРРИГЕННОГО КОЛЛЕКТОРА И РАЗГЛИНИЗАЦИИ ПРИЗАБОЙНОЙ ЗОНЫ ПЛАСТА | 2005 |
|
RU2301248C1 |



Изобретение относится к нефтегазодобывающей промышленности, в частности к кислотным обработкам терригенных коллекторов. Кислотный состав содержит, мас. %: фторид аммония 0,56-18,50, или бифторид аммония 0,43-14,25, или бифторид фторид аммония 0,51-17,00, сульфаминовую кислоту в эквимолекулярном количестве и пресную воду остальное. Состав может содержать водорастворимый ПАВ в количестве 0,05-0,5 мас.%. Кислотный состав отличается тем, что обладает пониженными скоростью реакции с породой и коррозионной активностью и не образует осадков при повышенной температуре. 1 з.п. ф-лы, 6 табл.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| П.М.Усачев | |||
| Гидравлический разрыв пласта | |||
| - М.: Недра, 1986 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| У.З.Ражетдинов и др | |||
| Применение бифторид фторид аммония для обработки скважин | |||
| Ж."Нефтяное хозяйство", 1984, N 4 | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| П.М.Южанинов и В.Н.Вилисов | |||
| Рациональные условия применения сульфаминовой кислоты при обработках скважин | |||
| Сборник научных трудов "Интенсификация процессов добычи нефти на месторождениях Пермского Прикамья" | |||
| - М.: ИГиРГИ, 1983 | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| В.П.Шалинов и др | |||
| Физико-химические методы повышения производительности скважин | |||
| Тематический научно-технический обзор | |||
| - М.: ВНИИОЭНГ, 1974, с | |||
| Коридорная многокамерная вагонеточная углевыжигательная печь | 1921 |
|
SU36A1 |
Авторы
Даты
1998-01-10—Публикация
1996-02-16—Подача