Изобретение относится к способам получения полупроводниковых, пьезо- и сегнетоэлектрических материалов с требуемыми свойствами, в частности тетратитаната бария, который является перспективным материалом для получения высокодобротной СВЧ-керамики, которая используется для элементов в микроволновых интегральных схемах и для подложек, на которых выполняются элементы схемы.
Известен способ получения тетратитаната бария, включающий приготовление смеси из диоксида титана и кислородсодержащего соединения бария, например, оксида бария, ее нагрев, выдержку, охлаждение и выделение кристаллов. Однако этим способом невозможно получить BaTi4O9 в виде нитевидных кристаллов высокой чистоты, который применяется в СВЧ-керамике.
Целью изобретения является получение однофазных нитевидных кристаллов (для СВЧ керамики тетратитаната бария BaTi4O9 с высокой добротностью).
Поставленная цель достигается тем, что в отличие от известного способа, включающего приготовление смеси из диоксида титана TiO2 и кислородсодержащего соединения бария, ее нагрев, выдержку, последующее охлаждение и выделение кристаллов, в предлагаемом способе исходный TiO2 берут в виде нитевидных кристаллов и предварительно обрабатывают серной кислотой в количестве 0,25-0,5 дм3 на 1 кг TiO2, в качестве кислородсодержащего соединения бария используют его с температурой плавления не выше 650oC, которое берут в количестве по отношению к TiO2, равном 0,5 - 0,8 в пересчете на BaO, а нагрев ведут при 1050-1150oC в течение 3 - 6 ч.
Чистоту используемых нитевидных кристаллов TiO2 можно повысить путем перевода примесей в растворимое состояние. Для этого предпочтительна обработка серной кислотой с плотностью 1,18-1,25 г/дм3 при соотношении: на 1 кг TiO2 - 0,25-0,5 дм 3 H2SO4. При этом при меньших соотношениях растворение примесей протекает значительно хуже и при одних и тех же расходах промывной воды в фильтрате содержится на порядок меньше ионов SO
Другой, наиболее важный эффект, который достигается после кислотной обработки - травление поверхности кристаллов и появление каналов между октаэдрами в структуре TiO2, по которым идет диффузия ионов Ba2-. Именно этот эффект, при прочих равных условиях, обеспечивает протекание реакции с образованием фазы BaTi4O9. Так, при проведении реакции между нитевидными кристаллами TiO2, которые не подвергались кислотной обработке, и, например, Ba(NO3)2 достигается выход фазы BaTi4O9 не более 60% мас., остальные 40% представляют собой фазы BaO, TiO2, BaTiO3. Таким образом, кислотная обработка нитевидных кристаллов TiO2 играет существенную роль для достижения поставленной цели.
Установлено, что реакция протекает между компонентами наиболее полно в нужном направлении, если до температуры начала взаимодействия кислородсодержащее соединение бария пропитывает структуру TiO2 и после пропитки начинает осуществляться интенсивная диффузия ионов Ba2- в структуру TiO2. Этот процесс осуществим при наличии достаточной пористости, что достигается в результате кислотной обработки и при условии превращения кислородсодержащего соединения бария в жидкую фазу до температуры разложения. Кроме того, как следует из теоретических предпосылок, процесс диффузии начинает интенсивно протекать при температурах 600 - 800 oC. Поэтому для достижения цели необходимо, чтобы кислородсодержащее соединение бария плавилось при температуре ниже 650 oC. При использовании кислородсодержащего соединения бария с температурой плавления выше 650oC не удается получить чистый тетратитанат бария. Получаемый продукт в этом случае имеет фазовый состав: BaCO3, BaTi4O9, BaTiO3, BaO, TiO2.
Другим важным фактором процесса является обязательный избыток кислородсодержащего соединения бария по отношению к стехиометрически необходимому. Соотношение кислородсодержащее соединение бария (в пересчете на BaO) : диоксид титана должно составлять 0,5 - 0,8. Ниже 0,5 - соотношение близко к стехиометрическому, более 0,8 - экономически нецелесообразно, т.к. имеет место повышенный расход бариевых соединений и большой расход воды на отмывку продукта.
Таким образом, данный способ позволяет получать тетратитанат бария BaTi4O9 в виде однофазных нитевидных кристаллов высокой чистоты.
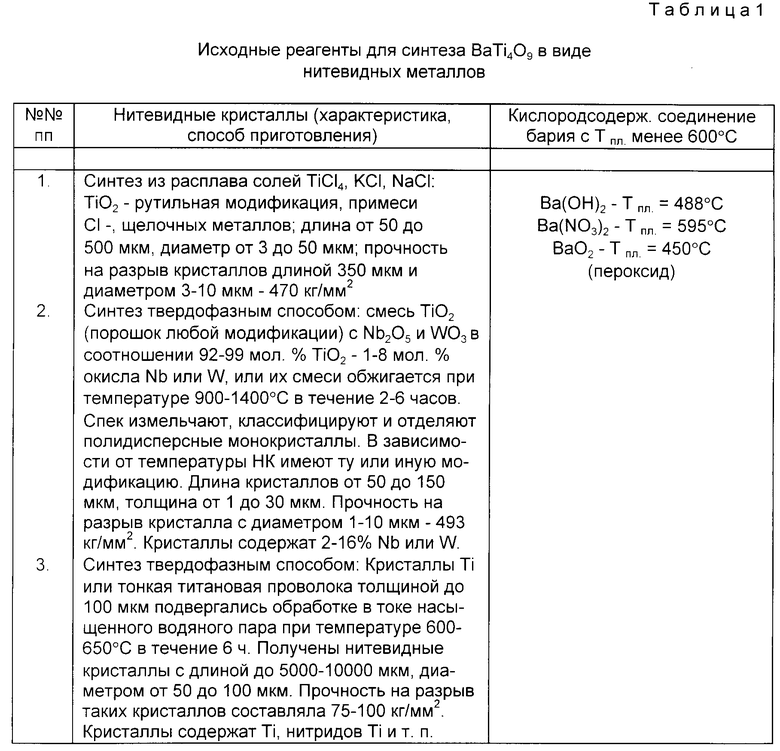
В табл.1 приведена характеристика исходных реагентов с подробным описанием режимов синтеза.
Предлагаемый способ осуществляют следующим образом. Нитевидные кристаллы диоксида титана любой структурной модификации, приготовленные любым методом, подвергают при необходимости измельчению и гидроклассификации, после чего обрабатывают серной кислотой с плотностью 1,18-1,25 г/дм3 при соотношении: 1 кг TiO2 - 0,25-0,5 дм3 H2SO4 в течение 15-35 мин. Затем НК TiO2 фильтруют, промывают дистиллированной водой с получением фильтрата, содержащего следы H2SO4 в количестве <0,0003 кг/дм3. Полученный продукт смешивают с кислородсодержащим соединением бария, имеющим температуру плавления ниже 650oC, в соотношении кислородсодержащее соединение бария (в пересчете на BaO) : диоксид титана = 0,5-0,8, а затем полученную смесь нагревают в течение 3-6 ч при температуре 1050-1150oC. Продукт отжига репульпируют дистиллированной водой, фильтруют, промывают дистиллированной водой с получением фильтрата с содержанием ионов бария < 0,0003%. Твердый осадок НК BaTi4O9 сушат при температуре 200-300oC. Фазовый состав продукта определяют с помощью рентгенофазового анализа на дифрактометре ДРОН-2 в Cu-Kα излучении при напряжении в трубке 35 кВ и силе тока 30 мА. Монохроматором является графит, что обеспечивает хорошее разрешение линий на дифрактограммах. Размеры кристаллов и их морфологию изучают на электронном микроскопе УЭМ-100. На прочность (на растяжение) кристаллы исследуют на установке ИКАН-2. Диэлектрическую проницаемость определяют стандартным методом.
Пример 1. 1000 г диоксида титана в виде нитевидных кристаллов, приготовленных по технологии 1 (табл. 1), со средними размерами: l = 1 мкм, d = 1,5 мкм, l/d = 66 подают в реактор из кварцевого стекла объемом 5 л, снабженный мешалкой. Одновременно в реактор подают раствор серной кислоты плотностью 1,18 г/дм3 в количестве 4л, что составляет соотношение TiO2 : H2SO4 = 1 : 0,5. Обработку кислотой осуществляют в течение 35 мин при постоянном перемешивании. Полученную суспензию фильтруют на барабанном вакуум-фильтре с рабочей поверхностью 0,5 м2, снабженном фильтровальной тканью канар, и в количестве 0,00025 кг/дм3. После промывки влажность твердого осадка составляет 10-12%. Соответственно количество твердой массы с учетом влажности составляет 1114,4 г. Полученный продукт подают в лопастной смеситель из нержавеющей стали, имеющий паровую рубашку и обогреваемый водяным паром с давлением 0,25 МПа (2,5). В рабочей зоне смесителя поддерживают температуру 95-98oC. Одновременно с подачей продукта в лопастной смеситель подают второй реагент Ba(NO3)2, имеющий температуру плавления 595 oC в количестве 1365 г, что составляет соотношение BaO:TiO2=1 :0,5. Компоненты перемешивают в течение 1 ч. Полученная смесь представляет собой гранулы (окатыши) размером 3-8 мм. После этого полученную смесь отжигают в течение 6 ч при температуре 1150oC во вращающейся электропечи (число оборотов печи - 0,5 об/мин, диаметр - 0,4 м, длина - 2 м, муфель выполнен из корунда). Продукт отжига обрабатывают дистиллированной водой в кварцевом реакторе емкостью 25 л при постоянном интенсивном перемешивании. Расход воды с температурой 96oC на массу полученного продукта составляет 45 л, обработку твердой массы осуществляют за три цикла, в каждом цикле объем воды составляет 15 л. В конечном фильтрате содержание ионов бария составляет 0,0001%. После последней фильтрации получают твердый осадок в количестве 1184 г, в том числе 12% H2O, т.е. целевой продукт в пересчете на сухое составил 1042 г. Затем твердый осадок подают в лопастную сушилку, где сушат до постоянного веса при температуре 200oC. В результате получают твердый продукт в количестве 1042,2 г.
Полученный продукт идентифицируют на дифрактометре ДРОН-2. В результате на дифрактограмме были получены пики, характерные для BaTi4O9. Микроскопический анализ показывает, что частицы представляют собой нитевидные кристаллы, близкие к праэдеритной структуре с аксиальным соотношением l/d ≈50. Распределение кристаллов по размерам подчиняется закону распределения случайной величины - закону Гаусса. Преобладающий размер кристаллов составляет l = (15 ± 1) мкм, d =(3 ± 0,2) мкм. Прочность кристаллов на разрыв - 150 кг/мм2.
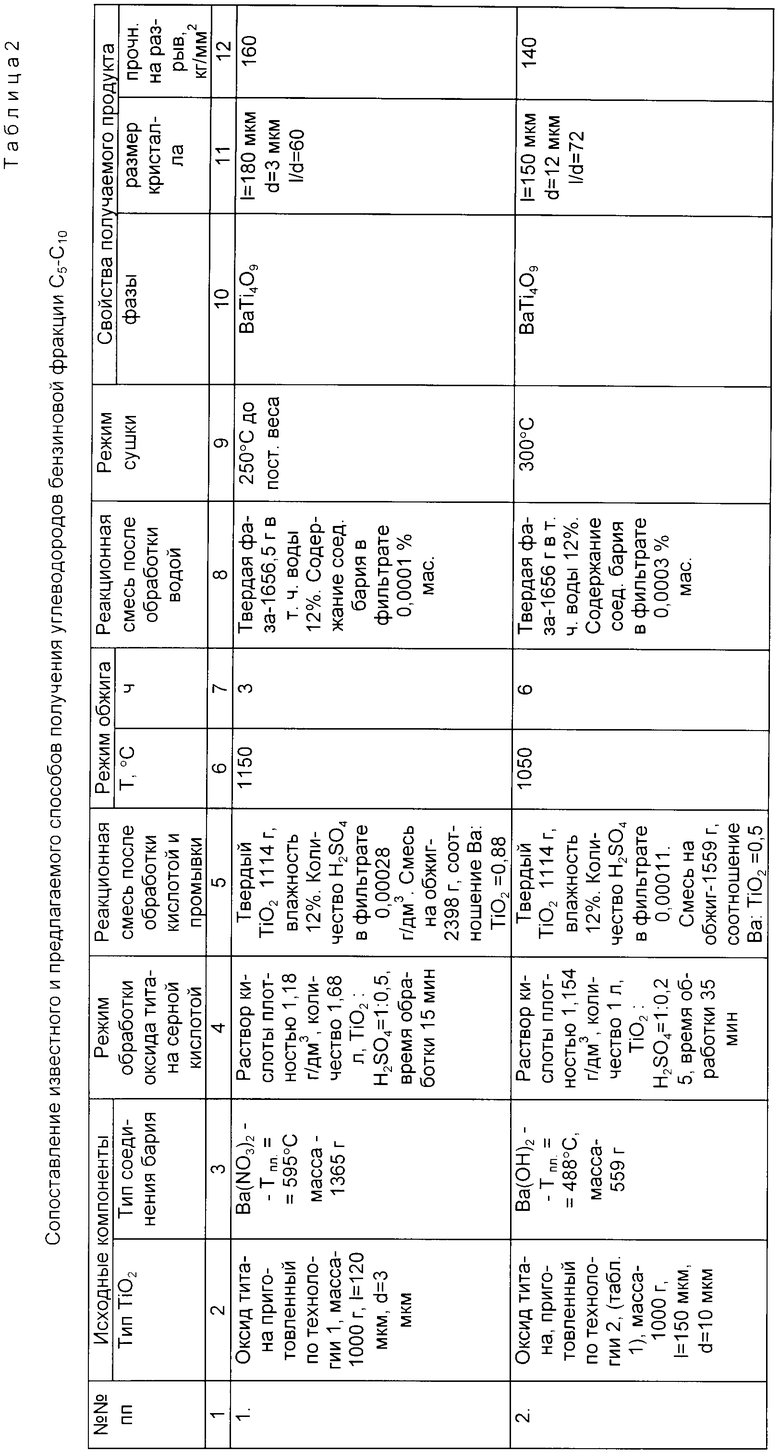
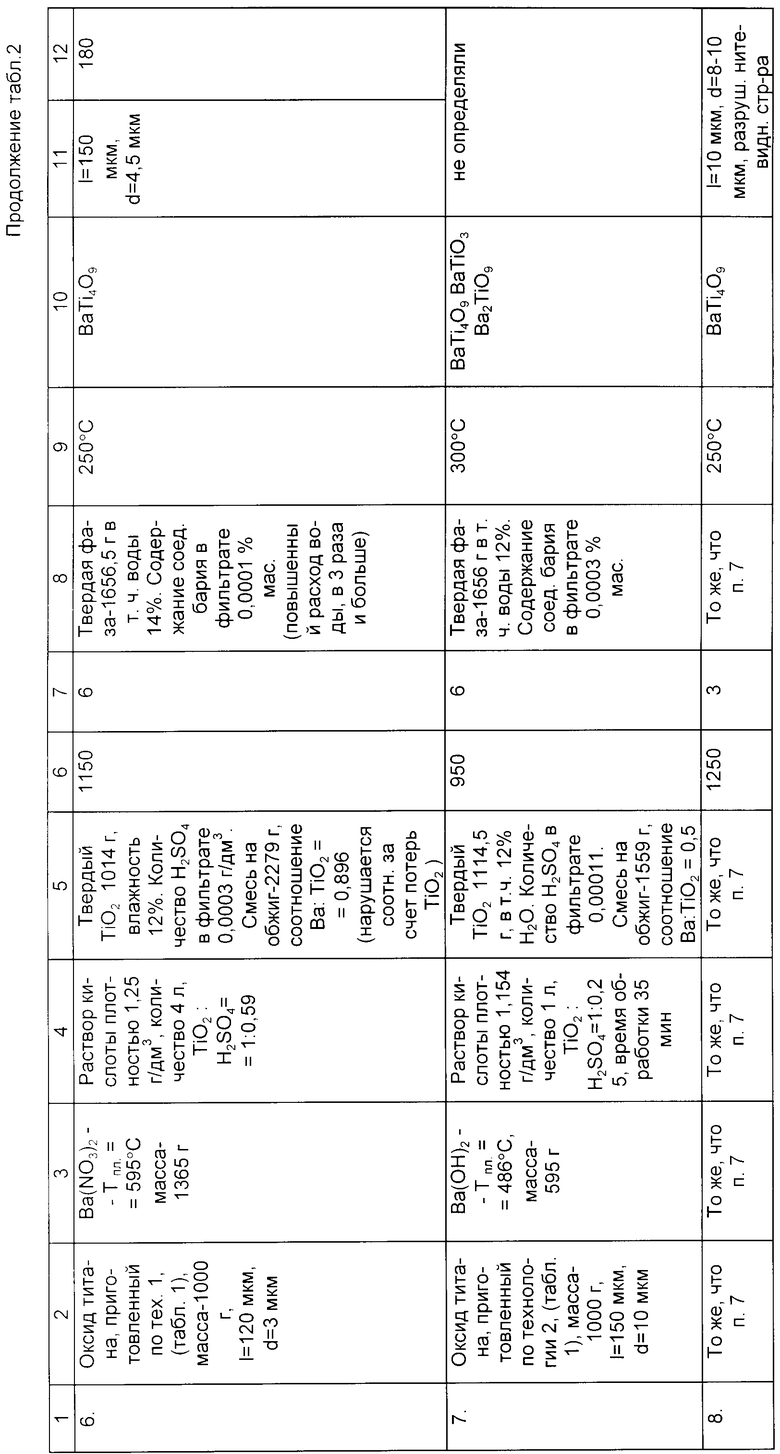
В таб. 2 приведены примеры, освещающие эффективность способа в заявляемых параметрах и при выходе за их пределы. Во всех примерах оборудование и последовательность операций аналогичны.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения керамического материала на основе оксидов бария и титана для пластин магнитных головок | 1990 |
|
SU1768562A1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ЦИНКА ИЗ ВАНН УЛАВЛИВАНИЯ ХЛОРАММИАКАТНЫХ ЭЛЕКТРОЛИТОВ | 1993 |
|
RU2080415C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФОТОКАТАЛИТИЧЕСКОГО ДИОКСИДА ТИТАНА МОДИФИКАЦИИ АНАТАЗ И БРУКИТ НА ПОВЕРХНОСТИ КЕРАМИЧЕСКОГО ИЗДЕЛИЯ ИЗ РУТИЛА, ПОЛУЧЕННОГО ОКИСЛИТЕЛЬНЫМ КОНСТРУИРОВАНИЕМ | 2017 |
|
RU2678206C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТИТАНОВОГО ДУБИТЕЛЯ ИЗ ТИТАНСОДЕРЖАЩЕГО СЫРЬЯ С ВРЕДНЫМИ ДЛЯ ДУБЛЕНИЯ ПРИМЕСЯМИ И СПОСОБ ВЫРАБОТКИ КОЖ | 1993 |
|
RU2085591C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПИГМЕНТА ДИОКСИДА ТИТАНА | 1990 |
|
RU2038300C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТИТАНСОДЕРЖАЩЕГО ПРОДУКТА ИЗ СФЕНОВОГО КОНЦЕНТРАТА | 2007 |
|
RU2356837C1 |
| СПОСОБ ПЕРЕРАБОТКИ ТИТАНСОДЕРЖАЩЕГО КОНЦЕНТРАТА | 2001 |
|
RU2207980C1 |
| СПОСОБ ПОЛУЧЕНИЯ КРИСТАЛЛИЧЕСКОГО ТИТАНАТА КАЛИЯ | 2008 |
|
RU2366609C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ФОРМОВАННОГО ВАНАДИЙ-ТИТАНОВОГО КАТАЛИЗАТОРА ДЛЯ ОЧИСТКИ ГАЗОВ | 1990 |
|
RU2050194C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИОКСИДА ТИТАНА | 1996 |
|
RU2102324C1 |


Использование: для получения высокодобротной СВЧ-керамики для элементов в микроволновых интегральных схемах и для подложек, на которых выполняются элементы схемы. Сущность изобретения: нитевидные кристаллы диоксида титана предварительно обрабатывают серной кислотой при соотношении 0,25-0,5 дм3 H2SO4 на 1 кг TiO2, смешивают с кислородсодержащим соединением бария, имеющим температуру плавления ниже 650oC, подвергают нагреву при температуре 1050-1160oC в течение 3-6 ч. Соотношение кислородсодержащее соединение бария (в пересчете на BaO) : диоксид титана составляет 0,5-0,8. Получают однофазные нитевидные кристаллы тетратитаната бария BaTi4O9 с высокой добротностью. 2 табл.
Способ получения тетратитаната бария BaTi4O9, включающий приготовление смеси из TiO2 и кислородсодержащего соединения бария, ее нагрев, выдержку, последующее охлаждение и выделение кристаллов, отличающийся тем, что, с целью получения однофазных нитевидных кристаллов для СВЧ-керамики, исходный TiO2 берут в виде нитевидных кристаллов и предварительно обрабатывают серной кислотой в количестве 0,25 0,5 дм3/кг TiO2, в качестве кислородсодержащего соединения бария используют его соединение с температурой плавления не выше 650oС, которое берут в количестве по отношению к TiO2, равном 0,5 0,8 в пересчете на ВаО, а нагрев ведут при 1050 -1150oС в течение 3 6 ч.
| Лучинский Г.П | |||
| Химия титана - М.: Химия, 1971, с.238. |
Авторы
Даты
1998-02-20—Публикация
1991-04-03—Подача